替吉奥联合顺铂与多西他赛联合顺铂治疗晚期食管癌的临床观察
2015-11-25马寅达郭斌
马寅达,郭斌
(辽宁医学院附属第一医院,辽宁锦州 121001)
食管癌为我国发病率及死亡率均较高的恶性肿瘤之一,本病病发后可严重影响患者的生命安全[1]。虽然早期手术治疗为治疗本病的主要治疗方法,临床有着较为理想的治疗效果[2],但是因本病发病常较为隐匿,患者发现时已处于食管癌晚期,往往已错过手术治疗本病的最佳时机。随着医疗技术的进步,化疗治疗已逐渐成为治疗晚期食管癌的主要手段,且在临床应用中发现,适当的化疗药物组合可在一定程度上可有效的改善患者的预后[3-5]。但是因目前应用于临床的化疗药物种类较多,不同的药物组合在临床应用过程中所达到的效果也存在一定的差异,为了更为有效的治疗本病,本研究将近年来我院在晚期食管癌治疗过程中所应用的两种化疗方案的治疗效果进行总结,报道如下。
1 资料与方法
1.1 一般资料 将我院于2013 年10 月至2014 年4 月接诊的112 例晚期食管癌患者作为观察对象,所有入选患者均需符合本研究的入选标准及排除标准。以接受联合替吉奥及顺铂治疗者为替吉奥组,患者58 例;以接受联合多西他赛及顺铂治疗者为多西他赛组,患者54 例。替吉奥组,男33 例,女25 例;年龄44~66 岁,平均(55.05 ±8.32)岁;病理分析:鳞癌41 例,腺癌17 例;分化程度:低分化19 例,中分化29 例,高分化10 例;KPS 评分61~88 分,平均(73.32 ±6.21)分。多西他赛组,男31 例,女23 例;年龄43~68 岁,平均(55.31 ±8.67)岁;病理分析:鳞癌40 例,腺癌14 例;分化程度:低分化18 例,中分化27 例,高分化9 例;KPS 评分62~87 分,平均(73.23 ±6.33)分。两组间性别、年龄、病理类型、分化程度及KPS 评分资料经统计学比较,无统计学差异,具可比性。
入选标准:(1)经病理学检查明确诊断为晚期食管癌;(2)严格遵照预定的治疗方案使用相同剂量药物的连续性病例;(3)影像学检查下存在可以测量的病灶;(4)具有完整的临床资料及随访资料;(5)预计生存期>3 个月;(6)KPS评分>60 分。
排除标准:(1)接受非本研究中化疗药物治疗者;(2)随访期间丢失随访者。
1.2 治疗方法 替吉奥组给予替吉奥(齐鲁制药有限公司,国药准字H20100151),按40~60 mg/d,日2 次口服治疗,服药2 w 后暂停服药1 w;顺铂(齐鲁制药 (海南)有限公司,国药准字H20073652),按30 mg,于开始口服替吉奥后第4至第6 日,日1 次静点治疗。多西他赛组给予多西他赛 (齐鲁制药有限公司,国药准字H20031244),按60 mg/m2+生理盐水250 mL,治疗第1 天静点治疗;顺铂按30 mg,于开始静点多西他赛后第4~6 天,日1 次静点治疗。两组均以3 w 为1 疗程。
1.3 观察方法 于患者入院接受治疗时开始统计,每周进行1 次随访,随访截止日期为2015 年4 月30 日。于患者接受2 个疗程治疗后,根据患者的临床症状、体征及检查结果对患者的治疗效果进行评价。以病灶完全消失者为完全缓解;以病灶最长直径较治疗前缩短>30%者为部分缓解;以病灶最长直径较治疗前缩短,但缩小未超过30%者为病情稳定;以病灶最长直径较治疗前增加为疾病进展。以完全缓解率及部分缓解率之和为治疗总有效率。对比两组治疗总有效率。同时统计两组患者在随访截止日期时存活患者例数,统计两组生存率并进行对比。并且对两组患者的中位生存期及无进展生存期进行统计,并进行对比。此外,统计并对比两组患者在接受治疗期间所出现的治疗副作用发生率。
1.4 统计方法 数据均经SPSS 19.0 分析,分别应用均数±标准差及百分率表示计量资料及计数资料,并应用t 检验及卡方检验对计量资料及计数资料进行分析。同时应用Kaplan-Meier 分析法绘制生存曲线,以log-rank 分析法对比较生存期差异。
2 结 果
2.1 近期治疗总有效率比较 替吉奥组近期治疗总有效率为51.72%,而多西他赛组近期治疗总有效率为55.56%,两组比较未见统计学差异(P >0.05),见表1。

表1 近期治疗总有效率比较
2.2 生存期相关指标比较 替吉奥组至随访截止日期时共有28 例患者存活,生存率48.28%,多西他赛组至随访截止日期时共有25 例患者存活,生存率46.30%,两组比较无统计学差异(χ2=0.044,P=0.833)。同时截止至随访日期时,替吉奥组中位生存期为10.91 月、中位无进展生存期为5.82 月,而多西他赛组为10.17 月、5.13 月,两组比较未见统计学差异 (χ2=0.196,P=0.658;χ2=3.021,P=0.082),见图1 和2。
2.3 两组治疗副作用发生率比较 两组随访期间治疗副作用发生率比较未见统计学差异 (P >0.05),见表2。
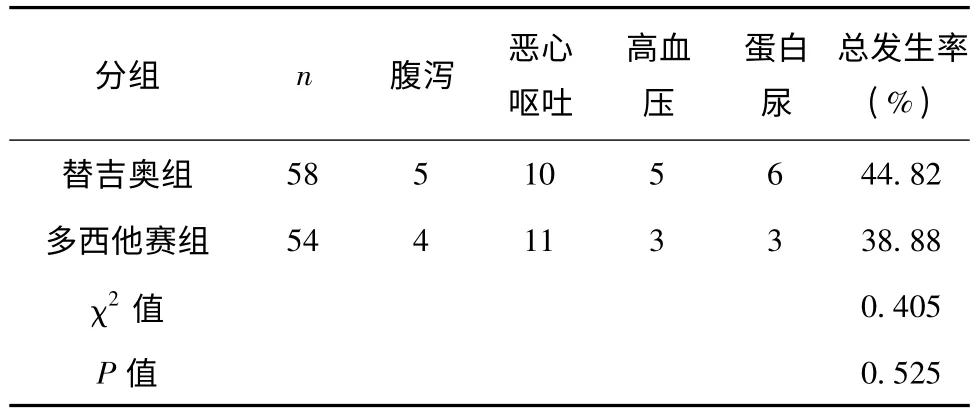
表2 两组治疗副作用发生率比较(n,%)
3 讨 论
替吉奥、多西他赛及顺铂均为目前临床常用的化疗药物,目前在临床应用中发现,其在包括胃癌[6-7]、乳腺癌[8]等多种恶性肿瘤的治疗中均有着较为理想的治疗效果。替吉奥是由替加氟、吉美嘧啶及奥替拉西钾三种成分所组成,其药物组成的三种成分间,可通过对胸苷酸合成酶产生抑制作用,从而达到干扰DNA 合成及抗肿瘤的作用[9]。而多西他赛则为通过促进微管蛋白形成微管,并导致所形成的微管束出现异常排列,使纺锤体的正常功能受到抑制从而达到抗肿瘤的作用[10]。而顺铂则为类抗肿瘤药物,也是目前临床研究较多的抗肿瘤药物之一,临床研究显示,顺铂可通过抑制肿瘤细胞内DNA 物质的合成,抑制肿瘤细胞增殖而达到抗癌的作用[11]。
故近年来我院在对晚期食管癌的临床治疗过程中,将替吉奥、多西他赛及顺铂应用于其中。而本研究为可更为全面的评价联合替吉奥及顺铂与联合多西他赛及顺铂两种治疗方案在晚期食管癌患者治疗中的应用价值,分别从近期疗效、生存期及治疗副作用发生率三方面对两组治疗方案的应用效果进行评价。首先,在近期疗效方法,应用了联合替吉奥及顺铂治疗的替吉奥组,其在近期治疗中,共有10 例患者达到完全缓解,20 例患者达到部分缓解,治疗总有效率为51.72%,而应用了联合多西他赛及顺铂治疗的多西他赛组,其在近期治疗中,共有11 例患者达到完全缓解,19 例患者达到部分缓解,治疗总有效率为55.56%,两组比较未见统计学差异。可见在接受了不同治疗方案的两组间,其近期治疗大致相同。随后本研究又通过对患者随访期间所统计的存活资料进行分析,结果显示,替吉奥组至随访截止日期时共有28 例患者存活,生存率48.28%,多西他赛组至随访截止日期时共有25 例患者存活,生存率46.30%,两组比较无统计学差异。同时截止至随访日期时,替吉奥组中位生存期为10.91 个月、中位无进展生存期为5.82 个月,而多西他赛组为10.17 个月、5.13 个月,两组比较未见统计学差异。可见虽然治疗方案不同,但两组的生存期并未见显著差异。最后本研究有对两组间的随访期间副作用发生率进行统计,结果显示,两组随访期间治疗副作用发生率比较未见统计学差异。通过本研究所得结果可见,无论联合替吉奥及顺铂治疗方案还是联合多西他赛及顺铂治疗方案,均对晚期食管癌有着较为理想的治疗效果,且两种治疗方案间近期治疗效果、生存期及治疗副作用发生率间均无统计学差异。但是,因本研究所观察的随访时间有限,故此无法对更长时间接受不同治疗方案患者的生存期进行对比,故尚需延长观察时间,以期可得到更为准确的观察结果。
综上所述,在晚期食管癌的临床治疗过程中,联合替吉奥及顺铂与联合多西他赛及顺铂两种治疗方案均有着较为显著的临床应用效果,在治疗晚期食管癌过程中,以上两组治疗方案均可应用。
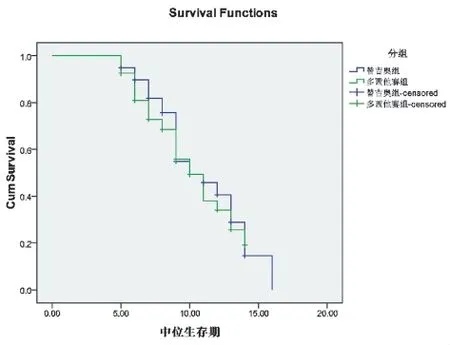
图1 两组中位生存期比较

图2 两组无进展生存期比较
[1]林蕾,王俊杰.(125)I 放射性粒子支架治疗食管癌进展[J].癌症进展,2013,1:41-43,67.
[2]Okumura Y,Mori K,Yamagata Y,et al.Two-stage operation for thoracic esophageal cancer:esophagectomy and subsequent reconstruction by a free jejunal flap [J].Surg Today,2014,44 (2):395-398.
[3]Yoon DH,Jang G,Kim JH,et al.Randomized phase 2 trial of S1 and oxaliplatin-based chemoradiotherapy with or without induction chemotherapy for esophageal cancer [J].Int J Radiat Oncol Biol Phys,2015,91 (3):489-496.
[4]Miyazaki T,Ojima H,Fukuchi M,et al.Phase II Study of Docetaxel,Nedaplatin,and 5-Fluorouracil Combined Chemotherapy for Advanced Esophageal Cancer [J].Ann Surg Oncol,2011,13 (3):26-32.
[5]Du J,Hu C,Zhang Y,et al.A retrospective study of paclitaxel combining nedaplatin chemotherapy for esophageal cancer[J].Anticancer Drugs,2015,26 (1):101-105.
[6]Yamada Y,Higuchi K,Nishikawa K,et al.Phase III study comparing oxaliplatin plus S-1 with cisplatin plus S-1 in chemotherapy-naive patients with advanced gastric cancer [J].Ann Oncol,2015,26 (1):141-148.
[7]Wang Y,Liu C,Luo M,et al.Chemotherapy-Induced miRNA-29c/Catenin-delta Signaling Suppresses Metastasis in Gastric Cancer [J].Cancer Res,2015,75 (7):1332-1344.
[8]von MG,Loibl S.Evolution of adjuvant chemotherapy for breast cancer [J].Lancet,2015,385 (9980):1812-1814.
[9]Kawahara M.Efficacy of S-1 in non-small cell lung cancer[J].Expert Opin Pharmacother,2014,15 (13):1927-1942.
[10]Li X,Yao R,Yue L,et al.FOXM1 mediates resistance to docetaxel in gastric cancer via up-regulating Stathmin [J].J Cell Mol Med,2014,18 (5):811-823.
[11]Karasawa T,Steyger PS.An integrated view of cisplatin-induced nephrotoxicity and ototoxicity [J].Toxicol Lett,2015,12 (3):26-28.
