正交试验法优选温热清口服液提取工艺*
2015-11-11孙文鹏韩在虹孙瑜高明
孙文鹏 韩在虹 孙瑜 高明△
(1.大连大学医学院,辽宁大连116622;2.黑龙江省齐齐哈尔市中医医院,黑龙江齐齐哈尔161005)
·研究报告·
正交试验法优选温热清口服液提取工艺*
孙文鹏1韩在虹2孙瑜2高明1△
(1.大连大学医学院,辽宁大连116622;2.黑龙江省齐齐哈尔市中医医院,黑龙江齐齐哈尔161005)
目的优选温热清口服液的提取工艺。方法采用正交试验,以挥发油含量为指标,考察药材蒸馏时间、料液比、超声时间3因素对挥发油提取的影响;以绿原酸含量和浸膏得率为综合指标,筛选提取工艺条件。结果优选的挥发油提取工艺为蒸馏4 h,加8倍量水,超声60 min;最佳提取工艺为加12倍量水煎煮3次,煎煮时间为50 min。结论该提取工艺合理、稳定,为温热清口服液工业生产提供参考。
温热清口服液正交试验绿原酸提取工艺
温热清口服液是齐齐哈尔市中医医院针对急性外感热病研制的复方中药制剂,由石膏、赤芍、连翘、柴胡、金银花、薄荷、鱼腥草和荆芥8味中药组成。临床应用已有10余年,疗效显著[1],但其提取工艺方面的报道少。原提取工艺采用均匀设计法[2],以芍药苷为指标对水提工艺进行考察。本文对原提取工艺进行改进,以超声辅助水蒸气蒸馏法提取挥发油,采用正交设计法以绿原酸含量及浸膏得率为综合指标,筛选最佳提取工艺。
1 仪器与材料
1.1仪器L-2130高效液相色谱仪(日本日立HITACHI)、V-detector L-2400检测器(日本日立HITACHI);N-2000色谱数据工作站(浙江大学智达信息工程研究所)、E-202F电子天平(奥豪斯仪器上海有限公司)、HH-S112电热恒温水浴锅(上海跃进医疗器械厂)、KH2200DB超声波清洗器(昆山禾创超声仪器有限公司)等。
1.2试药石膏购自辽宁,柴胡购自内蒙古,金银花购自河南,鱼腥草、连翘购自陕西,薄荷、荆芥购自安徽,赤芍购自甘肃,均经大连大学医学院中医中药学系高松副教授鉴定均为真品。绿原酸标准品购自中国食品药品检定研究院,批号110753-200413;乙腈和甲醇为色谱纯,磷酸为优级纯,其余试剂均为分析纯。
2 方法与结果
2.1正交试验法提取挥发油
2.1.1正交试验设计选择蒸馏时间(A)、料液比(B)、超声时间(C)为主要影响因素,每个因素选择3个水平,以挥发油含量为指标,按照L9(34)正交表进行试验,考察挥发油提取工艺。见表1。
2.1.2试验方法按处方分别称取柴胡、金银花、薄荷、鱼腥草和荆芥药材粗粉加入2000 mL圆底烧瓶中,按表1的料液比加入蒸馏水与沸石数粒,振摇均匀,浸泡30 min后超声波处理,圆底烧瓶与挥发油测定器、

表1 挥发油提取因素水平
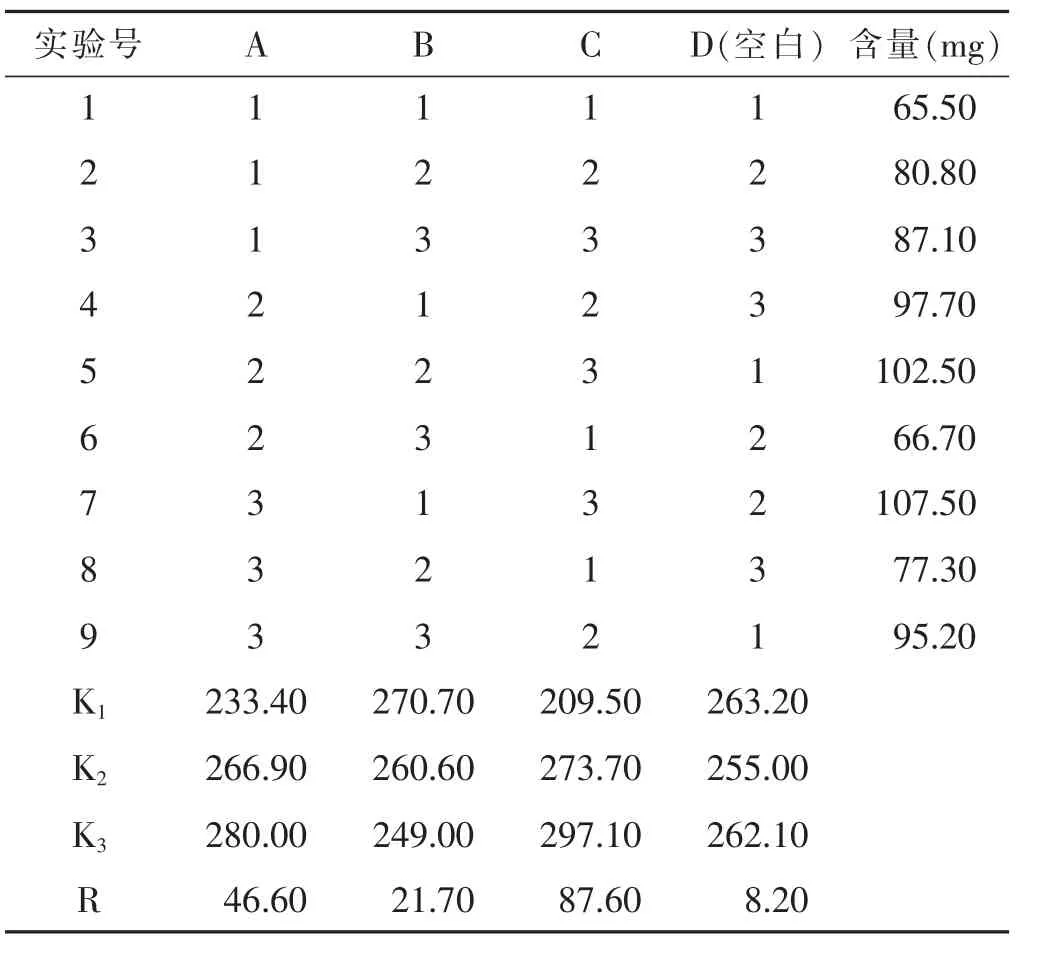
表2 挥发油提取工艺正交试验结果
2.1.3方差分析通过SPSS11.5软件对挥发油的正交试验结果进行方差分析,结果见表3。
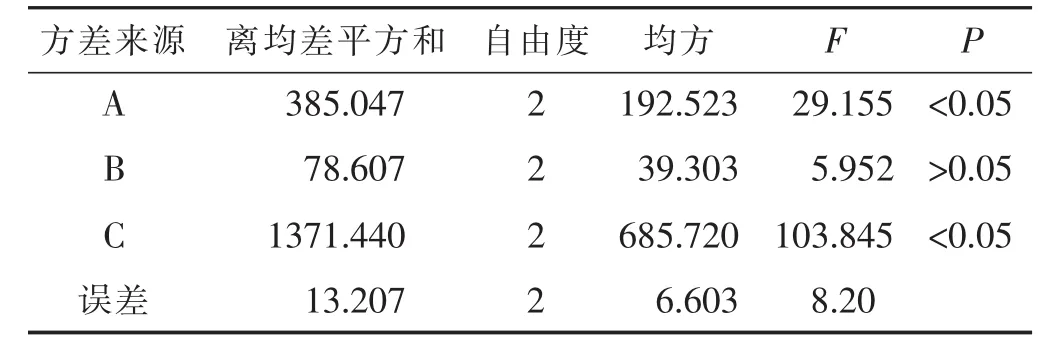
表3 挥发油提取方差分析
通过对表2、表3 3个因素的极差R进行比较,可知:RC>RA>RB,3个因素对挥发油提取工艺的影响程度依次为C>A>B,其中超声时间和蒸馏时间对挥发油提取得率的影响较大,差异有统计学意义(P<0.05),料液比对挥发油提取得率的影响不大,差异无统计学意义。根据实验结果,因素C选择最佳水平3,因素A选择最佳水平3,因为因素B水平间差异较小,所以选择水平2,因此确定挥发油提取的最佳工艺为A3B2C3,即蒸馏4 h,料液比1∶8,超声时间为60 min。
2.1.4验证试验按正交试验筛选的最佳提取工艺A3B2C3进行试验重复3次,3次试验的挥发油含量分别为108.10、107.50、108.70 mg,平均值为108.10 mg,RSD为0.56%。说明此提取条件下得到的挥发油得率较高,稳定可行。
2.2水提工艺的正交试验组方药材所含化学成分主要为黄酮类、皂苷类和有机酸类等极性成分,口服液工业生产中要本着节能高效的原则,所以综合考虑以水煎煮法为提取方法。
2.2.1正交试验设计根据药材的性质及结合实际生产考虑,选择加水量(A)、提取时间(B)、提取次数(C)为主要考察因素,每个因素选3个水平,以浸膏得率和绿原酸含量为综合指标,按照L9(34)正交表进行试验,考察水提最佳工艺。见表4。
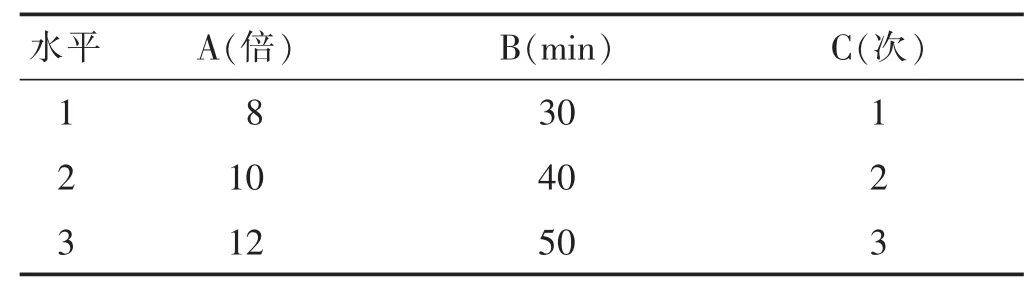
表4 水提法因素水平
2.2.2样品溶液的制备处方组成:石膏110 g,赤芍、连翘、柴胡、薄荷和荆芥各12 g,金银花15 g,鱼腥草23 g。称处方量的药材9份,粉碎成粗粉,加蒸馏水浸泡30 min,按照正交表进行试验。其中石膏先煎30 min,柴胡、金银花、薄荷、鱼腥草和荆芥提取挥发油后药渣与其他药材共同煎煮。煎煮后的药液用8层纱布过滤,滤液减压浓缩后定容至300 mL,密封备用。
2.2.3浸膏得率的测定将2.2.2项下得到的样品提取液,各精密量取20 mL,分别置于已干燥至恒重的蒸发皿中,水浴蒸干,残渣置于105℃干燥箱中5 h,干燥至恒重,取出,迅速置于干燥器中放冷后迅速精密称重,按以下公式计算浸膏得率:浸膏得率=(VW1/20W)×100%。公式中,V为每份药材提取液总体积,W1为20 mL提取液的浸膏质量,W为每份药材的质量。
2.2.4含量测定(1)色谱条件。色谱柱:Diamonsil钻石C18柱(250 mm×4.6 mm,5 μm),流动相为乙腈-0.4%磷酸(1∶9),流速1 mL/min,检测波长327 nm,柱温为室温,进样量10 μL。(2)对照品溶液的制备。精密称取绿原酸对照品2.07 mg,置于25 mL棕色容量瓶中,加50%甲醇溶解,超声5 min,并稀释至刻度,摇匀,即为对照品溶液,用0.45 μm有机系微孔滤器滤过,取续滤液备用(4℃保存)。(3)供试品溶液的制备。取各供试品溶液10 mL离心,精密吸取2 mL置于25 mL容量瓶中,加50%甲醇溶解,超声5 min,并稀释至刻度,摇匀,用0.45 μm有机系微孔滤器滤过,取续滤液即得。(4)阴性样品溶液的制备。称取处方组成中除金银花外的其余药材,按照生产工艺制备阴性样品,并按“2.2.4(3)”项下方法制备,即得阴性样品溶液。(5)专属性试验。取“2.2.4”项下的对照品、供试品及阴性样品溶液各10μL按“2.2.4(1)”项下的色谱条件进行测定,绿原酸色谱峰与供试品中其他组分的色谱峰分离良好,阴性样品溶液的色谱峰对绿原酸的测定无干扰,见图1。(6)线性范围考察。精密吸取绿原酸标准品溶液2、4、6、8、10 μL依次进样,以绿原酸含量(X,μg)为横坐标,峰面积(Y)为纵坐标做标准曲线,回归方程为Y= 3.1E+9X+13300(r=0.99905),其线性范围为0.1656~0.8280 μg。(7)精密度试验。精密吸取同一对照品溶液10 μL注入高液相色谱仪,重复进样5次,按“2.2.4(1)”项下色谱条件测定绿原酸峰面积,结果RSD值为1.31%(n=5),表明仪器精密度良好。(8)稳定性试验。精密吸取同一供试品溶液,于0、2、4、8、12、24 h分别进样,按“2.2.4(1)”项下色谱条件测定,记录色谱峰面积。结果RSD值为1.68%(n=6),表明供试品溶液在24 h内稳定性良好。(9)重复性试验。取同一批号温热清口服液6份,按“2.2.4(3)”项下方法制备供试品溶液,依法测定,其平均含量为0.9178 mg/mL。结果绿原酸含量的RSD值为1.89%(n=6),表明本方法重复性良好。(10)样品回收率试验。采用加样回收法。精密量取同一供试品3组(共6份每份1mL),3组分别精密加入绿原酸标准品2.06,2.45,3.31 mg,按上述色谱条件测定,计算回收率。绿原酸平均回收率为100.41%,RSD=1.78%(n=6)。(11)样品含量测定。精密吸取样品溶液10 μL,按上述色谱条件,依次进样测定。再按标准曲线项下各对应峰面积计算出各样品组绿原酸的含量(见图1)。水提正交试验结果见表5。
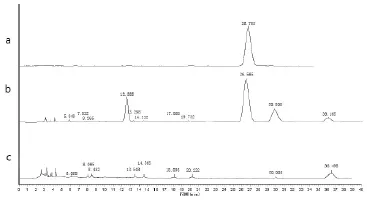
图1 绿原酸含量测定HPLC色谱
2.2.5结果分析通过SPSS11.5软件对表5中的绿原酸含量和浸膏得率两指标进行方差分析,结果见表6和表7。
从表5、表6中可以看出,因素A、因素B对绿原酸含量的影响有显著性差异;因素C对绿原酸含量的影响无差异;影响因素大小顺序为RB>RA>RC,通过表5和表7可以看出,因素A和因素C对干膏率的影响有显著性差异;因素B对干膏率的影响无差异;影响因素大小顺序为RC>RA>RB。综合绿原酸含量及干膏率两个考察指标,确定最佳组合为A3B3C3,即加水量12倍,煎煮次数3次,煎煮时间50 min。

表5 水提正交试验结果
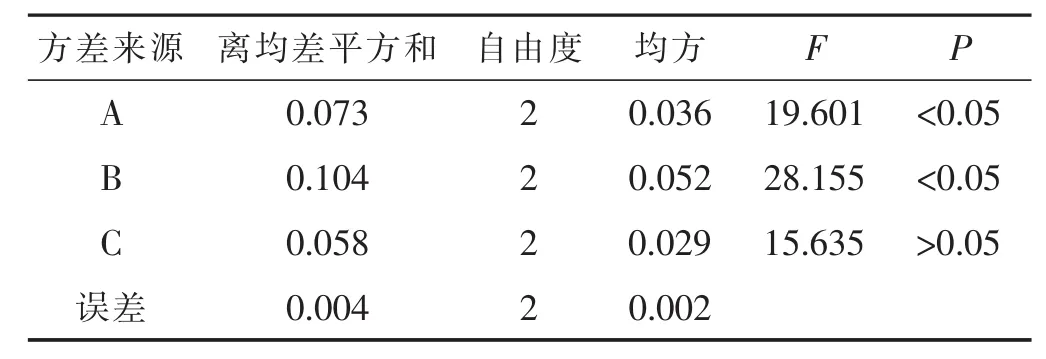
表6 水提正交试验绿原酸含量方差分析
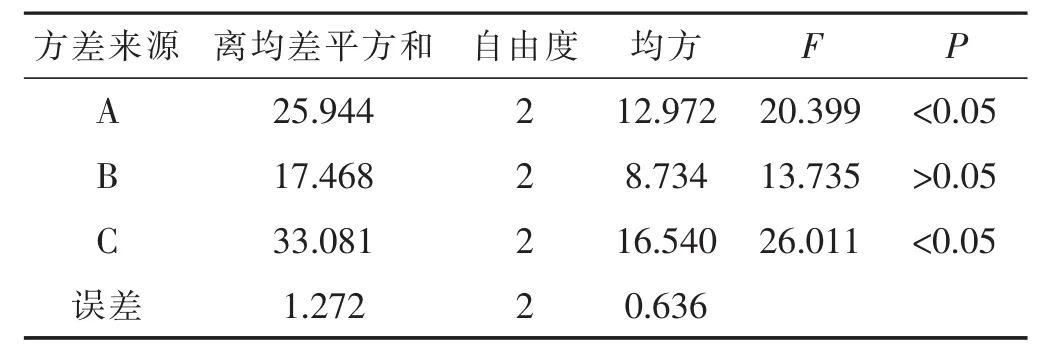
表7 水提正交试验浸膏得率方差分析
2.2.6验证试验取处方量的药材共3份,每份煎煮3次,加12倍量水;煎煮时间为50 min;提取后,每批药液按“2.2.4(3)”项下方法制备出3个样品,测定绿原酸含量和浸膏得率,结果见表8。表明优选出的最佳工艺稳定。
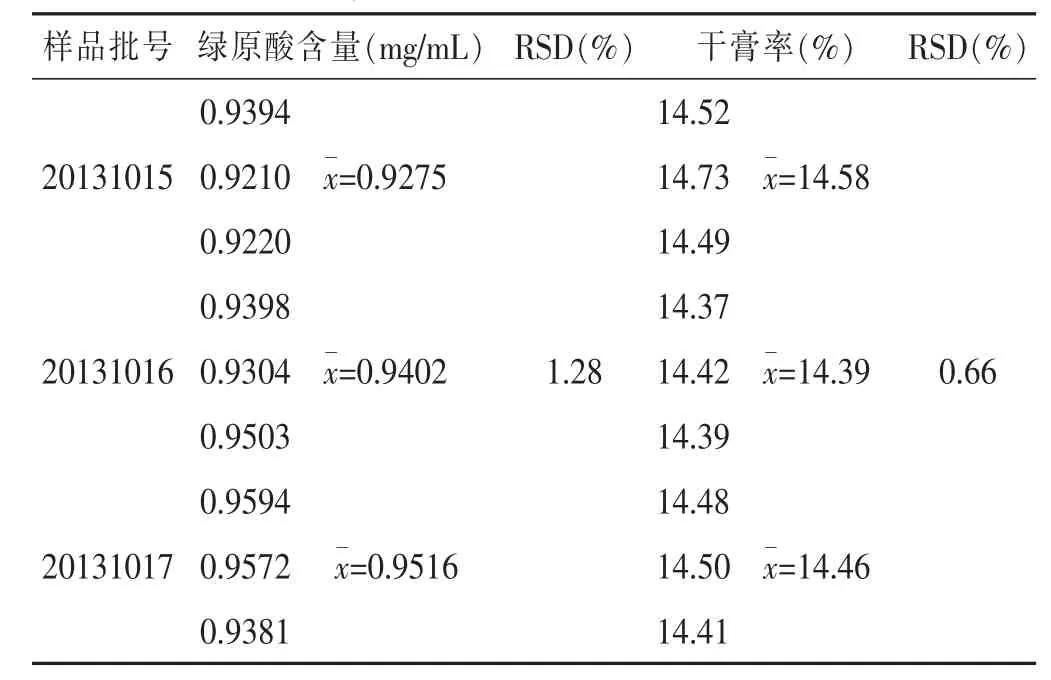
表8 3批样品测定结果
2.3提取工艺优化前后比较
2.3.1取处方量的药材6份,各取3份药材按照优化后提取工艺及原提取工艺进行提取,分别测定绿原酸含量、干膏率。优化后提取工艺:柴胡、金银花、薄荷、鱼腥草和荆芥5味药材粗粉在蒸馏4 h,料液比1∶8,超声时间为60 min的条件下提取挥发油,提取挥发油后的药渣与组方余药进行水提取。水提取条件为煎煮3次,加水倍数为12;煎煮时间为50 min。原提取工艺[2]:挥发油提取采用水蒸气蒸馏法,蒸馏时间4 h,料液比1∶8;水提取条件为煎煮2次,加水倍数分别为10倍量、8倍量;煎药时间为1.5 h、1 h。
2.3.2比较结果每批提取液选择3个样品测定绿原酸含量、干膏率和挥发油含量,测定结果取平均值,结果见表9,通过SPSS11.5软件对试验结果进行分析。见表10。
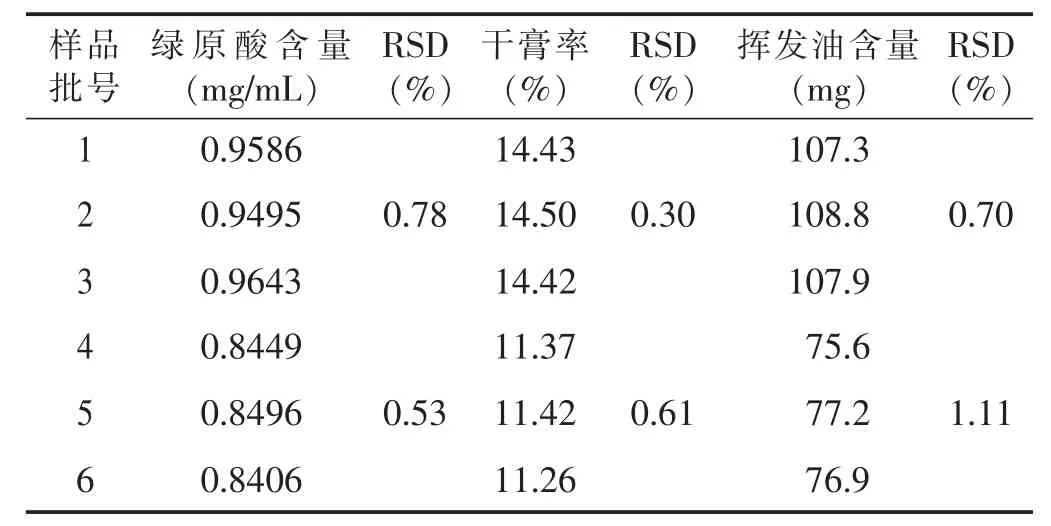
表9 两种工艺3批样品测定结果比较
通过表10分析结果可知,优化后工艺与原工艺绿原酸含量、干膏率以及挥发油含量均有显著性差异(P<0.01)。
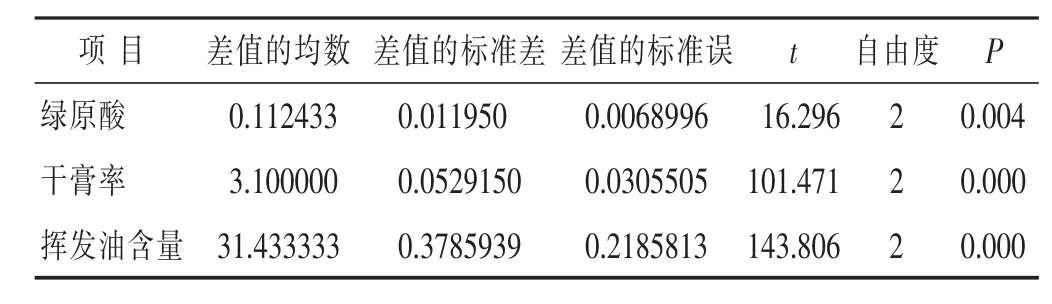
表10 两种提取工艺绿原酸含量、干膏率及挥发油含量的t检验
3 讨论
温热清口服液方中柴胡、金银花、薄荷、鱼腥草和荆芥均含有挥发油成分,为防止提取过程中挥发油损失,增强挥发油类有效成分的药效作用,故进行原工艺的提取方法优化,确定先进行挥发油提取,药渣与其他药材合并水煎煮。挥发油提取试验中采用超声波辅助水蒸气蒸馏法[3],利用超声波产生的空化效应,及强烈振动、高加速度、热效应、搅拌等超声波的许多次级效应,可以加速植物有效成分进入溶剂,有利于样品中有效成分转移从而提高提取率[4]。因挥发油提取时油量不足1 mL,故以质量进行测定。
该制剂方中金银花为臣药,其主要活性成分为绿原酸,具有解热抗炎、抗菌抗病毒,免疫调节等多种药理作用[5],且该制剂中绿原酸含量测定的样品处理简单,杂质峰少,色谱分离效果佳。故可选择绿原酸为该提取工艺的指标成分。考虑到中药复方制剂的协同作用,测定绿原酸含量的同时兼顾方中其他药物有效成分的提取,所以将总固量也作为考察指标,而原工艺没有进行绿原酸含量的检测。中药组成十分复杂,因此,该制剂提取工艺的合理性还有待于通过药理实验得到进一步验证。
通过对优化后提取工艺与原提取工艺的比较可知,在优化后工艺下进行试验中挥发油提取量,提取液中绿原酸含量及总固量均高于原提取工艺。优化后的提取工艺提取效率高,稳定、可靠,可为大生产提供依据。
[1]崔相烈,韩寿英.李鸿雕,等.小儿温热清灌肠液的试制及临床观察[J].黑龙江医药,2001,14(2):136.
[2]高明,韩在虹,金福厚,等.温热清口服液工艺条件的筛选[J].中国中医药信息杂志,2005,12(10)50-51.
[3]黄蓓,毛长智.正交实验设计优选荆芥穗挥发油超声波提取工艺[J].中国医药导报,2011,8(20):107-108.
[4]徐浩锋,杨华俊,俞岚.中药有效成分现代提取技术研究进展[J].海峡药学,2012,24(1):13-18.
[5]孙立娟.金银花的成分及药理学研究[J].中国实用医药,2011,6(30):239-240.
Extraction Technology Optimization for Wenreqing Oral Liquid by Orthogonal Test
SUN Wenpeng1,HAN Zaihong2,SUN Yu2,et al.
1 Medical College of Dalian University,Liaoning,Dalian 116622,China;2 Qiqihaer Hospital of Traditional Chinese Medicine,Heilongjiang Province,Heilongjiang,Qiqihaer 161005,China
Objective:To optimize extraction technology of Wenreqing Oral Liquid.Methods:The research had been screened out the best abstraction technological conditions of Wenreqing Oral Liquid by orthogonal test,using the weight of volatile oil to investigate the influence by the factors of distillation time,ratio of solid to liquid,ultrasonic time and so on.Chlorogentic acid content and extract yield rate were used as comprehensive indicators.Results:The optimization method of extraction technology of the volatile oil was distilling 4h with 8 times the amount of water and ultrasound for 1h.The best extracting process was decocting three times with 12 times the amount of water,and the three decocting durations were 50 minutes.Conclusion:The technology is reasonable and stable that can provide reference for industrial production.
Wenreqing Oral Liquid;Orthogonal test;Chlorogentic acid;Extraction technology
R283.6
A
1004-745X(2015)01-0059-04
10.3969/j.issn.1004-745X.2015.01.020
黑龙江省齐齐哈尔市科技局计划项目(SFGG-201344)
(电子邮箱:gm056@126.com)回流冷凝管连接。自冷凝管上端加入蒸馏水使充满挥发油测定器的刻度部分,至水溢流入圆底烧瓶时为止。将烧瓶置于电热套中加热至沸腾,保持微沸,达到蒸馏时间后停止加热,放置片刻,打开测定器下端的活塞,使水缓慢放出,水至油层上端到达0刻度线上5 mm处停止。放置1 h以上至挥发油凝固,取出,吸去固体表面的水分,精密称重,计算挥发油含量,结果见表2。
2014-06-06)
