三棱的环二肽类成分抗凝活性
2015-10-19王淑美王佰灵许亚韬闫二磊胡旭光梁生旺
刘 贝, 王淑美, 王佰灵, 许亚韬, 闫二磊, 胡旭光, 梁生旺
(广东药学院中药学院,广东 广州 510006)
三棱的环二肽类成分抗凝活性
刘 贝,王淑美,王佰灵,许亚韬,闫二磊,胡旭光,梁生旺*
(广东药学院中药学院,广东广州510006)
目的 研究从三棱中分离得到的环-(酪氨酸-亮氨酸)、环-(苯丙氨酸-苯丙氨酸)和环-(苯丙氨酸-酪氨酸)这3个环二肽类成分的体外抗凝活性。方法 使用试剂盒测定三棱乙醇提液分离得到3个环二肽类成分对取自雄性SD大鼠腹主动脉贫血小板血浆的凝血酶原时间(PT)、活化部分凝血活酶时间(APTT)及凝血酶时间(TT)。结果 环-(酪氨酸-亮氨酸)、环-(苯丙氨酸-苯丙氨酸)和环-(苯丙氨酸-酪氨酸)均可使大鼠血浆PT、APTT和TT显著延长(P<0.1)。前二者未呈现出量效关系,后者呈现正性量效关系。结论 三棱的环二肽类成分均具有抗凝活性,以环-(苯丙氨酸-酪氨酸)的抗凝作用尤为显著。
三棱;环-(酪氨酸-亮氨酸);环-(苯丙氨酸-苯丙氨酸);环-(苯丙氨酸-酪氨酸);抗凝血;凝血酶原时间;活化部分凝血活酶时间;凝血酶时间
三棱为黑三棱科植物黑三棱Sparganium stoloniferum Buch.-Ham.的干燥块茎,首载于《本草拾遗》,现为《中国药典》收载,其味苦、性平,入肝、脾经,具有破血行气、消积止痛等功能[1]。现代药理研究表明,三棱被广泛应用于心脑血管疾病,肿瘤及妇科各类疾病的治疗[2-3]。三棱的化学成分复杂,含有黄酮和黄酮苷、苯丙素苷、甾体及其苷、有机酸等化合物[4-5],虽然现代化学和药理研究已部分阐明了化学成分和临床应用之间的联系[6-7],但是还有很多活性成分未被找到。因此进一步揭示三棱中化学成分与临床医学应用之间的联系,对于指导临床用药和新药开发有非常重要的意义。
本课题组前期对三棱醇提液进行系统的化学研究,利用有效成分跟踪法从本植物中分离得到3个环二肽类成分:环-(酪氨酸-亮氨酸)(cyc1o-(Tyr-Leu))(化合物A),环-(苯丙氨酸-苯丙氨酸)
(cyc1o-(Phe-Phe))(化合物B),环-(苯丙氨酸-酪氨酸)(cyc1o-(Phe-Tyr))(化合物C)[8-9]。本实验通过观察其对凝血酶原时间(prothrombin time,PT)、活化部分凝血活酶时间(activated partia1 thrombop1astin time,APTT)及凝血酶时间(thrombin time,TT)的影响,对此3种环二肽进行体外抗凝活性的初步研究,以期为抗血栓天然药物的开发提供新的依据。
1 材料
1.1动物 雄性SD大鼠30只,体质量180~250 g,由广州中医药大学实验动物中心提供,许可证号:SCXK(粤)2008-0020。
1.2药物与试剂 凝血酶原时间PT试剂盒、活化部分凝血激酶时间APTT试剂盒和凝血酶时间TT试剂盒均购自南京建成生物工程研究所,批号分别是20130314、20130201、20130314;肝素(Sigma公司,批号20120509);水合氯醛(广州思乐生化试剂有限公司);生理盐水(贵州天地药业有限公司,批号A13011209);二甲基亚砜(DMSO)(分析纯,广州化学试剂厂);枸橼酸钠(分析纯,天津市百世化工有限公司,批号0110)。
1.3仪器 台式离心机(北京医用离心机厂);电热恒温水浴锅(HHS型,上海博讯实业有限公司医疗设备厂);FA1104型电子分析天平(上海天平仪器厂);秒表(上海星钻秒表有限公司);EP管(上海申翔化学试剂有限公司);移液枪(北京华汇通科技发展有限公司);注射器(上海楚定分析仪器有限公司)。
2 方法
2.1血浆制备 大鼠用10%水合氯醛(350 mg/kg)腹腔注射麻醉,腹主动脉取血,分装于含0.4 mL,109 mmo1/L枸橼酸钠抗凝液的塑料离心管,每管约3.6 mL,立即轻轻颠倒混匀。3 000 r/min离心15 min,收集上清,即得贫血小板血浆(PPP),在2 h内进行实验,或-20℃冻存备用。
2.2环二肽类成分的制备[9]
2.2.1三棱有效部位的提取 取中药三棱的干燥块茎14 kg,粉碎成粗粉,置多功能提取罐中,用60%乙醇加热回流提取3次,每次2 h,过滤,合并续滤液,回收乙醇,干燥,得总浸膏752 g。将总浸膏混悬于水中,超声20 min,依次用石油醚、三氯甲烷、乙酸乙酯、正丁醇萃取3次,合并各萃取液,减压回收,得石油醚部位浸膏26 g,三氯甲烷部位浸膏34 g,乙酸乙酯部位浸膏11.5 g,正丁醇部位浸膏42 g,见路线图1。

图1 三棱有效部位的提取路线图Fig.1 Extracting process of effective fraction of Sparganium stoloniferum Buch.-Ham.
2.2.2环二肽类成分的分离纯化 将所得乙酸乙酯部位11.5 g浸膏,使用约50 mL乙酸乙酯溶解样品,干法拌样,经硅胶(200~300目)柱层析粗分,以三氯甲烷-甲醇溶剂系统进行梯度洗脱,TLC检视,合并薄层行为相同的流份。图2所示为乙酸乙酯部位的粗分流程图。
Fr.38~Fr.40合并,减压浓缩,用适量甲醇溶解,室温放置,得到白色针状结晶。根据化合物1H-NMR,13C-NMR数据及文献比对结果,确定分得化合物为环-(苯丙氨酸-酪氨酸)(化合物C),结构式见图3。

图2 乙酸乙酯部位的粗分流程图Fig.2 Extracting process of ethyIacetate extract

图3 环-(苯丙氨酸-酪氨酸)(化合物C)Fig.3 Com pound C(cycIo-(Phe-Tyr))
Fr.41~Fr.43合并,减压浓缩,用适量三氯甲烷溶解,干法拌样,经硅胶(200~300目)柱层析细分,以三氯甲烷-甲醇溶剂系统进行梯度洗脱,TLC检视,合并相同的流份。将Fr.2~Fr.4合并,室温放置后析出白色针状结晶,依据1H-NMR,13CNMR光谱测定数据和文献比对结果,确定该结晶也为环-(苯丙氨酸-酪氨酸)。Fr.41~Fr.43段的细分流程见图4。将Fr.5~Fr.7合并,室温放置后析出白色针状结晶,通过测定1H-NMR,13C-NMR,HMBC,HMQC光谱和文献比对,确定分得化合物环-(酪氨酸-亮氨酸)(化合物A),结构式见图5。
Fr.44~Fr.47合并,减压浓缩,用适量三氯甲烷溶解,干法拌样,经硅胶(200~300目)柱层析细分,以三氯甲烷-甲醇溶剂系统进行梯度洗脱,TLC检视,合并相同的流份。将Fr.5~Fr.9合并,减压浓缩,用适量三氯甲烷溶解,干法拌样,经硅胶(200~300目)柱层析再细分,以三氯甲烷-甲醇等比例洗脱,TLC检视,合并Fr.8~Fr.11,析出白色针状色结晶,经反复重结晶得纯针状结晶化合物。根据化合物1H-NMR,13C-NMR数据及文献比对结果,确定分得化合物环-(苯丙氨酸-苯丙氨酸)(化合物B),结构式见图6。图7所示为Fr.44~Fr.47段的细分流程图。

图4 Fr.41~Fr.43段的细分流程图Fig.4 Extracting process of Fr.41-Fr.43

图5 环-(酪氨酸-亮氨酸)(cycIo-(Tyr-Leu))(化合物A)Fig.5 Compound A(cycIo-(Tyr-Leu))
2.3环二肽类成分的纯度测定 采用HPLC法对上述分得的3中环二肽进行纯度测定。色谱条件:色谱柱Phenomenex Luna(2)C18柱(250 mm× 4.6 mm,5μm);流动相乙腈-0.1%THF(20∶80);体积流量1.0 mL/min;柱温30℃;检测波长210 nm;进样量10μL。以面积归一化法计算,各化合物的质量分数均大于99.0%。
图6 环-(苯丙氨酸-苯丙氨酸)(cycIo-(Phe-Phe))(化合物B)Fig.6 Compound B(cycIo-(Phe-Phe))

图7 Fr.44~Fr.47段的细分流程图Fig.7 Extracting process of Fr.44-Fr.47
2.4抗凝活性测定 将化合物A、B、C用DMSO溶解成0.5、1.0、2.0、4.0 mg/mL的溶液,手工法测定各肽的APTT、PT和TT值。具体实验分别按照凝血酶原时间PT试剂盒、活化部分凝血激酶时间APTT试剂盒以及凝血酶时间TT试剂盒说明进行操作。对于每一个化合物,其4个质量浓度下的APTT、PT和TT指标各重复测定10次。
2.5结果记录 加入相应试剂立即混匀并开动秒表,试管仍浸于水浴中,至约10 s时取出,每隔2 s向上挑动至生成固体细丝终止计时,即得PT、APTT或TT时间。
3 结果
3.1化合物A的抗凝血活性 与空白组相比,化合物A的各质量浓度组均可显著延长大鼠血浆PT、APTT和TT值(P<0.10,图8),但并不表现出浓度依赖性。进一步分析,发现化合物A对PT指标作用明显(P<0.05),其次为APTT指标和TT指标。

图8 不同质量浓度化合物A对大鼠血浆PT,APTT,TT的影响Fig.8 InfIuence of com pound A on p Iasma APTT,TT and PT
3.2化合物B的抗凝血活性 与空白组相比,化合物B的各质量浓度组均可显著延长大鼠血浆PT、APTT和TT值(P<0.10,图9),但并不表现出抗凝时间随质量浓度增高而延长的特点。进一步分析,发现化合物B对TT指标作用明显(P<0.01),其次为APTT指标和PT指标。
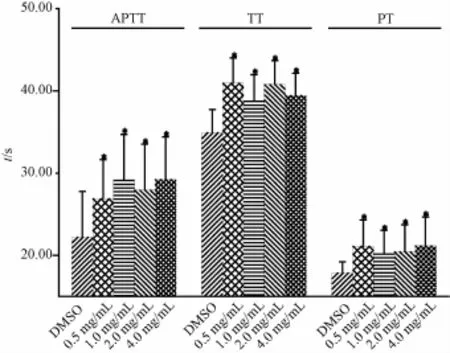
图9 化合物B对大鼠血浆PT,APTT,TT的影响Fig.9 InfIuence of compound B on p Iasma APTT,TT and PT
3.3化合物C的抗凝血活性 与空白组相比,化合物C的各质量浓度组均可显著延长大鼠血浆PT、APTT和TT值(P<0.10,图10),且表现出较明显的质量浓度依赖性(图11)。进一步分析,发现化合物C对PT、APTT和TT指标作用强度相当(P<0.01)。

图10 化合物C对大鼠血浆PT,APTT,TT的影响Fig.10 InfIuence of compound C on p Iasma APTT,TT and PT

图11 化合物C与PT,APTT,TT值的量效关系Fig.11 M eans p Iots of PT,APTT and TT against different concentrations of compound C
4 讨论
血液凝固是由凝血因子按一定顺序相继激活而生成的凝血酶最终使纤维蛋白原变为纤维蛋白的过程。因此,凝血过程可分为凝血酶原酶复合物的形成、凝血酶的激活和纤维蛋白的生成3个基本步骤。其中,凝血酶原酶复合物可以通过内源性凝血途径和外源性凝血途径生成。两条参与途径的主要区别在于启动方式和参与的凝血因子不相同,但两条途径中的某些凝血因子可以相互激活,两者间相互密切联系并非各自独立[10]。
本实验选取了凝血酶原时间PT、活化部分凝血活酶时间APTT及凝血酶时间TT作为化合物A、 B、C的体外抗凝活性检测指标[11-12]。APTT、PT和TT分别代表3条不同的凝血途径[13]。PT主要用于筛选检测外源凝血系统的FⅡ、Ⅴ、Ⅶ、Ⅹ及相关因子的抑制物的试验,通过在待测血浆中加入过量的组织凝血活酶和钙离子,使凝血酶原变为凝血酶,后者使纤维蛋白原转变为纤维蛋白。APTT常用于内源性凝血系统(Ⅷ、Ⅸ、Ⅺ、Ⅻ因子)的筛选及肝素抗凝治疗的监测。以各种激活剂(如白陶土)激活待测血浆中凝血因子Ⅻ,Ⅺ,再以磷脂作为凝血的活性表面,激活内源凝血途径,使凝血酶原转变成凝血酶,凝血酶使纤维蛋白原转变成纤维蛋白,导致血浆的凝固。TT是检测凝血、抗凝及纤维蛋白溶解系统功能的一个简便试验,检查待测血浆纤维蛋白原转变为纤维蛋白的能力。
实验中设定α值为0.10,当P值小于0.10为有显著性差异。大鼠个体间的血凝情况存在差异,考虑到本研究的目的在于考察三棱中环二肽的抗凝活性,所以在统一性别的基础上每组设置10只大鼠,而并未对其个体的血凝差异进行深入研究。依据现有结果,认为可通过增加样本量的方法来减小标准差。中药三棱是一味破血止痛的良药,有赖于其中多种化学物质组的共同作用而非某单体化合物的单一功效,本研究结果证明了三棱中的环二肽类化合物属于其药效物质成分之一,但具体的抗凝机制与构效关系有待进一步研究。
实验结果显示,化合物A、B、C均能在体外显著延长大鼠血浆PT、APTT、TT值,表现出抗凝活性。化合物C的3个指标项下的时间均数随质量浓度增高而延长,当达到4 mg/mL时,抗凝作用进一步加强,呈现出一定的量效关系但不显著,各剂量组间无显著性差异(P>0.10);实验中不同剂量梯度的化合物A和B对各指标的影响也未呈现出量效关系。这可能与实验的操作方法有关。本实验采用手工法进行化合物的体外抗凝活性评价,操作误差较大,从而使标准差过大,一定程度上削弱了不同药物浓度组间均数的差异[14]。可通过改用仪器测量的方法来减小标准差。
此外,不同化合物对PT、APTT及TT指标的作用强度也不尽相同:化合物A对PT指标作用明显,其次为APTT指标和TT指标;化合物B对TT指标作用明显,其次为APTT指标和PT指标;化合物C对PT、APTT和TT指标的作用强度相当。此3种化合物对各指标敏感性的不同提示各化合物的抗凝机制存在差异:化合物A主要通过外源性凝血途径产生抗凝作用;化合物B的抗凝机制主要与血浆纤维蛋白原水平及纤维蛋白形成的速度有关;化合物C可能对内源性及外源性凝血系统共同途径产生抗凝作用。结合化合物A、B、C的结构,发现A与C均含有对羟苯基的结构片段,B与C均含有苄基结构片段,A含有一个异丙基片段而B和C均不含此结构。可以推测,若化合物中含有对羟苯基的取代结构,则该物质更倾向于通过干扰外源性凝血途径而达到抗凝作用,同时也会激发内源性途径的某些凝血因子继而使凝血效应放大;抑或作用于内源性及外源性凝血系统共同途径产生抗凝效果。若化合物中含有苄基结构片段,则该物质更倾向于通过干扰血浆纤维蛋白原至纤维蛋白的转变而达到抗凝效果。本实验不能说明化合物的抗凝作用与其结构的疏水性有相关关系[15]。
综上,环-(酪氨酸-亮氨酸)、环-(苯丙氨酸-苯丙氨酸)及环-(苯丙氨酸-酪氨酸)均为首次从本植物中分离得到的环二肽类成分,经体外实验研究证实各化合物均具有抗凝活性,以环-(苯丙氨酸-酪氨酸)的抗凝作用尤为显著并呈现出一定的量效关系,进而分析推测了此三种化合物的体外抗凝作用机制。但在本实验中,各化合物的量效关系均不明显,且不清楚其究竟作用于凝血系统的何环节或作用于何因子,此外,当3种成分叠加作用时抗凝效果如何,这些都有待于深入研究。
[1]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010.
[2]袁 涛.中药三棱化学成分的研究[D].沈阳:沈阳药科大学,2006.
[3]戴仕林,吴启南,殷 婕.中药三棱的现代研究进展[J].中国民族民间医药,2011,17(1):63-64.
[4]梁侨丽,孔丽娟,吴启南,等.三棱的化学成分研究[J].中草药,2012,43(6):061-1064.
[5]王新胜,吴启南,陈广云,等.三棱化学成分与质量评价的研究进展[J].中国药房,2013,24(15):417-1420.
[6]邓英君.三棱不同提取物镇痛及抗凝作用研究[J].时珍国医国药,1999,10(12):882-883.
[7]孙 杰,王 芍,郭 斌,等.三棱黄酮体外诱导A549及MCF-7细胞S/G2周期停滞的研究[J].天然产物研究与开发,2011,23(2):224-227,282.
[8]邓小慧.三棱有效部位的化学成分研究[D].广州:广东药学院,2009.
[9]陈舒茵.三棱有效部位的化学成分研究[D].广州:广东药学院,2010.
[10]姚 泰.生理学[M].上海:复旦大学出版社,2005.
[11]柳青海,李天才.藏药牦牛肝蛋白体外抗凝血活性研究[J].时珍国医国药,2012,23(8):1927-1928.
[12]冯光军,朱正光,余传林,等.水蛭乙醇提取物体外抗凝血活性研究[J].中药材,2007,30(8):909-911.
[13]李艳玲,黄荣清,孙晓东.水蛭不同提取物抗凝活性的体外实验研究[J].中药材,2004,27(2):123-125.
[14]陈 燕,陈忠明,杨光辉,等.PT、APTT、TT手工法与凝血仪法对比分析在临床中的应用[J].医疗装备,2005,18(6):38-39.
[15]田 垒,霍建丽,王卫国,等.新的抗凝血三肽及其改造物的合成和生物活性[J].西北药学杂志,2009,24(3):191-194.
Anticoagu Iant activity of cycIic dipeptides from Sparganii Rhizome
LIU Bei, WANG Shu-mei, WANG Bai-1in, XU Ya-tao, YAN Er-1ei, HU Xu-guan,LIANG Shen-wang*
(Department of Chinese Traditional Medicine,Guangdong Pharmaceutical University,Guangzhou 510240,China)
AIM To study the in vitro anticoagu1antactivity of cyc1odipeptide(cyc1o-(Tyr-Leu),cyc1o-(Phe-Phe)and cyc1o-(Phe-Tyr))iso1ated from Sparganium stoloniferum Buch.-Ham.METHODS The specia1 kits were used to measure anticoagu1ant activity with p1ate1et poor p1asma co11ected from abdomina1 aorta ofma1e SD rats,inc1uding prothrombin time(PT),activated partia1 thrombop1astin time(APTT)and thrombin time(TT). RESULTS PT,APTT,TT were pro1onged by the addition of cyc1o-(Tyr-Leu),cyc1o-(Phe-Phe)and cyc1o-(Phe-Tyr).The former two presented no dose-effect re1ationship but the 1atter did.CONCLUSION Of three cyc1odipeptides from S.stoloniferum,a11 the three show anticoagu1ant activities with cyc1o-(Phe-Tyr)being by far themost effective.
Sparganium stoloniferum Buch.-Ham.;cyc1o-(tyr-1eu);cyc1o-(phe-phe);cyc1o-(phe-tyr);anticoagu1ation;prothrombin time(PT);activated partia1 thrombop1astin time(APTT);thrombin time(TT)
R285.5
A
1001-1528(2015)01-0034-06
10.3969/j.issn.1001-1528.2015.01.008
2014-02-14
刘 贝(1989—),女,硕士生,主要从事中药质量控制研究。Te1:(020)39352172,E-mai1:1iubei_cpu@163.com
梁生旺(1954—),男,教授,博士生导师,主要从事中药质量控制及新药研发研究。Te1:(020)39352172,E-mai1:sw1iang371@163.com
