不同直径卵泡排卵对自然周期冻融胚胎移植临床结局的影响
2015-08-10李玉梅李欣凝刘冬娥
李玉梅,李欣凝,刘冬娥
(中南大学湘雅医院生殖医学中心,长沙 410008)
与新鲜胚胎移植周期比较,冻融胚胎移植(FET)主要优点有:治疗周期短,简单易行,提高了累积妊娠率等,因此,FET 已经成为了体外受精-胚胎移植(IVF-ET)的重要组成部分。目前,临床上有许多方法来准备FET 的子宫内膜,其中最常用的方法是利用月经的自然周期FET 和使用外源性激素来准备内膜[1-5]。自然周期FET 不需要使用外源性激素,适用于平时有排卵,月经周期规律的患者[6]。
卵泡的生长发育和闭锁是一个复杂的生理过程。正常生理情况下,妇女每个月经周期卵泡经过募集、选择、单个卵泡发育成熟后在促黄体生成素(LH)峰作用下排卵是成功妊娠的必要条件。卵泡直径是预测卵母细胞成熟度和良好黄体功能的重要指标。个体间排卵前成熟卵泡的直径不尽相同,在1.735~2.859cm 之间。而小卵泡排卵在临床上虽然较为普遍,但尚无明确定义。一般认为,LH 峰日优势卵泡的直径平均值≤1.6cm 排卵者为小卵泡排卵[7]。文献报道小卵泡排卵是导致不孕的一个重要因素,在不孕不育患者中占65%[8]。小卵泡排卵的患者周期妊娠率低、流产率高,因此临床上监测排卵过程中如发现小卵泡排卵,一般建议患者取消自然周期,而通过促排卵等方案治疗可明显增加妊娠率,改善妊娠结局[9]。在自然周期FET 过程中,遇到小卵泡排卵是否应该取消周期,目前文献报道较少。本文回顾性分析2011年1月至2013年12月在我院生殖医学中心行自然周期FET 患者的临床资料,旨在观察小卵泡排卵对自然周期FET 的临床结局的影响。
资料与方法
一、研究对象
回顾性分析2011年1月至2013年12月间在我院生殖医学中心因鲜胚移植周期未孕,或因预防卵巢过度刺激综合征(OHSS)而行全胚冷冻,且于取卵后3个月第一次行自然周期FET 的427个周期患者的临床资料。其中135 个小卵泡(14~16 mm)排卵周期,为研究组;292 个周期为正常大小(17~26mm)卵泡排卵,为对照组。
研究组中鲜胚促排卵周期使用标准短效长方案促排卵122周期(90.4%),标准短方案促排卵8周期(5.9%),超长方案促排卵5周期(3.7%);对照组中使用标准短效长方案促排卵285周期(97.6%),标准短方案促排卵7周期(2.4%)。研究组中全胚冷冻63周期(46.7%),对照组中全胚冷冻125周期(42.8%)。全胚冷冻均为卵裂期胚胎冻存。
二、方法
1.排卵监测:按我院生殖中心操作手册标准。平时月经周期正常(25~34d)的患者,均先考虑自然周期排卵监测行FET,月经周期第8~10d开始定期阴道B 超监测卵泡和子宫内膜发育情况。如优势卵泡直径<14 mm 就消失,考虑卵泡闭锁,则取消本周期治疗;只有卵泡直径≥14 mm的卵泡发育排卵,同时子宫内膜≥7 mm 时才考虑FET。
卵泡排卵的标准:LH 峰后阴道B 超监测卵泡消失考虑排卵。排卵当天定义为D0,排卵后第3天行卵裂期胚胎移植。
2.小卵泡排卵的诊断标准:目前国内外尚没有统一标准诊断小卵泡排卵,我院生殖中心参照文献标准[7]以及本中心对小卵泡排卵的理解,把小卵泡定义为:优势卵泡平均径线≤16mm,尿LH 峰日优势卵泡平均直径≤16mm,同时阴道B 超提示有排卵改变。
3.胚胎解冻移植:我中心采用玻璃化方法冷冻胚胎,排卵后第3天按操作手册行胚胎解冻,同时重新对解冻后的胚胎进行评级,Ⅰ级和Ⅱ级胚胎为优质胚胎。胚胎解冻后有50%以上卵裂球存活的胚胎为存活胚胎,排卵后第3 天行卵裂期胚胎移植。所有患者移植胚胎数均≤2枚。
4.黄体支持:自然周期冻胚移植患者,排卵日起予以黄体酮胶囊(浙江爱生药业)200 mg,每日1次,进行黄体支持。
5.妊娠的诊断:胚胎移植后14d测血HCG,阳性者妊娠7周时行阴道超声检查明确妊娠位置和数目,B超观察到孕囊为临床妊娠。
三、统计学方法
采用SPSS 16.0统计软件对数据进行分析,计量资料用均数±标准差表示,计数资料比较采用卡方检验。P<0.05为差异有统计学意义。
结 果
一、基本临床资料
研究组中有6(4.4%)周期14 mm 卵泡排卵,41(30.4%)周期15mm 卵泡排卵,88(65.2%)周期16mm 卵泡排卵。
年龄、不孕年限、不孕原因、不孕类型、体重指数(BMI)、基础激素水平(鲜胚促排卵前)、平均获MⅡ卵数、平均促性腺激素(Gn)用量、平均移植胚胎数、平均移植优胚数及子宫内膜厚度在两组患者之间均无统计学差异(P>0.05)(表1)。
二、治疗结局比较
两组之间种植率、临床流产率、流产率、异位妊娠率及活产率比较均无统计学差异(P >0.05)(表2)。
表1 患者基本临床资料[±s,n(%)]
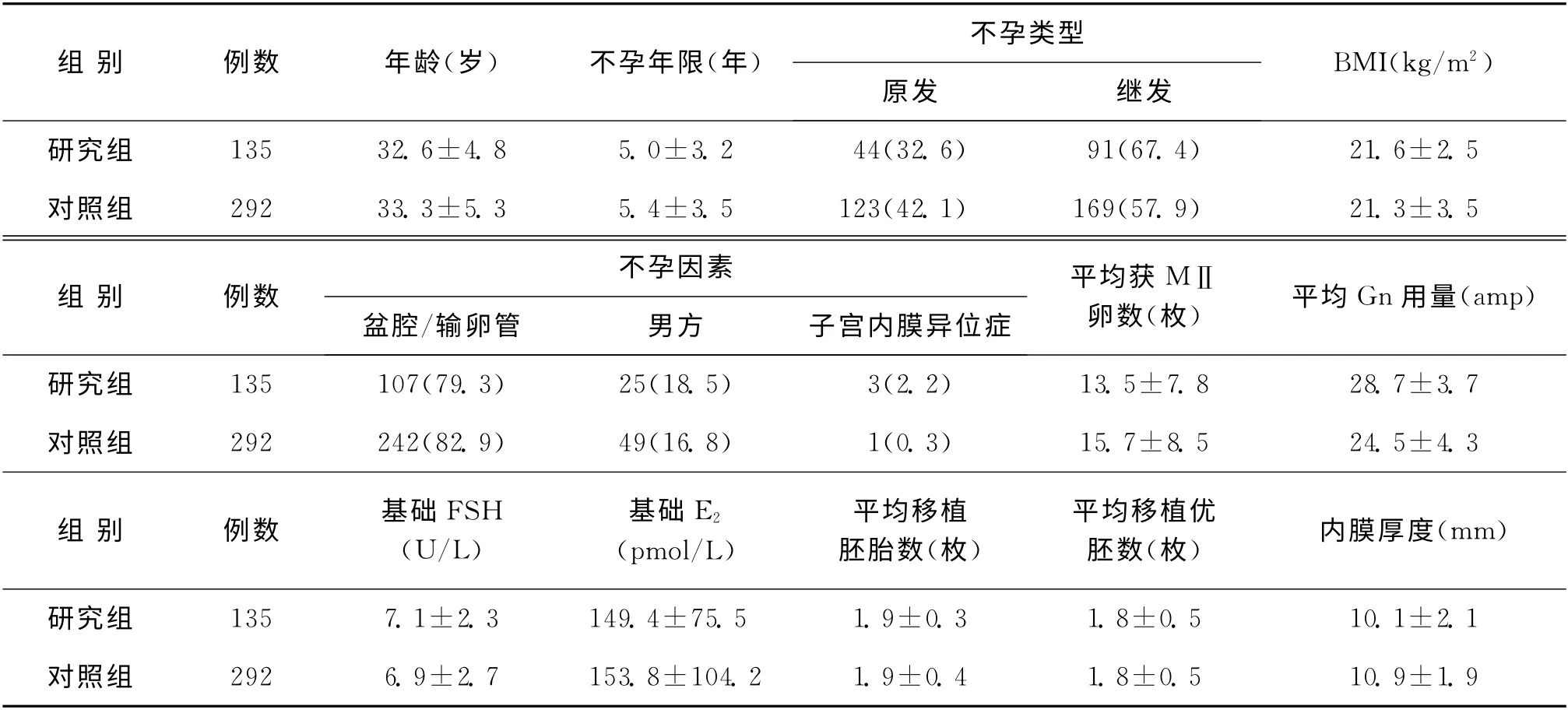
表1 患者基本临床资料[±s,n(%)]
组 别 例数 年龄(岁) 不孕年限(年)不孕类型BMI(kg/m2)原发 继发研究组 135 32.6±4.8 5.0±3.2 44(32.6) 91(67.4)21.6±2.5对照组 292 33.3±5.3 5.4±3.5 123(42.1) 169(57.9) 21.3±3.5组 别 例数不孕因素盆腔/输卵管 男方 子宫内膜异位症平均获MⅡ卵数(枚) 平均Gn用量(amp)研究组 135 107(79.3) 25(18.5) 3(2.2)13.5±7.8 28.7±3.7对照组 292 242(82.9) 49(16.8) 1(0.3) 15.7±8.5 24.5±4.3组别 例数 基础FSH(U/L)基础E2(pmol/L)平均移植胚胎数(枚)平均移植优胚数(枚) 内膜厚度(mm)研究组 135 7.1±2.3 149.4±75.5 1.9±0.3 1.8±0.5 10.1±2.1对照组 292 6.9±2.7 153.8±104.2 1.9±0.4 1.8±0.5 10.9±1.9

表2 两组临床妊娠结局比较(%)
讨 论
本研究结果显示,与正常大小卵泡排卵患者比较,小卵泡排卵后FET 获得了相似的临床妊娠结局。
优势卵泡的选择、发育成熟并排卵的机制非常复杂,受自分泌和旁分泌以及外周血内分泌激素的协同作用。目前国内外对小卵泡排卵的诊断标准尚未统一,我院生殖医学中心依据文献报道[7]及本中心对小卵泡排卵的理解,将小卵泡排卵的平均直径定为≤16mm。文献报道小卵泡排卵在不孕不育患者中发生率高,是导致不孕和流产的一个重要原因[10]。但小卵泡排卵导致不孕和流产的机制尚不清楚,考虑可能存在两方面机制[11]:小卵泡排卵时卵母细胞发育不成熟,受精能力下降从而导致不孕;受精后胚胎继续发育潜力差,同时可能由于激素水平低导致分泌期黄体功能不足而引起流产。与文献报道不相符,本研究小卵泡排卵在继发不孕患者中占67.4%,高于原发不孕患者。分析可能的原因:每个中心对于小卵泡排卵的定义不同,因此研究结果可能出现差异;同时,不孕患者不一定每个月经周期都出现小卵泡排卵。因此需要大样本前瞻性的研究来确定小卵泡排卵的机制、诊断标准及小卵泡排卵对不孕患者妊娠结局的影响。
有文献报道小卵泡排卵患者中黄体功能不全的发生率为53.13%,有57.1%的患者子宫内膜发生分泌延迟,据此推测黄体功能不全是导致小卵泡排卵患者流产的原因[12]。本研究中小卵泡排卵组流产率和活产率与对照组比较并没有升高,与文献报道不符。两组患者在新鲜周期促排卵治疗时的年龄、体重指数、不孕原因、Gn 用量等结果均无统计学差异,促排卵后3个月即进行FET,因此,影响冻胚移植妊娠结局的年龄,体重指数等因素变化不大;两组中移植的优质胚胎数无统计学差异,胚胎的发育潜力具有可比性;胚胎移植后两组都常规进行了黄体支持。是否由于黄体支持改善了小卵泡排卵组的黄体功能,因此获得了与正常大小卵泡排卵组相似的妊娠结局,有待于进一步大样本前瞻性的研究。
小卵泡排卵是否对子宫内膜容受性有影响,目前研究不多。众所周知,成功妊娠的建立主要依赖于优质的胚胎和子宫内膜良好的容受性。子宫内膜容受性的建立机制极其复杂,此过程需要卵巢性激素、子宫内膜局部分子以及胚胎及其分泌的胚胎性因子等参与。卵巢分泌的雌激素和孕激素在子宫内膜容受性形成方面发挥重要作用,排卵前足够的雌激素和排卵后孕激素对内膜的持续影响是子宫内膜容受性建立的必要条件[13]。目前临床上评估子宫内膜容受性的方法主要有阴道B 超评估子宫内膜厚度、体积、形态等参数,认为当子宫内膜厚度在10~14mm 时子宫内膜容受性好,对胚胎种植的接受力强,胚胎着床成功率高。Palatnik等[14]研究发现大卵泡产生的E2浓度高于小卵泡,因此更能刺激子宫内膜的发育。但影响子宫内膜容受性建立的E2浓度到底要多高,目前尚未形成共识。本研究中小卵泡排卵组子宫内膜厚度为10.1±2.1 mm,与对照组相比无统计学差异,同时种植率和临床妊娠率与对照组相比亦相似。分析可能的原因是:虽然是小卵泡排卵,但其产生的雌激素和孕激素浓度足以诱导子宫内膜容受性建立,在移植优质胚胎的情况下,种植率和妊娠率不受影响。本研究在收集资料过程中,发现FET 准备日并不是每一个患者都进行了相关内分泌的检查,有三分之一的患者缺失相关激素资料,因此没有办法评估小卵泡排卵患者移植准备日外周血雌激素和孕激素浓度,这也是本研究中的一个缺陷。
根据本研究结果,在自然周期排卵监测过程中,发现小卵泡排卵后,可择机行FET,并且能获得较满意的临床妊娠结局。本研究的不足之处在于这是一项回顾性的临床资料总结,因此需要前瞻性随机对照研究来验证小卵泡排卵对自然周期FET 临床结局的影响。
[1] Ghobara T,Vandekerckhove P.Cycle regimens for frozenthawed embryo transfer[J/CD].Cochrane Database Syst Rev,2008,23:CD003414.
[2] Mozozov V,Ruman J,kenigsberg D,et al.Natural cycle cryothaw transfer may improve pregnancy outcome[J].J Assist Reprod Genet,2007,24:119-123.
[3] Katharina H,Sabine M,Rolf M,et al.Patients undergoing frozen-thawed embryo transfer have similar live birth rates in spontaneous and artificial cycles[J].J Assist Reprod Genet,2012,29:403-407.
[4] Oehninger S,Mayer J,Muasher S.Impact of different clinical variables on pregnancy outcome following embryo cryopreservation[J].Mol Cell Endocrinol,2000,169:73-77.
[5] Dal Prato L,Borini A,Cattoli M,et al.Endometrial preparation for frozen-thawed embryo transfer with or without pretreatment with gonadotropin-releasing hormone agonist[J].Fetil Steril,2002,77:956-960.
[6] Adams SM,Terry V,Hosie MJ,et al.Endometrial response to IVF hormonal manipulation:comparative analysis of menopausal,down regulated and natural cycles[J].Reprod Biol Endocrinol,2004,2:21.
[7] 陈子江,刘嘉茵 主编.不孕不育专家推荐诊疗方案.妇产科名家讲坛系列[M].北京:人民军医出版社,2013:63.
[8] 刘文杰.B超监测卵泡发育对原因不明不孕的临床意义[J].南华大学学报(医学版),2005,33:382-383.
[9] 王慧芳,吕玉珍,平燕,等.三种方案治疗小卵泡排卵不育的比较[J].生殖医学杂志,2011,20:235-237.
[10] 刘伟.不育症患者小卵泡排卵的临床分析[D].内蒙古医学院,2007.
[11] 谭晓珊,谭兵兵,刁英,等.卵泡发育不良综合征患者的临床特征[J].中国综合临床,2005,21:651-653.
[12] 沈浣,雒雪,戴兆亨,等.小卵泡排卵不孕症患者的临床特征及妊娠结局[J].中国妇产科临床,2001,2:31-33.
[13] 徐慧颖,李娜,张云山 .胚胎植入-子宫内膜容受性是关键[J].生殖医学杂志,2014,23:198-202.
[14] Palatnik A,Strawn E,Szabo A,et al.What is the optimal follicular size before triggering ovulation in intrauterine insemination cycles with clomiphene citrate or letrozole?An analysis of 998 cycles [J].Fetil Steril,2012,97:1089-1094.e1-3.
