邻菲啰啉修饰冠醚的合成及离子识别研究
2015-07-18王咏梅崔金龙陈鑫李会芳段中余
王咏梅,崔金龙,陈鑫,李会芳,段中余
(河北工业大学化工学院,天津 300130)
邻菲啰啉修饰冠醚的合成及离子识别研究
王咏梅,崔金龙,陈鑫,李会芳,段中余
(河北工业大学化工学院,天津 300130)
邻菲啰啉及其衍生物具有优良的光学性能[1],且修饰性较强,可用于抗肿瘤药物、分子识别、DNA探针、自旋交叉配合物等领域[2-4],与超分子化合物结合后,可以设计出多种灵敏度高、响应速度快的荧光传感器[5].因此邻菲啰啉及其衍生物常作为特殊荧光性质传感器的修饰基团,一直以来受到人们的广泛关注.冠醚[6-12]作为第一代超分子化学主体,在超分子化学发展史上占有非常重要的地位.利用冠醚及其衍生物兼具亲脂性和亲水性两种特征,在配位键合离子或中性分子时仍能保持对称与极性的平衡,这使得分子识别[13]成为冠醚研究中重要的组成部分.M ichael Schm ittel等人[14]将一种邻菲啰啉修饰的氮硫杂冠醚与Ir(Ⅲ)配位,发现该配合物可用于检测水溶液中的Ag+,且检测效果优于同配体的Ru(Ⅱ)配合物.本文设计合成了一种邻菲啰啉修饰的苯并-15-冠-5(1),并通过紫外光谱和荧光光谱手段对主体化合物的离子识别性能做了初步的探索和研究.
1 实验部分
1.1 仪器与试剂
Vector-22型傅里叶变换红外光谱仪,ADVANCE400-Bruker型核磁共振仪,UV-1901PC型紫外可见光谱仪,CHI660D型荧光光谱仪.实验所用试剂三缩四乙二醇、3,4-二羟基苯甲醛、邻菲啰啉等均购自上海达瑞精细化学品有限公司,未经处理直接使用.
1.2 合成路线图
菲啰啉修饰的冠醚1的合成路线图如路线1所示.
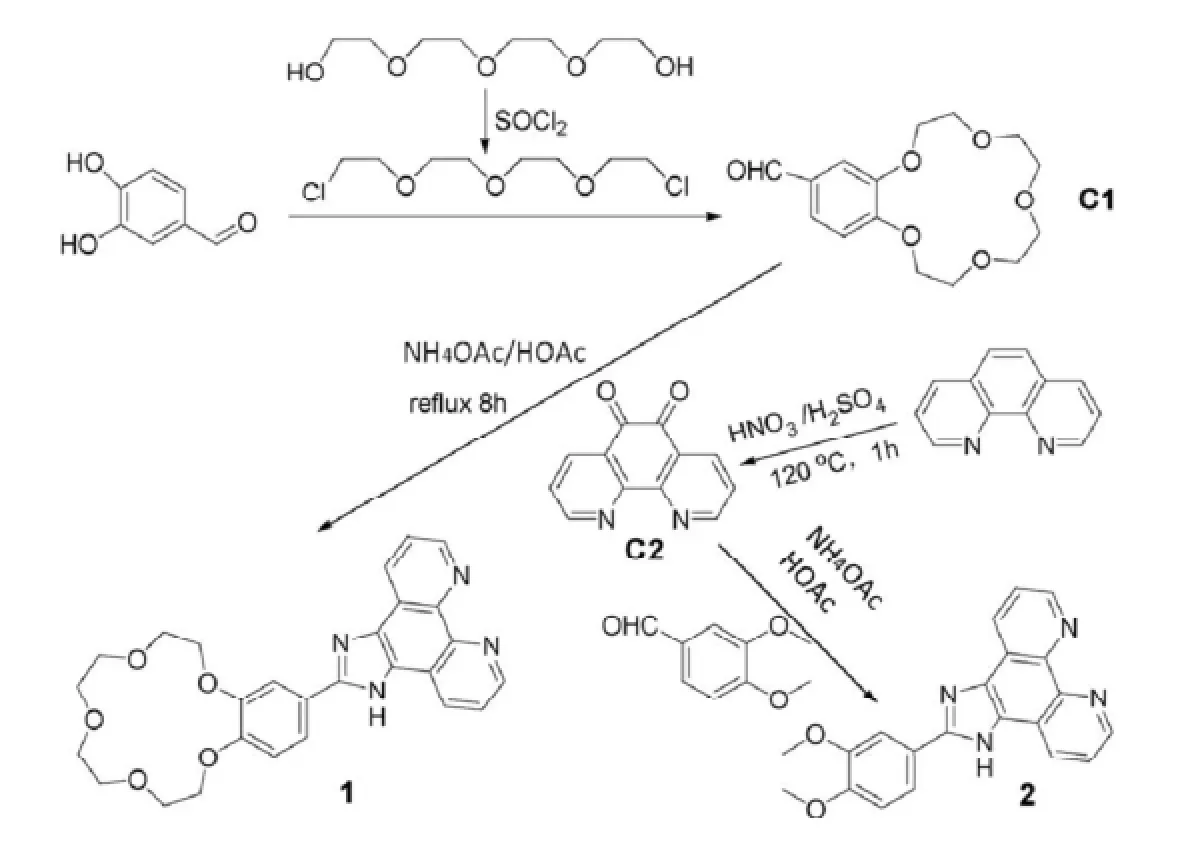
路线1菲啰啉修饰的冠醚1的合成路线图Scheme 1 Synthetic route of crown ether 1
1.3 合成步骤及产品表征
四甘醇二氯代物,4-醛基苯并-15-冠-5(C1),1,10-邻菲啰啉-5,6-二酮(C2),化合物2[18]均按照文献[15~18]方法合成.
化合物1的合成:称取0.19 g(0.89 mmol)1,10-邻菲啰啉-5,6-二酮、0.26 g(0.089 mmol)4-醛基苯并-15-冠-5及1.37 g(0.018 7 mol)醋酸铵溶于15 m L冰醋酸中,将混合溶液置于圆底三口烧瓶中搅拌均匀.在磁力搅拌下加热回流8 h,温度125℃,反应过程中用TLC监测.反应完全后停止加热冷却至室温.加入100 m L水,用浓氨水中和至中性,静置0.5~1 h,有固体析出,抽滤[19].将固体烘干后,用丙酮重结晶,析出黄色固体产物,用正己烷洗涤,干燥得到黄色固体化合物1.产率:17%;m.p.183~185℃.1H NMR(400MHz,CDCl3,in ppm):=3.518~3.654(m,12H),3.698(s,2H),3.880(s,2H),6.537~6.558(d,J=8.4 Hz,1H),7.282~7.334(d,J=20.8 Hz,2H),7.612~7.659(m,2H),8.756~8.825(q,4H).IR(KBr,max,cm1):3 418,2 930,2 872,1 608,1 566,1 523,1 266,1 219,1 128,1 073,938,867,812,742.FAB-MS m/z487.3(MH+),calcd.486.5.
1.4 紫外光谱测试
配制主体化合物1(C=1.0×104mol L1)和客体高氯酸盐(C=1.0×102mol L1)的乙腈溶液,(高氯酸钙配4.0×103mol L1的溶液,溶解度比较小)为以后使用.然后取2.5m L主体化合物1、0.5m L客体于10m L的容量瓶中(客体是主体浓度的20倍),用乙腈稀释至刻度,混合均匀后在超声波中超声,放置过夜,在室温下测其紫外-可见光谱.
紫外光谱滴定:取1m L主体化合物1的乙腈溶液,分别放于11个10m L的容量瓶中,然后分别在每个容量瓶中加入0m L、0.05m L、0.1m L、0.15m L、0.25mL、0.5m L、1m L、1.5m L、2m L、2.5m L的客体溶液,高氯酸钙溶液分别为0 mL、0.125 m L、0.25 m L、0.375 m L、0.5 m L、0.625 m L、1.25 m L、2.5 m L、3.75 mL、5 mL、6.25 m L.用乙腈稀释至刻度,使客体离子浓度分别为主体化合物浓度0、2、4、6、8、10、20、40、60、80、100倍,混合均匀后超声,放置过夜,在室温下测其紫外-可见光谱.
1.5 荧光光谱测试
激发波长为276 nm,response:0.5.溶液配制方法同紫外光谱测试.
2 结果与讨论
2.1 紫外光谱
为了能够直观地比较冠醚主体1和所选金属离子的配位能力和选择性,本文进行了定性实验.在实验中,配制一系列含有相同浓度冠醚1的乙腈溶液,分别加入Li+、Na+、K+、Mg2+、Ca2+5种离子,并保证各离子浓度基本相同,测试这5组溶液以及单一冠醚主体1的紫外光谱曲线,如图1所示.从图中可以看出,在加入Na+、K+离子后,主体1的紫外吸收峰位置变化不明显,吸收强度仅略有下降;而加入Li+,Mg2+,Ca2+后,都发生了较明显的峰形变化,吸收峰位置也发生了不同程度的蓝移,其中尤以Mg2+、Ca2+的蓝移(~6nm)最为明显.
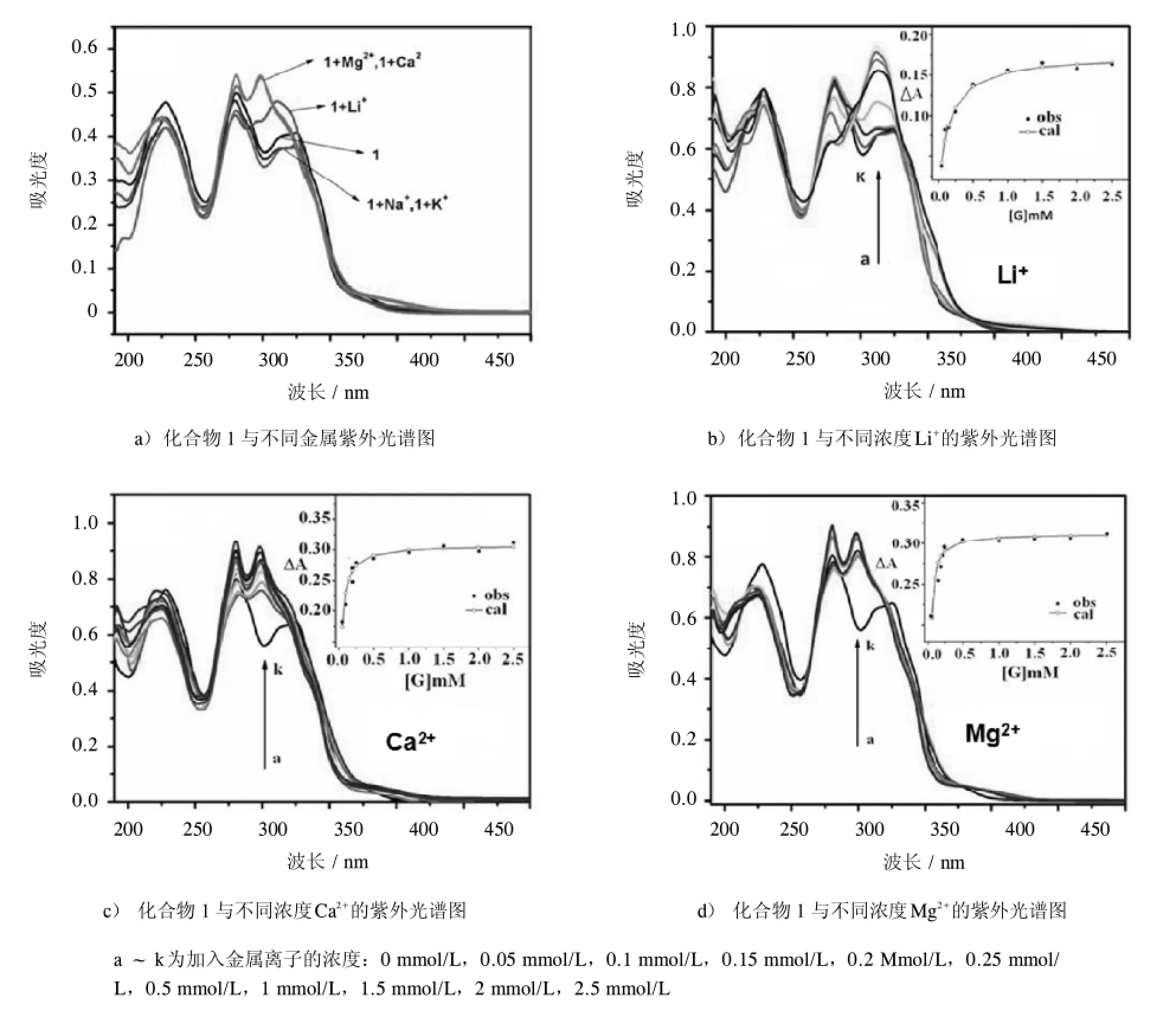
图1 化合物1的紫外光谱图Fig.1 UV-vis spectra of 1
在定性实验的基础上,本研究利用紫外光谱滴定技术定量地测定了主-客体间的配位稳定常数(Ks).图1代表性地给出了主体1在加入Li+,Mg2+,Ca2+前后的紫外光谱变化图.在光谱滴定实验中,随着客体离子浓度的增加,化合物1的324.5 nm处的紫外吸收峰发生位移至311 nm、298.5 nm和298.5 nm,且吸收峰强度逐渐上升.作为控制实验,同等条件下化合物2在加入各种离子后的紫外光谱图几乎没有变化,这充分说明邻菲啰啉处的氮原子与这些金属离子的配位效应是可以忽略不计的.
将测得的吸光度数据根据非线性最小二乘曲线拟合方法,可求得主体1与不同金属离子识别配位的稳定常数Ks,结果列于表1.由主体1与不同离子的曲线拟合图(图1b)、c)、d)的插图)可以看出,实验测定值与理论值吻合较好,说明实验结果准确可靠.采用此方法测得的配位稳定常数(Ks)及相应的自由能变化(G)列入表1中.从表中可以看出,冠醚主体1与Mg2+、Ca2+的键合常数明显高于其与碱金属的键合常数,其对应的log Ks值分别为4.77和4.56,这可能是因为碱土金属的半径比碱金属小,电荷数又多,所以跟主体冠醚环中的氧上的孤对电子作用更强之故.在碱金属离子中,主体1对Li+表现了较Na+、 K+更强的键合能力,其log Ks值为3.86,这也可以由Li+半径更小得以解释.
表1 化合物1与不同金属离子识别配位的稳定常数()Tab.1 Compound 1with variousmetalions recognition ligand stability constant()

表1 化合物1与不同金属离子识别配位的稳定常数()Tab.1 Compound 1with variousmetalions recognition ligand stability constant()
主体离子log Ks G/k J/mol Li+3.86 22.022 Na+3.13 17.849 1 K+2.42 13.818 Ca2+4.56 26.038 Mg2+4.78 27.259
2.2 荧光行为
菲啰啉基团作为优良的荧光基团,它的引入给利用荧光光谱测试冠醚主体与金属离子的包结配位作用提供了可能.本研究也利用荧光光谱考察了主体化合物1对碱金属、碱土金属的荧光识别性能.图2显示了主体化合物1与Li+、Na+、K+、Ca2+、Mg2+在乙腈中配位前后(1与各金属离子的浓度比为1∶20)荧光曲线的变化.从图中可以看出,1的荧光发射峰位于450 nm处,当其与所测的5种离子配位后荧光强度均有不同程度的减弱,其中1与Li+、Ca2+、Mg2+结合后荧光减弱程度较大,且荧光发射峰位置发生红移(分别为22 nm、 31 nm和32 nm);1与Na+、K+配位后发射峰略有蓝移(分别为13 nm和15 nm).

图2 化合物1加入不同离子的荧光光谱图Fig.2 Fluorescence spectra of 1 in CH3CN upon the variousmetal cations
从图3的荧光滴定光谱图可见:加入客体阳离子Li+、Na+、K+、Ca2+、Mg2+都能引起受体分子发射光谱不同程度的变化,Na+、K+的变化较小,而Li+、Ca2+、Mg2+的变化程度大,这与紫外可见光谱的结果一致.随着Li+浓度的增大,化合物1的荧光强度逐渐减弱;Ca2+和Mg2+的荧光滴定光谱变化趋势相似,随着Ca2+、Mg2+的不断加入,化合物1的荧光强度先急速减弱,之后逐渐增强.同样作为控制实验,同等条件下化合物2的荧光发射峰很弱以至于难以检测到,也可以充分说明邻菲啰啉处的氮原子与这些金属离子的配位效应是可以忽略不计的.

图3 化合物1与不同金属离子的荧光滴定光谱图Fig.3 Fluorescence titration spectrum of com pound 1 and differentmetal ions
3 结论
本文将菲啰啉基团引入到冠醚环的边臂上,合成了具有发色团的取代苯并-15-冠-5主体,产物结构经核磁、红外表征.通过紫外光谱、荧光光谱定性和定量地考察了该主体化合物与5种碱金属和碱土金属离子的配位识别性能.结果显示,主体化合物1对于Mg2+、Ca2+的键合能力明显强于Li+、Na+、K+;而在碱金属离子中,主体化合物1则对Li+显示了较强的相互作用.尺寸匹配效应和静电效应仍然是影响配合能力的重要因素.比较这些光物理行为将更能加深对与金属离子配位荧光起源的理解.
[1]Sahai R,Morgan L,Killema D P.Ruthenium(Ⅱ)cluster com plexes:aseries of homooligonuclear comp lexes based on bidentate bridging ligands[J].Inorg Chem,1988,27:3495-3500.
[2]Calabrese JC,Cheng L T,Green JC,etal.Molecular second-order optical nonlinearities ofmetallocenes[J].JAm Chen Soc,1991,113(19):7227-7232.
[3]Zhang X J,Wu JY,ZhangM L,etal.Two strong emitting coordination polymerswith chain and ladder structures[J].TransM etChem,2003,28(6):707-711.
[4]GirardotC,LemercieraG,Mulatiera JC,etal.Novel5-(oligofluoreny l)-1,10-phenenthroline type ligands:synthesis,linear and two-photon absorption properties[J].Tetrahedron Lett,2008,49(10):1753-1758.
[5]杨东瑞,张志军,张衡益,等.基于喹啉和三唑环的开链冠醚对金属离子的选择传感[J].高等化学学报,2011,32(9):2169-2174.
[6]Kim J,M orozum i T,Nakam ura H.Control between TICT and PET using chemicalmodification of N-pheny l-9-anthracenecarboxam ide and its app lication to a crown ether type chemosensor[J].Tetrahedron Lett,2008,64(47):10735-10740.
[7]Dubonosov A D,M inken V I,Bren V A,etal.Tautomeric crown-containing chemosensors foralkali-earthmetal cations[J].Tetrahedron Lett,2008,64(14):3160-3167.
[8]Han M,Zhang H Y,Yang L X,etal.A[2]Catenaneand pretzelanebased on sn-porphyrin and crown Ether[J].Eur JOrg Chem,2011,36:7271-7277.
[9]Rurack K,Reseh-Genger U,Bricks JL,etal.Cation-triggered'sw tching on'of the red/near in fra-red(NIR)fluorescenceof rigid fluorophorespacer-receptor ionophores[J].Chem Commun,2000:2103-2104.
[10]Ruraek K,Kollmannsberger M,Resch-Genger U,et al.A seleetive and sensitive fluoroionophore for HgIIAg,I,and CuIIw ith virtually decoupled fluorophore and receptor units[J].JAm Chem Soc,2000,122:968-969.
[11]秦海娟,杨洗,何永炳,等.基于酰胺的荧光双冠醚阴离子受体的合成和识别性能研究[J].化学学报,2006,64(22):2271-2274.
[12]He H,Mortellaro M A,Leiner M JP,etal.A fluorescent chemosensor for sodium based on photoinduced electron transfer[J].AnalChem,2003,75(3):549-555.
[13]Niu H,Jiang X,He J,etal.A highly selectiveand synthetically facileaqueous-phase cyanide probe[J].Tetrahedron Lett,2008,49(46):6521-6524.
[14]SchmittelM,Lin HW.Luminescent Iridium phenanthroline crown ether complex for the detection of silver(I)ions in aquueous[J].Inorg Chem,2007,46(22):9139-9145.
[15]Jimena R,Félix C G,JoséM G.Synthesis and radical polymerisation ofmethacrylicmonomersw ith crown ethers or their dipodal counterparts in the pendantstructure[J].React Funct Polym,2011,71:948-957.
[16]LindstenG,Wennerstroem O,Thulin B.Stilbene Bis-Crown ethers:synehesis,complexationand photoisomerization[J].Org Chem Biochem,1986,40(7):545-554.
[17]阮宁宁,李亮,陈志敏,等.1,10-邻菲咯啉-5,6-二酮制备反应中副产物的形成与控制[J].化学通报,2012,75(2):155-159.
[18]Zheng Y H,Tan C L,Drummen G PC,etal.Aluminescent lanthanide complex-based anion sensorw ith electron-donatingmethoxy groups for monitoringm ultip le anions in environmentaland biological processes[J].Spectrochim Acta Part A,2012,96:387-394.
[19]Steck E A,D ay A R.Reactionsof phenanthraquinoneand retenequinonew ithaldehydesand ammonium acetate in acetic acid solution[J].JAm Chem Soc,1943,65(3):452-456.
[责任编辑 田丰]
Synthesisand cation recognition research of a novel crown ether modified by phenanthroline
WANG Yong-mei,CUIJin-long,CHEN Xin,LIHui-fang,DUAN Zhong-yu
(Schoolof Chem ical Engineering,Hebei University of Technology,Tianjin 300130,China)
3,4-dihydroxy benzaldehyde,tetraethylene glycoland phenanthrolinewere used as the startingmaterial,a novelbenzo-15-crown-5 derivativemodified by phenanthrolinegroupwassynthesized through chlorination,cyclization, oxidation,condensation and other reactions.Identification and coordination propertiesof the compound 1 to alkali/alkalineearthmetal cations,suchas Li+,Na+,K+,Mg2+,Ca2+,werestudied by UV-Visand fluorescencespectra.The binding constant betw een the com pound and themetal ion was calculated by nonlinear least-squares curve fitting.As a result,the recognition capability of this compound to alkaline earth cations is stronger than that to alkali cations.
crown ether;phenanthroline;UV-Vis spectra;fluorescence spectra;ion recognition
以3,4-二羟基苯甲醛、三缩四乙二醇、邻菲啰啉为起始原料,经氯化、环合、氧化及缩合等一系列反应,设计合成并表征了一种邻菲啰啉修饰的苯并-15-冠-5(1);通过紫外可见光谱和荧光光谱考察了化合物对Li+、Na+、K+、M g2+、Ca2+等碱金属及碱土金属离子的识别与配位能力;运用非线性最小二乘曲线拟合方法计算了化合物与金属离子的键合常数,结果表明,邻菲啰啉修饰的苯并-15-冠-5对碱土金属离子配位识别能力强于碱金属离子.
冠醚;邻菲啰啉;紫外光谱;荧光光谱;离子识别
1007-2373(2015)01-0040-05
O641.4
A
10.14081/j.cnki.hgdxb.2015.01.008
2014-11-24
国家自然科学基金(51473045);河北省自然科学基金(B2014202209);教育部归国留学基金[(2011)1568];大学生创新创业训练计划(201310080031)
王咏梅(1988-),女(汉族),硕士生.通讯作者:段中余(1988-),女(汉族),副教授,Email:zyduan@hebut.edu.cn.
数字出版日期:2015-01-24数字出版网址:http://www.cnki.net/kcms/detail/13.1208.T.20150124.0949.005.htm l
