射频消融治疗器质性心脏病室性心动过速的严重并发症分析与处理
2015-07-11赵李颜张凤祥方震杨兵陈红武居维竹顾凯杨刚郦明芳曹克将陈明龙
赵李颜 张凤祥 方震 杨兵 陈红武 居维竹 顾凯 杨刚 郦明芳曹克将 陈明龙
射频消融术已成为器质性心脏病室性心动过速(室速)治疗的重要手段,可以显著减少因恶性室性心律失常(如持续性室速、心室颤动等)植入心律转复除颤器(implantable cardioverter diffibrillator,ICD)频繁治疗给患者带来的痛苦[1-2]。但器质性心脏病室速消融难度大、风险高,其起源点或折返环的关键峡部不仅可以位于心内膜面,也可位于心外膜面。因此,标测和消融有时仅心内膜就可完成,但大部分患者需要在心外膜进行标测与消融。在这一复杂的标测与消融过程中,难免会损伤邻近结构,如心脏本身、膈神经、腹腔脏器等,从而出现心脏周围脏器神经损伤、腹腔脏器血肿等严重并发症[3]。本文针对江苏省人民医院2009 年8 月至2015 年8 月器质性心脏病室速消融的严重并发症进行总结分析。
1 对象与方法
1.1 研究对象
收集2009 年8 月至2015 年8 月江苏省人民医院射频消融治疗的器质性心脏病室速患者42 例,其中男38 例,女4 例,平均年龄(46.7 ±16.2)岁。42例中扩张型心肌病(dilated cardiomyopathy,DCM)33例,致心律失常性右心室心肌病(arrthythmogenic right ventricular cardiomyopathy,ARVC)5 例,缺血性心肌病(ischemic cardiomyopathy,ICM)4 例;左心室射血分数(left ventricular ejection fraction,LVEF)平均为(53 ±14)%。
1.2 标测与消融
1.2.1 导管放置,电生理检查 手术开始前关闭ICD 治疗功能。术中穿刺左锁骨下静脉及股静脉分别置入右心室导管(4 极)至心尖部及冠状静脉窦(10 极)导管。基础状态下右心室心尖部两个程序刺激,分别为基础(400 ms 或300 ms)加早搏刺激,最多给予3 个室性期前收缩,每次刺激递减10 ms诱发出室速或至200 ms。根据室速的形态特征、血流动力学状况决定标测与消融方式。若不能诱发室速,直接行基质标测与消融。所有患者均先经心内膜标测与消融。
1.2.2 心内、外膜标测与消融 先经剑突下途径穿刺心包,使用专门心包穿刺针在X 线指引下行心包穿刺,进入心包时推注对比剂确认,之后置入导丝,确认导丝进入心包后再置入8 F 鞘。先在CARTO或NavX 指导下进行心内膜标测与消融,若有基质进行改良,而后行心外膜标测与消融。消融前行冠状动脉造影确认其与标测导管之间的距离后,先在起搏标测图形满意的部位消融,而后将晚电位区域行均质化消融。在左心室侧壁消融前,常规以2 ms×10 mA 的输出进行起搏,以避免在膈神经附近放电导致损伤。消融设置为温控模式:40 W,43℃,30 ml/min。消融时用芬太尼镇痛。并通过鞘引流出心包内液体。消融后右心室心尖部程序刺激诱发室速。手术结束时打开ICD 治疗功能。
2 结果
42 例患者共消融50 次,其中28 次为心内膜消融,22 次为心内膜与心外膜联合消融。其中3 例患者术中及术后发生较严重并发症(表1)。
患者1,男,68 岁,因扩张型心肌病,持续性室速,NYHA 心功能Ⅱ级,LVEF 45%,于2013 年7 月在外院植入ICD。术后因室速风暴ICD 频繁治疗,于2014 年7 月16 日在本院行心内、外膜联合标测与消融治疗。心包穿刺成功后,在CARTO3 指导下先行心内膜标测消融,而后心外膜基质标测消融。在右心室心外膜瘢痕消融时出现低血压,X 线透视与心脏超声证实心包积液,从心包引流出不凝血性液体1000 ml,出血未止,遂转外科开胸探查,在右心室游离壁发现破口,修补成功(图1)。患者术后恢复良好,胺碘酮能有效控制室速发生。消融术后继续使用β 阻滞剂、血管紧张素转化酶抑制剂(ACEI)等药物强化治疗。术后经13.3 个月随访,未见ICD治疗。
患者2,男,29 岁,因胸闷晕厥,心电图记录室速,NYHA 心功能Ⅰ级,LVEF 60%,于2010 年9 月在外院植入ICD。术后ICD 频繁治疗,于2011 年5月在本院行心内、外膜联合消融。术中左心室外膜心底部与外侧壁标测出瘢痕,考虑室速发生与此瘢痕有关,行基质改良,临床未能诱发室速。术后次日出现胸闷,X 线透视见膈肌活动度较术前明显减弱,无呼吸困难。1 周后基本恢复,随访1 个月时完全恢复。消融术后继续使用β 阻滞剂、ACEI 等药物强化治疗。术后经52.0 个月随访,未见ICD 治疗。

表1 3 例严重并发症患者情况分析
患者3,女,45 岁,因心脏结节病,持续性室速,NYHA 心功能Ⅰ级,LVEF 60%,于2014 年7 月在本院植入ICD。术后因室速ICD 频繁治疗,于2015 年1 月5 日全麻下行心内、外膜联合标测消融,手术顺利。术后返回病房,患者出现腹痛,查血常规,血红蛋白逐渐下降,CT 示肝血肿(图2)。遂行肝血管造影加靶小动脉栓塞,出血停止,术后待肝血肿液化后穿刺引流。患者恢复良好。消融术后继续使用β阻滞剂、ACEI 等药物强化治疗。术后经5.8 个月随访,未见ICD 治疗。

图1 患者1 心脏压塞影像;
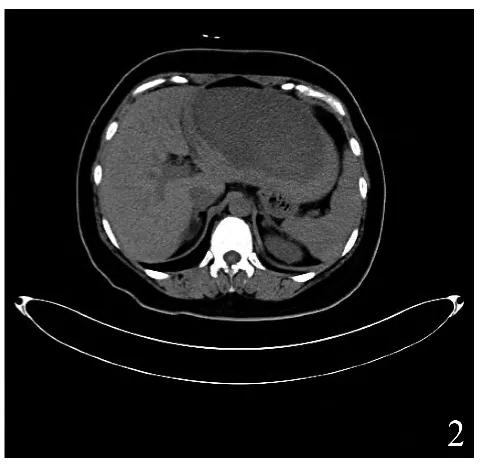
图2 患者3 CT 示肝巨大血肿
3 讨论
随着介入性治疗的广泛开展与推广应用,射频消融术已成为治疗各类快速性心律失常的有效措施,尤其是近年来心外膜消融的开展,射频消融造成的并发症引起了临床医师的关注。心外膜消融主要应用于心肌病室速、心肌梗死后室速、心外膜旁路等治疗[4]。
非ICM 室速多起源于左心室前侧壁近二尖瓣环处,电压标测显示主要低电压区位于左心室侧壁,左侧膈神经大多经此处心外膜走行。因此,心外膜途径消融此处起源的室速时容易出现膈神经损伤(phrenic nerve injury,PNI)[5-7]。其损伤机制主要是消融热量与高强电磁作用所致。消融时间与温度也是影响PNI 程度的因素[8-9]。详细了解膈神经与心脏的解剖关系是预防PNI 的关键。术中应常规膈肌刺激,并采用各种措施尽可能避免在靠近膈神经的部位进行消融,高度警惕并尽快明确诊断和停止放电,可有效减少PNI 的发生。
心脏压塞是心脏介入性治疗最严重的并发症之一,一旦发生应尽早明确诊断,根据心脏压塞程度采取相应处理措施。室性心律失常射频消融术并发心脏压塞的原因主要有术中放置冠状窦电极致静脉破裂、右心室电极或标测与消融电极致右心室穿孔等[1,10]。成人右心室壁厚度一般仅为4 mm 左右,这是容易发生穿孔的一个重要原因。因此,在介入治疗过程中,一旦患者发生胸闷、头晕、血压下降、心率加快等情况均应仔细进行检查,观察有无颈静脉充盈或怒张,密切监测血压与心率的动态改变,并与主动脉夹层、腹膜后血肿及迷走性血管舒张反射等可能的并发症进行鉴别。急诊床旁心脏超声检查、X 线透视观察心影等可帮助诊断。对于确诊为心脏压塞的患者,最有效的治疗方法为急诊心包穿刺及引流,同时给予快速静脉扩容及升血压药物维持重要器官血供。对于内科保守治疗效果不理想的患者,应积极进行心胸外科修补手术[11]。患者1 在右心室流出道心外膜消融,消融参数设置为:功率40 W,温度43℃,灌注流量30 ml/min,消融过程中发生心脏压塞后经心包穿刺引流未见明显好转,开胸探查发现右心室破裂,外科修补成功。
肝血肿也是心包穿刺的严重并发症之一,多见于肝左叶,处理措施包括肝动脉栓塞、穿刺引流,部分患者需要外科手术[4]。患者3 发生肝血肿与肝左叶过大有关,术前常规B 超或CT 检查可有助于避免血肿并发症发生。
综上所述,器质性心脏病室速心外膜消融手术难度大、风险高,手术过程中并发症难以避免,但术前认真复习相关解剖,术中规范操作,可有效减少并发症发生,及时正确处理可有利于并发症转归。
[1]薛玉梅,詹贤章,廖洪涛,等. 经皮心包穿刺术进行室性心律失常心外膜标测和消融的应用体会. 中华心律失常学杂志,2015,19:15-18.
[2]沈才杰,陈晓敏,何斌,等. 心房颤动致心动过速性心肌病及导管射频消融术后左心室射血分数恢复的影响因素分析. 中国介入心脏病学杂志,2013,21:34-40.
[3]邵海军,刘树孝. 心脏手术中的周围神经损伤. 第二军医大学学报,2003,10:1149-1151.
[4]Sarkozy A,Tokuda M,Tedrow UB,et al. Epicardial ablation of ventricular tachycardia in ischemic heart disease. Circ Arrhythm Electrophysiol,2013,6:1115-1122.
[5]Killu AM,Friedman PA, Mulpuru SK, et al. Atypical complications encountered with epicardial electrophysiological procedures. Heart Rhythm,2013,10:1613-1621.
[6]邹彤,杨杰孚.心脏再同步化治疗新指南要点及进展.中国介入心脏病学杂志,2014,22:538-540.
[7]Sosa E,Scanavacca M,d'Avila A,et al. A new technique to perform epicardial mapping in the electrophysiology laboratory. J Cardiovasc Electrophysiol,1996,7:531-536.
[8]Sánchez-Quintana D,Cabrera JA,Climent V,et al. How close are the phrenic nerves to cardiac structures?Implications for cardiac interventionalists. Cardiovasc Electrophysiol,2005,16:309-313.
[9]师睿,姚焰. 心脏导管消融与膈神经损伤. 中华心律失常学杂志,2011,6:470-472.
[10]Peichl P,Wichterle D,Pavlu L,et al. Complications of catheter ablation of ventricular tachycardia:a single-center experience.Circ Arrhythm Electrophysio,2014,7:684-690.
[11]蔡衡,万征,张文娟,等. 心脏介入治疗中急性心脏压塞的原因分析及处理. 中国介入心脏病学杂志,2006,14:54.
