奥马珠单抗治疗慢性特发性荨麻疹荟萃分析
2015-07-07孙康悦陈晓红
孙康悦,李 建,陈晓红
(1.中南大学湘雅医学院2013级在读本科学生,湖南长沙410013;2.中南大学湘雅医学院检验系临床微生物学免疫学教研室,湖南长沙410013;3.第三军医大学药学系药理学教研室,重庆400038)
奥马珠单抗治疗慢性特发性荨麻疹荟萃分析
孙康悦1,李 建2,陈晓红3
(1.中南大学湘雅医学院2013级在读本科学生,湖南长沙410013;2.中南大学湘雅医学院检验系临床微生物学免疫学教研室,湖南长沙410013;3.第三军医大学药学系药理学教研室,重庆400038)
目的系统荟萃分析奥马珠单克隆抗体(单抗)治疗慢性特发性荨麻疹的疗效与安全性。方法采用PubMed数据库、Cochrane图书馆临床对照试验数据库、中国生物医学文献数据库、中国知网全文数据库及万方科技期刊全文数据库等收集文献,研究文献为奥马珠单抗治疗慢性特发性荨麻疹的随机双盲对照试验,观察对象为年龄大于12岁,经抗H1受体拮抗剂治疗未达到满意效果的慢性特发性荨麻疹患者。应用RevMan5.0.24软件对数据进行meta分析,评价奥马珠单抗的疗效及安全性。结果共纳入4项随机双盲对照试验,1 128例患者。各组7 d荨麻疹活动性评分(UAS7)<6分的病例数比较:75 mg奥马珠单抗治疗组优于安慰剂对照组,差异有统计学意义[相对危险度(RR)=1.73,95%可信区间(95%CI):1.10~2.71,P=0.020],300 mg奥马珠单抗治疗组优于75 mg奥马珠单抗治疗组,差异有统计学意义(RR=0.45,95%CI:0.33~0.60,P=0.001);各组治疗后UAS7降低值比较:75 mg奥马珠单抗治疗组优于安慰剂对照组,差异有统计学意义[均方差(MD)=5.03,95%CI:1.72~8.34,P=0.003],300 mg奥马珠单抗治疗组优于75 mg奥马珠单抗治疗组,差异有统计学意义(MD=-7.73,95%CI:-11.15~-4.30,P=0.001);各组1周瘙痒严重程度评分比较:75 mg奥马珠单抗治疗组优于安慰剂对照组,差异有统计学意义(MD=1.75,95%CI:0.55~2.95,P=0.004),300 mg奥马珠单抗治疗组优于75 mg奥马珠单抗治疗组,差异有统计学意义(MD=-3.35,95%CI:-4.97~-1.73,P=0.001)。300 mg奥马珠单抗治疗组总的不良反应和严重不良反应发生情况与安慰剂对照组比较,差异均无统计学意义(RR=1.07、0.39,95%CI:0.97~1.18、0.39~1.38,P=0.200、0.340)。75 mg奥马珠单抗治疗组总的不良反应发生情况与300 mg奥马珠单抗治疗组比较,差异也无统计学意义[RR= 0.91,95%CI:0.78~1.06,P=0.240]。结论慢性特发性荨麻疹患者在常规治疗未奏效时加用奥马珠单抗治疗可改善疗效,且安全性高。
抗体,单克隆/治疗应用;荨麻疹/药物疗法;治疗结果;Meta分析;奥马珠单抗
慢性特发性荨麻疹(chronic idiopathic urticaria,CIU)或慢性自发性荨麻疹(chronic spontaneous urticaria,CSU)是由皮肤、黏膜小血管扩张和通透性增加而导致的一种局限性水肿反应,持续时间超过6周,其病因及病理机制非常复杂,找不到确切病因[1-2]。荨麻疹的治疗首先应积极去除诱发因素,使用非镇静类H1受体拮抗剂阶梯式治疗方案,对使用非镇静类H1抗组胺药标准剂量治疗症状无明显改善的患者可增加剂量至4倍标准剂量或改用其他非镇静类H1抗组胺药;严重者还包括应用白三烯受体拮抗剂(leukotrienereceptorantagonist,LTRA)、奥马珠单克隆抗体(单抗,Omalizumab)和免疫调节剂[3-4]治疗等。
奥马珠单抗是一种抗免疫球蛋白E(immunoglobulin E,IgE)单克隆抗体,可干扰IgE与肥大细胞和嗜酸粒细胞的IgE高亲和力受体(FcεRI受体)结合。该抗体为人源化单克隆抗体,因此,可用于治疗过敏性疾病,抑制肥大细胞和嗜酸粒细胞活化,减少组胺、白三烯、白介素-4等细胞因子和趋化因子的释放,进而减少嗜酸粒细胞、单核细胞等的趋化。奥马珠单抗在治疗难治性哮喘方面已取得了公认的结果[5-6]。目前,奥马珠单抗治疗 CIU已经有较多研究[7-8]。本文拟对相关研究进行meta分析,探讨奥马珠单抗治疗CIU的疗效及安全性。
1 资料与方法
1.1 资料
1.1.1 纳入标准
1.1.1.1 文献类型 纳入奥马珠单抗治疗CIU/CSU患者的随机对照试验,采用双盲法观察奥马珠单抗的疗效和安全性,文献语种为英文和中文。
1.1.1.2 研究对象 CIU/CSU患者年龄大于12岁,经抗H1受体拮抗剂治疗未取得满意疗效者。
1.1.1.3 干预措施 研究组:常规治疗加皮下注射奥马珠单抗;每4周皮下注射一次奥马珠单抗的剂量为75、150、300、600 mg。对照组:常规治疗加皮下注射安慰剂。常规治疗均为第2代非镇静类H1受体拮抗剂。
1.1.1.4 观察指标 (1)7 d荨麻疹活动评分(urticaria activityscore,UAS7),连续7 d记录风团数目和瘙痒程度,满分为42分;(2)1周瘙痒严重程度评分(itch severity score,ISS),连续7 d ISS之和,无瘙痒为0分,轻度瘙痒为1分,中度瘙痒为2分,重度瘙痒为3分,分值为0~21分;(3)1周风团数目评分,连续1周,每天观察2次荨麻疹风团数目,无风团为0分,1~6个为1分,7~12个为2分,>12个为3分,分值为0~21分;(4)总不良反应发生率;(5)严重不良事件发生率。
1.1.2 排除标准 (1)B级以下文献;(2)同一临床研究项目如有多篇报道者只纳入1篇;(3)全文无法获取者。
1.2 方法
1.2.1 文献检索 采用主题词、关键词检索,结合文献追溯及手工检索。中文检索词:奥马珠单抗、荨麻疹、抗IgE。英文检索词:urticaria、anti-immunoglobulin E、omalizumab、anti-IgE antibody。检索PubMed数据库、万方科技期刊全文数据库、Cochrane图书馆临床对照试验数据库、中国知网全文数据库、中国生物医学文献数据库等,文献检索时间从奥马珠单抗用于临床的2000年1月至2015年1月。
1.2.2 资料提取 阅读全文,由2名研究者独立提取资料包括论文题目、作者、论著出版的杂志名称、发表时间、卷、期、页码等。患者和健康对照者年龄、一般情况、给药方法、剂量和时间;荨麻疹急性发作人数、具体的单抗使用剂量、缓解期干预药物使用情况、荨麻疹症状、风团和瘙痒及不良反应等。第3名研究者实时介入仲裁前2名研究者在收集资料时遇到的分歧,并讨论达成统一意见。
1.2.3 文献质量评价 分为A、B、C 3级,按Cochrane荟萃手册分级。
1.3 统计学处理 应用Revman5.0软件进行数据分析。若合并的研究I2<50.0%、P>0.100则认为无异质性,选用固定效应模型进行meta分析,若I2>50.0%、P<0.100则认为有异质性,进一步分析异质性可能原因,并按亚组重新进行合并统计量计算,若仍有异质性,采用随机效应模型计算合并统计量。计量资料当各研究对同一结局指标采用的测量方法及单位完全相同时计算加权均方差(weighted mean difference,WMD)及其95%可信区间(95%confidence interval,95%CI);否则计算标准化均方差(standardized mean difference,SMD)及其95%CI。计数资料计算相对危险度(relativerisk,RR)及其95%CI。若纳入meta分析的研究较多则采用漏斗图分析观察是否存在发表偏倚。
2 结 果
2.1 纳入奥马珠单抗治疗CIU/CSU研究的一般情况及质量评价 对奥马珠单抗治疗CIU的721篇可能符合纳入标准的文献进行筛选,4项随机临床对照试验符合纳入标准,共1 128例患者,失访及退出351例,见表1~3。
2.2 meta分析结果
2.2.1 各组UAS7<6的病例数比较 75 mg奥马珠单抗治疗组与安慰剂对照组无明显异质性(I2=3.0%,P=0.310),采用固定效应模型合并分析,75 mg奥马珠单抗治疗组明显优于安慰剂对照组,差异有统计学意义(RR=1.73,95%CI:1.10~2.71,P=0.020);300 mg奥马珠单抗治疗组与安慰剂组也无明显异质性(I2=0.0%,P=0.730),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组也明显优于安慰剂对照组,差异也有统计学意义(RR= 4.09,95%CI:2.93~5.70,P=0.001),见图1(文献[9]缺乏相关数据,未纳入)。漏斗图左右对称,不存在发表偏倚。75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗治疗组无明显异质性(I2=0.0%,P=0.520),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组明显优于75 mg奥马珠单抗治疗组,差异有统计学意义(RR=0.45,95%CI:0.33~0.60,P=0.001),见图2(文献[10]缺乏相关数据,未纳入)、表4。

表1 纳入研究基本资料
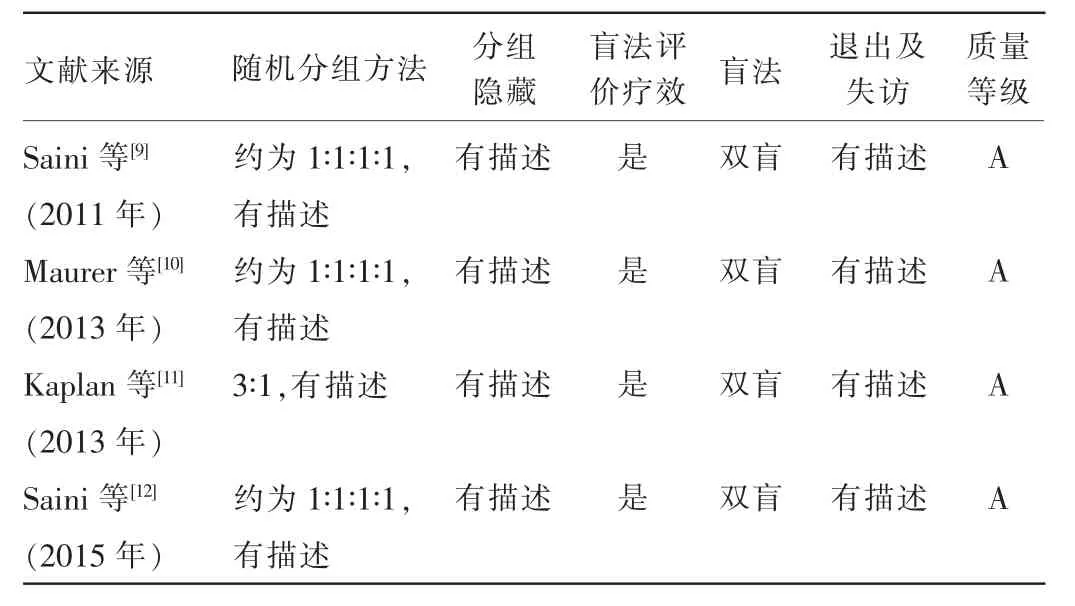
表2 纳入研究方法学质量评价
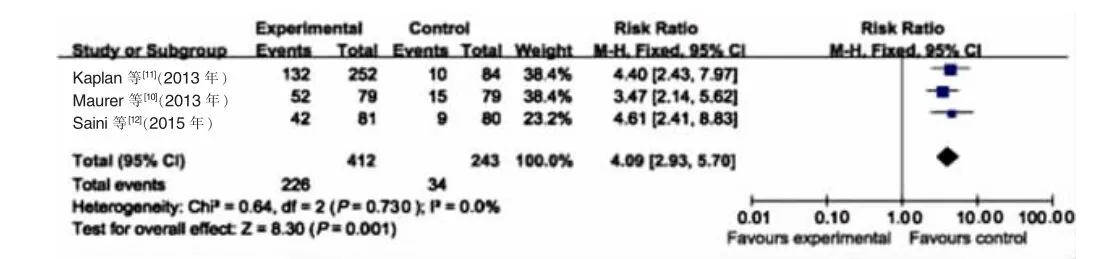
图1 300 mg奥马珠单抗治疗组与安慰剂对照组UAS7<6的病例数比较

图2 75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗组UAS7<6的病例数比较
表3 纳入研究的各项评价指标(±s)

表3 纳入研究的各项评价指标(±s)
注:-表示未测。
文献来源Saini等[9](2011年)干预措施n 年龄(岁)IgE(IU/mL) 基线UAS7(分)基线ISS(分)基线风团数目评分(分)Maurer等[10](2013年)251.5±389.6 170.5±178.5 134.9±142.9 297.4±748.9 168.2±321.9 ---Kaplan等[11](2013年)Saini等[12](2015年)75 mg奥马珠单抗300 mg奥马珠单抗600 mg奥马珠单抗安慰剂75 mg奥马珠单抗150 mg奥马珠单抗300 mg奥马珠单抗安慰剂300 mg奥马珠单抗安慰剂75 mg奥马珠单抗150 mg奥马珠单抗300 mg奥马珠单抗安慰剂23 25 21 21 82 83 79 79 252 84 78 80 81 80 38.8±15.5 42.9±15.7 40.0±11.1 41.2±16.2 39.7±15.0 43.0±13.2 44.3±13.7 43.1±12.5 42.7±17.9 44.3±14.7 40.7±15.2 41.1±14.0 42.4±13.2 40.4±15.6 162.3±306.4 147.2±224.4 ----27.3±8.3 27.3±7.2 26.8±7.0 31.0±7.3 30.7±6.9 31.4±7.0 29.5±6.9 31.0±6.6 31.2±6.6 30.2±6.7 31.7±6.7 30.3±7.3 31.3±5.8 31.1±6.7 13.1±3.5 13.0±3.7 12.6±3.2 14.0±4.2 14.0±3.7 14.2±4.1 13.7±3.5 14.0±3.4 14.0±3.6 13.8±3.6 14.5±3.6 14.1±3.8 14.2±3.3 14.4±3.5 14.2±5.7 14.7±4.6 14.2±4.8 17.0±4.8 16.8±4.2 17.1±4.1 15.8±4.6 17.0±4.2 17.1±4.2 16.4±4.6 17.2±4.2 16.2±4.6 17.1±3.8 16.7±4.4
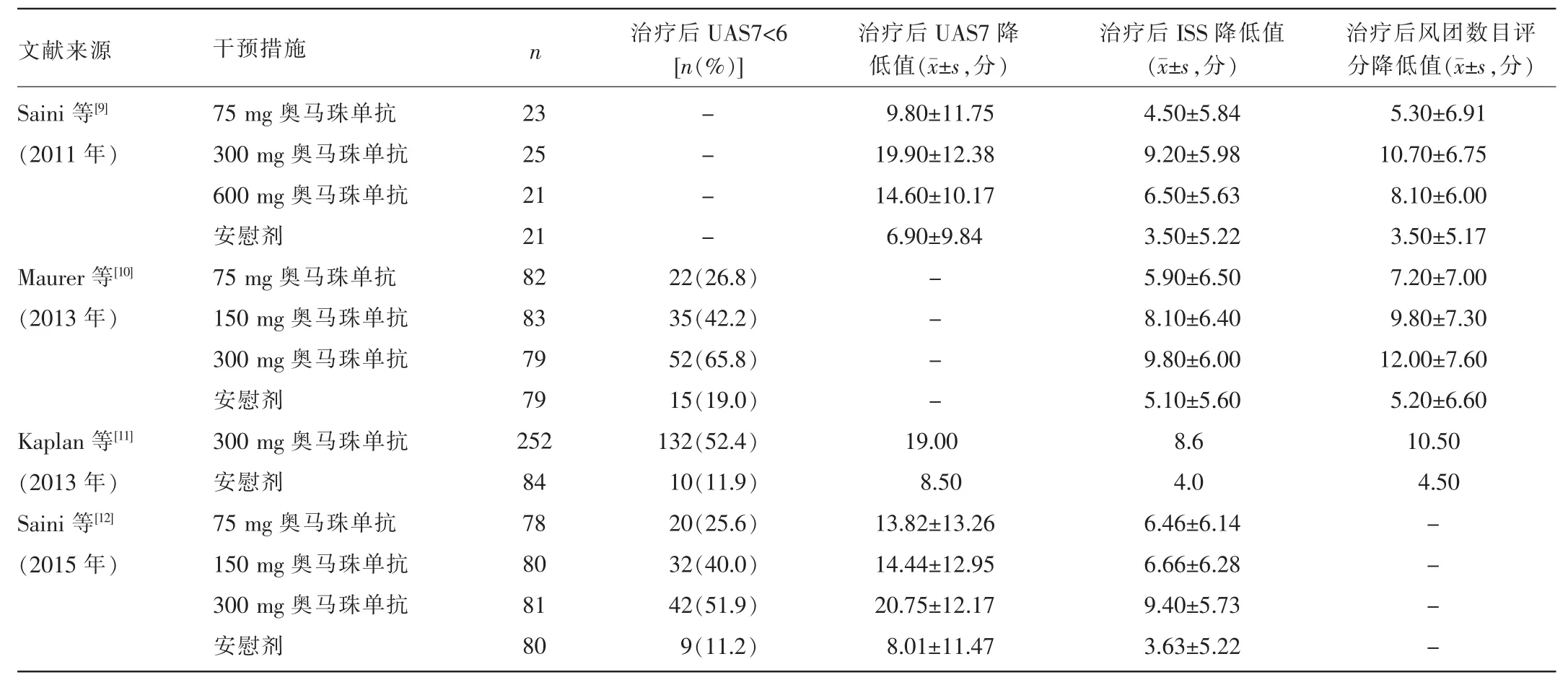
表4 各相关指标meta分析
2.2.2 各组治疗后UAS7降低值比较 纳入的4项研究中有2项研究的75 mg奥马珠单抗治疗组与安慰剂对照组无明显异质性(I2=0.0%,P=0.440),采用固定效应模型合并分析,75 mg奥马珠单抗治疗组较安慰剂对照组能更有效降低UAS7,差异有统计学意义[均方差(mean difference,MD)=5.03,95%CI:1.72~8.34,P=0.003];300 mg奥马珠单抗治疗组与安慰剂对照组也无明显异质性(I2=0.0%,P=0.950),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组较安慰剂治疗组能更有效降低USA7,差异有统计学意义(MD=12.8,95%CI:9.63~15.98,P=0.001),见图3(文献[10]、[11]缺乏相关数据,未纳入)。75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗组也无明显异质性(I2=0.0%,P=0.430),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组较75mg奥马珠单抗治疗组能更有效降低UAS7,差异有统计学意义(MD=-7.73,95%CI:-11.15~-4.30,P=0.001),见图4(文献[10]缺乏相关数据,未纳入)、表4。
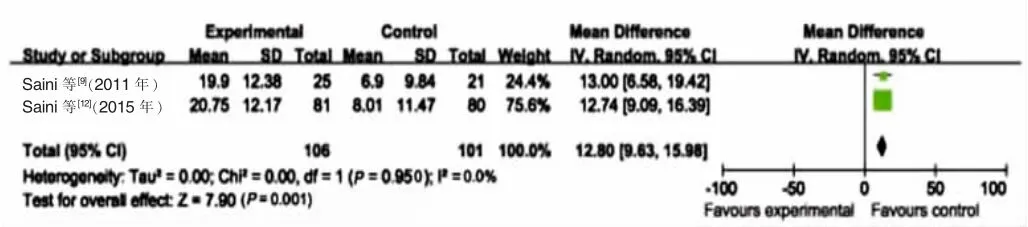
图3 300 mg奥马珠单抗治疗组与安慰剂对照组治疗后UAS7降低值比较

图4 75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗组治疗后UAS7降低值比较
2.2.3 各组ISS比较 75 mg奥马珠单抗治疗组与安慰剂对照组无明显异质性(I2=23.0%,P=0.270),采用固定效应模型合并分析,75 mg奥马珠单抗治疗组优于安慰剂对照组,差异有统计学意义(MD=1.75,95%CI:0.55~2.95,P=0.004);300 mg奥马珠单抗治疗组与安慰剂对照组也无明显异质性(I2=0.0%,P=0.680),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组优于安慰剂对照组,差异也有统计学意义(MD=5.33,95%CI:4.17~6.48,P=0.001),见图5(文献[11]缺乏相关数据,未纳入)。75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗组无明显异质性(I2=0.0%,P=0.370),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组优于75 mg奥马珠单抗治疗组,差异有统计学意义(MD=-3.35,95%CI:-4.97~-1.73,P=0.001),见图 6(文献[10]缺乏相关数据,未纳入)、表4。
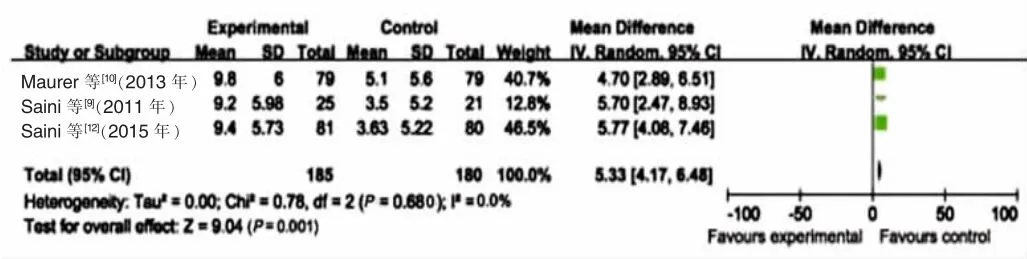
图5 300 mg奥马珠单抗治疗组与安慰剂对照组ISS降低值比较

图6 75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗组ISS降低值比较
2.2.4 各组风团数目评分比较 75 mg奥马珠单抗治疗组与安慰剂对照组无明显异质性(I2=0.0%,P=0.920),采用固定效应模型合并分析,75 mg奥马珠单抗治疗组较安慰剂对照组能更有效地降低患者风团数目,差异有统计学意义(MD=1.95,95%CI:0.14~3.76,P=0.040);300 mg奥马珠单抗治疗组与安慰剂对照组也无明显异质性(I2=0.0%,P=0.850),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组较安慰剂对照组能更有效地降低患者风团数目,差异也有统计学意义(MD=6.92,95%CI:5.05~8.78,P=0.001),见图7(文献[11]、[12]缺乏相关数据,未纳入)。75 mg奥马珠单抗治疗组与300 mg奥马珠单抗治疗组无明显异质性(I2=0.0%,P=0.790),采用固定效应模型合并分析,300 mg奥马珠单抗治疗组较75 mg奥马珠单抗治疗组能更有效地降低患者风团数目,差异有统计学意义(MD=-4.95,95%CI:-6.90~-3.00,P=0.001),见表4。
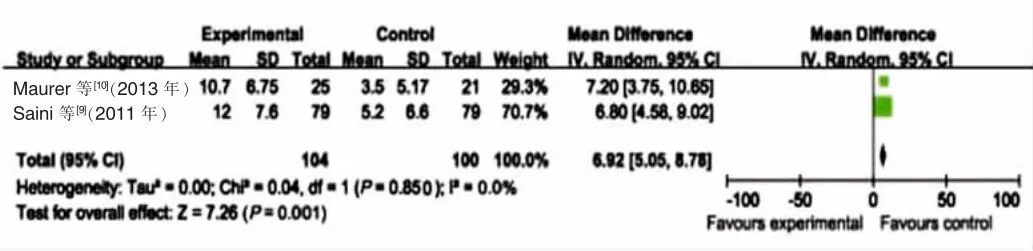
图7 300 mg奥马珠单抗治疗组与安慰剂对照组风团数目评分降低值比较
2.2.5 各组不良反应发生情况比较 纳入的4项研究均报道了各种不良反应发生情况,包括头痛和呼吸道感染等。300 mg奥马珠单抗治疗组总的不良反应和严重不良反应发生情况与安慰剂对照组比较,差异均无统计学意义(RR=1.07、0.39,95%CI:0.97~1.18、0.39~1.38,P=0.200、0.340),见图8。75 mg奥马珠单抗治疗组总的不良反应发生情况与300 mg奥马珠单抗治疗组比较,差异也无统计学意义[RR=0.91,95%CI:0.78~1.06,P=0.240]。
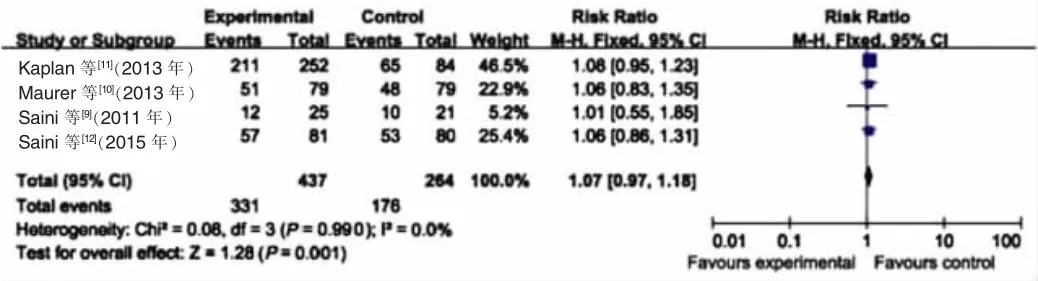
图8 300 mg奥马珠单抗治疗组与安慰剂对照组总不良反应发生情况比较
3 讨 论
CIU严重影响患者生活质量。常规抗组胺疗效欠佳,发病机制复杂。部分荨麻疹患者在使用LTRA或免疫调节剂治疗未能取得满意疗效时可使用奥玛珠单抗。尽管奥玛珠单抗在国内的研究资料很少,但其在治疗哮喘方面的安全性已得到证实[13-14]。参照文献[15-16],作者首次对奥马珠单抗治疗CIU的文献进行了系统性分析评价,共入选1 128例患者,除失访及退出351例外,其余患者均接受了至少1次奥马珠单抗治疗。
本研究采用 4项指标评价奥马珠单抗疗效。(1)UAS7<6的病例数:连续7 d UAS<6,意味着每天UAS<1,即患者可能几乎没有瘙痒或风团,该指标接近于治愈率;(2)治疗后UAS7降低值:反映了荨麻疹患者风团体征和瘙痒症状的总体改善情况;(3)ISS:反映了瘙痒症状的改变;(4)风团数目评分:反映风团体征的改善情况。结果表明,300 mg奥马珠单抗治疗组以上4项指标均明显改善,总体效果优于75 mg奥马珠单抗治疗组,与安慰剂对照组比较,差异均有统计学意义(P<0.05),且300 mg奥马珠单抗治疗组疗效优于75 mg奥马珠单抗治疗组。在使用奥马珠单抗治疗方面从单剂量使用到每月1次连用3~6次,尽管单剂量300 mg奥马珠单抗也确实具有明显疗效。在疗效观察方面,不同作者使用了不同的评价指标,可能会影响相互比较的结果。
总之,300 mg奥马珠单抗在治疗CIU方面具有确切疗效,但其也伴随较多的头痛和上呼吸道感染等不良反应的发生。由于多数观察对象都为德国和美国人群,故今后应观察奥马珠单抗在其他人群中的使用情况,并进一步确定高疗效、低不良反应发生率的恰当剂量的奥马珠单抗治疗CIU的使用疗程。
[1]Kulthanan K,Jiamton S,Thumpimukvatana N,et al.Chronic idiopathic urticaria:prevalence and clinical course[J].J Dermatol,2007,34(5):294-301.
[2]Saini SS.Chronic spontaneous urticaria:etiology and pathogenesis[J].Immunol Allergy Clin North Am,2014,34(1):33-52.
[3]Nam YH,Kim JH,Jin HJ,et al.Effects of omalizumab treatment in patients with refractory chronic urticaria[J].Allergy Asthma Immunol Res,2012,4(6):357-361.
[4]Maurer M,Weller K,Bindslev-Jensen C,et al.Unmet clinical needs in chronicspontaneousurticaria.AGA2LEN task forcereport[J].Allergy,2011,66(3):317-330.
[5]Francés L,Leiva-Salinas M,Silvestre JF.Omalizumab in the treatment of chronic urticaria[J].Actas Dermosifiliogr,2014,105(1):45-52.
[6]Lefévre AC,Deleuran M,Vestergaard C.A long term case series study of the effectofomalizumabon chronic spontaneous urticaria[J].Ann Dermatol,2013,25(2):242-245.
[7]Corren J,Casale TB,Lanier B,et al.Safety and tolerability of omalizumab[J]. Clin Exp Allergy,2009,39(6):788-797.
[8]Kaplan AP,Popov TA.Biologic agents and the therapy of chronic spontaneous urticaria[J].Curr Opin Allergy Clin Immunol,2014,14(4):347-353.
[9]Saini S,Rosen KE,Hsieh HJ,et al.A randomized,placebo-controlled,dose-ranging study of single-dose omalizumab in patients with H1-antihistamine-refractory chronic idiopathic urticaria[J].Allergy Clin Immunol,2011,128(3):567-573.
[10]Maurer M,Rosén K,Hsieh HJ,et al.Omalizumab for the treatment of chronic idiopathic or spontaneous urticaria[J].N Engl J Med,2013,368(10):924-935.
[11]Kaplan A,Ledford D,Ashby M,et al.Omalizumab in patients with symptomatic chronic idiopathic/spontaneous urticaria despite standard combination therapy[J].J Allergy Clin Immunol,2013,132(1):101-109.
[12]Saini SS,Bindslev-Jensen C,Maurer M,et al.Efficacy and safety of omalizumab in patients with chronic idiopathic/spontaneous urticaria who remain symptomatic on H1 antihistamines:A randomized,placebo-controlled study[J].J Invest Dermatol,2015,135(3):925.
[13]Carrillo DC,Borges MS,García E,et al.Omalizumab vs.placebo in the management of chronic idiopathic urticaria:a systematic review[J].World Allergy Organ J,2014,7(1):72.
[14]孙康悦,陈晓红.奥马珠单抗治疗过敏性疾病及其相关进展[J].中国药房,2014,25(22):2083-2085.
[15]Chang TW,Shiung YY.Anti-IgE as a mast cell-stabilizing therapeutic agent[J].J Allergy Clin Immunol,2006,117(6):1203-1212.
[16]Fahy JV,Fleming HE,Wong HH,et al.The effect of an anti-IgE monoclonal antibody on the early-and late-phase responses to allergen inhalation in asthmatic subjects[J].Am J Respir Crit Care Med,1997,155(6):1828-1834.
Meta analysis on omalizumab for treating c hronic idiopathic urticaria
Sun Kangyue1,Li Jian2,Chen Xiaohong3
(1.The Undergraduates of Grade 2013,Xiangya Medical College,Central South University of China,Changsha,Hunan 410013,China;2.Teaching and Researching Section of Clinical Microbiology and Immunology,Xiangya Medical College,Central South University of China,Changsha,Hunan 410013,China;3.Teaching and Researching Section of Pharmacology,Department of Pharmacy,Third Military Medical University,Chongqing 400038,China)
ObjectiveTo perform the systematical meta analysis on the efficacy and safety of omalizumab for treating chronic idiopathic urticaria(CIU).MethodsThe double blind randomized controlled trials(RCT)on omalizumab for treating CIU were retrieved from the Cochrane Central Register of Controlled Trials,PubMed,CBM,CNKI and Wanfang database.The observation subjects were the CIU patients aged over 12 years old without satisfactory effect to the H1 receptor antagonist therapy. The obtained data were performed the meta analysis by using the RevMan 5.0 software.The curative effect and safety of omalizumab were evaluated.Results4 double blind RCT were included involving 1 128 patients.In the comparison of urticaria activity score on 7 d(UAS7)<6 points among various groups,the omalizumab 75 mg group was superior to the placebo group and the control group[RR=1.73,95%CI(1.10~2.71),P=0.020]and the omalizumab 300 mg group was superior to the omalizumab 75 mg group,the differences were statistically significant[RR=0.45,95%CI(0.33~0.60),P=0.001];in the comparison of UAS7 decreased values after treatment among various groups,the omalizumab 75 mg group was superior to the placebo group and the control group[MD= 5.03,95%CI(1.72~8.34),P=0.003]and the omalizumab 300 mg group was superior to the omalizumab 75 mg group,the differences were statistically significant[MD=-7.73,95%CI(-11.15~-4.30),P<0.001];in the comparison of 1-week itching degrees among various groups,the omalizumab 75 mg group was superior to the placebo group and the control group[MD=1.75,95%CI(0.55~2.95),P=0.004]the omalizumab 300 mg group was superior to the omalizumab 75 mg group,the differences were statistically significant [MD=-3.35,95%CI(-4.97~-1.73),P<0.00].The total adverse reactions and severe adverse reactions had no statistical difference between the omalizumab 300 mg group with the placebo group and the control group(RR=1.07,0.39,95%CI:0.97~1.18,0.39~1.38,P=0.200,0.340).Furthermore,the occurrence situation of the total adverse reactions also had no statistical difference between the omalizumab 75 mg group and omalizumab 300 mg group[RR=0.91,95%CI(0.78~1.06),P=0.240].ResultsAdding omalizumab in CIU patients without effect to the conventional therapy can improve the curative effect with high safety.
Antibodies,monoclonal/therapeutic use;Urticaria/drug therapy;Treatment outcome;Meta-analysis;Omalizumab
10.3969/j.issn.1009-5519.2015.17.004
A
1009-5519(2015)17-2578-05
2015-04-21)
孙康悦(1995-),女,重庆沙坪坝人,主要从事分子生物学与疾病的研究;E-mail:xymedisky@csu.edu.cn。
李建(Email:990297364@qq.com);陈晓红(Email:pharma3061@163.com)。
