铁氰化锰修饰过氧化聚吡咯电极的制备及其电催化性质
2015-06-07乔金丽
金 君,于 浩,乔金丽
(延安大学 化学与化工学院,陕西 延安 716000)
铁氰化锰修饰过氧化聚吡咯电极的制备及其电催化性质
金 君,于 浩*,乔金丽
(延安大学 化学与化工学院,陕西 延安 716000)
采用循环伏安法制备了铁氰化锰-过氧化聚吡咯(MnHCF/PPyox/CCE)修饰电极,研究了MnHCF/PPyox/CCE电极对肼的电催化行为。结果表明,MnHCF在PPyox/CCE电极和裸电极上的沉积过程不同,且该修饰电极对肼有良好的电催化活性,响应时间短(t<2 s)。在优化条件下,安培法检测肼的线性范围为2.0×10-7~2.3×10-3mol·L-1(R=0.9993),检出限(3 Sb)为8.0× 10-8mol·L-1,该法已用于模拟水样中肼的测定。
铁氰化锰;过氧化聚吡咯;肼;电催化氧化
肼在工业上被广泛的用作催化剂、防腐剂、乳化剂[1]等。但对皮肤和黏膜有强烈的腐蚀性,在药理学上被认为是导致癌症和肝病的物质[2],因此建立简单快速、准确的检测肼的方法是十分必要的。
金属铁氰化物是一类重要的微溶混合价态金属化合物。作为电子递质,其具有良好的电化学可逆性和高度的稳定性,且铁氰化物修饰电极易于制备、重现性好、具有良好的电化学活性、催化性、离子选择性等特点,已成为电分析化学领域一个十分活跃的研究方向[3-7]。单一过渡金属铁氰化物如PB[8]、CuHCF[9]、NiHCF[10]等化学修饰电极的制备及应用已有不少报道。然而关于铁氰化锰修饰电极的报道较少[11,12]。
本文以复合陶瓷碳电极为基础电极,采用在线电化学方法制备了性能稳定的MnHCF/PPyox/CCE修饰电极,研究了该修饰电极对肼的电催化活性。结果表明,该修饰电极具有很好的稳定性。
1 实验部分
1.1 仪器和试剂
LK98B-Ⅱ型电化学工作站(天津市兰力科化学电子高技术有限公司)。实验采用三电极系统,以修饰电极为工作电极,铂电极为辅助电极,饱和甘汞电极(SCE)为参比电极。文中所用的电位值均是相对于SCE的电位。
石墨粉(光谱纯,国药集团化学试剂有限公司),吡咯(Py,AR,国药集团化学试剂有限公司,用前进行减压蒸馏),硫酸锰(AR,西安化学试剂有限公司),硫酸肼(AR,天津市科密欧化学试剂有限公司),其余试剂为分析纯,实验用水为去离子水。
1.2 电极的制备
1.2.1 基础电极(CCE)的制备
采用复合陶瓷碳电极(CCE)为基础电极,其制备方法参考Lev等人的工作[13]。
1.2.2 过氧化聚吡咯电极(PPyox/CCE)的制备
将处理好的CCE电极置于含0.10 mol·L-1Py和0.10 mol·L-1KCl溶液中,采用单电位阶跃计时电流法控制工作电位0.80 V,电沉积10 s。取出电极,用去离子水充分冲洗,再将其置于0.20 mol·L-1NaOH溶液中,采用单电位阶跃计时电流法控制工作电位1.0 V,过氧化处理30 min。即为PPyox/CCE。
1.2.3 MnHCF/PPyox/CCE电极的制备
MnHCF/PPyox/CCE电极的制备参考刘有芹等人的工作[14]:将处理好的PPyox/CCE电极置于1.0 ×10-3mol·L-1Mn2++1.0×10-3mol·L-1K3Fe (CN)6+0.05 mol·L-1PBS(Na)+0.30mol·L-1NaCl(pH7.0)的混合溶液中,以100 mV·s-1的扫速在1.1~-0.2V范围内扫描一定圈数。记为Mn-HCF/PPyox/CCE。
2 结果与讨论
2.1 MnHCF/PPyox/CCE修饰电极的制备
实验研究了铁氰化锰在PPyox/CCE电极表面上的沉积过程。根据Mn2+/3+电对的氧化还原峰电流(/)的变化,整个沉积过程分为三个阶段(图 1)。第一阶段(图1A),Mn2+/3+电对的氧化还原峰电流随扫描的进行逐渐减小,氧化峰电位负移,直至峰电流与峰电位达不再变化。第二阶段(图1B),在该阶段,氧化还原峰电流停止增长。第三阶段,峰电流随扫描的进行稳定增长(图1C),表明铁氰化锰膜逐渐沉积于PPyox/CCE电极表面[14]。
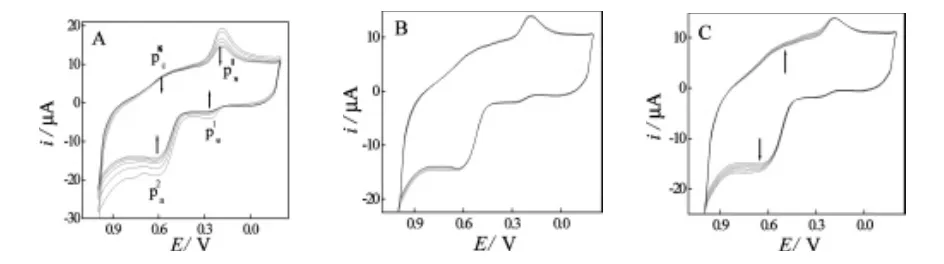
图1 铁氰化锰膜在PPyox/CCE电极表面生长过程的循环伏安图
2.2 膜厚度的影响
实验中,电化学沉积过程必须进行到第三个阶段并持续适当的时间才能获得均匀、致密的膜修饰电极。因此通过改变沉积圈数来控制膜的厚度。实验中研究了沉积圈数在50~170之间变化时的修饰电极的性能。当沉积圈数为80圈时,能形成均匀、致密的薄膜,并且对肼有较大的催化活性。因此选择沉积圈数为80圈。
3 修饰电极的电化学性能
3.1 MnHCF/PPyox/CCE的电催化氧化
采用循环伏安法研究了MnHCF/PPyox/CCE对N2H4的电催化氧化行为(图2A)。
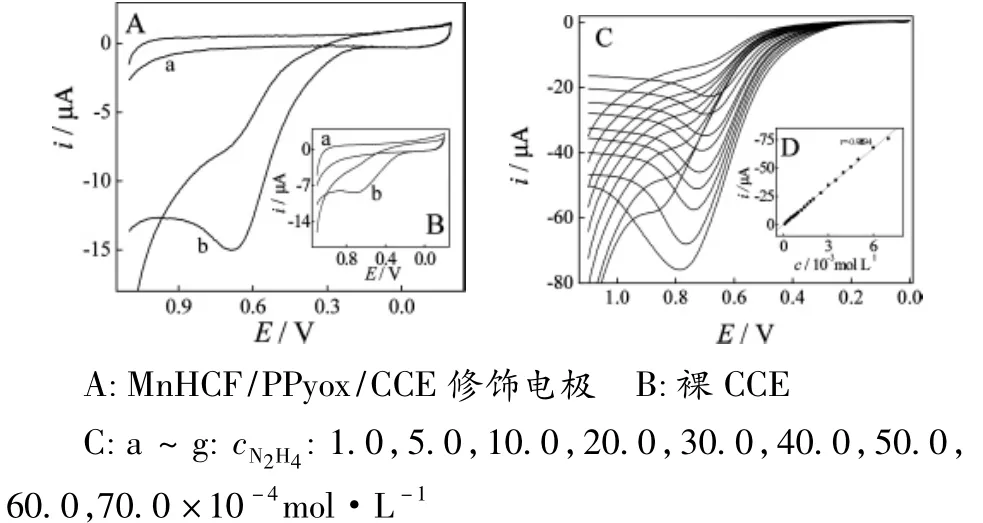
图2 N2H4在裸CCE与MnHCF/PPyox/CCE电极上的循环伏安响应
图2A中曲线a为MnHCF/PPyox/CCE电极在空白底液中的循环伏安图,b为加入1.4×10-3mol ·L-1N2H4后的循环伏安图。由图可见,当加入N2H4后,氧化峰电流迅速增大,而在裸CCE电极上,氧化峰电流较小(图2B-a,b),电流响应的增大表明MnHCF/PPyox/CCE修饰电极对N2H4具有较强的电催化氧化能力。向空白溶液中连续加入一定浓度的N2H4,随着N2H4的加入,氧化峰电流逐渐增加(图2C),其值与cN2H4在1.0×10-4~7.0×10-3mol·L-1范围内具有良好的线性关系,相关系数为0.9994(图2D)。
3.2 扫速的影响
采用循环伏安法考察了扫描速度的影响(图3)。结果表明:当扫描速率较低(10~100mV·s-1),峰电流与扫速的二分之一次方成线性关系,阳极峰电位也随之向正的方向移动,表明该电极反应是一扩散控制的过程。
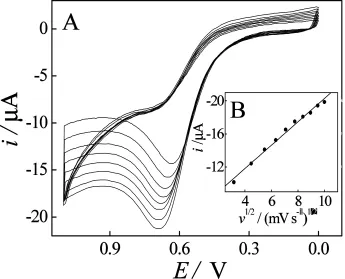
图3 加入N2H4后阳极峰电流与扫速的关系(A):ipa~v1/2;cN2H4:2mmol·L-1;scan rate:10~100mV·s-1
4 安培法检测N2H4
4.1 工作电位的选择
由伏安法结果可知,修饰电极对N2H4具有良好的催化活性,为了提高测定的灵敏度,对工作电位进行了选择。图4曲线a和b分别为5.0×10-4mol ·L-1N2H4在裸CCE电极和MnHCF/PPyox/CCE电极上的流体动力学伏安图。由图可知,当工作电位为0.68 V时修饰电极对N2H4电流响应达到最大,因此在安培检测中选择0.68 V为工作电位。
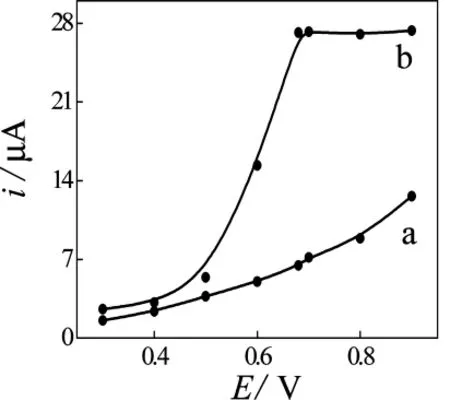
图4 N2H4在裸CCE(a)和MnHCF/PPyox/CCE(b)电极上的流体动力学伏安图
4.2 安培法检测N2H4
控制工作电位为0.68 V,向不断搅拌的0.050 mol·L-1PBS和0.10 mol·L-1NaCl溶液中连续加入不同浓度的N2H4并记录i~t曲线(图5)。由图可见,随着N2H4的加入,电流以台阶状逐渐增加,符合稳态电流的特征。电流值与cN2H4在2.0×10-7~2.3×10-3mol·L-1(r=0.9993)之间具有良好的线性关系,检出限为(3sb)8.0×10-8mol·L-1,响应时间小于2 s。
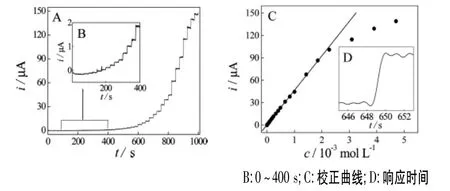
图5 动态安培响应
4.3 干扰实验
实验中研究了不同离子对测定的干扰,对于1.0×10-4mol·L-1N2H4溶液,当测定相对误差不大于±5%时,10倍Fe3+,Cu2+,Ni2+对测定均有干扰,10倍均不产生干扰。
4.4 样品分析
取已知的适量的肼加入到含支持电解质0.050 mol·L-1PBS+0.10 mol·L-1NaCl的模拟水样中,在选定的实验条件下,按照实验方法进行加标回收实验,分析结果见表1。
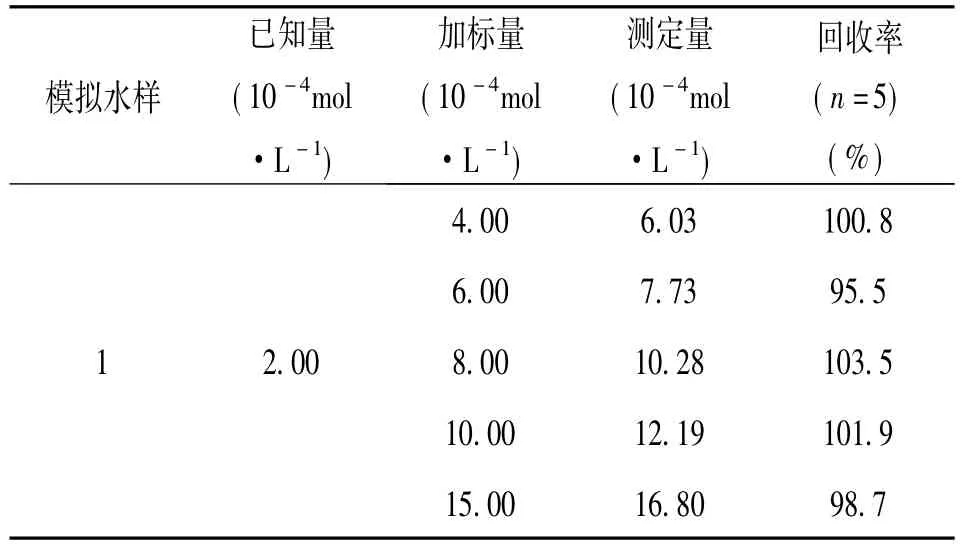
表1 Results of recovery test
4.5 修饰电极的稳定性及重复性
在优化实验条件下,用MnHCF/PPyox/CCE修饰电极对1.0×10-4mol·L-1N2H4溶液连续进行10次平行测定,RSD为4.2%。电极于室温下放置1个月后再次进行测试,其对N2H4的响应电流几乎不变,表明该修饰电极具有良好的稳定性和重现性。
5 小结
采用循环伏安法制备了铁氰化锰-过氧化聚吡咯(MnHCF/PPyox/CCE)修饰电极,研究了MnHCF/ PPyox/CCE电极对肼的电催化行为。结果表明,MnHCF在PPyox/CCE电极和裸电极上的沉积过程并不同,且该修饰电极对肼的响应时间短(t<2 s)。
[1]张晓媛,雷和稳.微量肼含量的测定[J〛.河北化工,2007,30(8):77-78.
[2]王晓燕,张云.铁氰酸镍碳纳米管修饰电极对肼的电催化氧化[J〛.四川有色金属,2009,2:43-46.
[3]刘海燕,王艳玲,张国荣.铁氰化镍/银复合无机膜修饰电极对肼的催化氧化作用[J〛.分析科学学报,2003,19 (4):330-332.
[4]Yamada M,Sato T,Miyake M,et al.Temporal evolution of composition and crystal structure of cobalt hexacyanoferrate nano-polymers synthesized in reversed micelles.J.Col. Inter.Sci[J〛.2007,315:369-375.
[5]Karyakin A A,Karyakina E E,Gorton L.On themechanism of H2O2reduction at prussian bluemodified electrodes[J〛.E lectrochem Commun,1999,1(2):78-82.
[6]Wu X Q,Guo X M,Wang R,et al.Cholesterol biosensor based on platinium electrodemidified by prussian blue[J〛. Anal Chem,2001,29(11):1273-1275.
[7]刘赵荣,王玉春,弓巧娟,等.电化学掺铜(Ⅱ)类普鲁士蓝膜修饰电极的制备及其对亚硝酸根的测定[J〛.分析化学研究简报,2010,38(7):1040-1043.
[8]Zhang Y,Luo H Q,Li N B.Hydrogen peroxide sensor based on Prussian blue electrodeposited on(3-mercaptopropyl)-trimethoxysilane polymer“modified”gole electrode[J〛. Bioprocess Biosyst Eng,2011,34:215-221.
[9]Ojani R,Raoof J B,Norouzi B.Cu(Ⅱ)hexacyanoferrate (Ⅲ)modified carbon paste electrode:application for electrocatalytic detection of nitrite[J〛.Electroanalysis,2008,20 (18):1996-2002.
[10]Prabakar S.JR,Narayanan SS.Catalytic oxidation of dopamine ata nickelhexacyanoferrate surfacemidified graphite wax composite electrode coated with nafion[J〛.Electroanalysis,2009,21(13):1481-1489.
[11]Jayasri D,Sriman Narayanan S.Amperometric determination of hydrazine atmanganese hexacyanoferrate modified graphite-wax composite electrode[J].Journal of Hazardous Materials,144(2007):348-354.
[12]Jayasri D,Sriman S,Narayanan,et al.Manganese(Ⅱ) hexacyanoferrate based renewable amperometric sensor for the determination of butylated hydroxyanisole in food products[J].Journal of Hazardous Materials,101(2007):607~614.
[13]Tsionsky M,Gun J,Glezer V,et al.Sol-gel-derived ceramic-carbon composite electrodes:introduction and scope of applications[J].Anal.Chem,1994,66(10):1747-1753.
[14]刘有芹,金松子,刘六战,等.铁氰化锰修饰玻碳电极的制备及其电化学行为[J].分析化学研究简报,2004,32 (7):847-851.
[15]Bacskai H,Martinusz K,Czirok E,et al.Polynuclear nickel hexacynoferrates:monitoring of film growth and hydrates counter-cation flux/storage during redox reactions[J〛. Journal of Electroanalytical chemistry,1995,385(2):241-248.
[16]Itaya K,Uchida I,Toshima S.Mediated electron transfer reactions between redox centers in Prussian blue and reactants in solution[J〛.J.Phys.Chem.,1983,87(1):105-112.
[责任编辑 李晓霞]
Preparation of M anganese Hexacy anoferrate M odified Ceram ic Carbon Composite Electrode of Peroxide Polypyrrole and Its Electrocatalytic Property
JIN JUN,YU HAO*,QIAO Jin-li
(College of Chemistry and Chemical Engineering,Yan'an University,Yan'an 716000,China)
A manganese hexacyanoferrate(MnHCF)film modified ceramic carbon composite electrode of peroxide polypyrrole was fabricated by using cyclic voltammetry.The paper investigated the electrochemical behavior of hydrazine in MnHCF/PPyox/CCE electrode and determinatedmicroscale hydrazine by using the single electron-current chronopotentiometricmethod in MnHCF/PPyox/CCE electrode.The experimental results showed that the resulting electrode exhibited high sensitivity towards the reduction of hydrazine.Under the optimal conditions,the oxidation peak current showed a linear relationship with the concentration of hydrazine in the range from 2.0×10-7to 2. 0×10-3mol/L with a correlation coefficient of 0.9997 and a detection limit(3 Sb)of 8.0×10-8mol/L.This method had been applied to the determination of hydrazine in stimulantwater samples.
manganese hexacyanoferrate;peroxide polypyrrole;hydrazine;electrocatalytic oxidation
O657.1
A
1004-602X(2015)03-0042-04
10.13876/J.cnki.ydnse.2015.03.042
2015 -04 -17
陕西省自然科学基金项目(2010JQ2005)
金 君(1987—),女,河南周口人,延安大学助理实验师。 *为通讯作者
