坦度螺酮治疗功能性消化不良合并焦虑的临床观察
2015-06-01庞敏朱丽明方秀才王智凤柯美云
庞敏,朱丽明,方秀才,王智凤,柯美云
1中国医学科学院北京协和医学院北京协和医院消化内科,北京1007302北京市平谷区医院消化内科,北京101200
坦度螺酮治疗功能性消化不良合并焦虑的临床观察
庞敏1,2,朱丽明1,方秀才1,王智凤1,柯美云1
1中国医学科学院北京协和医学院北京协和医院消化内科,北京1007302北京市平谷区医院消化内科,北京101200
目的观察坦度螺酮治疗功能性消化不良 (functional dyspepsia,FD)合并焦虑状态患者的疗效和安全性。方法2012年3月至2013年12月北京协和医院消化内科门诊就诊的31例FD合并焦虑状态患者,既往常规治疗无效,口服坦度螺酮10 mg/次,3次/d,治疗4周,比较治疗前、治疗2周及治疗4周时FD症状积分;比较治疗前和治疗4周时Zung焦虑、抑郁自评量表 (Zung anxiety and depression self-rating scales,SAS、SDS)评分,汉密尔顿焦虑、抑郁量表(Hamilton anxiety and depression scales,HAMA、HAMD)评分,生活质量 (SF-36)评分,液体营养餐负荷试验的变化,分析评价疗效,同时观察记录不良反应。结果治疗前、治疗2周、4周时总体症状积分分别为10.45±5.66、8.48± 5.96、7.39±5.46,治疗2周、4周时均较治疗前明显下降 (P=0.002,0.020);餐后饱胀不适和早饱两个单项症状积分在治疗2周、4周时较治疗前明显下降,差异有统计学意义 (P均<0.05)。SAS、HAMA及HAMD评分治疗4周较治疗前下降 (P=0.028,0.002,0.000)。生活质量 (SF-36)评分中生理功能、躯体疼痛、总体健康状况分数在治疗4周时有改善 (P=0.033,0.022,0.041)。液体营养餐负荷试验阈值饮入量和饱足饮入量治疗前后差异无统计学意义 (P=0.285,0.532)。治疗期间有5例 (16.1%)患者出现皮疹、瘙痒等不良反应,其中1例因不良反应停药。结论坦度螺酮治疗功能性消化不良合并焦虑患者安全有效,可以作为常规治疗无效时的一个选择。
坦度螺酮;功能性消化不良;焦虑
Med J PUMCH,2015,6(2):115-118
功能性消化不良 (functional dyspepsia,FD)是临床常见的功能性胃肠疾病,发病机制不清。精神心理因素的参与是导致FD常规治疗效果不佳的原因之一。近年来临床上开始使用抗焦虑抑郁药物治疗FD患者,新型抗焦虑药坦度螺酮对FD合并焦虑作用的研究目前仅有一些国外资料,国内研究很少。本研究目的是观察坦度螺酮治疗FD合并焦虑患者的疗效及安全性。
对象和方法
对象
纳入2012年3月至2013年12月在北京协和医院消化内科门诊就诊的FD合并焦虑状态患者,病例纳入标准:符合罗马Ⅲ的FD诊断标准[1];合并焦虑状态 [Zung焦虑自评量表(Zung anxiety self-rating scales,SAS)评分≥50分,汉密尔顿焦虑量表(Hamilton anxiety scales,HAMA)评分≥14分];FD经常规治疗无效;近期未使用过其他抗焦虑抑郁药物;同意参加该临床研究,并签署知情同意书。
用药方法
给予患者口服 (温水送服)枸橼酸坦度螺酮片,10 mg/次,3次/d,治疗4周,期间停服其他药物。
评估方法
基线期评估内容包括消化不良症状评分、焦虑抑郁评分、生活质量评分、液体营养餐负荷试验。分别于治疗后2周、4周评估消化不良症状变化;治疗后4周评估焦虑抑郁评分、生活质量评分和液体营养餐负荷试验,同时观察记录不良事件。
消化不良症状评分:评价的症状包括餐后饱胀不适、早饱、上腹痛、上腹部烧灼感,按照症状的程度和频度分别计分,相加计算出单个和整体症状积分。程度计分标准:0分为无症状;1分为轻度(需注意才能感觉到有症状);2分为中度 (有症状,但不影响工作和生活);3分为重度 (症状明显,影响工作和生活)。频度计分标准:0分为无;1分为1~2 d/周;2分为3~4 d/周;3分为5~6 d/周;4分为≥6 d/周。
焦虑抑郁评分:分别采用SAS、Zung抑郁自评量表 (Zung depression self-rating scales,SDS)、HAMA、汉密尔顿抑郁量表 (Hamilton depression scales,HAMA)评估。
生活质量评分:采用SF-36量表评估。
液体营养餐负荷试验:参照文献 [2]方法,测量阈值饮入量和饱足饮入量。
统计学处理
研究使用EpiData录入数据,SPSS 13.0软件进行统计分析,采用秩和检验进行组间比较,P<0.05为差异有统计学意义。
结果
一般资料
纳入31例FD合并焦虑状态患者,其中男性7例,女性24例,平均年龄 (42.0±10.3)岁,平均病程 (57.0±4.8)个月。
FD症状积分变化情况
与治疗前比较,患者治疗2周和4周时餐后饱胀不适、早饱症状和总体症状积分均下降,差异有统计学意义 (P<0.05);治疗2周与治疗4周比较,症状积分差异无统计学意义 (表1)。
心理量表评定
治疗4周与治疗前比较,患者SAS、HAMA及HAMD评分均下降,差异有统计学意义 (P均<0.05) (表2)。
生活质量评分
治疗4周与治疗前相比,患者生活质量问卷中生理功能、躯体疼痛、总体健康状况改善计分差异有统计学意义 (P均<0.05)(表3)。
液体营养餐负荷试验
饮入法液体营养餐负荷试验显示,治疗前与治疗4周后阈值饮入量 [(226.13±138.82)ml比 (246.13± 127.14)ml,P=0.285]和饱足饮入量 [(676.45± 231.35)ml比 (700.00±207.77)ml,P=0.532]差异无统计学意义。
安全性评价
31例中有5例 (16.1%)出现不良反应,主要是瘙痒、皮疹,可能与用药有关;1例因用药出现颜面水肿、皮疹、瘙痒,第5天患者停药。
讨论
FD是临床最常见的功能性胃肠疾病,主要临床表现为上腹痛、上腹不适 (烧灼或胀感)、早饱、食欲不振、嗳气、恶心等症状。其发病机制尚未完全阐明,目前认为与多种因素有关,包括胃肠动力紊乱[3]、内脏敏感性增加[4]、胃酸分泌增多[5]、脑肠轴功能异常等。大量研究表明,心理社会因素在FD发病中起重要作用[6-7],精神心理因素的参与是导致FD治疗效果不好的主要原因之一。Haug等[8]研究表明,100例FD患者中以消化不良为首要症状者仅26例,而以焦虑为首要症状者占2/3。潘小平等[9]研究表明,FD患者普遍存在抑郁、焦虑情绪,焦虑较抑郁更为突出。研究发现抗抑郁药物治疗FD患者有效[10],亦佐证FD与精神心理因素之间的内在联系。国外一项关于功能性胃肠病使用抗抑郁药治疗的11个随机对照临床研究的荟萃分析显示,抗抑郁药治疗FD有效[11]。
表1功能性消化不良合并焦虑状态患者的功能性消化不良症状积分 (±s)

表1功能性消化不良合并焦虑状态患者的功能性消化不良症状积分 (±s)
与治疗前比较,*P<0.05
时间餐后饱胀不适早饱上腹痛上腹部烧灼感总体症状治疗前4.35±2.602.70±2.892.48±2.131.06±2.0310.45±5.66治疗2周3.32±2.47*1.77±2.49*2.23±2.401.16±1.998.48±5.96*治疗4周3.00±2.08*1.26±2.32*2.06±2.071.19±1.857.39±5.46*
表2功能性消化不良合并焦虑状态患者的心理量表评分 (±s)

表2功能性消化不良合并焦虑状态患者的心理量表评分 (±s)
SAS:Zung焦虑自评量表;SDS:Zung抑郁自评量表;HAMA:汉密尔顿焦虑量表;HAMD:汉密尔顿抑郁量表
SASSDSHAMAHAMD治疗前49.32± 9.9654.30±12.0023.00±6.2118.65±6.时间0.0280.3690.0020.000 02治疗4周47.06±10.3750.68±11.2716.55±6.5514.03±9.93 P值
表3功能性消化不良合并焦虑状态患者的生活质量评分 (?±s)
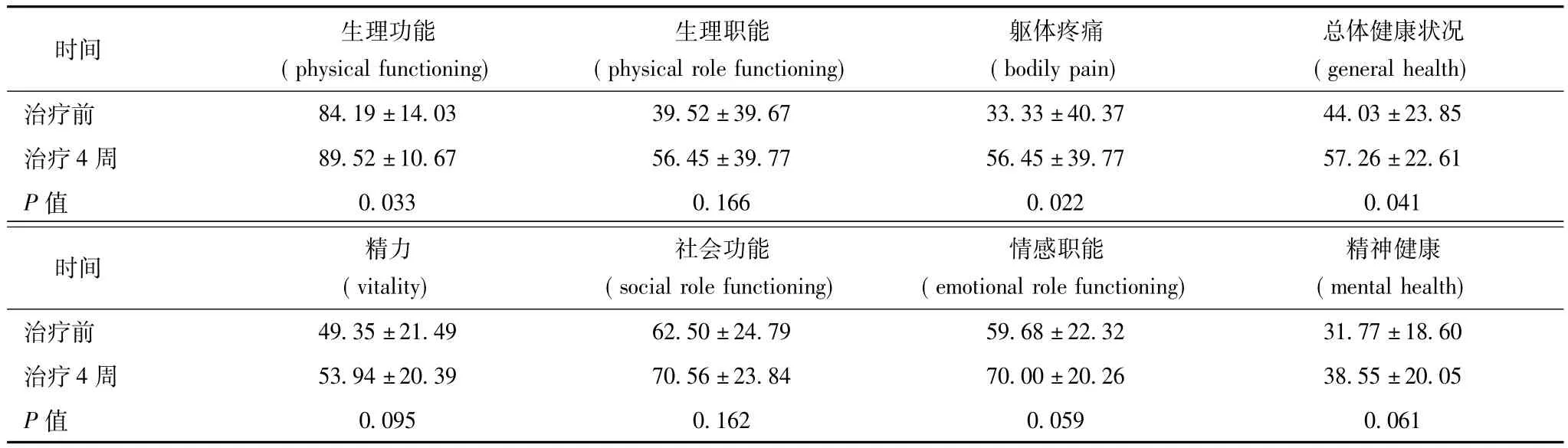
表3功能性消化不良合并焦虑状态患者的生活质量评分 (?±s)
时间生理功能(physical functioning)生理职能(physical role functioning)躯体疼痛(bodily pain)总体健康状况(general health)治疗前84.19±14.0339.52±39.6733.33±40.3744.03±23.85治疗4周89.52±10.6756.45±39.7756.45±39.7757.26±22.61 P值0.0330.1660.0220.041时间精力(vitality)社会功能(social role functioning)情感职能(emotional role functioning)精神健康(mental health)治疗前49.35±21.4962.50±24.7959.68±22.3231.77±18.60治疗4周53.94±20.3970.56±23.8470.00±20.2638.55±20.05 P值0.0950.1620.0590.061
尽管多项研究显示抗焦虑抑郁药对治疗FD有一定效果,但是长期使用苯二氮卓类药物可导致患者出现镇静催眠、药物依赖等不良反应;精神抑制类药物长期使用可能出现药物依赖性及药源性焦虑;部分5-羟色胺 (5-hydroxytryptamine,5-HT)再摄取抑制剂治疗初期可引起激越、焦虑和失眠,均影响患者使用。坦度螺酮是一种5-HT1A受体激动剂,可选择性地与5-HT1A受体结合,具有抗焦虑作用,经过一段时间的治疗,可下调突触前膜5-HT1A自身受体密度而起到抗抑郁作用[12]。
与治疗前比较,坦度螺酮治疗2周、4周后,餐后饱胀不适、早饱症状和总体症状积分均下降,提示该药物在改善消化不良症状方面有效;其中早饱症状的明显改善,提示坦度螺酮可能具有改善胃的容受性的作用,这与其他研究[13]报道相符。治疗后的液体营养餐的阈值及饱足饮入量数值均较治疗前有所增加,但差异无统计学意义,可能与研究样本量少有关。
本研究结果表明SAS、HAMA、HAMD分数治疗4周较治疗前下降;治疗4周后HAMA分数下降一半以上者占32.3%(10/31),HAMD分数下降一半者占38.7%(12/31),与日本学者的研究结果相符[14-15]。提示坦度螺酮抗焦虑作用明确,消化道症状缓解可能与焦虑情绪改善有关。SF-36生活质量量表测定显示患者治疗后生理功能、躯体疼痛以及总体健康状况和生活质量改善。抗焦虑治疗取得较好疗效也间接证明了FD与情绪障碍之间存在内在联系[16]。
综上,本研究结果提示坦度螺酮可用于FD合并焦虑状态的患者,作为在常规经验治疗无效时的选择。
[1] Drossman DA.功能性胃肠病和罗马Ⅲ的制定[M]//柯美云,方秀才,译.罗马Ⅲ:功能性胃十二指肠病.北京:科学出版社,2008:372-397.
[2]张静,孙晓红,王志凤,等.灌注法液体营养餐负荷试验——一种评价近端胃适应性的新方法[J].中华消化杂志,2010,8:518-521.
[3]Mizuta Y,Shikuwa S,Isomoto H,et al.Recent insights into digestive motility in functional dyspepsia[J].J Gastroenterol,2006,41:1025-1040.
[4]Keohane J,Quigley EM.Functional dyspepsia:the role of visceral hypersensitivity in its pathogenesis[J].World J Gastroenterol,2006,12:2672-2676.
[5]Ruiz García A,Gordillo López FJ,Hermosa Hernán JC,et al.Effect of the Helicobacter pylori eradication in patients with functional dyspepsia:randomized placebo-controlled trial[J].Med Clin(Barc),2005,124:401-405.
[6]Li Y,Nie Y,Sha W,et al.The link between psychosocial factors and functional dyspepsia:an epidemiological study[J].Chin Med J(Engl),2002,115:1082-1084.
[7]De la Roca-Chiapas JM,Solís-Ortiz S,Fajardo-Araujo M,et al.Stress profile,coping style,anxiety,depression,and gastric emptying as predictors of functional dyspepsia:a casecontrol study[J].J Psychosom Res,2010,68:73-81.
[8]Haug TT,Withelmsenl,Ursin H,et al.What are the real 8 problems for patients with functional dyspepsia[J].Scand J Gasteroenterol,1995,30:97-100.
[9]潘小平,李瑜元,沙卫红,等.抗抑郁药治疗功能性消化不良的临床研究 [J].中华消化杂志,1999,19: 162-164.
[10]Talley NJ,Herrick L,Locke GR.Antidepressants in functional dyspepsia[J].Expert Rev Gastroenterol Hepatol,2010,4:5-8.
[11]Jackson JL,O'Malley PG,Tomkins G,et al.Treatment of functional gastrointestinal disorders with antidepressant medications:a meta-analysis[J].Am J Med,2000,108: 65-72.
[12]Hamik A,Oksenberg D,Fischette C,et al.Analysis of tandospirone(SM-3997)interactions with neurotransmitter receptor binding sites[J].Biol Psychiatry,1990,28: 99-109.
[13]Coulie B,Tack J,Janssens J.Influence of buspirone-induced fundus relaxation on the perception of gastric distension in man[J].Gastroenterology,1997,110:A767.
[14]Kinoshita Y,Hashimoto T,Kawamura A,et al.Effects of famotidine,mosapride and tandospirone for treatment of functional dyspepsia[J].Aliment Pharmacol Ther,2005,21: S37-S41.
[15]Seno H,Nakase H,Chiba T.Usefulness of famotidine in functional dyspepsia patient treatment:comparison among prokinetic,acid suppression and antianxiety therapies[J].Aliment Pharmacol Ther,2005,21:S32-S36.
[16]Hojo M,Miwa H,Yokoyama T,et al.Treatment of functional dyspepsia with antianxiety or antidepressive agents:systematic review[J].J Gastroenterol,2005,40:1036-1042.
Clinical Observation of Tandospirone in Treating Functional Dyspepsia Patients with Anxiety
PANG Min1,2,ZHU Li-ming1,FANG Xiu-cai1,WANG Zhi-feng1,KE Mei-yun1
1Department of Gastroenterology,Peking Union Medical College Hospital,Chinese Academy of Medical Sciences&Peking Union Medical College,Beijing 100730,China2Department of Gastroenterology,Pinggu District Hospital,Beijing 101200,China
ObjectiveTo observe the efficacy and safety of tandospirone in treating patients with functional dyspepsia(FD)co-morbid with anxiety.MethodsThirty-one patients diagnosed with FD co-morbid with anxiety and failed to respond to routine therapy were recruited from the outpatient clinic of gastroenterology in Peking Union Medical College Hospital during the period of March 2012 to December 2013.The patients were treated with tandospirone citrate tablets 10 mg thrice a day for 4 weeks.FD symptom scores before treatment,after 2-week treatment and after 4-week treatment were compared.The Zung anxiety and depression self-rating scales (SAS and SDS),Hamilton anxiety and depression scales(HAMA and HAMD),quality of life questionnaire (SF-36),and liquid nutrient load test results after 4-week treatments were compared with those before treatmentto evaluate the efficacy of tandospirone treatment.Adverse reactions were recorded.ResultsThe total symptom scores 2 weeks and 4 weeks after treatment were 8.48±5.96 and 7.39±5.463,both significantly lower than that prior to treatment(10.45±5.66;P=0.002,0.020).Compared with before treatment,the discomfort after meal and early satiety symptom scores decreased significantly after 2-week and 4-week treatment(all P<0.05).The SAS,HAMA and HAMD scores declined significantly after 4-week treatment compared with pre-treatment score(P=0.028,0.002,0.000).SF-36 indicated significantly improved physiological function,body pain and total health condition after 4-week treatment(P=0.033,0.022,0.041).The threshold volume and satiety volume in liquid nutrient load test showed no significant change after treatment(P=0.285,0.532).During treatment,there were adverse reactions in 5 patients(16.1%,e.g.rash and pruritus)and one case withdrew from the therapy.ConclusionTandospirone is effective and safe in treating functional dyspepsia patients with anxiety,offering an option when routine therapy fails.
tandospirone;functional dyspepsia;anxiety
ZHU Li-mingTel:010-69156892,E-mail:1581606364@qq.com
R573.9
A
1674-9081(2015)02-0115-04
10.3969/j.issn.1674-9081.2015.02.008
2014-12-04)
朱丽明电话:010-69156892,E-mail:1581606364@qq.com
