XELOX方案联合恩度一线治疗晚期胆系肿瘤的临床观察
2015-06-01任铁军单风晓侯建峰薛琪
任铁军 单风晓 侯建峰 薛琪
作者单位:471000 洛阳 郑州大学附属洛阳中心医院肿瘤内科
临床研究
XELOX方案联合恩度一线治疗晚期胆系肿瘤的临床观察
任铁军 单风晓 侯建峰 薛琪
作者单位:471000 洛阳 郑州大学附属洛阳中心医院肿瘤内科
目的 观察卡培他滨和奥沙利铂(XELOX方案)联合重组人血管内皮抑制素(恩度)一线治疗晚期胆系肿瘤的临床疗效及毒副反应。方法 收集2008年1月至2013年12月我院肿瘤科收治的胆系肿瘤Ⅳ期患者42例,随机分为联合组(n=18)和单纯化疗组(n=24)。单纯化疗组应用XELOX方案化疗:卡培他滨1.25 g/m2口服,d1~d14;奥沙利铂85mg/m2静脉滴注,d1。联合组在应用以上药物的同时给予恩度15mg静滴3~4 h,d1~d14。21 d为1个周期,每2个周期评价疗效、生活质量(QOL)及毒副反应,比较两组有效率(RR)、疾病控制率(DCR)、中位无疾病进展生存期(mPFS)和中位生存时间(mOS)。结果 单纯化疗组患者获CR 0例,PR 6例,SD 8例,PD 10例,RR为25.0%,DCR为58.3%;mPFS为5个月,mOS为9.5个月,QOL改善稳定率为66.7%。联合组患者获CR 0例,PR 5例,SD 6例,PD 7例,RR为27.8%,DCR为61.1%;mPFS为7.5个月,mOS为14个月,QOL改善稳定率为77.8%。两组mPFS、mOS和QOL改善稳定率比较,差异均有统计学意义(P均<0.05)。两组毒副反应主要为消化道反应、手足综合征、骨髓抑制、神经毒性及口腔黏膜炎,多为Ⅰ级/Ⅱ级,Ⅲ级/Ⅳ级少见,差异均无统计学意义(P均>0.05)。结论 XELOX方案联合恩度一线治疗晚期胆系肿瘤的疗效较好,毒副反应可耐受,安全性良好,值得进一步观察及临床推广应用。
胆管肿瘤;XELOX方案;重组人血管内皮抑制素;联合化疗;疗效
恶性胆系肿瘤(biliary tract neoplasms,BTCs)是指胆道系统的原发性恶性肿瘤,来源于肝内、肝外胆管上皮及胆囊上皮细胞,主要分为胆囊癌和胆管癌,后者又分为肝内胆管癌、肝外胆管癌及汇管区胆管癌,临床上较少见,但近年来有增加趋势,发病率位于消化道肿瘤的第5位[1,2]。手术切除是胆系肿瘤主要的治疗手段,但因其发病隐匿,恶性程度较高,确诊时往往已达晚期,大部分患者失去手术治疗机会,5年生存率仅为2%~5%,80%以上的患者诊断后1年内死亡,主要治疗方法为姑息治疗[3]。恩度是我国自主研发的重组人血管内皮抑制素,自上市以来,通过大量临床实践发现,恩度联合化疗药物治疗多种恶性肿瘤显示出较好的疗效[4]。本文应用恩度联合XELOX方案治疗晚期胆系恶性肿瘤,与单纯应用XELOX方案对比,具有较好的疗效和安全性,现报道如下。
1 资料与方法
1.1 一般资料
收集2008年1月至2013年12月我院肿瘤科收治住院的胆系肿瘤Ⅳ期患者42例,均经手术(肿瘤病灶切除加周围淋巴结清扫)后病理或B超、CT引导下穿刺病理学诊断确诊。其中男性17例,女性25例;年龄37~75岁,中位年龄58岁;病变位于胆囊23例,肝内胆管8例,肝外胆管11例;8例术后复发,其余均为首诊晚期胆系肿瘤。侵及肝脏或(和)肝转移25例,侵及十二指肠5例,腹腔淋巴结转移20例,骨转移3例,肺转移4例,19例因阻塞性黄疸行姑息性减黄引流术。所有患者预计生存期≥3个月,KPS评分均≥60分,血常规、肝肾功能及心电图基本正常,无其他并发症。42例患者随机分成两组:18例患者接受恩度联合XELOX方案化疗(联合组),24例患者接受单纯XELOX方案化疗(单纯化疗组)。两组患者一般资料差异无统计学意义(P>0.05),具有可比性。
1.2 治疗方法
两组患者均接受XELOX方案化疗:卡培他滨1.25 g/m2口服,d1~d14;奥沙利铂85 mg/m2静滴,d1。化疗前常规应用托烷司琼、甲氧氯普胺、苯海拉明预防消化道反应。用药期间注意保暖,避免冷刺激。21 d为1个周期,每2个周期后评价疗效。联合组在XELOX方案化疗基础上联合恩度治疗:恩度注射液15mg静滴3~4 h,d1~d14。21 d为1个周期。所有病例均接受至少2个周期化疗,如疾病未出现进展,继续化疗至6~8个周期。每个周期随时评价毒副反应,恩度应用至疾病进展或患者拒绝继续应用。
1.3 疗效评价
客观疗效评价按照实体瘤疗效反应评价标准(RECIST 1.1),分为完全缓解(CR):所有目标病灶消失,且维持在4周以上;部分缓解(PR):基线病灶长径总和缩小≥30%;病灶稳定(SD):基线病灶长径总和缩小但未达PR或增加但未达PD;疾病进展(PD):基线病灶长径总和增加≥20%或出现新病灶。以CR+PR计算有效率(RR),CR+PR+SD计算疾病控制率(DCR)。生活质量(QOL)评价参考Karnofsky(KPS)变化情况,改善:治疗后KPS增加≥10分;稳定:KPS变化<10分;下降:KPS减少≥10分。无疾病进展生存期(PFS)定义为化疗开始至疾病进展或因任何原因的死亡。所有患者采用按时返院复查或电话随访,随访至患者死亡或2013年12月31日,联合组及单纯化疗组各有2例失访,无因不能耐受毒副反应而中途退出者。毒副反应按照美国国立癌症研究所通用的毒性标准NCI-CTC 3.0(2003年)进行评价,分为0~Ⅳ级,级别越大,毒副反应越强。
1.4 统计学方法
采用SPSS 16.0统计学软件对数据进行处理。计数资料的比较用χ2检验,用Kaplan-Meier法计算生存率并绘制生存曲线。以P<0.05为差异有统计学意义。
2 结果
2.1 总体疗效
所有患者共完成216个周期化疗,单纯化疗组完成117个周期化疗,平均化疗4.90个周期;联合组共接受99个周期化疗,平均化疗5.50个周期。所有患者均完成不少于2个周期化疗,均可评价疗效。单纯化疗组无CR病例,PR 6例,SD 8例,PD 10例;RR为25.0%,DCR为58.3%。联合组无CR病例,PR 5例,SD 6例,PD 7例;RR为27.8%,DCR为61.1%。两组RR与DCR比较差异均无统计学意义(P均>0.05)。
2.2 生存分析
单纯化疗组患者的mPFS和mOS分别为5个月和9.5个月,联合组患者分别为7.5个月和14个月。联合组患者的mPFS和mOS均较单纯化疗组有所延长,差异均有统计学意义(P均<0.05)。见图1、图2。
2.3 生活质量评价
单纯化疗组24例患者中,生活质量改善7例,稳定9例,降低8例,生活质量改善率为29.2%,改善稳定率为66.7%。联合组18例患者中,改善7例,稳定7例,降低4例,生活质量改善率为38.9%,改善稳定率为77.8%,两组患者生活质量改善稳定率比较差异有统计学意义(P<0.05)。
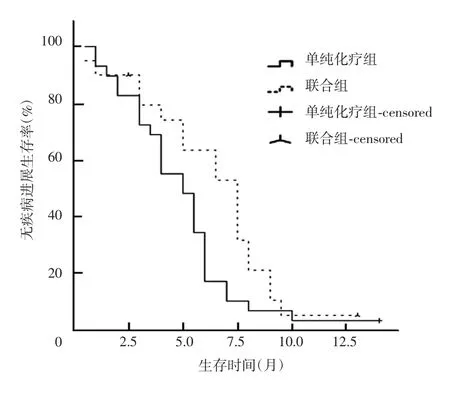
图1 两组患者m PFS的生存曲线
2.4 毒副反应
单纯化疗组和联合组各有1例Ⅲ级腹泻,经给予止泻、补液,3 d后缓解,无相关感染发生。两组患者Ⅲ级手足综合征各1例,经停用卡培他滨后服用维生素B6100mg,3次/d,同时涂抹尿素霜,4 d后缓解。单纯化疗组Ⅲ~Ⅳ级白细胞下降3例,联合组2例,经粒细胞集落刺激因子治疗,血象恢复,无粒细胞缺乏性发热。两组患者的神经毒性多为Ⅰ级,停药后可恢复,未予特殊处理。其他毒副反应如口腔黏膜炎、恶心、呕吐、乏力和肝功能异常等,多为Ⅰ~Ⅱ级,两组比较差异均无统计学意义(P均>0.05)。见表1。

图2 两组患者mOS的生存曲线

表1 两组患者毒副反应的情况[n(%)]
3 讨论
胆系肿瘤早期缺乏特异性临床表现,患者确诊时大多已属晚期,失去了手术治疗的最佳时机,因此化疗成为晚期胆系肿瘤重要的治疗方法。
卡培他滨是一种可在体内借助胸腺嘧啶磷酸化酶转变成5-FU的抗代谢氟嘧啶脱氧核苷氨基甲酸酯类药物。与正常组织相比,肿瘤组织内胸腺嘧啶磷酸化酶活性较高,而卡培他滨具有选择性活化作用,一定程度上可增强药物的抗肿瘤作用,且降低毒性作用,为一种高效的靶向疗法[5,6]。奥沙利铂是继顺铂和卡铂之后开发的第三代铂类抗癌药物,属细胞毒类药物,主要作用于DNA,抑制其转录及复制,抗瘤谱较广,具有铂类化合物的一般毒性反应,但并未出现顺铂的肾脏毒性,亦无卡铂的骨髓毒性,毒副反应相对较轻,在临床上应用较广[7,8]。卡培他滨与奥沙利铂联合的XELOX方案是目前治疗胆系肿瘤的常用化疗方案之一。有报道卡培他滨联合第三代铂类药物治疗胆系肿瘤有较高的有效率和疾病控制率[9],可能是5-FU类制剂与草酸铂类药物联合的最佳组合。
多项研究表明肿瘤生长依赖肿瘤血管的形成[10,11],抗血管生成药物成为近年肿瘤治疗研究的热点之一。恩度正是此类药物,其靶点为肿瘤新生血管,主要作用是通过抑制内皮细胞迁移,达到有效抑制肿瘤细胞增殖或转移的目的。研究表明恩度联合化疗药物治疗晚期肿瘤具有较好的疗效[12],毒性较低、安全性较好[13],具有不易产生耐药及复发等优点[14]。消化道肿瘤属富含血管肿瘤,研究表明抗肿瘤血管生成靶向药物在胃癌、结直肠癌、肝癌、胰腺癌等的治疗中均有显著作用[15~19]。有临床研究发现在血管形成期应用恩度的效果优于血管成熟期,提示在肿瘤的早期治疗中应用恩度可能效果更好,即应用于一线治疗可能优于二线、三线治疗[20]。本研究发现XELOX方案联合恩度作为晚期胆系肿瘤的一线治疗方案,显示出较好的疗效。单纯化疗组与联合组的RR与DCR比较差异无统计学意义,但中位PFS与中位OS的差异均有统计学意义,且联合组的QOL改善稳定率高于单纯化疗组(P<0.05)。本组患者毒副反应程度较轻,多为Ⅰ~Ⅱ级,最常见为消化道反应、手足综合征、骨髓抑制、神经毒性及口腔黏膜炎,均为可逆。未出现因严重毒副反应而中断治疗的病例。由此可见,恩度并未增加化疗的毒性。
综上所述,XELOX方案联合恩度一线治疗晚期胆系肿瘤具有较好的疗效,安全性和耐受性较好。⑸于本研究样本量少,因此XELOX方案联合恩度治疗胆系肿瘤的临床效果仍有待进一步证实。
[1] M a r in o D,L e o ne F,C a v a llo ni G,e t a l.B i l ia r y tr ac t ca r cin o ma s:fro m chem ot he r apy to t a r ge t e d t he r apy[J].C r i t R e v O nc ol H ema tol,2013,85(2):136-148.
[2] G or e R M,S he l hame r R P.B i l ia r y tr ac t ne o p l a s m s:d iagn os i s an d st aging[J].C ance r I maging,2007,7:S15-23.
[3] S a s a k i T,I s ayama H,N a k ai Y,e t a l.I mp rov emen t of p ro gn os i s for un r e s ec t a bl e b i l ia r y tr ac t cance r[J].World J Ga stro en t e rol,2013,19(1):72-77.
[4] X u F,M a Q,S ha H.O p t imi z ing dr ug d e l i v e r y for enhancing t he r apeu t ic e ff icacy of r ec o m b inan t human en dost a t in in cance r tr ea t men t[J]. C r i t R e v T he r D r ug C a rr ie r S y st,2007,24(5):445-492.
[5] N eh ls O,K l ump B,A rk enau H T,e t a l.O x a l ip l a t in,fl u oro u r aci l an d l euc ovor in for a dv ance d b i l ia r y s y st em a d en o ca r cin o ma s:a p ros pect i v e pha s e II tr ia l[J].B r J C ance r,2002,87(7):702-704.
[6] 刘云军,何志江,黄毅超,等.多西他赛联合希罗达在晚期胃癌的疗效分析[J].中南医学科学杂志,2012,40(6):585-587.
[7] 彭志霞,潘伟杰.希罗达对胃肠癌患者的化疗效果应用研究[J].中国实用医药,2014,9(13):163-164.
[8] 王静,谷华伟,洪永贵.卡培他滨联合奥沙利铂治疗晚期结肠癌65例临床观察[J].中国实用医刊,2014,41(9):34-36.
[9] 林万隆,陈强.奥沙利铂的药理作用及临床应用[J].中国肿瘤临床,2000,27(11):872-874.
[10]F olk man J.R ol e of angi o gene s i s in t um or g rowt h an d me t a st a s i s[J]. S emin O nc ol,2002,29(6 S upp l 16):15-18.
[11]S e ss a C,Gui b a l A,D e l C o n t e G,e t a l.B i o ma rk e rs of angi o gene s i s for t he d e v e lo pmen t of an t iangi o genic t he r apie s in o nc olo gy:tools or d ec or a t i o n s?[J].N a t C l in Pr ac t O nc ol,2008,5(7):378-391.
[12]章骏,赵怡,杨志刚,等.恩度联合化疗治疗多种恶性复发肿瘤转移灶的疗效观察[J].实用癌症杂志,2011,26(1):69-70.
[13]彭济勇,曾建伦,汤江林,等.恩度联合化疗治疗多种晚期恶性肿瘤的临床观察[J].药品评价,2007,4(5):380-381.
[14] F e ld man AL,R e st i fo N P,A l e x an d e r H R,e t a l.A n t iangi o genic gene t he r apy of cance r u t i l i z ing a r ec o m b inan t a d en ov i r u s to e l e v a t e s y st emic en dost a t in l e v e ls in mice[J].C ance r R e s,2000,60(6):1503-1506.
[15]马耀先.恩度与化疗联合治疗晚期消化道肿瘤的临床疗效[J].中国老年学杂志,2014,34(14):4065-4066.
[16]J ung Y D,M an sf ie ld P F,A k agi M,e t a l.E ff ec ts of c o m b ina t i o n an t iv a s cu l a r en dot he l ia l g rowt h f ac tor r ecep tor an d an t i-epi d e r ma l g rowt h f ac tor r ecep tor t he r apie s o n t he g rowt h of ga str ic cance r in a nu d e m o u s em od e l[J].E u r J C ance r,2002,38(8):1133-1140.
[17]沈琳,王晰程.直肠癌的靶向药物治疗[J].临床外科杂志,2014,22(4):245-247.
[18]P ang R W,Poo n R T.F ro m m ol ecu l a r b i olo gy to t a r ge t e d t he r apie s for hepa to ce ll u l a r ca r cin o ma:t he f u t u r e i s n ow[J].O nc olo gy,2007,72:30-44.
[19]张则伟,赵彩芳.胰腺癌的抗血管生成治疗研究进展[J].浙江医学,2008,30(1):94-97.
[20]秦叔逵,刘秀峰,王琳,等.重组人血管内皮抑素与化疗联合治疗肺外晚期恶性肿瘤的临床研究[J].临床肿瘤学杂志,2007,12(10):728-735.
[2014-10-03收稿][2014-11-19修回][编辑 罗惠予]
Efficacy and safety of combined XELOX and Endostar therapy as first-line treatm ent for patientsw ith advanced biliary tract carcinoma
REN Tiejun,SHAN Fengxiao,HOU Jianfeng,XUE Qi(Luoyang Center Hospital Affiliated of Zhengzhou University,Luoyang 471000,P.R.China)
SHAN Fengxiao.E-mail:xiaofengshan1988@163.com
Objective To observe the efficacy and safety of the combination of Endostar therapy with capecitabine and oxaliplatin therapy as a first-line treatment for patients with advanced biliary tract carcinoma.Methods Records were retrospectively reviewed for 42 patients with stageⅣ primary biliary tract carcinoma confirmed by pathology and imaging,who were treated at our hospital from January 2008 to December 2013.Eighteen patients were treated with Endostar+XELOX,while 24 were treated with XELOX alone.The XELOX regimen involved capecitabine at 1.25 g/m2,po,d1-d14 and oxaliplatin at 85mg/m2,ivgtt,d1.Endostarwas given at a dose of 15 mg,ivgtt,d1-d14,on a 21-day cycle.After 2 cycles,efficacy,quality of life(QOL),safety,median progression-free survival(mPFS)and median overall survival(mOS)were compared between the two treatment groups.Results In the XELOX group after 2 treatment cycles,no patientwas in CR,6 were in PR,8 were in SD,and 10 were in PD;the response rate(RR)was 25.0%,disease control rate(DCR)was 58.3%,mPFSwas 5.0months and mOSwas 9.5months.QOL improved as a result of treatment,and 66.7%patientswere in stable condition.In the Endostar+XELOX group after 2 cycles,no patientwas in CR,5 were in PR,6 were in SD,and 7 were in PD;RR was 27.7%,DCR was 61.1%,mPFSwas 7.5 months and mOSwas 14.0 months.QOL improved as a result of therapy,and 77.8%of patients achieved a stable condition.mPFS and mOSwere significantly longer for patients who received combination therapy(P<0.05).The two therapieswere associated with similar types and rates of adverse events,themost frequent ofwhich were gastrointestinal reactions,hand-foot syndrome,myelosuppression,neurotoxicity,and stomatitis(mainly gradeⅠ-Ⅱ). Conclusion Endostar+XELOX shows good efficacy asa first-line treatment for advanced biliary tract carcinoma,and it iswell tolerated,justifying its further study and potentially wider implementation in the clinic.
Biliary tract neoplasm;XELOX regimen;Rh-endostatin/Endostar;Combination therapy;Efficacy
R735.8
A
1674-5671(2015)01-04
10.3969/j.issn.1674-5671.2015.01.09
单风晓。E-mail:xiaofengshan1988@163.com
