高效液相色谱法测定骨疏灵颗粒中淫羊藿苷含量
2015-05-07朱裕林陈卫东
俞 吉,朱裕林,桑 冉,屈 彪,陈卫东*
0 引言
骨质疏松症(Osteoporosis,OP)是以骨量减少、骨质量受损及骨强度降低,导致骨脆性增加、易发生骨折为特征的全身性骨病[1]。单味中药淫羊藿煎服治疗绝经后骨质疏松症在缓解骨痛症状、改善骨代谢生化指标、提高松质骨密度等与性激素替代疗法比较差异无统计学意义[2-3]。骨疏灵颗粒是安徽中医药大学方朝晖教授针对引起老年性骨质疏松症的“气虚、阳虚、血淤”的病机,以“益气、温阳、活血”为法,用淫羊藿、黄芪、牛膝、牡蛎4味中药组方,该药治疗骨质疏松症的作用是多方面的,既能抑制骨的吸收,又能刺激成骨,产生较多骨基质,使骨代谢转为正态平衡,延缓衰老,是治疗骨质疏松的良药[4-7]。其中淫羊藿为君药,而淫羊藿苷为淫羊藿的主要活性成分。为进一步完善骨疏灵颗粒的标准,更好地控制该制剂的质量,本文采用高效液相色谱法测定该药中淫羊藿苷的含量。
1 仪器、试药与样品
日本岛津1260高效液相色谱仪,二极管阵列检测器(DAD);Cosmosil C18色谱柱(250 mm×4.6 mm,5 μm);旋转蒸发仪(金坛市华欧实验仪器厂);减压干燥箱(江苏南京海汪制药机械装备有限公司);分析天平(上海市天平仪器厂);超声波清洗机(上海市声波仪器厂);抽滤瓶(GB-17);真空泵(SHB-Ⅲ);离心机(LC-4016)。
淫羊藿苷对照品(中国食品药品检定研究院,批号:110737-200415),乙腈(色谱纯),水为超纯水,甲醇为分析纯,其他试剂为分析纯。骨疏灵颗粒(安徽中医药大学药学实验室自制,批号:141001、141002、141003),淫羊藿、黄芪、牛膝、牡蛎(购自亳州市药材大市场,经安徽中医药大学刘鹤龄教授鉴定均符合中国药典2010年版规定)。
2 方法与结果
2.1 色谱条件Cosmosil C18色谱柱(250 mm×4.6 mm,5 μm),柱温为室温;流动相:乙腈 -水(3∶7);流速:1 mL/min;紫外检测波长:270 nm。
2.2 溶液的制备
2.2.1 对照品溶液的制备 精密取淫羊藿苷对照品2.5 mg,置10 mL容量瓶中,加甲醇至刻度,摇匀,配成浓度为0.25 mg/mL的溶液。
2.2.2 供试品溶液的制备 按照发明专利处方配比,取淫羊藿饮片15 g,黄芪饮片20 g,牛膝饮片12 g,牡蛎饮片8 g。淫羊藿与牛膝,以8倍(第1次多加3倍)70%乙醇、回流提取3次,每次2 h;黄芪与牡蛎,以8倍(第1次多加1.5倍)水煎煮2次,每次1 h。将醇提取药液回收乙醇后与水提取液合并挥干浓缩,在减压干燥箱以55℃、-0.09~-0.1 Mpa条件下干燥至恒重后取出标记批号。上述操作重复操作 3次,得批号为 141001、141002、141003的骨疏灵颗粒3批。再精密称取自制骨疏灵颗粒1.0 g,置于50 mL容量瓶中,精密加入稀乙醇定容,密塞,超声处理20 min,摇匀,0.22 μm微孔滤膜过滤,取滤过液即得。取淫羊藿药材粉末按《中国药典》2010年版记载方法制得淫羊藿药材溶液备用。
2.2.3 阴性对照溶液的制备 取处方中除淫羊藿外的其余药材,按骨疏灵颗粒的工艺制备不含淫羊藿的阴性对照制剂,按照“2.2.2”项下的方法制备阴性对照溶液。
2.3 专属性试验 精密量取上述对照品溶液、淫羊藿药材供试品溶液、骨疏灵颗粒供试品溶液及阴性对照溶液注入液相色谱仪中,按照“2.1”项下色谱条件分别进样,记录色谱图,在与对照品色谱图主峰相同的保留时间上,供试品溶液有对应峰显示,阴性对照溶液无对应峰。结果表明,阴性溶液对检测结果无干扰,结果见图1。
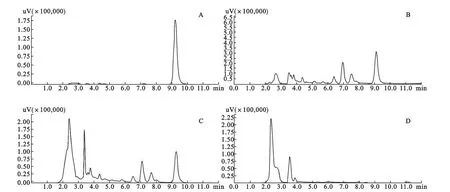
图1 色谱图注:A.淫羊藿苷对照品,B.淫羊藿药材,C.骨疏灵颗粒,D.阴性对照品
2.4 标准曲线的绘制 取淫羊藿苷对照品适量,加甲醇分别制成每1 mL含淫羊藿苷10、50、80、100、200、250 μg 的溶液,分别精密吸取 20 μL 注入液相色谱仪,记录色谱图,以进样浓度(mg/mL)为横坐标(X)、峰面积为纵坐标(Y),绘制淫羊藿苷的标准曲线,得回归方程:Y=5×107X+102 087,r=0.999 9。结果表明,淫羊藿苷在0.01~0.25 mg/mL浓度范围内线性关系良好。见图2。
2.5 精密度试验 取线性关系项下0.01 mg/mL的对照品溶液连续进样5次,以峰面积计算,平均值为561 724.2,计算精密度,RSD为0.06%(n=5),表明仪器精密度良好。
2.6 稳定性试验 以对照品溶液中淫羊藿苷的吸收峰面积变化,考察供试品溶液的稳定性。取对照品溶液,分别在 0、2、4、6、8、12 h 测定对照品溶液的峰面积,得RSD为1.6%,结果表明,该成分在12 h内稳定。
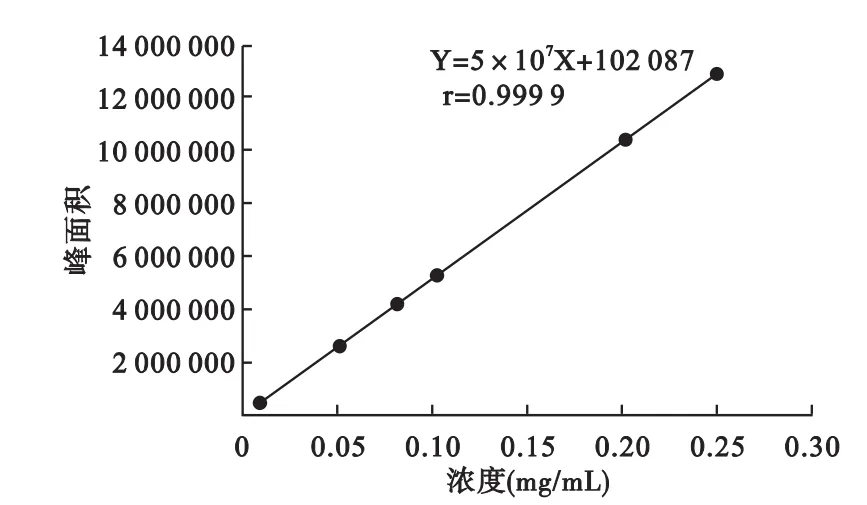
图2 淫羊藿苷标准曲线
2.7 重复性试验 取同一批骨疏灵颗粒,精密称取适量(约1 g),平行操作5份,按“2.2.2”项下供试品溶液的处理方法制备供试品溶液,进样测定,计算淫羊藿苷的含量,结果RSD为1.8%,表明方法重复性良好。
2.8 回收率试验 精密称取已知含量的同一批本品颗粒(批号:141003,淫羊藿苷含量:2.23 mg/g)6份,每份约900 mg,分别置于25 mL容量瓶中,精密加入稀乙醇定容,密塞,超声处理20 min,摇匀,0.22 μm微孔滤膜过滤,取过滤液分别进样。再精密加入淫羊藿苷对照品溶液(0.081 mg/mL)1 mL,制备供试品溶液,再次进样测算峰面积,计算加样回收率。见表1。
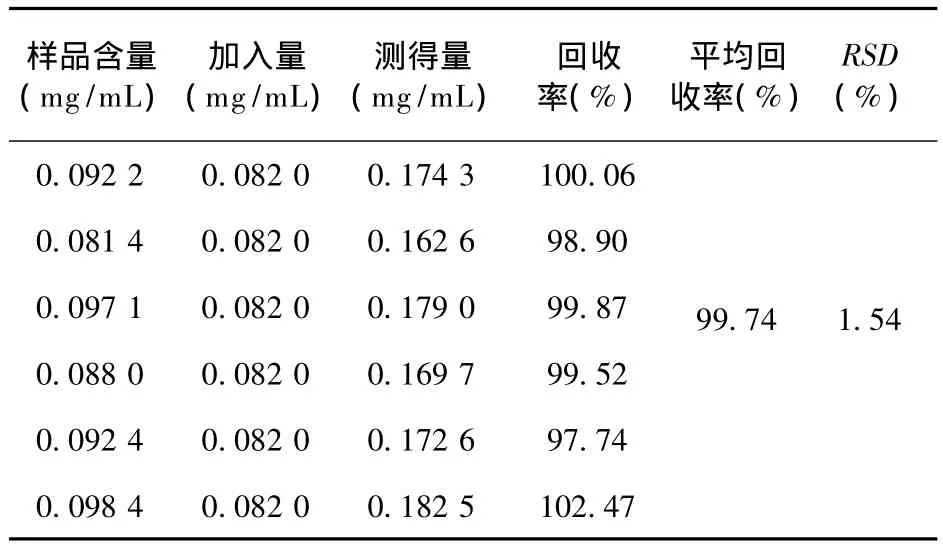
表1 加样回收率实验测定结果(n=6)
2.9 含量测定 取3批本品颗粒,每批称取1.0 g,精密称定,按照药材含量处理方法制备样品溶液,精密量取20 μL注入HPLC色谱仪中,测定峰面积,根据淫羊藿苷标准曲线计算含量,结果批号为141001、141002、141003的骨疏灵颗粒中淫羊藿苷含量分别为2.16、2.24、2.13 mg/g,平均2.17 mg/g。
3 讨论
目前,文献报道中关于淫羊藿苷的含量检测有紫外分光光度法、导数光谱法、室温燐光法、薄层扫描法、高效液相色谱法、毛细管胶束电动色谱法[8],但最为常见的是 HPLC法,后者具有方便、快捷等特点。淫羊藿苷具有可溶解于乙醇、乙酸乙酯的性质,笔者在试验中曾尝试使用30%、50%、70%的乙醇分别回流醇提,分别醇提2次、3次、4次,并分别进行含量比较。结果显示,醇提3次和4次的淫羊藿苷含量明显较醇提2次高,但醇提3次和4次之间淫羊藿苷含量差异无统计学意义。所以在淫羊藿苷醇提中,选择70%乙醇回流醇提3次的工艺。
经全波长扫描,淫羊藿苷在270 nm处吸收较大,结果与中国药典2010版记载一致,因此确定淫羊藿苷的检测波长为270 nm。在流动相选择上,有报道乙腈-水有拖尾影响[9]。笔者尝试使用甲醇-水、甲醇-0.1%冰醇酸、乙腈-3.8%冰醇酸(28∶72)为流动相进行试验,发现乙腈-水(30∶70)出峰良好,且分离度高,经试验,阴性样品对测定无干扰,淫羊藿苷的保留时间约为9 min,保留时间、分离度及淫羊藿苷理论板数均符合实验要求。综上所述,本文采用的测定方法简单易行,结果准确,重现性好,可有效控制该复方制剂的质量。
[1] 张智海,刘忠厚,李娜,等.中国人骨质疏松症诊断标准专家共识(第三稿·2014版)[J].中国骨质疏松杂志,2014,(9):1007-1010.
[2] 曾炎辉,张泽玫,林永城,等.绝经后骨质疏松症患者骨代谢生化指标检测及淫羊藿作用初探[J].国际医药卫生导报,2005,11(6):24-26.
[3] 赵丽娜.淫羊藿防治骨质疏松临床效果评价[J].现代中西医结合杂志,2003,12(9):922-923.
[4] 徐晓东,郑洪新.肾虚与骨质疏松症[J].辽宁中医药大学学报,2007,9(4):45-46.
[5] 方朝晖,刘健,章小平,等.骨疏灵改善维甲酸诱导的骨质疏松症大鼠骨质代谢作用的研究[J].中国实验方剂学杂志,2000,6(5):40-42.
[6] 方朝晖,刘健,章小平,等.骨疏灵对维甲酸诱导的实验性骨质疏松症的影响[J].中国中医药信息杂志,2001,8(1):36-37.
[7] 方朝晖,耿家金,张有志,等.186例老年性骨质疏松症的中医证候调查对照研究[J].中国中医药信息杂志,2004,11(7):614-615.
[8] 尹志峰,刘敬闪,张兰桐.淫羊藿苷的含量测定方法[J].中国医院药学杂志,2003,(8):47-49.
[9] 崔晓红,袁志芳,张兰桐.益肾强身片中淫羊藿苷的含量测定[J].中国新药杂志,2005,(11):78-80.
