WC/MMT纳米复合材料制备及其对PNP的电催化活性
2015-04-01李国华杨威佟明兴郑翔
李国华,杨威,佟明兴,郑翔
(1浙江工业大学化学工程学院,浙江 杭州 310014;2绿色化学合成技术国家重点实验室培育基地,浙江 杭州 310014)
引言
碳化钨(WC)是一种具有高硬度、良好导电性、耐高温、耐酸性的功能材料;在催化作用过程中,碳化钨具有类铂催化性能[1-2],还具有较强的抗CO及 H2S中毒能力[3],但其催化活性远低于铂等贵金属催化剂[4-5]。因此,提高碳化钨的催化活性是其走向实际应用的关键。
研究表明,选择适当的载体组成纳米复合材料是提高碳化钨催化性能的有效技术手段。活性炭[6]、碳纳米管[7-9]、石墨烯[10]、Al2O3[11]、TiO2[12]、SBA-16[13]等均可作为碳化钨催化剂的载体,并可较好地提高其电催化性能。但以这些材料为载体的复合材料存在一些不足之处。如Al2O3[11]和TiO2[12]本身易团聚,导致碳化钨催化剂颗粒较大;SBA-16[13]在高温还原碳化过程中其结构容易破坏而影响催化剂的性能;纳米碳管[7-9]和石墨烯[10]在使用前分别要进行纯化和剥离氧化,且在高温还原碳化过程中其结构也会遭到破坏。因此,寻找新的碳化钨复合材料载体是进一步提高其催化性能的关键问题之一。
蒙脱石(MMT)是一种具有2:1型层状结构的天然硅酸盐黏土矿物,其具有表面电负性强、比表面积大、吸附性强及阳离子交换性能好等特点[14]。研究表明,将 Pt[15]、Au[16]、Pd[17]、Ru[18]、Fe[19]等金属及CdS[20]、ZnO[21]等纳米粒子负载于蒙脱石层间和表面,可使纳米粒子的稳定性增强,均匀性更好,尺寸更小,并可明显提高其催化性能。
本文以剥离后的蒙脱石为载体,采用浸渍法将W6+离子基团负载到蒙脱石表面,再利用原位还原碳化技术将其还原成碳化钨,得到了碳化钨与蒙脱石的纳米复合材料,并考察了其对对硝基苯酚的电催化还原性能。
1 实验材料和方法
1.1 材料
实验所用六氯化钨及结晶氯化锂购自阿拉丁试剂(上海)有限公司,碱性钠基蒙脱石为浙江三鼎有限公司生产,对硝基苯酚的生产厂家为华东师范大学化工厂,制备电极所用Nafion溶液为上海河森电气有限公司出品的杜邦D520型5% Nafion膜溶液。实验所用其他试剂均为分析纯,去离子水为自制。
1.2 实验仪器
实验所用管式电阻炉为上海实验电炉厂生产的SK-2-2-10型管式电阻炉;样品的晶体结构采用荷兰PANalytical公司生产的X’PertPRO型X射线衍射仪进行分析,实验采用 CuKα靶(λ=0.154056 nm)管流40 mA,管压45 kV,步长0.04°,2θ的扫描速度为 2.4(°)·min-1,扫描范围为 5°~80°;样品的形貌特征和显微结构采用配备有X射线能量散射谱仪(EDS)的HitachiS-4700Ⅱ型场发射扫描电镜和荷兰Philips-FEI公司的300 kV高分辨透射电子显微镜(Tecnai G2 F30 S-Twin)进行观察。
1.3 样品的制备
1.3.1 蒙脱石的剥离 将一定量干燥后的蒙脱石(MMT)加入70 ml 8 mol·L-1LiCl溶液中,超声分散后移至100 ml水热反应釜中,在140℃下水热反应24 h,然后用50%的乙醇对样品进行洗涤,干燥后即得剥离后的蒙脱石(E-MMT)样品。
1.3.2 WO3/MMT前驱体的制备 称取 1.6023 g WCl6溶于50 ml无水乙醇中,称取1.000 g E-MMT加入上述溶液中,超声分散10 min后移至30℃恒温水浴中搅拌24 h,然后将样品洗涤、干燥、研磨,即得WO3/MMT前驱体。
1.3.3 WC/MMT纳米复合材料的制备 将一定量的WO3/MMT前驱体放入石英舟内,将石英舟放入管式电阻炉中指定位置,在 800℃条件下、CH4/H2气氛中还原碳化5 h,氮气保护下自然冷却后得到碳化钨与蒙脱石纳米复合材料。
1.4 电化学性能测试
样品的电催化性能测试采用CHI660e型电化学工作站(上海辰华仪器公司),测试在298 K下采用循环伏安法和三电极体系进行。工作电极为玻碳电极,辅助电极为1 cm2的99.99% Pt片,参比电极为饱和甘汞电极(SCE),工作电极与辅助电极之间用多孔陶瓷隔膜隔开。
工作电极的制备:准确称取 10 mg WC/MMT样品置于小号样品管中,用移液枪依次加入 10 μl 5%的Nafion溶液和40 μl异丙醇,超声分散30 min;用移液枪移取2 μl上述溶液至玻碳电极表面,自然晾干后得到工作电极。
2 结果与讨论
2.1 样品的结构和形貌
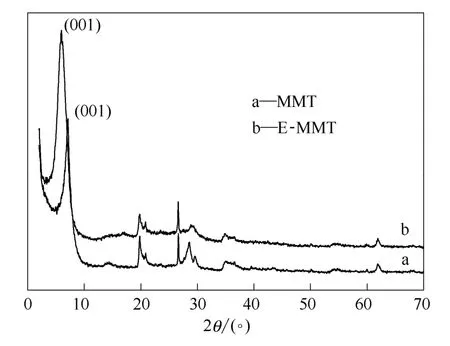
图1 剥离前后蒙脱石的XRD谱图Fig.1 XRD patterns of montmorillonite samples

图2 剥离前后蒙脱石的SEM图Fig.2 SEM images of montmorillonite samples MMT and E-MMT
2.1.1 剥离前后的蒙脱石 图1为剥离前后蒙脱石的XRD谱图。其中,曲线a为剥离前的蒙脱石,曲线b为剥离后的蒙脱石。从图1可以看出,剥离前后蒙脱石的衍射峰没有明显的变化,仅(001)晶面的特征衍射峰强度增大,且其2θ由7.153°向左偏移到5.965°。这说明(001)晶面间距有所扩大。根据 Bragg方程 2dsinθ=nλ(λ=0.154 nm,n=1)计算,蒙脱石(001)的晶面间距d001从1.23 nm增加到 1.50 nm。这是由于氯化锂中的锂离子经水热反应后插层到蒙脱石的层间,使蒙脱石的片层受到剥离,层状结构变薄,层间距扩大所致。
剥离前后蒙脱石结构特征如图2所示。其中,图2(a)为剥离前的蒙脱石,图2(b)为剥离后的蒙脱石。对比图2(a)与图2(b)可发现,未剥离的蒙脱石为块状结构,片层结构比较完整;剥离后的蒙脱石的片层分开,可明显观察到片层处于剥离状态,片层厚度约为10 nm。这种片层结构更加有利于钨离子基团的负载。
2.1.2 WO3/MMT 负载钨后的WO3/MMT前驱体的形貌和化学组成如图3所示。从图3可看出,蒙脱石表面不再光滑,而是分布着许多小颗粒。结合EDX谱图可知,前驱体中除了蒙脱石的主要化学组成O、Si、Al、Fe和Mg外,还有一定量的W元素。这说明W离子基团已经负载到了蒙脱石上。
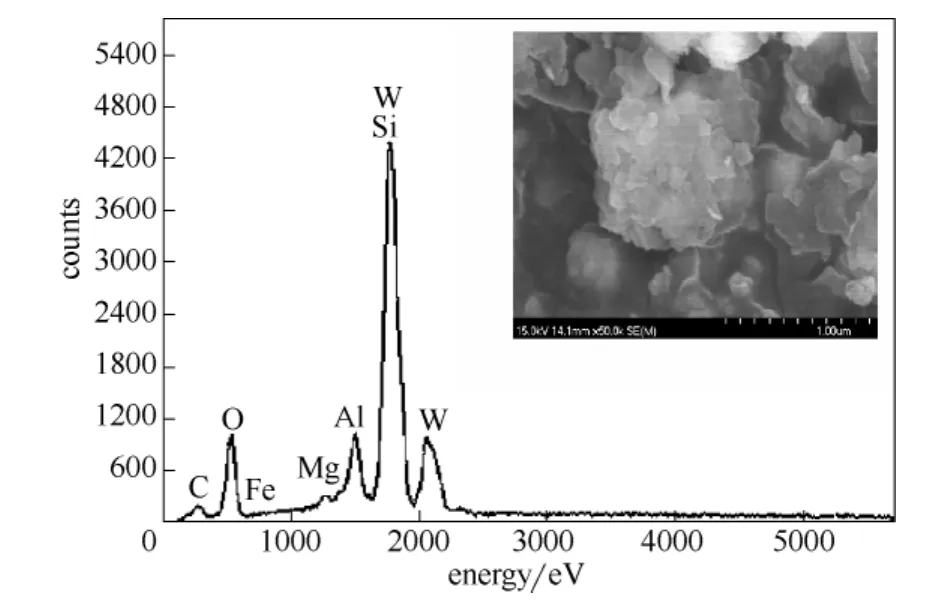
图3 WO3/MMT的SEM照片及EDX谱图Fig.3 SEM image and EDX pattern of WO3/MMT
2.1.3 WC/MMT 图 4为 WC/MMT样品的 XRD谱图。从图4中可看出,样品主要由WC(PDF:51-0939)、W2C(PDF:35-0776)和MMT组成。
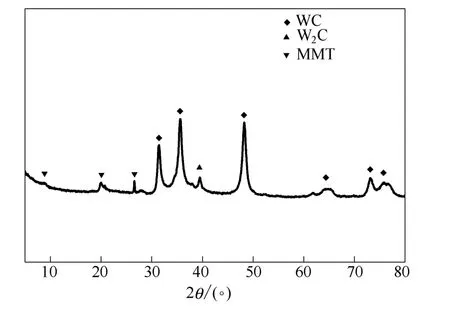
图4 WC/MMT样品的XRD谱图Fig.4 XRD pattern of WC/MMT
WC/MMT样品的形貌和微结构特征如图5所示。图5(a)中,浅色薄片为蒙脱石,其片状结构明显,厚度在30 nm以下;黑色颗粒为碳化钨,均匀地分散于蒙脱石表面。图5(b)为图5(a)的局部放大图,经Digital Micrograph软件测量,黑色颗粒的晶面间距约为0.2455 nm。这与WC(100)的晶面间距0.2517接近。结合XRD分析结果,可进一步证实上述黑色颗粒为WC晶粒。

图5 WC/MMT样品的TEM图Fig.5 TEM images of WC/MMT
2.2 复合材料的电催化性能
图6是WC/MMT样品分别在0.5 mol·L-1硫酸(H2SO4)(曲线a)和0.1 mol·L-1对硝基苯酚(PNP)及0.5 mol·L-1H2SO4(曲线b)溶液中循环伏安图。扫描速度为 100 mV·s-1,扫描方向为-0.8~0~-0.8 V。从图6曲线a中可看出,在H2SO4溶液中,电位在-0.8~0 V的范围内,样品的循环伏安曲线没有出现明显的氧化还原峰;从图6曲线b中可看出,在酸性PNP溶液中,当电位为-0.568 V时,样品的循环伏安曲线中出现了一个明显的还原峰,其峰电流密度达到了2.310 mA·cm-2。对比图6中的曲线a和b说明,在酸性溶液中,样品对PNP具有明显的还原作用,且有较好的导电性。
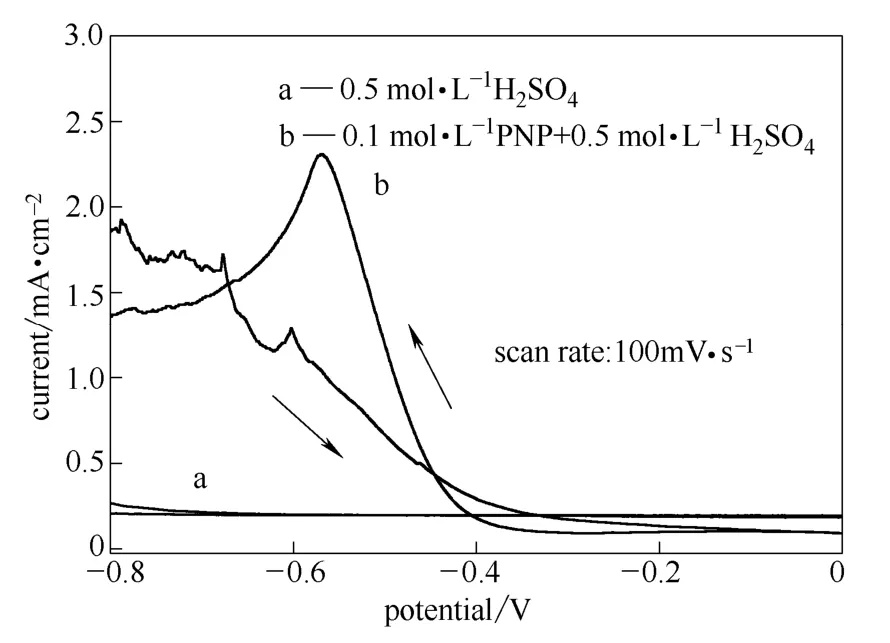
图6 WC/MMT的循环伏安曲线Fig.6 Cyclic voltammograms of WC/MMT
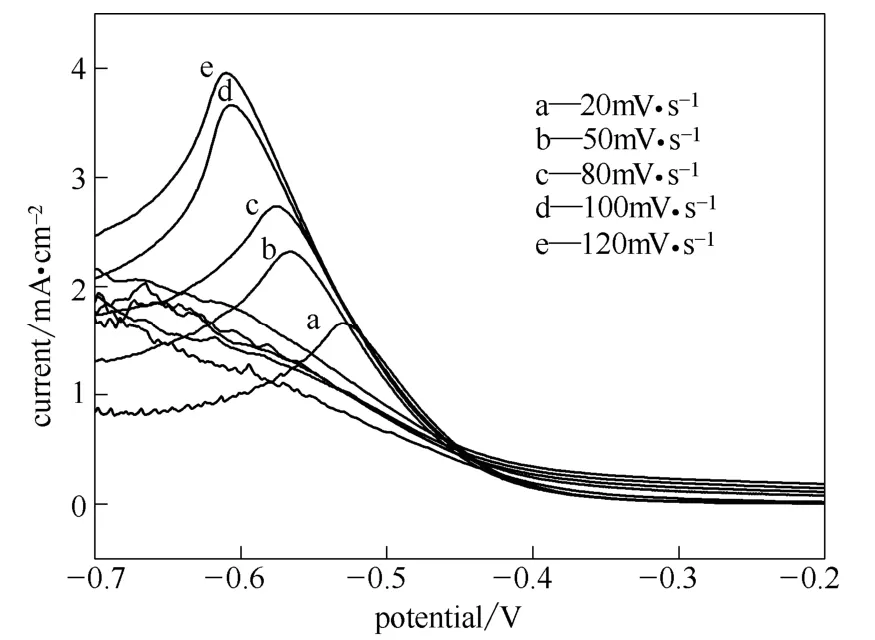
图7 不同扫描速度下WC/MMT样品的循环伏安图Fig.7 Cyclic voltammograms of WC/MMT at different scan rate (0.1 mol·L-1PNP+0.5 mol·L-1H2SO4)
为了进一步研究PNP在WC/MMT上的电化学行为,测试了WC/MMT样品在不同扫描速度和不同扫描圈数情况下对PNP的电催化性能,结果如图7所示。从图中可看出,PNP的电催化还原峰电位及峰电流随着扫描速度的增加呈现出规律性的变化。即随着扫描速度的增加,还原峰的峰电流逐渐增加,还原峰的电位逐渐向负方向移动。这说明PNP在电极上的催化还原过程为一不可逆过程。
为探讨还原峰电流与扫描速度的关系,选取了扫描速度分别为20、50、100和120 mV·s-1的峰电流为研究对象,并以峰电流(Ip)为纵坐标,扫描速度的1/2次方(v1/2)为横坐标作图(图8)。峰电流值对扫描速度的 1/2次方具有良好的线性关系。其线性方程为
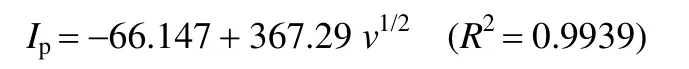
由此可以说明,在20~120 mV·s-1的扫速范围内,PNP在WC/MMT电极上的电还原过程是线性扩散,电极过程受扩散控制。
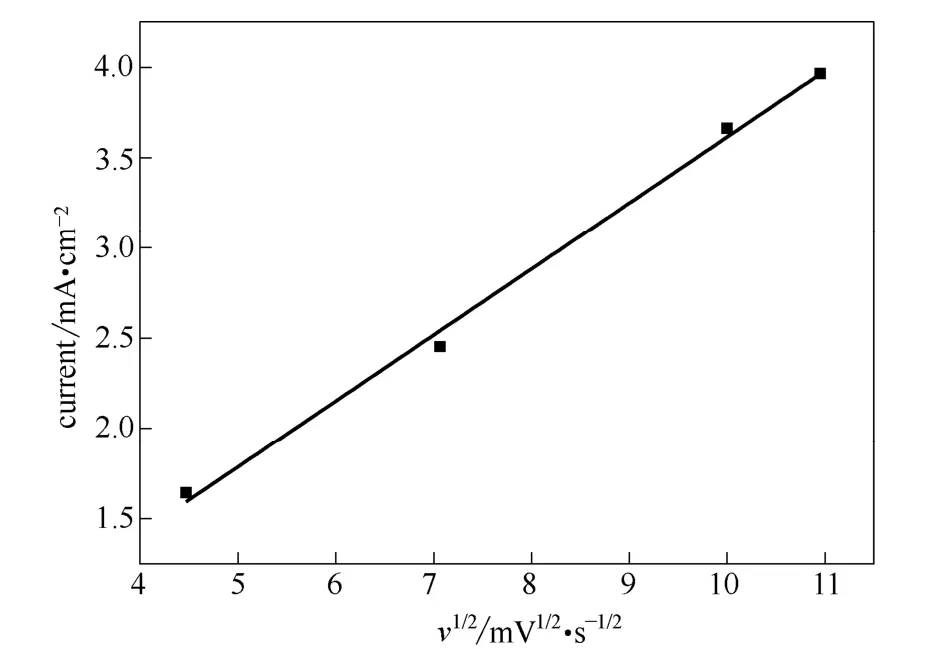
图8 不同扫速下峰电流的变化曲线Fig.8 Curve of current and scan rates
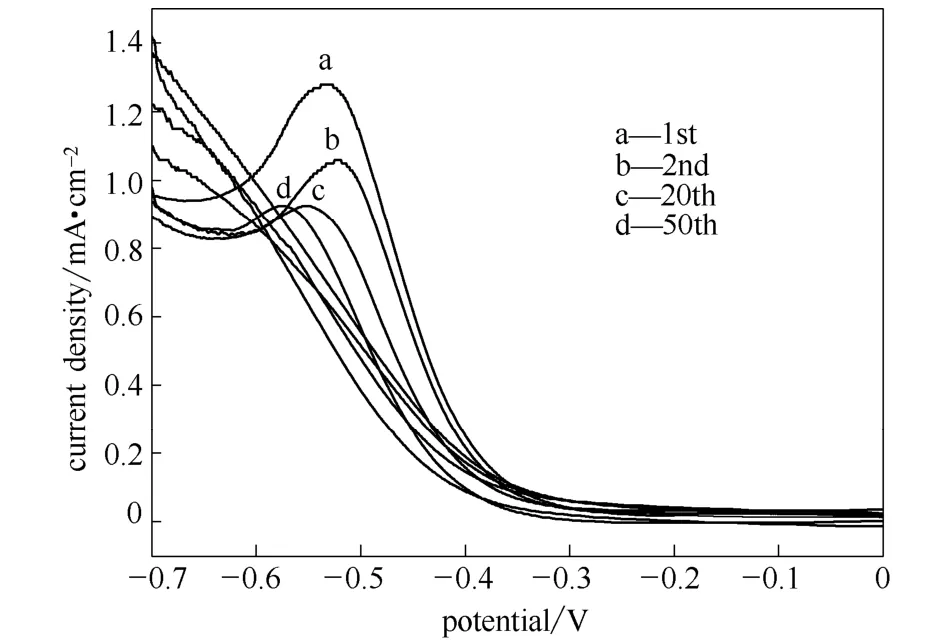
图9 WC/MMT样品不同扫描圈数的循环伏安曲线(0.1 mol·L-1PNP-0.5 mol·L-1H2SO4)Fig.9 Cyclic voltammograms of WC/MMT under different scan cycles (0.1 mol·L-1PNP-0.5 mol·L-1H2SO4)
为了研究WC/MMT纳米复合材料的稳定性,将电极置于0.1 mol·L-1PNP+0.5 mol·L-1H2SO4溶液中,以100 mV·s-1的扫描速度在电极电势为-0.7~0 V的范围内连续扫描50圈,结果如图9所示。从图9中可看出,PNP的电还原过程在第1循环圈中出现的还原峰电流比其他循环圈的高出许多;从第2循环圈开始,还原峰电流明显下降,与第1循环圈相比,其还原峰电流密度衰减了17.18%;经20圈循环后,电流基本稳定,其电流密度与第1循环圈相比衰减了 27.97%,为 0.922 mA·cm-2;第50循环圈的电流密度与第20循环圈的接近,衰减仅为0.6%。
导致上述现象的原因是多方面的。一方面,蒙脱石具有孔隙结构,可明显增加电极的催化面积,提高了催化反应的效率,会使还原峰电流变大;另一方面,由于蒙脱石具有较好的吸附性能。当其置于溶液中达到吸附平衡后,吸附于WC/MMT电极表面的PNP浓度会明显高于其在溶液中的浓度,即复合材料电极的吸附性能能够使 PNP初步富集于电极表面,致使电催化还原过程的反应区间——电极表面的反应物浓度增大,导致第1循环圈的还原峰电流明显大于其他循环圈的还原峰电流。随着循环的进行,电极表面初步富集的PNP不断被催化还原,并逐步被消耗。此时,在电极表面被电催化还原的PNP来自两个方面,一是电极表面因吸附而初步富集的,二是从电解液中经扩散至电极表面的。由于电极表面预先富集的 PNP浓度随着反应的进行而逐步下降,PNP的电催化还原速度逐渐降低,还原峰电流稳步变小。这一过程相当于电催化还原的第1循环圈到第20循环圈。当电极表面初步富集的PNP基本被还原后,在电极表面被电催化还原的PNP均为从电解液中扩散至电极表面时,PNP被电催化还原的速度与其从电解液中的扩散速度相当,电催化还原反应基本稳定,还原峰电流没有明显变化,且随着溶液中PNP浓度的降低而变小。这相当于电催化还原的第20循环圈到第50循环圈。这充分说明WC/MMT材料对PNP的电还原具有较好的化学稳定性。
3 结 论
(1)以LiCl剥离后的蒙脱石为载体,以WCl6为钨源,将浸渍法和原位还原技术相结合制备了WC/MMT纳米复合材料。复合材料的物相以碳化钨和蒙脱石为主,蒙脱石的片层结构保留完好,碳化钨以纳米微晶的形式均匀地分布于蒙脱石外表面。
(2)WC/MMT纳米复合材料对对硝基苯酚具有良好的电催化还原作用,并有很好的化学稳定性。
(3)蒙脱石是碳化钨催化剂的良好载体,其特殊的片层结构和天然的表面电负性,有助于碳化钨纳米粒子在其表面分散;其良好的吸附性能有助于被催化对象的初步富集;其独特的孔隙结构不仅可增加电极的表面积,还可增大催化剂与反应物的接触概率,有利于催化反应的进行。蒙脱石的这些独特性质不仅可应用于碳化钨基复合催化剂的制备中,也可应用于其他复合催化材料的制备过程中。
[1] Böhm H. New non-noble metal anode catalysts for acid fuel cells [J].Nature, 1970, 227 (5257):483-484.
[2] Levy R B, Boudart M. Platinum-like behavior of tungsten carbide in surface catalysis [J].Science, 1973, 181 (4099):547-549.
[3] Palanker V Sh, Sokolsky D V, Mazulevsky E A, Baybatyrov E N.Catalytic activity and capacitance of tungsten carbide as a function of its dispersity and surface sate [J].Electrochim.Acta,1977, 22 (6):661-667.
[4] Zellner M B, Chen J G G. Surface science and electrochemical studies of WC and W2C PVD films as potential electrocatalysts [J].Catal.Today,2005, 99 (3/4):299-307.
[5] Mcintyre D R, Burstein G T, Vossen A. Effect of carbon monoxide on the electrooxidation of hydrogen by tungsten carbide [J].J.Power Sources, 2002, 107 (1):67-73.
[6] Meng H, Shen P K. Novel Pt-free catalyst for oxygen electroreduction[J].Electrochim.Commun., 2006, 8 (4):588-594.
[7] Ma Chun’an (马淳安), Tang Junyan (汤俊艳), Li Guohua (李国华),Sheng Jiangfeng (盛江峰). Preparation and electro-property of tungsten carbide/carbon nanotube composite [J].Acta Chim.Sinica(化学学报), 2006, 64 (20):2123-2126.
[8] Li Guohua (李国华), Tian Wei (田伟),Tang Junyan (汤俊艳), Ma Chun’an (马淳安). Preparation and electrocatalytic property for methanol oxidation of WC/CNT nanocomposite [J].Acta.Phys.-Chim.Sin. (物理化学学报), 2007, 23 (9):1370-1374.
[9] Wang Xiaojuan (王晓娟), Ma Chun’an (马淳安), Li Guohua (李国华), Shen Tianjun (沈田君). Preparation and electrocatalytic activity of WC/CNT nanocomposite for nitrobenzene electroreduction [J].Journalof Chemical Industry and Engineering(China) (化工学报),2008, 59 (11):2904-2909.
[10] Liu W M, Shi M Q, Lang X L, Zhao D, Chu Y Q, Ma C A. Highly dispersed nanocrystallines WC supported on microwave exfoliated RGO by ionic liquid and its catalytic performance in electroreduction of nitrobenzene [J].Catal.Today, 2013, 200:87-93.
[11] El-Eskandarany M S. Fabrication and characterizations of new nanocomposite WC/Al2O3materials by room temperature ball milling and subsequent consolidation [J].J.Alloys Compd., 2005, 391 (1/2):228-235.
[12] Hu S J, Shi B B, Yao G X, Li G H, Ma C A. Preparation and electrocatalytic activity of tungsten carbide and titania nanocomposite[J].Mater.Res.Bull., 2011, 46 (10):1738-1745.
[13] Ma Na (马娜), Ji Shengfu (季生福), Wu Pingyi (吴平易), Hu Linhua(胡林华), Nie Pingying (聂平英). Preparation, characterization and catalytic performance for hydrodesulfurization of WxC/SBA-16 catalysts [J].Acta Phys.-Chim.Sin. (物理化学学报), 2007, 23 (8):1189-1194.
[14] Tong Dongshen (童东绅), Xia Housheng (夏厚胜), Zhou Chunhui(周春晖). Designed preparation and catalysis of smectite clay-based catalytic materials [J].Chin.J.Catal. (催化学报), 2009, 30 (11):1170-1187.
[15] Varade D, Haraguchi K. Synthesis of active and thermally stable nanostructured Pt/clay materials by clay-mediatedin situreduction [J].Langmuir, 2013, 29 (6):1977-1984.
[16] Paek S M, Jang J U, Hwang S J, Choy J H. Exfoliation-restacking route to Au nanoparticle-clay nanohybrids [J].J.Phys.Chem.Solids,2006, 67 (5/6):1020-1023.
[17] Papp S, Dekany I. Stabilization of palladium nanoparticles by polymers and layer silicates [J].Colloid.Polym.Sci., 2003, 281 (8):727-737.
[18] Zhou Limei (周丽梅), Fu Haiyan (付海燕), Li Qiang (李强), Chen Huan (陈华), Li Ruixiang (李瑞祥), Li Xianjun (李贤均).Preparation of highly dispersed Ru/MMT catalyst and its catalytic activity for quinolone hydrogenation [J].Chin.J.Catal. (催化学报),2010, 31 (6):695-700.
[19] Fan M D, Yuan P, Chen T H, He H P, Yuan A H, Chen K M, Zhu J X,Liu D. Synthesis, characterization and size control of zerovalent iron nanoparticles anchored on montmorillonite [J].Chin.Sci.Bull., 2010,55 (11):1092-1099.
[20] Ma X C, Xu F, Chen L Y, Du Y, Zhang Z D. Fabrication of the stable adduct CdS/CTAB/Cly with sandwich-like nanostructures [J].J.Nanopart.Res., 2006, 8 (5):661-668.
[21] Hur S G, Kim T W, Hwang S J, Hwang S H, Yang J H, Choy J H.Heterostructured nanohybrid of zinc oxide-montmorillonite clay [J].J.Phys.Chem.B, 2006, 110 (4):1599-1604.
