药物洗脱球囊制备工艺探讨
2015-04-01刘国柱徐立霞时晓嫚李昕跃
刘国柱,徐立霞,时晓嫚,李昕跃
(大连大学 环境与化学工程学院,辽宁 大连 116622)
1977 年,瑞典医生Gruentzing 成功进行首例经皮冠状动脉腔内形成术(PTCA),标志着介入医学的开端。21 世纪初,药物洗脱支架(DES)的出现使PCI 术后的再狭窄率降至10%以内,取得了长足的进步,但再狭窄问题仍未彻底解决[1-3]。
近年来,出现了预防介入治疗术后血管再狭窄的新技术——药物洗脱球囊(DEB),已经取得初步临床应用效果[4]。DEB 是在球囊扩张术或球囊成形术等介入技术基础上发展起来的新型治疗性球囊药物释放技术,它是将抗血管内膜增生的药物涂置于球囊表面,当球囊到达病变血管壁并被撑开、扩张,与血管壁内膜接触时,通过撕裂血管内膜并加压快速释放、转移药物至局部血管壁内的技术,药物在局部起到抗血管内膜增生的作用,从而预防血管介入术后再狭窄[5-6]。目前认为,治疗血管介入术后再狭窄最有效的药物主要是紫杉醇-碘普罗美复合物(前者为抗组织增生药物、后者为载体分子),在球囊扩张的最初10 s 内药物释放进入血管壁的速度最快[7]。
本文以尼龙-12 球囊导管为材料,采用直接涂覆的方式制备紫杉醇药物洗脱球囊导管,考察了胶黏剂溶液浓度、紫杉醇溶液浓度、风干时间和风速对紫杉醇载药量的影响。
1 实验部分
1.1 试剂与仪器
紫杉醇、碘普罗胺、胶黏剂、无水乙醇均为分析纯;原料管生料管、尼龙-12 均为工业品。
药物球囊涂层机,自制;LC1000 型液相色谱仪;BP211D 电子天平;HK-250 超声波清洗器;Hitachi TM-1000 扫描电镜。
1.2 实验方法
药物洗脱球囊导管,主要由球囊、标志环、药物涂层、远端杆、导丝通道、近端杆及导管座6 部分组成(图1)。球囊位于远端杆末梢,可在建议压力下扩张到一定直径和长度;两个标志环位于球囊内,分别位于球囊的两个肩部,在血管内起显影定位作用;涂层药物为紫杉醇,位于球囊肩部之间的外表面;导丝通道位于远端杆内腔,可通过导引导丝。

图1 药物洗脱球囊导管示意图Fig.1 The schematic of drug-eluting balloon catheter
1.2.1 球囊的制备 原料管经拉伸、吹塑成型,制成半成品球囊。经标志环锻打、近远端焊接、Rx 口焊接、打褶、卷边,焗炉10 h 定型,制成成品球囊。用酒精擦拭干净,备用。
1.2.2 溶液的配制
1.2.2.1 胶黏剂溶液 用电子天平准确称取600 mg 胶黏剂,溶解到10 mL 无水乙醇中,搅拌30 min。
1.2.2.2 紫杉醇溶液 用电子天平准确称取30 mg碘普罗胺,100 mg 紫杉醇,溶解到8 mL 60%乙醇溶液中,超声振荡30 min。
1.2.3 涂覆 将胶黏剂溶液置于药物涂层机的1号样品管中,将球囊以所需的速度浸入到胶黏剂溶液中,停留一段时间后以一定的速度提拉出来,以特定的风速风干。上述步骤重复进行一次。
将紫杉醇溶液置于药物涂层机的2 号样品管中,将已涂好胶黏剂的球囊以同样的涂覆方式涂覆10 次。用酒精擦去球囊肩部标志环以外的涂药部分,打褶、卷边。
1.3 载药量检测
将样品扩张后剪下球囊,分别放入棕色瓶中,加入适量乙醇溶液浸提。将棕色瓶放入超声水浴中,处理10 min,在漩涡混合器中混合30 s。作为检验液。
紫杉醇的HPLC 检测方法,色谱柱为安捷伦C18(4.6 mm×250 mm,5 μm),柱温45 ℃,检测波长227 nm,进样量80 μL,流速1.2 mL/min,流动相为乙腈∶注射用水=60∶40。运行时间为10 min。
2 结果与讨论
2.1 胶黏剂浓度对紫杉醇药量的影响
胶黏剂溶液的浓度太小,则紫杉醇的药量达不到规定药量,且紫杉醇涂层粘结不牢固,易脱落。胶黏剂溶液浓度太大,则紫杉醇的药量超出规定药量,且药物的释放率也达不到要求。不同球囊规格时,胶黏剂溶液浓度对紫杉醇药量的影响见图2。药物球囊紫杉醇的规定药量为3 μg/mm2,3 015、3 020、3 520 的 球 囊 规 定 药 量 分 别 为 423,565,659 μg/mm2。
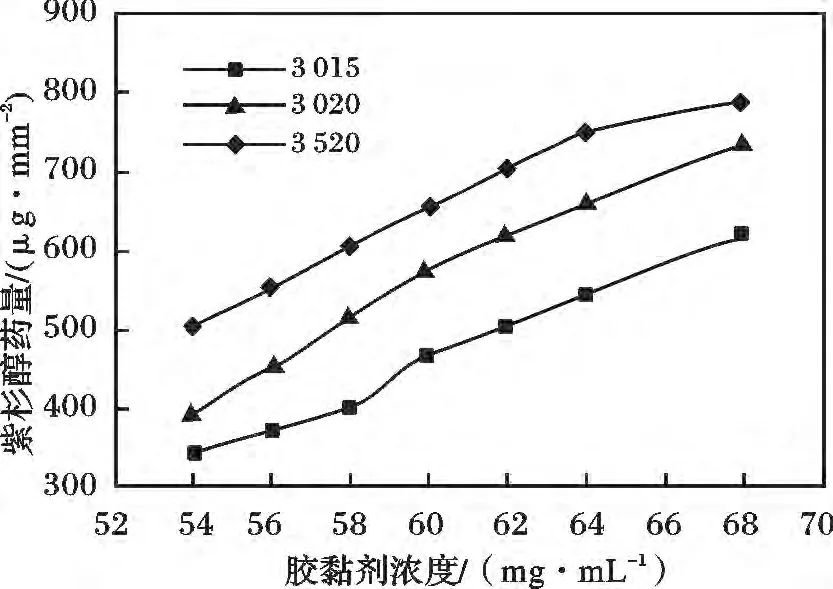
图2 胶黏剂溶液浓度对不同球囊规格紫杉醇药量的影响Fig.2 The effect of adhesive concentration on different balloon specifications of paclitaxel dosage
由图2 可知,不论球囊为何种规格,随着胶黏剂溶液浓度的增大,紫杉醇的药量逐渐增大,但是当黏剂溶液浓度超过64 mg/mL 时,紫杉醇的药量超过了规定药量,在治疗的过程中有可能引起副反应。当胶黏剂溶液浓度低于56 mg/mL 时,紫杉醇的载药量不足,导致治疗效果不好。由于每次涂覆时,紫杉醇的药量都存在一定的波动。故为了涂覆的药量在规定的范围内,胶黏剂溶液的最佳浓度为60 mg/mL。
2.2 紫杉醇溶液浓度对药量的影响
紫杉醇作为球囊的涂层药物,其浓度的大小直接影响到紫杉醇的药量。不同球囊规格时,紫杉醇溶液浓度对药量的影响见图3。
由图3 可知,不论球囊为何种规格,随着紫杉醇浓度的逐渐增大,药量也逐渐增大,但是当紫杉醇溶液浓度超过13.0 mg/mL 时,紫杉醇的药量超过了规定药量,在治疗的过程中有可能引起副反应。当紫杉醇溶液浓度<12.0 mg/mL 时,有可能紫杉醇的载药量不足,导致治疗效果不好。由于每次涂覆时紫杉醇的药量都存在一定的波动。故为了每次涂覆的药量都在规定的范围内,紫杉醇溶液的最适宜浓度为12.5 mg/mL。

图3 不同球囊规格时紫杉醇溶液浓度对药量的影响Fig.3 When the different balloon specifications paclitaxel solution concentration on the effect of the dosage
2.3 涂覆次数对紫杉醇药量的影响
涂覆次数对紫杉醇药量的影响见表1。
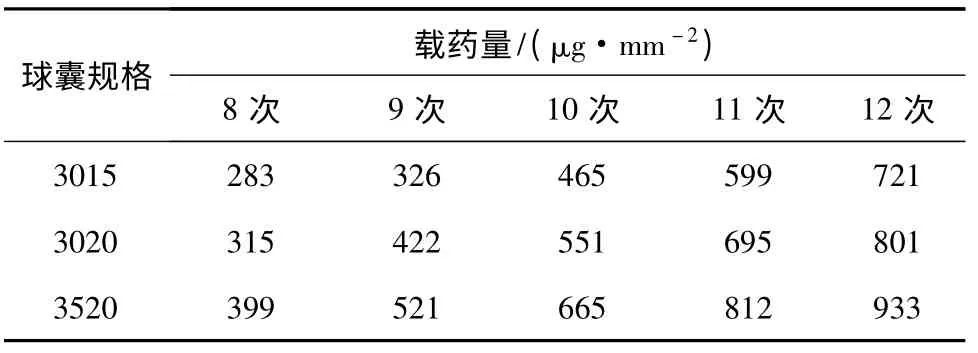
表1 涂覆次数与紫杉醇药量的关系Table 1 The relation of coating times and paclitaxel dose
由表1 可知,当涂覆次数为9 或11 次时,紫杉醇的药量不符合规定药量。涂覆10 次时,紫杉醇的药量符合规定药量。所以,确定紫杉醇的涂覆次数为10 次。
2.4 风速及风干时间对紫杉醇药量的影响
风速决定着药物球囊涂层的外观及均匀程度。风速过大,则涂层不均匀,风速过小,则涂层风干时间过长。选择5 m/s 的风速进行风干,风干时间对药量的影响见表2。

表2 风干时间与紫杉醇药量的关系Table 2 The relation of air-dry time and paclitaxel dose
由表2 可知,风干时间低于35 s 时紫杉醇的药量低于规定药量;风干时间长于35 s 时,紫杉醇的药量波动很小,且药量符合规定药量。所以,确定适宜的风速为5 m/s,风干时间为35 s。
2.5 表面形貌
用体视显微镜观察药物球囊涂覆前后的表面形貌,结果见图4。由图4 可知,未涂覆的球囊为透明状,涂覆后在球囊表面有一层白色的药物,可以起到治疗狭窄病变的作用。

图4 未涂覆的球囊(a)与涂覆后的球囊(b)外观对比Fig.4 Uncoated balloon (a)compared with the appearance of the coated balloon (b)
用扫描电镜观察药物球囊涂覆前后的表面形貌,结果见图5。
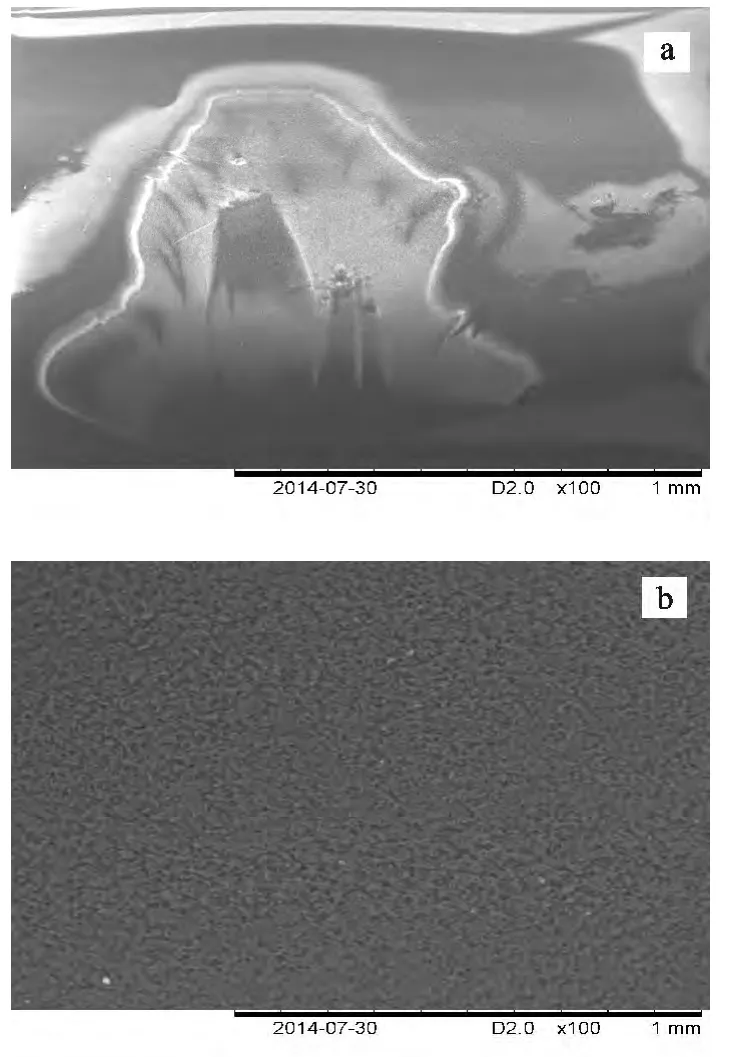
图5 未涂覆的球囊(a)与涂覆后的球囊(b)外观对比Fig.5 Uncoated balloon (a)compared with the appearance of the coated balloon (b)
由图5 可知,未涂覆的球囊表面光滑、出现反光,涂覆后的球囊表面呈现均匀的颗粒。
3 结论
(1)用胶黏剂和紫杉醇可以在尼龙-12 球囊表面制得紫杉醇药物涂层,而且药量符合规定。
(2)制备药物洗脱球囊的最适宜条件为:胶黏剂溶液浓度为60 mg/mL,紫杉醇的浓度为12.5 mg/mL,风速5 m/s,风干时间35 s。
[1] Maisel W H.Unanswered questions-drug-eluting stents and the risk of late thrombosis[J].New England Journal of Medicine,2007(356):981-984.
[2] Lemos P A,Hoye A,Goedhart D,et al.Clinical,angiographic,and procedural predictors of angiographic restenosis after sirolimus-eluting stent implantation in complex patients——An evaluation from the rapamycin-eluting stent evaluated at rotterdam cardiology hospital(RESEARCH)study[J].Circulation,2004 (109):1366-1370.
[3] Iofina E,Langenberg R,Blindt R,et al.Polymer-based paclitaxel-eluting stents are superior to nonpolymer-based paclitaxel-eluting stents in the treatment of de novo coronary lesions[J].The American Journal of Cardiology,2006(98):1022-1027.
[4] vander Giessen W J,Lincoff A M,Schwartz R S,et al.Marked inflammatory sequelae to implantation of biodegradable and nonbiodegradable polymers in porcine coronary arteries[J].Circulation,1996(94):1690-1697.
[5] Scheller B,Speck U,Abramjuk C,et al.Paclitaxel balloon coating,a novel method for prevention and therapy of restenosis[J].Circulation,2004(110):810-814.
[6] Kirtane A J,Gupta A,Iyengar S.Safety and efficacy of drug-eluting and bare metal stents comprehensive metaanalysis of randomized trials and observational studies[J].Circulation,2009(119):3196-3198.
[7] Radke P W,Joner M,Joost A.Vascular effects of paclitaxel following drug-eluting balloon angioplasty in a porcine coronary model:the importance of excipients[J].Eurointervention,2011(7):730-737.
