宣肺清热合剂质量标准的建立
2015-04-01陈群力周淑琴赵春草
陈群力 李 洁 杨 骏 周淑琴 赵春草 吴 飞
1.上海健康医学院药学院,上海 201318;2.上海市黄浦区香山中医医院药剂科,上海 200020;3.上海中医药大学中药现代制剂技术教育部工程研究中心,上海 201203
宣肺清热合剂是上海市黄浦区香山中医医院的医院制剂,处方由麻黄、黄芩、桑白皮、枳壳、浙贝母、桔梗、甘草、苦杏仁、鱼腥草9 味中药组成,主要用于治疗慢性支气管炎所致的痰黄、咳喘等症,长期的临床实践证明其宣肺止咳平喘效果显著[1-3],但制剂的工艺水平和质量控制不够合理[3-4],原质量标准仅有检查项。为更好地控制制剂质量、保证临床疗效,需建立定性鉴别和定量测定方法,提高质量控制水平,为其质量标准提高和修订提供依据[5-7]。
1 仪器与试药
1.1 仪器
高效液相色谱仪(Agilent 1200 型,美国安捷伦科技有限公司),半自动薄层点样仪(Linomat 5 型瑞典卡玛科技有限公司),分析天平(TE214S 型,0.1 mg,德国赛多利斯科技有限公司), 分析天平 (XP205 型,0.01 mg,瑞士梅特勒-托利多科技有限公司),超纯水机(Milli-Q 型,密理博中国科技有限公司),离心机(TGL-18C 型,上海安亭科学仪器厂),旋转蒸发仪(R2003KE 型,上海申生科技有限公司),干燥箱(DZF-6050 型号,上海一恒科技有限公司),电热套(PTHW型,巩义市予华仪器有限责任公司),pH 计(PHS-3E型,上海精密科学仪器有限公司)。
1.2 试药
黄芩苷对照品(批号:110715-201016),枳壳对照药材(批号:120981-200403),桑白皮对照药材(批号:121124-200903)均购自中国药品生物制品检定所。硅胶G 板购自烟台江友硅胶开发有限公司。 色谱纯乙腈、甲醇均购自美国Merck 公司;其余试剂均为分析纯,购自国药集团化学试剂有限公司。
宣肺清热合剂(批号分别为120607、120609 和120611,规格:200 mL/瓶)和阴性样品,均由上海市黄浦区香山中医医院药剂科提供。
2 方法与结果
2.1 薄层色谱鉴别
2.1.1 枳壳薄层鉴别[8]229-230取5 mL 样品,加水稀释至20 mL,用乙醚萃取2 次,每次20 mL,弃去乙醚液,合并水溶液,再用乙酸乙酯提取2 次,每次20 mL,合并乙酸乙酯提取液,水浴蒸干,残渣加甲醇1 mL 溶解,作为供试品溶液。取0.2 g 枳壳(麸炒)对照药材,加甲醇10 mL,超声处理30 min,滤过,滤液蒸干,残渣加甲醇5 mL 使溶解,作为对照药材溶液。
照薄层色谱法(《中国药典》2010 年版一部附录ⅥB)试验,吸取供试品溶液、对照药材溶液各5 μL,点于同一块硅胶G 板, 以三氯甲烷-乙酸乙酯-甲醇-水(15︰40︰22︰10)在5~10℃下放置12 h 后分取的下层液为展开剂,展开,取出,晾干,喷以3%三氯化铝乙醇溶液显色,105℃烘干, 在366 nm 下检视。 供试品色谱中,比移值(Rf)约0.4 的位置处显蓝黄色斑点,Rf 约0.6 的位置处显蓝色斑点。 同法制得的供试品阴性样品色谱中,未见有相应斑点。 见图1(封三)。
2.1.2 桑白皮薄层鉴别[8]280取5 mL 样品,加水稀释至20 mL,加盐酸调节pH 至1~2,过滤,滤液用乙酸乙酯振摇萃取2 次,每次20 mL,合并乙酸乙酯提取液,蒸干,残渣加1 mL 甲醇溶解,得供试品溶液。 取2 g 桑白皮对照药材,加20 mL 饱和碳酸氢钠溶液,超声20 min,滤过,滤液加盐酸调节pH 至1~2,静置30 min,滤过,滤液用乙酸乙酯振摇萃取2 次,每次20 mL,合并乙酸乙酯液,蒸干,残渣加1 mL 甲醇溶解,作为对照药材溶液。
照薄层色谱法(《中国药典》2010 年版一部附录ⅥB)试验,吸取供试品溶液、对照药材溶液各5 μL,点于同一块硅胶G 板,以二氯甲烷-甲醇(5︰1)为展开剂,展开,取出,晾干,在366 nm 下检视。 供试品色谱中,Rf 约0.8 的位置处显蓝黄色荧光斑点。 同法制得的供试品阴性样品色谱中,未见有相应斑点。 见图2(封三)。
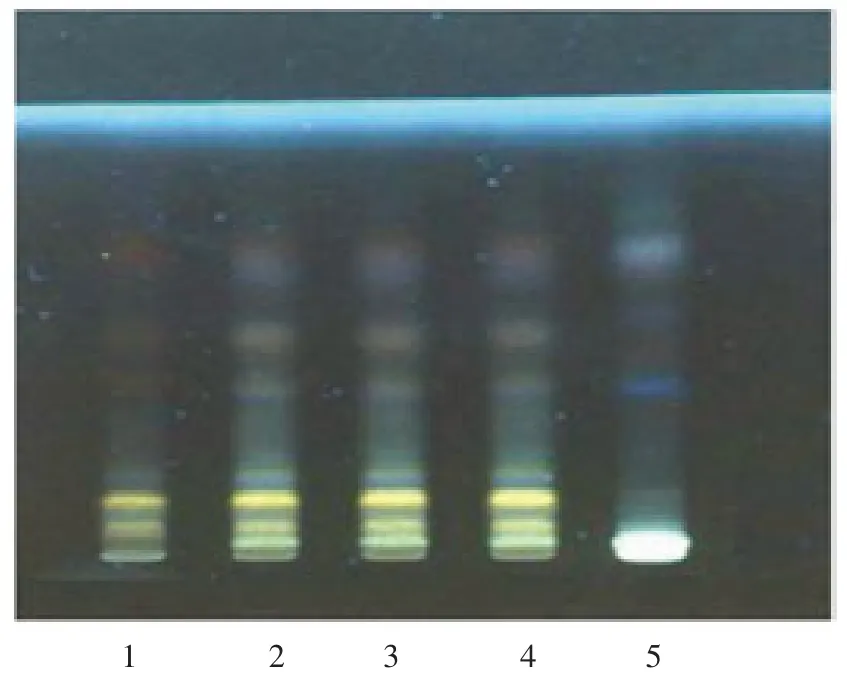
图1 宣肺清热合剂中枳壳的TLC 鉴别

图2 宣肺清热合剂中桑白皮的TLC 鉴别
2.2 黄芩苷含量测定
2.2.1 色谱条件 Kromasil C18色谱柱(4.6 mm×250 mm,5 μm),流动相为甲醇-水-磷酸(47︰53︰0.2),流速为1.0 mL/min,检测波长为280 nm,柱温为3℃,进样体积10 μL,理论塔板数以黄芩苷计不低于5000。
2.2.2 对照品溶液的制备 精密称取黄芩苷对照品适量, 以乙醇溶解, 制得浓度分别为259.44 μg/mL 和164.69 μg/mL 的黄芩苷对照品溶液。
2.2.3 供试品溶液的制备 精密量取宣肺清热合剂样品0.1 mL,置于10 mL 容量瓶中,加水至刻度,摇匀;取一部分溶液于塑料离心管内,以5000 r/min 的转速离心5 min,取上清液,以0.45 μm 微孔滤膜过滤,作为供试品溶液。
2.2.4 阴性样品溶液的制备 按照工艺制备宣肺清热合剂阴性样品(缺黄芩),按照“2.2.3”项下配制阴性样品溶液。
2.2.5 专属性试验 将黄芩苷对照品、供试品溶液和阴性样品溶液按“2.2.1”项下条件下分别进样,记录色谱图,黄芩苷的保留时间为13.4 min 左右(图3)。 高效液相色谱图显示在黄芩苷峰位处,阴性样品中无杂质干扰,方法专属性良好。
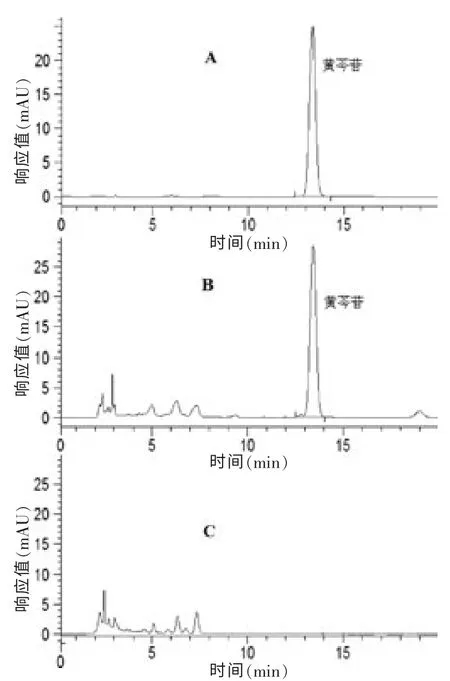
图3 宣肺清热合剂中黄芩苷高效液相色谱测定
2.2.6 线性关系考察 精密移取浓度为259.44 μg/mL的黄芩苷对照品溶液适量, 加乙醇制成浓度分别为3.24、32.43、64.86、97.29、129.72、194.58 和259.44 μg/mL的对照品溶液,分别进样10 μL,记录色谱图,以峰面积对黄芩苷的进样质量(μg)绘制标准曲线,线性回归方程为Y=3×106X-23 620,r = 0.9996。 结果表明,在0.032~2.59 μg 范围内,峰面积与黄芩苷进样质量呈良好的线性关系。
2.2.7 精密度试验 取浓度为64.86 μg/mL 黄芩苷对照品溶液,重复进样6 次,峰面积RSD 为0.08%,表明进样精密度良好。
2.2.8 稳定性试验 取宣肺清热合剂样品(批号120607),按“2.2.3”项下制备,于0、1、2、4、8、16 和24 h 进行测定,峰面积RSD 为0.9%,结果表明在24 h 内供试品溶液稳定性良好。
2.2.9 重复性试验 取宣肺清热合剂样品(批号120607),按“2.2.3”项下制备,平行处理6 份,测定峰面积,峰面积RSD 为1.9%,结果表明重复性良好。
根据外标法计算供试品溶液中黄芩苷的浓度为77.05 μg/mL,宣肺清热合剂中黄芩苷含量为7.70 mg/mL。2.2.10 回收率试验 取0.05 mL 宣肺清热合剂样品(批号120607,浓度7.70 mg/mL)9 份置于10 mL 容量瓶中,作为低、中、高水平组分别加入浓度为164.69 μg/mL的黄芩苷对照品2.0、3.0 和4.0 mL,每个浓度3 份,按照“2.2.3”项下操作,依次定容、摇匀、离心、过滤,进样测试,记录色谱图,计算黄芩苷各浓度水平的加样回收率。结果表明,平均加样回收率为100.08%,RSD 为1.6%,回收率符合要求。 见表1。

表1 黄芩苷含量测定加样回收试验结果
2.2.11 样品测定 按照上述验证的方法, 取不同批次的宣肺清热合剂测定黄芩苷的含量, 批号120607、120609 和120611 的样品中黄芩苷的含量分别为7.70、7.94、7.75 mg/mL。 按照3 批样品计算,以均值的80%作为含量下限[9-12],每瓶宣肺清热合剂中黄芩苷应不少于1240 mg。
3 讨论
已有研究通过建立制剂中麻黄碱和伪麻黄碱的高效液相色谱鉴定法来提高其质量控制水平[3,13]。 本研究针对方中另一味君药黄芩建立其指标性成分的含量测定方法,并进行了方法学验证,除此之外还对枳壳和桑白皮建立了定性鉴别的方法,有效提升了制剂的质量控制水平。
枳壳的薄层色谱鉴别试验中, 对于样品的前处理,药典和多数文献均是直接采用甲醇提取[14-17],本实验在研究过程中发现,简单的前处理无法避免阴性干扰,所以先采取乙醚萃取除杂,然后用乙酸乙酯萃取得到有效成分,制得符合要求的样品用以薄层色谱点样分析。实验中曾考察了以水溶性较好的柚皮苷作为对照品,但是在目前的展开条件下Rf 不到0.1,所以未设定此指标成分的对照鉴别。
桑白皮的鉴别试验中,药典中桑白皮药材的薄层色谱鉴别采用聚酰胺作为固定相,有研究采用硅胶G板作为固定相,展开剂类型各异[18-20]。本研究采用硅胶G 板作为固定相,对展开剂进行了优化,分别考察了乙酸乙酯-二氯甲烷-环己烷、 二氯甲烷-甲醇-乙酸乙酯-水、 二氯甲烷-甲醇、 二氯甲烷-甲醇-乙酸乙酯-水等作为展开剂,最后选定了二氯甲烷-甲醇作为展开剂。
在定性鉴别试验中,还考察了苦杏仁药材的薄层色谱鉴别方法[21-22]。 分别使用乙醚萃取除杂后正丁醇萃取、 乙酸乙酯萃取和氯仿萃取3 种方法制备样品,以药典方法[8]187-188制备对照药材(除了除杂溶剂为石油醚外,其余条件均不变),与苦杏仁苷对照品一起点样于硅胶G 板,以三氯甲烷-乙酸乙酯-甲醇-水(15︰40︰22︰10)5~10℃下放置12 h 分取下层作为展开剂,分别在紫外灯(366 nm)下直接检视,以磷钼酸硫酸溶液喷雾显色后检视(日光下和紫外灯366 nm 下)。实验结果表明,由于苦杏仁苷极性较小,无法从药材转移到制剂产品中,而对于对照药材来说,通过优化展开条件后仍不能有效排除阴性样品的干扰,故未建立鉴别方法。
基于有效的临床经验方开发医院制剂和提高现有医院制剂的质量控制水平是现代中药复方制剂研究政策支持的重要方向,也是研究的热点方向。 提高现有医院制剂质量控制水平的手段包括增加含量的测定指标,增加定性鉴别指标,将定性鉴别项提升为定量测定项,增加检查项,提高对检查项的控制水平等。 本研究课题组建议增加一些特殊的质量控制项目, 对一些传统制剂环节或技术的现代研究形成标准,如散剂的含量均匀度检查,贵重药材的混合均匀度检查等[23]。 基于有效的临床经验方进行医院制剂的开发进而进行中药新药的研发,也是上海等地的药品相关部门大力鼓励的药品研究方向[24]。 几十年来的中药新药研发观念认为, 提取工艺可以采用水提取、醇提取、水提取醇沉淀等方式,通过药效学或者正交试验的对比优选最佳工艺及参数。 本研究组认为,来自于临床经验方的中药制剂研发应受到更多的约束:制剂用药材应与临床用法保持一致(炮制及产地),制剂的提取工艺应与临床用法保持一致(提取溶剂和煎煮程度),药物服用特点也应与临床用法保持一致(服用时间、方法和频率)。
[1] 李洁,任世禾.慢性支气管炎的中医药治疗[J].吉林中医药,2012,32(8):786-788.
[2] 李洁,许伟英,朱虹,等.宣肺清热合剂治疗慢性支气管炎(痰热壅肺证)的临床观察[J].中成药,2013,35(8):1829-1830.
[3] 刘惠军,陈睿,王娟.HPLC 测定宣肺清热合剂中盐酸麻黄碱与盐酸伪麻黄碱含量[J].药学实践杂志,2010,28(3):199-201.
[4] 李仪奎.中药药理实验方法学[M].上海:上海科技出版社,1991:157-158.
[5] 魏引平,徐虹.从药材种植、饮片加工、质量标准三个重点环节谈中药质量管理[J].中国药事,2015,29(1):36-39.
[6] 仕海涛.扶正化积合剂质量标准研究[J].中国医药导报,2015,12(6):91-95.
[7] 李哲,常暖,李黎.中药院内制剂政策历史、现状及对策[J].中国中医药图书情报杂志,2014,38(1):38-41.
[8] 国家药典委员会.中国药典[S].一部.北京:中国医药科技出版社,2010.
[9] 吴承云,郑清明,周亚莉,等.试论中药制剂规格标示的合理性及规范性[J].中国药事,2012,26(1):47-49.
[10] 周跃华.中药新药质量标准研究中常见问题浅析[J].中成药,2004,26(11):972-975.
[11] 周跃华.浅谈中药新药质量标准研究的特点及常见问题[J].中国中医药信息杂志,2008,15(9):1-4.
[12] 马秀璟,张永文,阳长明.中药新药申请生产药学审评中的常见问题及建议[J].中国中药杂志,2014,39(17):3395-3398.
[13] 李军.气管炎合剂质量标准研究[J].辽宁中医药大学学报,2015,17(3):43-45.
[14] 王发英,徐欢,杨武亮,等.枳壳质量标准研究[J].中成药,2009,31(12):1897-1901.
[15] 魏良兵,吴溪,杜红芳,等.枳壳健胃颗粒的质量控制研究[J].中国中医药信息杂志,2013,20(1):54-56.
[16] 喻丽元,任斌,张俊鹏.气滞通胶囊中枳壳的鉴别与含量测定[J].中山大学学报(医学科学版),2008,29(3S):31-32.
[17] 周毅,蒋东旭,冯彪,等.东风桔口服液的薄层色谱鉴别[J].中药新药与临床药理,2005,16(2):124-126.
[18] 贺云杰,赵晨,李妍,等.参附强心丸中人参、大黄、桑白皮的薄层色谱鉴别及乌头碱限度检查[J].世界科学技术—中医药现代化,2009,11(3):468-471.
[19] 张锦兴,李运景,李卓亚,等.清肺合剂薄层色谱鉴别研究[J].亚太传统医药,2013,9(6):30-31.
[20] 段志涛,高英,周刚.桑白皮药材的质量标准研究[J].中药材,2013,36(4):553-557.
[21] 刘倩,陈金月,文隽,等.麻杏二陈汤煮散质量标准[J].中国实验方剂学杂志,2015,21(9):71-73.
[22] 李改茹,刘玉花,常军民,等.天山花楸平喘胶囊的质量标准研究[J].中成药,2014,36(1):106-111.
[23] 王瀛峰,张继全,赵春草,等.中药贵重药材的等量递增混合法实践[C]//第十二届全国青年药学工作者最新科研成果交流会论文集. 北京: 中国药学会,2014:389-395.
[24] 上海市科学技术委员会.上海市2013 年度“科技创新行动计划”医学与农业领域项目指南[Z].http:// www.stcsm.gov.cn/gk/ywgz/tzgs/ktsbzn/331966.htm.
