完全腹腔镜脾切除联合贲门周围血管离断术在肝硬化门脉高压症中的应用
2015-03-27张安元康世洲吴涯昆
张安元,康世洲,吴涯昆
(1.重庆市荣昌县人民医院,重庆,402460;2.遂宁市中心医院)
在我国,各种原因导致的肝硬化患者人数众多。肝硬化在失代偿期主要表现为门静脉高压为主的系列临床综合征,而消化道出血及脾肿大、脾功能亢进是门静脉高压的两大严重并发症。脾切除联合贲门周围血管离断术(splenectomy and esophagogastric devascularization,SED)因具有阻断上消化道出血效果确切、部分改善肝功能、术后肝性脑病发生率较低及同时纠正脾功能亢进等优点,是目前治疗门静脉高压症患者上消化道出血与脾功能亢进的主要外科方法[1]。但传统开腹手术创伤较大,对患者肝功、术后恢复影响较大。随着近年腹腔镜技术的发展,超声刀、血管闭合切割系统(LigaSure)及腔内直线切割闭合器(Endo-GIA)等腹腔镜器械的应用,逐渐出现手助腹腔镜或完全腹腔镜巨脾切除及贲门周围血管离断术的报道[2-6]。2013年1月至2014年7月我院为25 例肝硬化门静脉高压患者分别行完全腹腔镜与开腹脾切除及贲门周围血管离断术。现将资料报道如下。
1 资料与方法
1.1 临床资料 2013年1月至2014年7月我们将25 例肝硬化门静脉高压患者随机分为两组,分别行完全腹腔镜及开腹脾切除及贲门周围血管离断术(手术方式的选择术前均征得患者及家属知情同意)。腹腔镜组包括乙肝后肝硬化8例,丙肝后肝硬化2 例,酒精性肝硬化3 例,不明病因肝硬化1 例。术前有上消化道出血史12 例,胃镜证实食管下段胃底静脉重度曲张13 例。开腹组中乙肝后肝硬化7 例,酒精性肝硬化2 例,丙肝后肝硬化1 例,自身免疫性肝硬化1 例。术前有上消化道出血史9 例,胃镜证实食管下段或胃底静脉重度曲张8 例。两组患者性别、年龄、合并症、术前肝功能分级、脾脏大小等差异均无统计学意义,具有可比性(P>0.05)。见表1。
表1 两组患者术前一般资料的比较(±s)
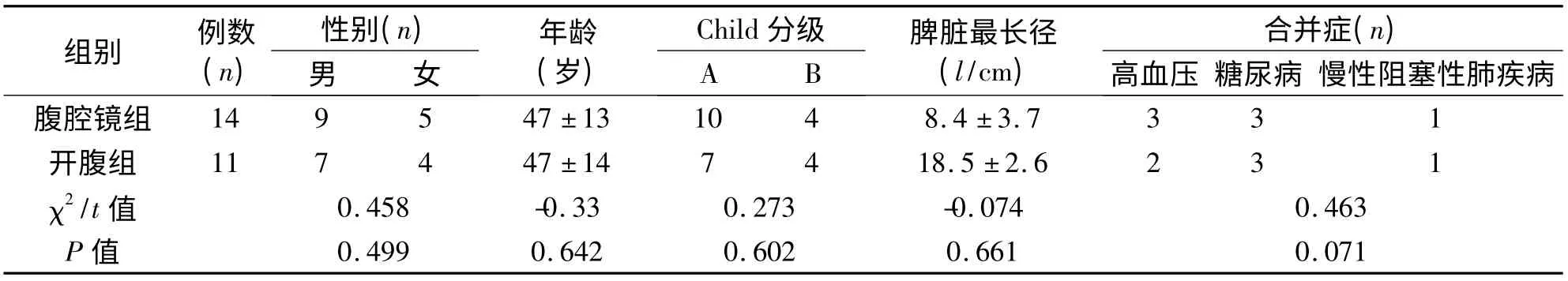
表1 两组患者术前一般资料的比较(±s)
?
1.2 纳入标准 术前经CT 或穿刺活检证实为肝硬化、门静脉高压症;有上消化道出血史,胃镜证实食管下段胃底静脉重度曲张或红色征;影像学检查提示脾肿大,血常规WBC <3 ×109/L,PLT <50 ×109/L;肝功能Child-Pugh 分级为A 级或B 级,或C 级经治疗恢复至A~B 级,无严重心肺疾病及合并症,能耐受腹腔镜或开腹手术。合并肿瘤、肝功能Child-Pugh 分级为C 级不易纠正、存在严重凝血功能障碍、有上腹部手术史或原发性腹膜炎病史视为手术禁忌证[7]。
1.3 手术方法
1.3.1 腹腔镜组 (1)体位与操作孔的建立:患者气管插管全身麻醉,左腰背部垫高、右斜卧位。于肚脐下缘切开皮肤穿刺10 mm Trocar,建立气腹并作为腹腔镜观察孔,分别于左锁骨中线、脐水平线上及剑突下2~3 cm 处穿刺10 mm Trocar作为主操作孔,于左腋前线、脾下极下方穿刺5 mm Trocar作助手辅助操作孔。主刀立于患者右侧,助手立于患者左侧,手术时手术床右倾约30 度。(2)脾脏切除:牵引胃及大网膜,应用超声刀逐步离断胃结肠韧带,在胰腺上方脾动脉起始处分离脾动脉主干,用4 号丝线双重结扎或用Hem-o-lok 夹夹闭。自脾下极开始应用超声刀离断脾结肠韧带、脾肾韧带,切开覆盖脾蒂的腹膜、分离二级脾蒂,Hem-o-lok夹夹闭增生曲张的血管并用超声刀离断,逐支分离出脾动、静脉(图1)。左手用吸引器将脾脏向上顶,暴露脾膈韧带后用超声刀逐步离断,往上分离出胃短血管后予以夹闭、切断。分离脾蒂周围组织,直至脾蒂完全暴露,Endo-GIA 钳夹脾蒂、切断,至完全切除脾脏(图2)。(3)贲门周围血管离断:离断小网膜后,将胃向左上方牵拉,用超声刀或Hem-o-lok 夹离断胃左血管及其以上曲张静脉,包括高位食管支、异位食管支、穿支静脉和左膈下静脉。离断膈下食管前浆膜,分离至食管下段6~8 cm,逐一将食管外曲张的静脉夹闭离断,注意离断血管时紧贴胃壁且勿伤及浆膜。将脾脏装入标本袋,经脐左侧操作孔提出标本袋前端,延长切口至3~5 cm,用血管钳和剪刀将脾剪成小块后取出。重新建立气腹,彻底冲洗腹、盆腔,检查无出血后,脾窝放置24 号橡胶引流管1 根。
1.3.2 开腹组 取左肋缘下切口或左上腹反“L”形切口,常规方法行脾切除后再行贲门周围血管离断术。
1.4 观察指标 观察两组患者手术时间、术中出血量、术后第1 天疼痛指数、肠功能恢复时间、术后住院时间及并发症发生情况。疼痛指数评分标准:依照国际视觉模拟量化表,0~10 代表不同程度的疼痛。0 为无疼痛,1~3 为轻度疼痛,4~6 为中度疼痛,7~9 为重度疼痛,10 为剧痛[8]。
1.5 统计学处理 采用SPSS 17.0 统计学分析软件对数据进行分析处理。计量资料用(±s)表示,行组间t 检验;计数资料采用χ2检验。P <0.05 为差异有统计学意义。
2 结 果
腹腔镜组1 例分离脾动脉时脾静脉损伤出血从而影响腹腔镜操作视野,1 例用Endo-GIA 切割闭合一级脾蒂后切割闭合器无法松开,导致中转开腹,余12 例均于完全腹腔镜下完成手术。开腹组按常规手术方法均顺利完成手术。腹腔镜组与开腹组手术时间差异无统计学意义(P >0.05),腹腔镜组术中出血量、住院时间少于开腹组,两组相比差异有统计学意义(P <0.05)。术后第1 天疼痛指数、肠功能恢复时间腹腔镜组优于开腹组;两组术后并发症主要包括发热、腹水、出血、胸腔积液、切口感染及门静脉系统血栓等,并发症发生率两组差异有统计学意义(P <0.05),见表2。术后两组均无因出血再次手术及死亡病例,术后第7 天复查血常规,WBC 均>3×109/L,PLT >50 ×109/L。
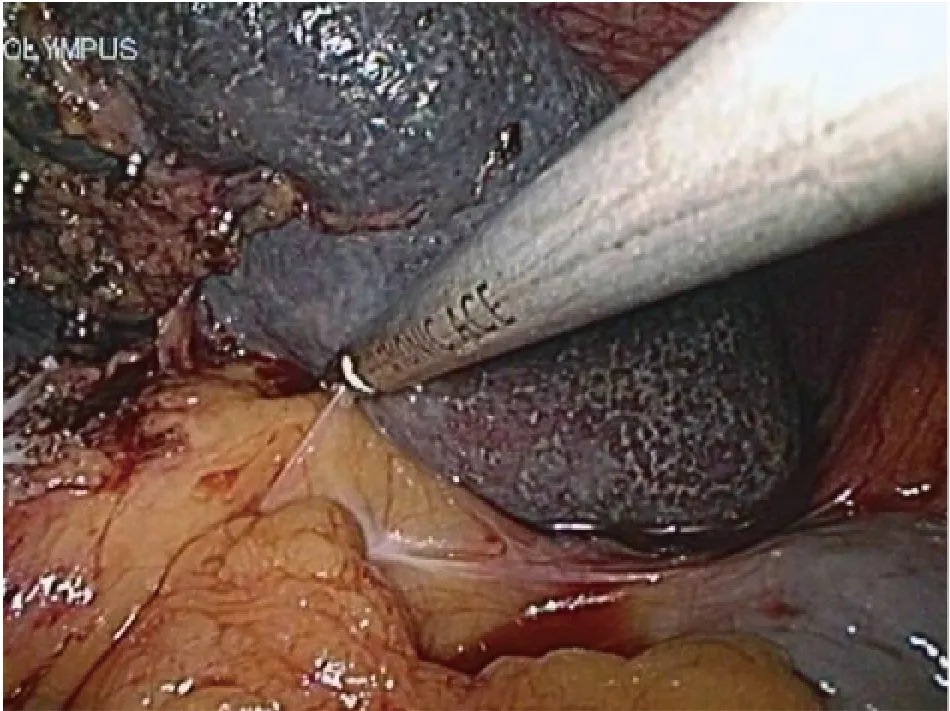
图1 超声刀分离脾周韧带
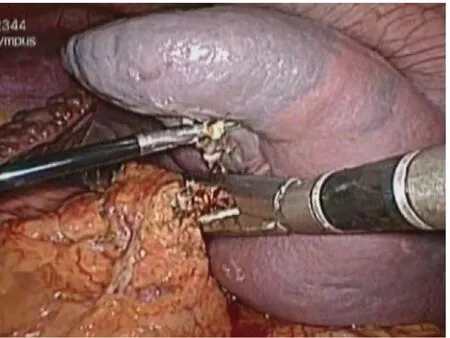
图2 腔内直线切割闭合器切断脾蒂
表2 两组患者术中及术后情况的比较(±s)
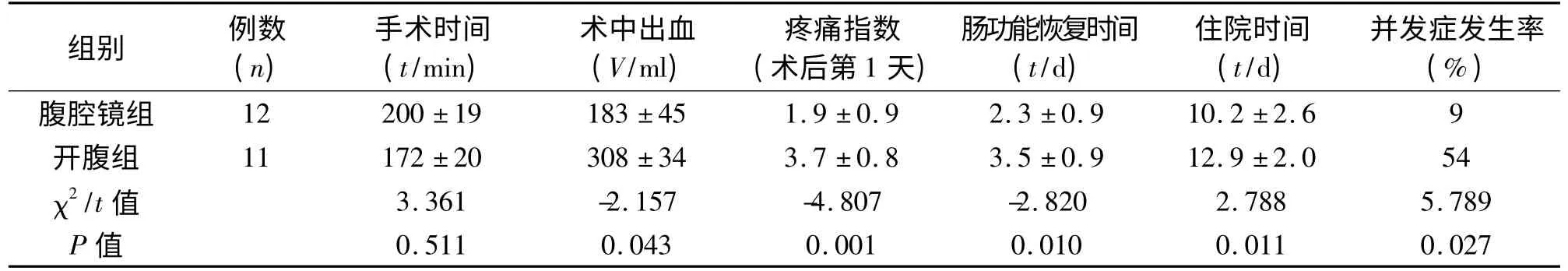
表2 两组患者术中及术后情况的比较(±s)
?
3 讨 论
门静脉高压症的是临床常见症状,而肝硬化尤其肝炎后肝硬化是门静脉高压症的高危因素[5,9]。肝硬化门静脉高压症患者在失代偿期通常会反复出现上消化道出血、脾肿大、腹水、呕血、黑便等症状,严重者可能因消化道大出血而死亡[10]。因此,对于治疗门静脉高压症,不仅要缓解临床症状,更需要积极预防消化道出血。裘法祖院士于1981年首先在国内提倡开展贲门周围血管离断术治疗门静脉高压症导致的上消化道出血,经过30 多年的发展,脾切除联合贲门周围血管离断术仍是目前治疗门静脉高压症患者上消化道出血、脾功能亢进的主要外科方法[1,11]。但由于门静脉高压症患者存在肝硬化基础病变,术前肝功能较差,凝血机制障碍,而且后腹膜曲张血管壁薄、压力高,因此传统开腹手术创伤较大,对患者肝功、术后恢复影响较大,手术风险很高[12]。
由于肝硬化门静脉高压症患者脾脏体积较大,且门奇静脉交通支血管增生、迂曲导致腹腔镜脾切除术治疗门静脉高压症手术操作难度较大,门静脉高压症也曾被欧洲内镜外科学会列为腹腔镜脾切除术的相对禁忌证[4]。近年,随着腹腔镜微创外科技术的发展及腹腔镜器械的改进,国内外较多微创中心逐渐开展了手助腹腔镜及完全腹腔镜脾切除联合贲门周围血管离断术,并初步证明了其安全性、有效性[2-6,13]。
本研究为25 例肝硬化门静脉高压患者行完全腹腔镜及开腹手术,通过对比分析发现两组手术时间差异无统计学意义,但腹腔镜组术中出血量少于开腹组,术后住院时间短,并发症发生率低,肠功能恢复及疼痛指数均优于开腹组,也证实了完全腹腔镜脾切除联合贲门周围血管离断术是安全、可行且有效的。在开展此术式初期,还是会面临较大的困难与风险。我们的初步体会是在围手术期及术中操作方面需注意以下问题:(1)病例的选择:除满足纳入标准的条件外,我们认为脾脏大小对手术难度及成功影响较大。有学者认为,完全腹腔镜脾切除的脾脏长径应<22 cm[14],但门静脉高压患者的脾脏大多数情况下体积均较大;也有学者认为脾脏长径<25 cm,或下极不超过脐水平、内侧不超过正中线时,行此手术是完全可行的。如果脾脏超过此范围,则可能影响腹腔镜Trocar 的置入及手术的操作[7,15]。(2)术中操作:众所周知,此手术最大的风险及成功的关键为术中难以控制的出血。因此术中需特别注意动作轻柔,一旦撕裂脾脏被膜、小静脉或脾静脉等造成出血时,手术视野会受到极大的影响。术中应常规分离出脾动脉并结扎,从而减少脾脏血流使脾脏缩小,利于脾脏的分离。分离脾蒂时,可采用一级脾蒂法与二级脾蒂法相结合,如二级脾蒂较细,可予以丝线结扎或Hem-o-lok 血管夹夹闭后逐渐离断;当脾蒂较粗大,分支结扎血管困难时可分离脾蒂后在远离胰尾、靠近脾门处用Endo-GIA 切割闭合离断。但使用一级脾蒂法时需注意切割闭合器尖端一定要穿过脾蒂后方,且钳夹处组织不得有丝线或血管夹等。本研究中腹腔镜组1 例患者Endo-GIA 切割脾蒂后无法松开,中转开腹后发现是脾蒂处有结扎分支血管的丝线卡入Endo-GIA 的钉仓所致;(3)术野清晰时,仔细检查有无副脾存在,有则一并切除;(4)预防并发症:术后常见并发症主要有发热、腹水及门静脉血栓等。除一般的术后治疗外,术后第2 天我们开始在无明显出血倾向的情况下常规使用低分子肝素钙皮下注射3~5 d,复查血PLT>300 ×109/L 时,开始口服抗凝剂,以预防门静脉系统血栓的发生;术后早期纠正低蛋白血症利于减少腹水的发生及切口的愈合。
总之,经过选择的肝硬化门静脉高压症患者,完全腹腔镜脾切除联合贲门周围血管离断术可有效治疗肝硬化门静脉高压引起的上消化道出血,改善脾功能亢进症状,与传统开腹手术相比,具有创伤小、术中出血少、术后并发症发生率低、康复快、住院时间短等优点,在外科治疗门脉高压症中是安全、可行、有效的,值得临床进一步推广。
[1]姚英民,张朋飞,郑鑫.腹腔镜脾切除联合贲门周围血管断流术和术后常见的并发症及处理原则[J/CD].中华临床医师杂志(电子版),2013,7(20):9019-9022.
[2]洪德飞,郑雪咏,彭淑牖,等.完全腹腔镜巨脾联合贲门周围血管离断术治疗门静脉高压症[J].中华医学杂志,2007,87(12):820-822.
[3]Koshenkov VP,Németh ZH,Carter MS. Laparoscopic splenectomy:outcome and efficacy for massive and supramassive spleens[J].Am J Surg,2012,203(4):517-522.
[4]Habermalz B,Sauerland S,Decker G,et al.Laparoscopic splenectomy:the clinical practice guidelines of the European Association for Endoscopic Surgery (EAES)[J].Surg Endosc,2008,22(4):821-848.
[5]刘金钢,田忠.腹腔镜脾切除贲门周围血管离断术应用及其评价[J].中国实用外科杂志,2010,30(3):183-186.
[6]Hama T,Takifuji K,Uchiyama K,et al.Laparoscopic splenectomy is a safe and effective procedure for patients with splenomegaly due to portal hypertension[J].J Hepatobiliary Pancreat Surg,2008,15(3):304-309.
[7]姚英民,郑鑫.腹腔镜治疗门静脉高压症现状[J].中国普外基础与临床杂志,2013,20(1):4-9.
[8]蒋国庆,陈平,钱建军,等. 改良腹腔镜脾切除联合断流术在门脉高压症老年患者中的应用[J]. 中华肝胆外科杂志,2014,20(3):205-207.
[9]Zheng X,Liu Q,Yao Y.Laparoscopic splenectomy and esophagogastric devascularization is a safe,effective,minimally invasive alternative for the treatment of portal hypertension with refractory variceal bleeding[J].Surg Innov,2013,20(1):32-39.
[10]Zhou J,Wu Z,Cai Y,et al.The feasibility and safety of laparoscopic splenectomy for massive splenomegaly:a comparative study[J].J Surg Res,2011,171(1):e55-60.
[11]董瑞,杜锡林,王青,等.腹腔镜脾切除联合断流术治疗门静脉高压症[J].中华普通外科杂志,2014,29(2):105-107.
[12]王钊,洪德飞,司亚卿.完全腹腔镜脾切除断流术治疗肝硬化门静脉高压症[J].中华普通外科杂志,2012,27(5):353-356.
[13]Kawanaka H,Akahoshi T,Kinjo N,et al.Technical standardization of laparoscopic splenectomy harmonized with hand-assisted laparoscopic surgery for patients with liver cirrhosis and hypersplenism[J].J Hepatobiliary Pancreat Surg,2009,16(6):749-757.
[14]贺新新,罗汉传,陆文奇,等.腹腔镜与开腹脾切除联合贲门周围血管离断术的对比研究[J].中华肝胆外科杂志,2013,19(11):864-866.
[15]吕金利,李雪平,杨世伟,等.腹腔镜下巨脾切除联合贲门周围血管离断术15 例[J].中国微创外科杂志,2013,13(5):406-408.
