快速灵敏检测水中Fe(Ⅲ)的化学发光传感体系研究*
2015-03-26耿方兰赵利霞
耿方兰,赵利霞
(中国科学院 生态环境研究中心 环境化学与生态毒理国家重点实验室,北京100085)
0 引 言
铁是自然界中含量第二的金属元素,对整个生态系统有着十分重要的作用[1]。作为水质分析的常规程序,铁离子的检测方法多有报道。由于传统的比色法灵敏度较低,不能满足分析要求,因此,新方法的研究一直备受关注,如原子吸收分光光度法、离子色谱与化学发光联用技术[2]、电感耦合—等离子质谱(ICP-MS)[3]、电化学[4]以及一些包括荧光和化学发光在内的光谱法等。氨基罗丹明作为荧光探针,Fe(Ⅲ)与KI 反应生成的I-3可以将探针的荧光淬灭,从而实现检测目的,虽然检测限较低,但是体系较为复杂且特异性较差[5];Ussher S J 等人[6]使用化学发光法检测Fe(Ⅲ),但是预处理过程较为繁琐。因此,构建简单快捷,灵敏特异的Fe(Ⅲ)检测体系十分必要。
本实验室用化学发光手段对碳点光学性质进行研究,发现碳点不加入任何氧化剂或者化学发光试剂,仅仅是强碱性的条件下,就可以产生化学发光,对这一现象的机理进行了研究[7]。
本文对碳点—NaOH 化学发光体系进一步研究发现,在所检测水体中的金属离子中发现,仅将Fe(Ⅲ)加入上述体系之后,体系的化学发光强度有明显的增强,在此基础上构建了Fe(Ⅲ)的化学发光传感检测体系。建立了Fe(Ⅲ)检测的标准曲线,并对三种不同实际水样进行了加标回收测定。最后,对此体系化学发光机理进行了推测。
1 实 验
使用BPCL 超微弱化学发光分析仪与配套滤光片(中国科学院生物物理研究所)构建静态注射化学发光检测体系。将100 μL 碳点溶液和100 μL 样品(或标准溶液)加入反应杯中,100 μL NaOH 通过微量进样器注射进入反应杯,以光电倍增管(PMT)放大信号后,传输至信号检测器。图1为静态注射装置示意图。
2 结果与讨论
2.1 碳点的合成与表征
称取1 g 葡萄糖与2 g PEG1500 放入50 mL 的烧杯中,加入7 mL 超纯水,用微波炉高火加热15 min,冷却后加入10 mL 超纯水稀释,之后将稀释液用MWCO2000 透析袋用超纯水透析10 天左右以去除未反应的原材料和反应过程中产生的其他杂质,得到深棕色胶体溶液。在高分辨透射电镜下观察,合成的碳点类似球形,粒径较为均一。粒径范围为4.5 ~6.5 nm,平均粒径在5.4 nm 左右。在不同波长的激发光激发下,碳点的荧光发射强度呈现先增加后降低的现象,同时荧光光谱也随激发光波长的增加而发生红移。
2.2 化学发光检测Fe(Ⅲ)体系的建立
碳点在强碱存在条件下即可产生化学发光,当向碳点—NaOH 体系中加入Fe(Ⅲ)之后,此体系的化学发光信号明显增强(见图2(a));而且,此信号随着Fe(Ⅲ)浓度的变化而变化。对其他十种不同金属离子进行筛查,如图2(b)所示,Fe(Ⅲ)能够特异性增敏碳点—NaOH 化学发光体系。
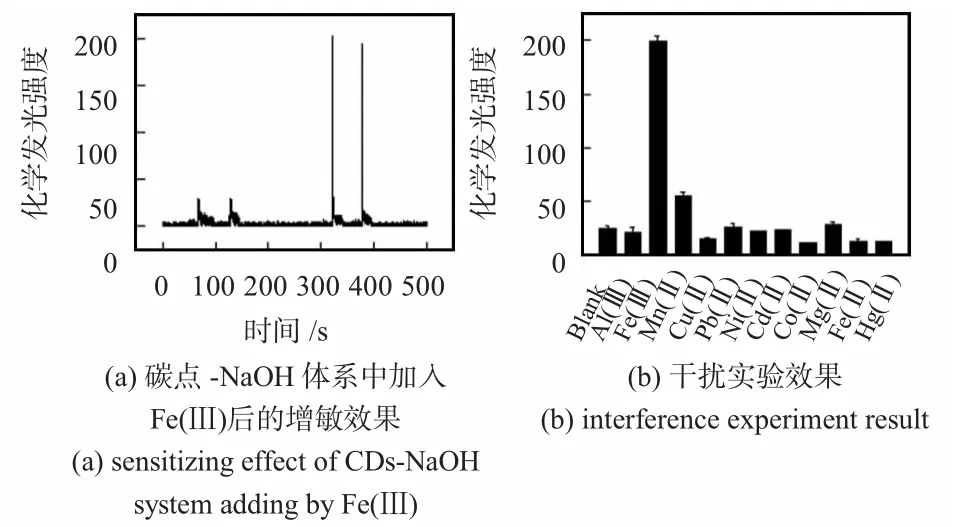
图2 碳点—NaOH 体系中加入Fe(Ⅲ)后的增敏效果与干扰实验结果Fig 2 Sensitizing effect of CDs-NaOH system adding by Fe(Ⅲ)and interference experiment result
基于上述实验结果,经过条件优化实验,得出碳点浓度为1 mg/mL,NaOH 浓度为0.1 mol/L 为最优条件,建立了Fe(Ⅲ)的化学发光传感检测体系。图3 所示为传感检测体系的标准曲线。线性范围为2×10-6~2×10-3mol/L,最低检测限1.45×10-6mol/L。
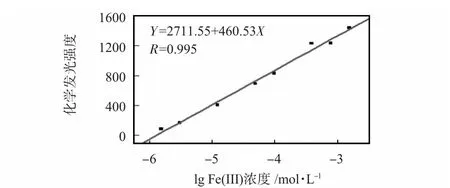
图3 Fe(Ⅲ)检测的标准曲线Fig 3 Standard curve of Fe(Ⅲ)detection
对三种不同类型的实际水样进行了加标回收测定,见表1。从表中能够看到三种不同类型水样中加标回收率分别为117%,111%,94%,均能满足要求。

表1 三种实际水样加标回收测定结果Tab 1 Labelling and recovery test results of three kinds of practical water samples
与目前常用的Fe(Ⅲ)检测方法相比较,上述方法具有灵敏度高、特异性好、检测方便快捷、成本低的优势,为其实际应用创造了条件。
2.3 碳点—NaOH—Fe(Ⅲ)体系化学发光机理研究
利用不同波长的滤光片(460,475,490,505,535,555,575,590,605 nm)对碳点—NaOH—Fe(Ⅲ)体系的化学发光光谱进行测定。结果如图4 所示。图中化学发光波长范围为480 ~580 nm 之间,最大化学发光波长为530 nm。与碳点的荧光光谱基本一致,说明此体系化学发光物质为碳点。最大化学发光波长525 nm 相较于荧光光谱的480 nm 发生明显红移,这可能是由于荧光主要表现的是纳米颗粒核态性质,而化学发光反应的是纳米颗粒的表面过渡态特性[8,9]。
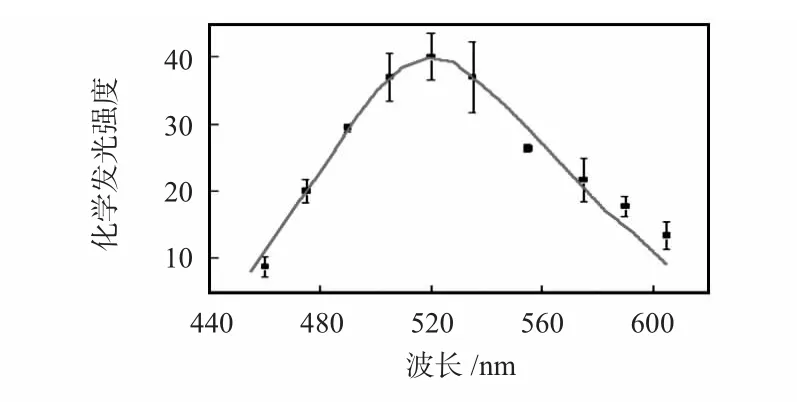
图4 碳点—NaOH—Fe(Ⅲ)化学发光体系化学发光光谱Fig 4 CL spectrum of CDs—NaOH—Fe(Ⅲ)system
已有文献报道碳点表面存在单电子轨道,既能作为电子受体,又能作为电子供体[10]。此体系中碳点化学发光很可能是由于碳点表面得失电子引起的电子空穴复合作用。实验室之前的工作证明,NaOH 化学还原作用可以向碳点表面注射电子,此时碳点作为电子受体[7]。Fe(Ⅲ)作为铁的高价态,具有一定的氧化作用。所以,本文推测在此化学发光体系中,Fe(Ⅲ)可能充当氧化剂而向碳点表面注射空穴。这种状态下,碳点表面的空穴比单纯热激发产生的空穴量应该高。所以,碳点—NaOH—Fe(Ⅲ)的体系化学发光强度较碳点—NaOH 体系高。
综上所述,如图5 所示,推测碳点—NaOH—Fe(Ⅲ)体系的化学发光是由于Fe(Ⅲ)作为氧化剂得电子而向碳点表面注射空穴,而NaOH 以化学还原作用方式向碳点表面注射的电子,空穴与电子复合的过程产生化学发光。
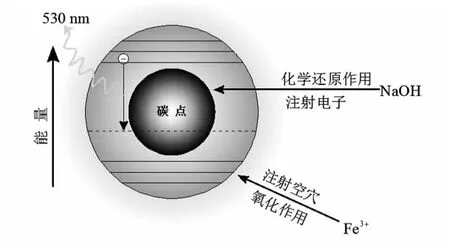
图5 碳点—NaOH—Fe(Ⅲ)体系化学发光原理图Fig 5 Principle of CL of CDs—NaOH—Fe(Ⅲ)system
3 结 论
本文研究采用化学发光法对微波水热反应合成的碳点进行光学性质研究,发现Fe(Ⅲ)可以特异性增敏碳点—NaOH 体系的化学发光信号,以此构建了碳点—NaOH—Fe(Ⅲ)化学发光传感检测体系,实现了快速便捷的高灵敏特异性检测实际水样中的Fe(Ⅲ),并且对体系中碳点的化学发光机理进行了初步研究,认为是Fe(Ⅲ)作为氧化剂向碳点表面注射的空穴与NaOH 化学还原作用注射的电子相复合而产生化学发光。
[1] Cabon J Y,Giamarchi P,Bihan A Le.Determination of Fe in seawater by electrothermal atomic absorption spectrometry and atomic fluorescence spectrometry:A comparative study[J].Analy-tica Chimica Acta,2010,664(2):114-120.
[2] Chen Yun-chieh,Jian Yu-ling,Chiu Kong-hwa,et al.Simultaneous speciation of Fe(II)and Fe(Ⅲ)by ion chromatography with chemiluminescence detection[J].Analytical Sciences,2012,28:795-799.
[3] Lacan Francois,Radic Amandine,Labatut Marie,et al.High-precision determination of the isotopic composition of dissolved Fe in Fe depleted seawater by double spike multicollector-ICPM-S[J].Analytical Chemistry,2010,82:7103-7111.
[4] Shervedani R K,Akrami Z.Gold-deferrioxamine nanometric interface for selective recognition of Fe(Ⅲ)using square wave voltammetry and electrochemical impedance spectroscopy methods[J].Biosensors and Bioelectronics,2013,39(1):31-36.
[5] Du Yanyan,Chen Min,Zhang Yingxue,et al.Determination of Fe(Ⅲ)based on the fluorescence quenching of rhodamine B derivative[J].Talanta,2013,106:261-265.
[6] Ussher S J,Milne A,Landing W M,et al.Investigation of Fe(Ⅲ)reduction and trace metal interferences in the determination of dissolved Fe in seawater using flow injection with luminol chemiluminescence detection[J].Analytica Chimica Acta,2009,652(1/2):259-265.
[7] Zhao Lixia,Di Fan,Guo Lianghong,et al.Chemiluminescence of carbon dots under strong alkaline solutions:A novel insight into carbon dot optical properties[J].Nanoscale,2013,5(7):2655-2658.
[8] Poznyak Sergey K,Talapin Dmitri V.Weller Horst,et al.Quantum Dot Chemiluminescence[J].Nano Letters,2004,4(4):693-698.
[9] Myung Noseung,Bae Yoonjung,Bard Allen J.Effect of surface passivation on the electrogenerated chemiluminescence of CdSe/ZnSe nanocrystals[J].Nano Letters,2003,3(8):1053-1055.
[10]Dou Xiangnan,Lin Zhen,Lin Jinming,et al.Production of superoxide anion radicals as evidence for carbon nanodots acting as electron donors by the chemiluminescence method[J].Chemical Communications(Camb),2013,49(52):5871-5873.
