肾小管上皮及肾脏局部病理改变对肾结石形成的临床价值分析
2015-03-22四川省广元市第四人民医院内科广元628001
四川省广元市第四人民医院内科(广元 628001)
邓武成
·临床病理·
肾小管上皮及肾脏局部病理改变对肾结石形成的临床价值分析
四川省广元市第四人民医院内科(广元 628001)
邓武成
目的:探讨肾小管上皮及肾脏局部病理改变在肾结石形成中的作用机制。方法:选取89例肾结石患者作为实验组,90例肾癌患者的肾标本作为对照组,检测两组肾小管上皮的骨桥蛋白、骨形成蛋白-2(BMP-2)和II型胶原的表达情况。结果:实验组患者结石多以混合的形式存在;两组肾小管上皮及肾脏局部病理改变中均可见骨桥蛋白表达,实验组高于对照组,差异有统计学意义,骨桥蛋白主要在肾集合管和肾小管上皮细胞胞浆内表达;BMP-2、II型胶原在肾小管上皮及肾脏病理局部组织中均未见表达。结论:骨桥蛋白在肾结石患者的肾小管上皮细胞中表达,BMP-2、II型胶原未见表达,因此肾小管上皮及肾脏局部病理改变时骨桥蛋白可能促进肾结石的形成。
肾结石是机体内病理生物矿化的结果,草酸钙是其主要成分。肾小管上皮细胞损伤既可以导致细胞与晶体相互作用,同时细胞与晶体相互作用也可以促进肾小管上皮细胞的损伤进而加重至形成肾结石[1,2]。本研究探讨了肾小管上皮及肾脏局部病理改变在肾结石形成中的作用机制,现报道如下。
资料与方法
1 一般资料 收集2012年1月至2013年12月我院收治的行经皮肾镜碎石术(PCNL)的肾结石患者89作为本研究的实验组。其中男52例,女37例;年龄18~76岁,平均年龄47.5±8.3岁。于同一时间收集肾内科肾癌患者90例的结石标本作为本研究的对照组。其中男57例,女33例;年龄21~74岁,平均年龄46.8±8.9岁。两组基线资料具有可比性(P>0.05)。
2 方 法
2.1 分析结石成分:患者于PCNL手术后收集患者结石作结石成分分析。①打开红外光谱仪电源,打开计算机。②开启红外光谱工作站,初始化后仪器自检。③设置红外光谱的范围为4000~5000cm-1。④进行扫描。⑤制备并检测样品。⑥保存并分析结果。
2.2 电镜扫描观察:将草酸钙分别加到置于12孔板的细胞中,然后用D-Hanks对细胞进行洗涤。加入戊二醛(2.5%)固定2h,用乙醇脱水、二氧化碳进行干燥,最后喷金包被在电镜(美国Philips公)下观察,观察晶体生长情况、晶体的组分和细胞的形态。
2.3 细胞损伤检测:用酶标仪[美谷分子仪器(上海)有限公司]检测细胞的吸光度A值,设置波长n=450nm。
3 检测指标 分别检测两组肾结石中的的骨桥蛋白、骨形成蛋白-2(BMP-2)和II型胶原的表达情况。

结 果
1 实验组肾结石成分分析结果 经过分析,实验组患者结石多以混合的形式存在,见表1。
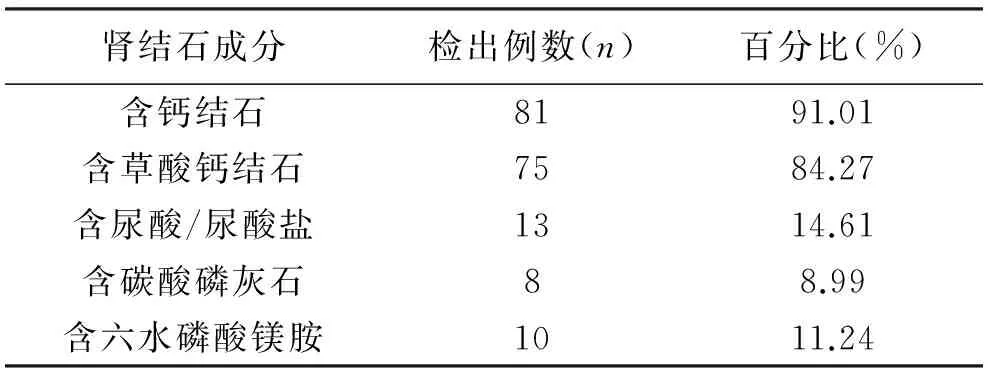
表1 实验组肾结石成分分析结果
2 骨桥蛋白在肾小管上皮及肾脏病理局部组织中的表达 实验组与对照组中均可见骨桥蛋白表达,见表2。
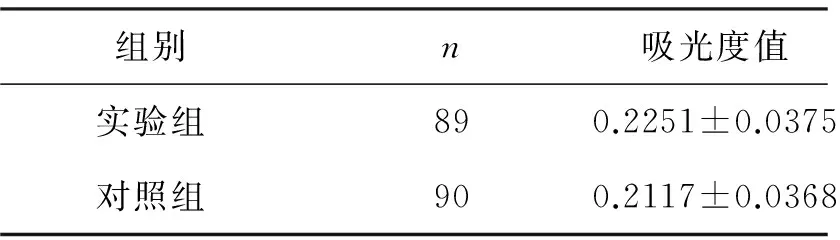
表2 骨桥蛋白在两组的表达的比较
注:两组比较P<0.05
讨 论
人体的正常细胞可以通过细胞间的紧密连接来完成细胞间的信号转导,同时也有利于抵抗外来的不利因素[3,4]。肾结石是由机体内病理生物矿化所产生的,草酸钙是其主要成分,因此草酸钙水平过高是尿石病的主要危险因素。导致肾结石的主要因素是肾小管上皮细胞的损伤,因为肾小管上皮细胞损伤会促进草酸钙的生成。细胞损伤之后,形态改变,紧密连接结构被破坏,磷脂双分子层不再对称,膜的极性消失,细胞的防御机制被破坏[5]。细胞损伤部位是晶体形成的主要位置,细胞损伤的产物可促进细胞与晶体的黏附,因而促进了肾结石的形成。由此可知,肾小管上皮细胞损伤既可以导致细胞与晶体相互作用,同时细胞与晶体相互作用也可以促进肾小管上皮细胞的损伤进而加重至形成肾结石。细胞损伤还会导致蛋白分子表达量发生变化,肾小管上皮细胞受损会使骨桥蛋白、跨膜糖蛋白、胶原蛋白、唾液酸糖蛋白等的含量增加,这些蛋白含量的变化与肾小管上皮细胞的损伤有密切关系[6]。
正常的肾小管上皮细胞具有抑制晶体黏附的作用,表明暴露的部分成核位点可形成COD,并无明显的促进结石形成的作用。晶体增大的过程中,肾小管上皮细胞能够诱导单个的COD的生成,不利于晶体的成核生长,因此具有抑制晶体黏附的作用。正常人体内含有草酸钙晶体,但是不形成结石。因为正常人草酸钙晶体的COD水平较高,而结石患者的草酸钙晶体中主要是COM,由此表明COD对人体无害,并且可能是人体中的一种保护机制用来抵制尿液中草酸钙过饱和的状态。
本研究探讨了肾小管上皮及肾脏局部病理改变在肾结石形成中的作用机制。研究结果表明骨桥蛋白含量的变化与肾小管上皮细胞的损伤有密切关系。BMP-2、II型胶原在肾小管上皮及肾脏病理局部组织中均未见表达。结果说明尿结石成分分析可以有效的反映由于结石的形成对尿液造成的改变,以及对正常机体形成的影响。目前肾小管上皮细胞损伤在肾结石形成中的作用是很明确的,所以想要预防肾结石的发生,必须及早的抑制肾小管上皮细胞的损伤,由此可知如能对已损伤的上皮细胞进行修复,也是一种治疗肾结石的有效方法。
骨桥蛋白在肾结石患者的肾小管上皮细胞中表达,BMP-2、II型胶原未见表达,因此肾小管上皮及肾脏局部病理改变时骨桥蛋白可能促进肾结石的形成,对肾结石的形成有很重要的临床价值,值得继续研究。
[1] 陈书尚,孙颖浩,高小峰,等. 草酸和草酸钙结晶损伤肾小管上皮细胞的差异蛋白质组学研究[J].中华泌尿科杂志.2011,32(6):387-391.
[2] 孟冬冬,邓耀良,黎承阳,等. 钙化性纳米微粒与人肾小管上皮细胞相互作用的实验研究[J].中华泌尿科杂志.2011,32(11):754-757.
[3] 余小祥,张瑞明,周大庆,等.502例尿路结石患者资料分析[J].华南国防医学杂志,2012,26(6):599-601.
[4] 刘建河,潘 骏. 钙化纳米微粒诱导人肾小管上皮细胞自噬的研究[J].中华泌尿科杂志,2012,33(1):37-40.
[5] 辛文虎,明 星. 肾小管上皮细胞损伤与草酸钙肾结石形成机制的研究进展[J].国际泌尿系统杂志.2013,33(4):539-542.
[6] 王艳梅, 赵豫凤, 杨加周, 等. TGF-β-1 在人胎儿肾脏发育中的表达[J]. 陕西医学杂志, 2012 41(8): 959-961.
(收稿:2015-08-06)
Clinical value analysis of renal tubular epithelium and renal local pathological changes on kidney stone formation Department of Internal Medicine,The Mental Health Center In GuangYuan
(Guangyuan 628001)
Deng Wucheng
Objective: To study the role of renal tubular epithelium and kidney local pathological changes in kidney stone formation. Methods: 89 cases of renal calculi patients were selected as the experimental group, 90 cases of patients with renal cell carcinoma renal specimens as control group, the expression of renal tubular epithelial osteopontin, bone morphogenetic protein-2 (BMP-2) and type II collagen were detected. Results: The calculi mostly existed in the form of mixture, including of mixture was the calcium calculi (91.01%), calcium oxalate calculi (84.27%), uric acid/uric acid salt (14.61%), carbonate apatite (8.99%), and ammonium magnesium phosphate hexahydrate (11.24%). Osteopontin was expressed in both two groups and the experimental group was significantly higher than that in the control group. Osteopontin was mainly expressed in the cytoplasm of renal collecting renal tubular epithelial cells. Expression of BMP-2 and collagen II were not observed in renal tubular epithelial or renal pathological local tissues. Conclusion: Osteopontin is expressed in the renal tubular epithelial cells of patients with kidney stones, while BMP-2 and type II collagen were not. Thus, osteopontin might promote the formation of kidney stones during the pathological change of renal tubular epithelium osteopontin and kidney local.
Kidney calculi/ Pathology @Renal tubular epithelial cell
肾结石/病理学 @肾小管上皮细胞
R692.4
A
10.3969/j.issn.1000-7377.2015.12.059
