DDQ促进的异色满苄基位C—O键的构建研究
2015-03-20朱佳丹陈雪琴章凌琼史鑫霞
朱佳丹,陈雪琴,章凌琼,史鑫霞,王 民
(杭州师范大学材料与化学化工学院,浙江杭州310036)
近年来,关于C—H 官能团化的一个方向是在杂原子导向的sp3杂化的C—H 位α 位的官能团化.它们大多都是在N 原子的α 位引入新的C—X 键,而关于在O 原子的α 位的官能团化的研究较少.对于含氧化合物,特别是苄醚类化合物在医药方面仍然具有实用意义及药用价值,如一些药物中具有异色满骨架.对于O 原子的α 位不对称官能团化,到目前为止报道较少,大都以取代的异色满为底物,如2008年Jacobsen 小组[1](缩酮底物)、2011年Watson 小组(缩酮底物)[2]、2014年山东大学娄红祥、刘磊(缩醛底物)[3]发展的不对称反应.因此,研究对DDQ 促进的异色满苄基位C—O 的引入就变得具有一定意义,所得缩酮底物可以进一步运用于不对称反应中. 第一例DDQ 促进下的脱氢偶联反应在李朝军小组发现以来[4],CDC 反应得到广泛的研究及应用;对于脱氢偶联试剂来说,有过渡金属、过氧化物、DDQ 等,大部分的报道集中于过渡金属.我们小组于2011年开始苄基醚的脱氢偶联反应研究,在研究过程中发现,在一些反应中加入NHPI 来促进反应时,除了正常的产物外,还有部分NHPI 加成的产物.2012年,Urabe 小组在过渡金属铁催化的异色满的偶联反应[5],过氧叔丁醇作为共氧化剂,以78%的收率得到产物;2013年,浙江大学包伟良小组报道了DDQ 促进下异色满与肟的C—O 键构建反应[6]. 我们发现异色满与NHPI 在DDQ 促进下,可以得到与包伟良小组相类似的结果,鉴于包小组详细考察了不同的氮氧源对该反应的影响,我们主要考查溶剂以及异色满的取代基对反应的影响.
1 实验部分
1.1 试剂与仪器
反应所用试剂为分析纯,直接使用;二氯二氰基苯醌(DDQ)、异色满、N-羟基邻苯二酰亚胺(NHPI)、取代苯乙醇均从安耐吉购买,直接使用.
TLC:青岛海洋200-300 目GF254;
NMR:布鲁克AX-500 MHz 或AX-400 MHz(TMS 为内标,CDCl3为溶剂);ESI:安捷伦1290 -6530QTOF.
1.2 底物的合成
异色满类化合物的合成方法有很多,在此主要采用苯乙醇的衍生物为原料进行合成,具体合成方法如下:
合成方法:在惰性气体氮气保护下,将苯基乙醇取代物(10 mmol),氯甲基甲醚(15 mmol),N,N-二异丙基乙基胺(20 mmol)加入到二氯甲烷(25 mL)中,室温搅拌反应至原料点消失,然后用水(2 ×50 mL)洗涤、无水硫酸钠干燥、减压浓缩得粗MOM 缩醛类产物.0 ℃下,将粗缩醛溶于乙腈中,慢慢滴加TMSOTf(10mmol),反应至原料点消失,反应体系用1 M NaHCO3淬灭反应、饱和食盐水洗涤有机层、无水硫酸钠干燥,柱层析得异色满.
1H NMR (400 MHz,CDCl3)δ 7.13 (d,J=8.0 Hz,2H),6.98 (d,J=8.0 Hz,2H),6.91 (s,1H),4.70 (s,2H),3.89 (t,J =5.7 Hz,2H),2.74 (t,J =5.6 Hz,2H),1.22 (s,9H).13C NMR (101 MHz,CDCl3)δ 149.03,134.42,130.29,128.62,123.55,121.11,68.28,65.55,34.45,31.40,27.95.

图1 异色满类化合物的合成Fig. 1 The paration of isochromans
1.3 C—O 键构建的一般方法
在DDQ 促进的异色满苄基位C—H 官能团化研究中,对C—O 的构建一般方法如下:
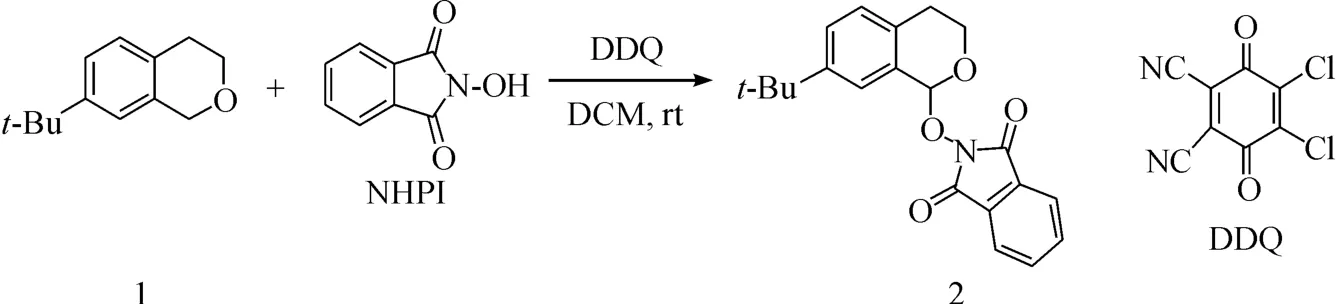
图2 C—O 官能团化的一般方法Fig. 2 General method for construct C—O bond
以叔丁基取代异色满为例,取代异色满与NHPI(N-羟基邻苯二甲酰亚胺)在DDQ(二氯二氰基苯醌)的作用下,以DCM(二氯甲烷)为溶剂所制备.柱层析分离得产物.
1H NMR (500 MHz,CDCl3)δ 7.89 -7.88(m,2H),7.78 -7.76(m,3H),7.44 -7.41(m,1H),7.18 -7.16(m,1H),6.24 (s,1H),4.73 -4.68(m,1H),4.06 -4.03(m,1H),3.11 -3.04(m,1H),2.74 -2.70(m,1H),1.39 (s,9H).13C NMR (125 MHz,CDCl3)δ 163.85,149.761,134.29,131.82,129.20,128.89,128.09,126.81,125.21,123.38,102.43,59.71,34.50,31.28,27.03.
HRMS(ESI-MS):calculated for (C21H21NO4+Na)374.1368,found 374.1358.
2 结果与讨论
2.1 溶剂对反应的影响
实验结果表明,二氯甲烷作溶剂时产率最高,可达到70%.以四氢呋喃、N,N-二甲基甲酰胺、乙腈、甲苯等作溶剂时产率相对较低.而升高反应的温度,产物收率并没有升高,反而有所下降.因此以二氯甲烷为溶剂时,在室温下反应最佳.
2.2 反应底物的拓展
在最优的条件下考察了异色满上苯环取代基以及吡喃环取代基的影响.由表2 可知,当异色满7 位具有卤素取代基(F,Cl,Br)时,可以得到相类似的结果,但收率有所下降,只有40%左右,而7 位取代基为叔丁基时,结果与异色满相类似,收率65%;当卤素取代基在6 位和8 位时,只有极少量的产物生成,可能的原因是由于NHPI 具有较大的位阻,导致收率很低.当甲基取代基在吡喃环2 位时,收率可达50%.

表1 溶剂的优化aTab. 1 The optimization of the solvent
当我们考查其它的N-O 源,如TEMPO(2,2,6,6-四甲基哌啶氧化物)时,并没有得到所需产物.
2.3 反应机理的讨论研究
根据李朝军等人的报道,推测实验可能的机理为异色满先与DDQ 作用生成氧鎓正离子中间体后,NHPI 作为亲核试剂进攻,生成取代产物
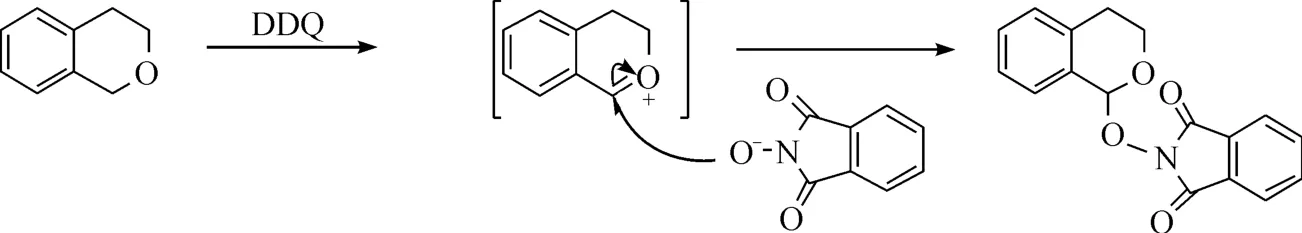
图3 反应可能的机理Fig. 3 The possible reaction mechanism
3 结 论
本次研究提供了一种构建异色满苄基位C—O 键的方法.通过优化条件得出较为完善的反应体系,即在DDQ 的促进下异色满与NHPI 在二氯甲烷中常温下构建C—O 键体系.该反应具有一定的研究价值,所得含氧化合物,特别是苄醚类化合物在医药方面具有一定的实用意义,且所得产物可以进一步作为活性底物运用于一些不对称合成反应中.
[1]Reisman S E,Doyle A G,Jacobsen E N. Enantioselective thiourea-catalyzed additions to oxocarbenium ions[J]. Journal of the American Chemical Society,2008,130(23):7198-7199.
[2]Maity P,Srinivas H D,Watson M P. Copper-Catalyzed Enantioselective Additions to Oxocarbenium Ions:Alkynylation of Isochroman Acetals[J]. Journal of the American Chemical Society,2011,133(43):17142-17145.
[3]Meng Z,Sun S,Yuan H,et al. Catalytic Enantioselective Oxidative Cross-Coupling of Benzylic Ethers with Aldehydes[J]. Angewandte Chemie,2014,126(2):543-557.
[4]Li Z P,Li C J. Catalytic Enantioselective Alkynylation of Prochiral sp3C—H Bonds Adjacent to a Nitrogen Atom[J]. Organic Letters,2004,6(26),4997-4999.
[5]Iwata S,Hata T,Urabe H. Synthesis of tert-Butyl Peroxyacetals from Benzyl,Allyl,or Propargyl Ethers via Iron-Promoted C—H Bond Functionalization[J]. Advanced Synthesis & Catalysis,2012,354(18):3480-3484.
[6]He H F,Wang K,Xing B,et al. Formation of C–O Bond via Cross-Dehydrogenative Coupling between Isochroman and Oxime under Metal-Free Oxidation Conditions[J]. Synlett,2013,24(2):211-214.
