癌胚抗原定量测定试剂盒(化学发光免疫分析法)的临床性能评价
2015-03-10梁丽萍李志雄董志宁吴英松
梁丽萍 李志雄 董志宁 李 明 吴英松★
癌胚抗原定量测定试剂盒(化学发光免疫分析法)的临床性能评价
梁丽萍1李志雄1董志宁1李明2吴英松2★
[摘要]目的对自制的癌胚抗原定量测定试剂盒(化学发光免疫分析法)进行临床应用研究及临床性能评价。方法用自制试剂盒检测采集到的血清1 156例和101例血浆,以罗氏公司癌胚抗原定量测定试剂盒(电化学发光法)为对照试剂,雅培公司癌胚抗原测定试剂盒(化学发光微粒子免疫检测法)作为复核试剂,对自制试剂盒的一致性和相关性等指标进行计算分析。结果同罗氏试剂盒相比,自制试剂盒异常符合率达96.1%,正常符合率达97.8%,总符合率达97.3%,Kappa值达0.931(P<0.01)。从定量测定值分析,与罗氏试剂盒测值相比,自制试剂盒测值的线性回归方程为Y=0.091+1.009X,相关系数为0.987(P<0.01),相关性良好。结论本试剂盒检测性能满足临床应用的需要。
[关键词]癌胚抗原;临床研究;化学发光免疫分析法
作者单位:1.广州市达瑞生物技术股份有限公司,广东,广州510665 2.南方医科大学生物技术学院,广东,广州510515
The clinic research of the carcinoembryonic antigen (CEA) quantitative diagnostic kit by chemiluminescent immunoassay (CLIA)
LIANG Liping1, LI Zhixiong1, DONG Zhining1, LI Ming2, WU Yingsong2★
(1. Darui Biotechnology Co., Ltd., Guangzhou, Guangdong, China, 510665; 2. School of Biotechnology, Southern Medical University, Guangzhou, Guangdong, China, 510515)
[ABSTRACT] Objective To investigate the clinic research of the carcinoembryonic antigen (CEA) quantitative diagnostic kit by chemiluminescent immunoassay (CLIA) (CEA-CLIA).Methods 1 156 cases of serum and 101 cases of plasma were detected with the self-made kit. Roche carcinoembryonic antigen quantitative determination kit (ECL) were used as control agents, and Abbott carcinoembryonic antigen determination kit (CMIA) were used as a reagent in review. Consistency and correlation were calculated. Results The positive accordant ratio, the negative accordant ratio,the Kappa value was 96.1%,97.8%, 0.931 (P<0.01), respectively. Compared to Roche's kit in the quantitative analysis, the linear regression equation of the reagent was Y=0.091+1.009X.The correlation coefficient was 0.987 (P<0.01). And the correlation coefficient was satisfy. Conclusion CEA-CLIA was a valuable diagnostic kit for clinic application.
[KEY WORDS] Carcinoembryonic antigen (CEA); Clinic research; Chemiluminescent Immunoassay (CLIA)
癌胚抗原(carcinoembryonic antigen,CEA)是一种分子量为175 kDa~200 kDa糖蛋白抗原,1965年首先由加拿大学者Gold和Freedman从胎儿及结肠癌组织中发现[1]。胚胎期主要存在于胃肠道、肝脏和胰腺等器官,出生后含量很低。其浓度与多种肿瘤尤其是消化道肿瘤相关,如结肠癌、直肠癌、胃癌、胰腺癌、胆管癌等,肺、乳腺及泌尿生殖系统的恶性肿瘤也升高[2]。在临床中CEA常与多个肿瘤标志物联合检测,用于肺癌、胃癌、结直肠癌等多种肿瘤的早期诊断、疗效和预后评价[3-5],在临床上已作为一项常规的检查项目。
本文对自行研制的癌胚抗原定量测定试剂盒(化学发光免疫分析法)进行了临床性能评价,分析比较了其与现行使用的进口试剂盒在样本检测中的符合率、相关性和一致性等指标,对其有效性及安全性提供了重要依据。
1 材料与方法
1.1材料
1.1.1自制癌胚抗原定量测定试剂盒(化学发光免疫分析法)
罗氏公司的癌胚抗原定量测定试剂盒(电化学发光法),对照用试剂;雅培公司的癌胚抗原测定试剂盒(化学发光微粒子免疫检测法),复核用试剂。
1.1.2CEA质控品
质控品C1(7 ng/mL~13 ng/mL)、质控品C2 (21 ng/mL~39 ng/mL)、质控品C3(70 ng/mL~130 ng/mL)为广州市达瑞生物技术股份有限公司自配。
1.1.3样本
(1)血清样本:临床结肠癌患者或其他肿瘤(如肺癌、肝癌、乳腺癌等)患者和正常查体者血清,共有1 156例。(2)血浆样本:101例,同一病例的血浆样本包含于上述血清样本中。(3)特异性样本:甲胎蛋白11例、类风湿因子11例、抗核抗体12例、溶血13例、脂血11例、黄疸12例。以上样本分别由中国人民解放军第302医院、南方医科大学南方医院、北京地坛医院和厦门大学附属第一医院提供,均用罗氏公司的癌胚抗原定量测定试剂盒(电化学发光法)测定血清CEA浓度。
1.1.4实验仪器
应用厦门优迈科医学仪器有限公司的全自动化学发光免疫分析仪Caris200。
1.2方法
1.2.1试验设计
(1)将采集的血清样本病例编码,采用对照方法和自制试剂盒同时进行盲法检测,试验结束后揭盲,对不符样本采用复核方法进行复核。(2)用自制试剂盒对采集的同一病例的血清与血浆样本同时进行检测,结果进行统计。
1.2.2样本正常参考值
罗氏试剂盒、雅培试剂盒及自制试剂盒的正常参考值均为0 ng/mL~5 ng/mL。
1.2.3统计处理
利用SPSS 13.0统计软件进行一致性及相关性分析;用Medcalc软件进行Bland-Altman定量分析。
2 结果
2.1血清样本的检测结果分析
2.1.1一致性分析
自制试剂盒和罗氏公司对照试剂盒相比较(见表1),正常符合率为97.8%,异常符合率为96.1%,总符合率为97.3%;Kappa值为0.931(P<0.01)(见表2)。说明自制试剂盒的测定结果与罗氏公司试剂盒的测定结果符合率较高,有较好的一致性。

表1 临床检测结果统计归纳表Table 1 Statistical induction of clinical detection results
2.1.2相关性分析
利用SPSS13.0统计软件对自制试剂盒和对照试剂盒的临床检测结果进行相关性分析。相关系数r值为0.987(P<0.01)(见表3),线性回归方程为Y=0.091+1.009X(见表4),散点图见图1。可见自制试剂盒与对照试剂测值相关性良好。
2.1.3Bland-Altman分析
以待考核试剂与对照试剂测值的均值为X轴,以两者的差异值为Y轴,绘制散点图(见图2)。由图2可见,2.8%(32/1 156)的点在95%一致性界限外;在一致性界限范围(9.8,-10.2)内,待考核试剂的测值与对照试剂的测值相比,差值的绝对值最大为9.35 ng/mL,而两者的测量结果平均为100.725 ng/mL,这种相差的幅度在临床上可以接受。因此认为待考核试剂与对照试剂的测试结果具有较好的一致性。

表2 Kappa值的计算结果Table 2 The calculated results of Kappa values

表3 相关性分析结果Table 3 The results of correlation analysis

表4 线性回归分析表Table 4 The analysis of linear regression
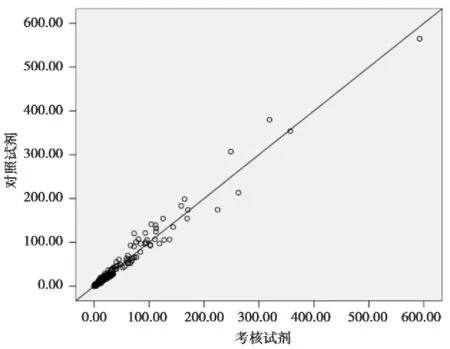
图1 血样测值相关性分析散点图Figure 1 The scatter plot of correlation analysis
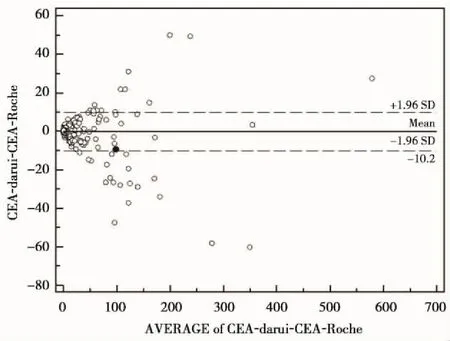
图2 Bland-Altman分析图Figure 2 The chart of Bland-Altman analysis
2.1.4差异样本的分析
本次临床考核共进行了1 156例血清样本的测试考核,其中有31例样本自制试剂盒和对照试剂盒的检测结果判断不一致。对这31例差异样本用复核试剂盒进行检测。复核试剂盒检测结果显示有21例样本与考核试剂盒检测结果一致,有10例与对照试剂盒检测结果一致。说明该待考核试剂盒测定结果较为准确、稳定和可靠。
可能的差异原因:差异样本的CEA测值在正常参考值的上限附近,临界值导致了判断结果的不确定性。需要多次重复测定或进行第三方检测并作临床追踪检测,才可明确实验结果和临床意义。
2.2血清与血浆样本的测值对比
本次临床试验对101例同一病例的血清和血浆样本用自制试剂盒进行检测,结果101例样本判定结果一致(见表5)。经统计分析,与血清检测结果相比,血浆的检测结果Kappa达1.000(P<0.01)(见表6),两者测值相关系数r值达0.991(P<0.01)(见表7),线性回归方程为Y=-1.292+1.097X(见表8),散点图见图3。结果表明待考核试剂盒对血清或血浆的检测结果一致性及相关性较好,待考核试剂盒适用于血清及血浆样本的检测。

表5 同一病例血清血浆对比表Table 5 The comparative table of the same patient serum and plasma

表6 同一病例血清和血浆Kappa值统计结果表Table 6 The statistical results of the same patient serum and plasma
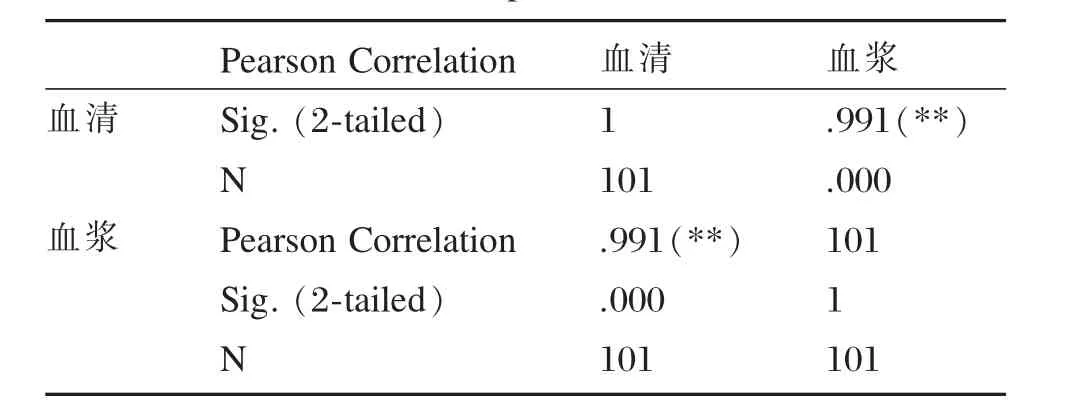
表7 血浆与对应血清测值相关性Table 7 The correlation analysis of the same patient serum and plasma

表8 血浆与对应血清测值线性回归分析表Table 8 The linear regression analysis of the serum and plasma
2.3特异性样本试验分析
本次临床试验共纳入了70例特异性样本,分别为甲胎蛋白11例、类风湿因子11例、抗核抗体12例、溶血13例、脂血11例、黄疸12例,均使用自制试剂盒与对照试剂进行检测,两者检测结果均正常,表明待考核试剂盒检测血样时不受甲胎蛋白、类风湿因子、抗核抗体、溶血、脂血、黄疸的干扰。
2.4可靠性分析
本实验在对质控验证后方进行测试,质控结果表明标准差及浓度测值均符合质控标准要求,实验准确可靠。
3 讨论
临床上检测CEA的方法有放射性免疫分析法、酶联免疫吸附测定等。近年来发展了荧光免疫分析法、化学发光免疫分析法等,化学发光分析方法与免疫分析相结合已经成为近年来检测分析技术的研究热点。化学发光免疫分析技术是二十世纪八十年代继放射免疫分析、酶联免疫分析和荧光免疫分析后发展起来的一项新的免疫分析技术,具有灵敏度高、快速、准确、重复性好、效期长并安全无毒无污染等优点[6]。
本研究以罗氏的癌胚抗原定量测定试剂盒(电化学发光法)为对照试剂,对自制的癌胚抗原定量测定试剂盒(化学发光免疫分析法)进行临床检测性能评价。同对照试剂比较,自制试剂盒的正常符合率为97.8%,异常符合率为96.1%,总符合率为97.3%;Kappa值为0.931(P<0.01);两者测值相近,相关系数达0.987(P<0.01),线性回归方程为Y=0.091+1.009X,相关性良好。采用Bland-Altman统计学方法对两组测定结果进行分析,有97.2%的点在一致性界限内,两者的测定结果具有较高的一致性。且通过对同一病例的血清与血浆的测值比较,两者测值一致,相关系数r值达0.991(P<0.01),说明本试剂盒适用于人血清或血浆中CEA含量的检测。同时,不受甲胎蛋白、类风湿因子、抗核抗体、溶血、脂血、黄疸的干扰。说明自制的试剂盒与目前临床广为应用的进口试剂在指标检测性能上具有良好的等效性,可替代国外昂贵试剂应用于临床检测和基础医学的研究。

图3 血浆与对应血清测值相关性分析散点图Figure 3 The scatter plot of correlation analysis of the serum and plasma
参考文献
[1]Gold P, Freedman SO. Demonstration of tumor-specific antigens in human colonic carcinomata by immunological tolerance and absorption techniques[J]. J Exp Med, 1965,121:439-462.
[2]尚高峰,张翠歌.癌胚抗原检测的临床意义[J].内蒙古中医药, 2014,33(33):57-58.
[3]潘丽兰.血清CEA、CA199、CA125、CA153、AFP联合检测对胃癌的诊断价值[J].中国实验诊断学, 2013,17 (12):2192-2195.
[4]张海英.癌胚抗原和糖类抗原125联合检测在肺癌诊断中的应用[J].检验医学与临床, 2013,(24):3335-3336.
[5]卢灿荣,张士武,张勇,等.联合检测癌胚抗原、糖链抗原19-9和C反应蛋白对结肠癌的诊断价值[J].标记免疫分析与临床, 2012,19(1):3-6.
[6]农天雷.常用化学发光免疫分析技术及其特点[J].现代医药卫生, 2011,27(14):2156-2158.
通讯作者:★吴英松,E-mail:yingsongwu@hotmail.com
基金项目:国家高技术研究发展计划(863计划)(2011AA02A101)
