新诊断糖尿病患者的生活方式干预
2015-03-02万学思李延兵
万学思 李延兵
中山大学附属第一医院内分泌科
新诊断糖尿病患者的生活方式干预
万学思 李延兵
中山大学附属第一医院内分泌科
Lifestyle Intervention for Patients with Newly Diagnosed Diabetes Mellitus

万学思 中山大学附属第一医院内分泌科主治医师,从事2型糖尿病胰岛β细胞功能保护及胰岛素抵抗诊治的研究,先后主持广东省卫生厅青年基金和广东省自然科技基金自由申请项目,发表SCI论著8篇。
良好的生活方式是健康的基石,对于糖尿病患者尤为重要。大庆研究结果显示,对糖尿病前期人群进行6年的生活干预,能够使以后14年里的2型糖尿病的累计发生风险下降43%,而且预防作用长期持久,可持续23年以上[1,2]。我们科的跟踪性研究也显示,对于经过短期胰岛素泵强化[3]治疗的新诊断2型糖尿病患者,积极的个人生活方式管理能有助于维持更长的无药缓解期。所以对于糖尿病的新患者,医护人员为之制定合适的生活方式干预目标,将有助于他们在未来的日子里越过越甜蜜。下面我们将按饮食、运动、睡眠以及情绪的管理,逐一阐述。
糖尿病饮食
合理饮食是治疗糖尿病最重要、也是最基本的一环。早在19世纪70年代普法战争的时代,法国因食物短缺不得不定量供应。在此期间,一位医生偶然发现定量供应食物能够使部分的糖尿病患者血糖明显下降,于是产生了进行饮食治疗的方法。此后,这种治疗方法逐渐被广泛接受。但在临床上,糖尿病饮食治疗常常走进误区,往往只重视治疗效果,却忽视患者的感受和要求。再完美的糖尿病饮食方案,如果得不到患者的认同和执行,也是纸上谈兵。
另一方面,大部分新诊断糖尿病的患者都会注意饮食,但由于缺乏相应的知识,往往欲速而不达,甚至南辕北辙。最常见的两种错误有:一是以为不吃甜食就可以了;二是以为吃米饭会血糖高,不敢吃淀粉类主食。那么,规范的糖尿病饮食治疗是怎样的呢?
2013年中国糖尿病医学营养治疗指南[4]以及2015年美国糖尿病协会的糖尿病诊疗指南[5]都作了详细的介绍,以下是笔者整合指南的观点进行详述。
普通糖尿病患者的饮食控制
糖尿病患者饮食方案设计应注意控制总热量,各营养成分合理搭配,个性化选择食物种类及交换份,健康的烹调方式和饮食的次序。
(1)总热量:应当根据患者的年龄、性别、身高、体重、代谢特点、生活方式、工作、运动等因素灵活制定治疗措施,个体化设计,尽量使糖尿病患者的饮食和生活更加接近正常人。针对亚洲人群,2005年世界卫生组织(WHO)和国际糖尿病联盟(IDF)发表声明,以BMI 23kg/m2作为亚洲成人超重的界限,BMI 25kg/m2作为亚洲成人肥胖的界限。那么,轻中重体力劳动又是怎么划分?比如搬运或田间劳动是重体力劳动,公务员、教师、内科医生等以脑力劳动为主的算轻体力劳动,中等体力劳动介于这两者之间,比如外科医生,既要动脑子,又有体力劳动。
例如,患者一为50岁的农民,女,身高153cm,体重60kg,BMI 25.63kg/m2,属于肥胖的重体力劳动者,应予以35kcal/kg理想体重。她的理想体重是153-105=48kg。故每日推荐总热量是35kcal/ kg*48kg=1680kcal。
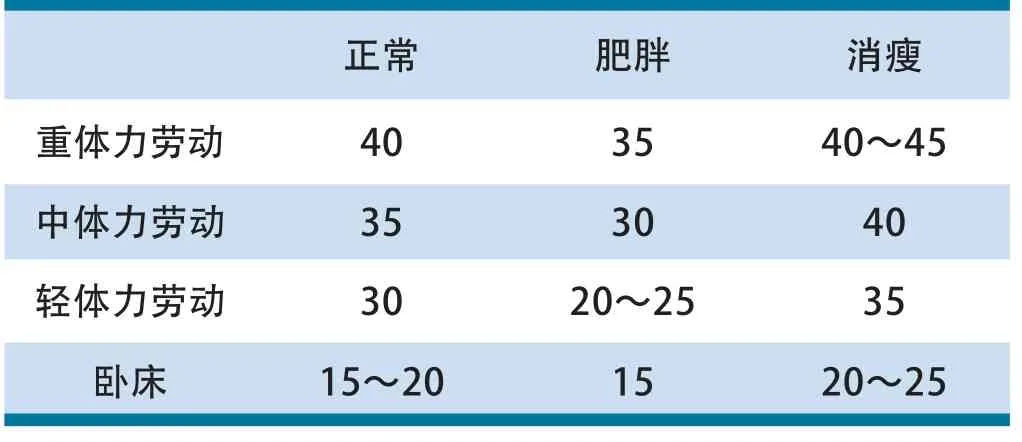
表1 糖尿病患者每日总热量(kcal/kg理想体重)
再如,患者二为47岁的教师,男,身高170cm,体重65kg,BMI 22.49kg/m2,属于正常的轻体力劳动者,应予以30kcal/kg理想体重。他的理想体重是170-105=65kg。故每日推荐总热量是65kcal/ kg*30kg=1950kcal。
(2)各营养成分合理搭配:确定了每日的总热量后就可以进一步挑选食品了。总的原则是平衡膳食、选择多样化、营养合理的食物。
美国糖尿病协会的2015年糖尿病诊疗指南[5]提出,所有糖尿病患者并没有一个理想的碳水化合物、蛋白质和脂肪的热量来源比例;所以宏量营养素的分配应根据目前饮食方式、喜好和代谢控制目标的个体化评估。许多饮食方式(不同的食物或食物种类的组合)对于治疗糖尿病是可以接受的。而2013年中国糖尿病医学营养治疗指南[4]则推荐平衡膳食,能量摄入应符合体重管理目标,其中45%~60%来自碳水化合物,25%~35%来自脂肪,15%~20%来自蛋白质。
例如,上文提及的患者一属于肥胖体型,脂肪供能比控制在30%以内更有利于减重,可以选择25%的脂肪,20%的蛋白质,55%来源为低升糖指数、高膳食纤维含量的碳水化合物。折合为:1680kcal×25% ÷9 =47g 脂肪,1680kcal×20%÷4=84g 蛋白质,1680kcal×55%÷4 =231g碳水化合物。
(3)个性化选择食物种类及交换份:为了让病人更直接方便地选择食物,按照日总热量计算食物交换份也是比较好的办法。食物交换份是以可提供能量为90kcal作为一个交换单位,按食物的来源、性质分类,每单位交换份的同类食物所含的蛋白质、脂肪、碳水化合物和能量相近,食物交换份的使用应在同类食物间进行。为了保证营养充足、全面,糖尿病患者每餐都要有谷薯类、蔬菜,每天都要吃肉类、奶类食品和水果。
如上述的女患者,每天需要18.5交换份。9~10份富含碳水化合物的主食,3份蔬果,3~4份肉类(如有1份奶类就相应减少一份肉类),油小于3份。
碳水化合物分为低聚糖和多糖。指导碳水化合食物的选择时,要注意升糖指数(GI)和血糖负荷(GL), 低GI/GL饮食有助于降低血糖和HbA1c。低GI饮食有助于糖尿病患者血糖和体重控制。为保持身体健康,应建议患者优先从蔬菜、水果、全谷食物、大豆和奶制品中摄入碳水化合物,而非其他碳水化合物来源,尤其是那些含有添加脂肪、糖类或钠的食品。米饭、面粉、土豆等食物中的淀粉不会使血糖急剧增加,并且体积大,饱腹感强,应作为碳水化合物的主要来源。一般的米面制品是每交换份是25g,馒头和饼类是35g,而玉米是200g。如上述的患者一,选择米饭或面条作为主食,每天可达225~250g。
膳食纤维虽然也属于糖类,但是由于人体缺乏专门的消化酶,因而不会转化为葡萄糖,所以不会影响血糖。同时它也不会被人体吸收,又容易使人食用后有饱感,且有降脂、防癌的作用,适宜糖尿病患者食用。糖尿病患者膳食纤维摄入可高于健康成年人推荐摄入量,推荐25~30g/d或10~14g/1000kcal。蔬果是纤维的主要来源之一。建议糖尿病患者每天摄入至少3份蔬果。蔬菜每500g为一交换份,水果多数是150~200g为一交换份。
蔗糖是一种双糖,除升高血糖外,还能升高甘油三酯水平,不推荐糖尿病患者进食蔗糖。但是蔗糖引起的血糖升高幅度并不比相同能量的淀粉引起的升幅更高,在血糖控制理想的情况下,未必需要绝对禁止患者摄入蔗糖或含蔗糖的食物。
脂肪的质量比脂肪的数量更重要。糖尿病患者饮食中饱和脂肪、胆固醇和反式脂肪的建议摄入量与普通人群相同,要限制其摄入量,其中饱和脂肪酸的摄入量不应超过供能比的10%,每日胆固醇摄入量不宜超过300mg。增加植物脂肪占总脂肪摄入的比例,其中单不饱和脂肪酸是较好的膳食脂肪来源,宜大于总能量的12%,多不饱和脂肪酸不宜超过总能量的10%。建议选择富含ω-3多不饱和脂肪酸的植物油。烹调宜用植物性油脂,以不饱和脂肪为主:如橄榄油、山茶油、玉米油等,每10g为一交换份。推荐每周吃鱼2~4次(尤其是ω-3多不饱和脂肪酸含量丰富的海鱼)。另外,在临床上常常被患者忽略的往往是“看不到的脂肪”,如调味料里的辣椒油、花生酱,零食里的坚果等,脂肪含量极高,另外,不少肉类的脂肪含量也不低,稍不注意就已经摄入了大量的脂肪。尽量少吃胆固醇含量高的食物,例如心、肝、肾等动物内脏类食物以及猪皮、鸡皮、鸭皮等食物。值得注意的是,血液中的胆固醇多来自体内的合成,膳食摄入所占比例不足30%,单纯控制饮食并不足以降低大部分高脂血症患者的胆固醇水平,因此,不应过于强调饮食控制而忽略降胆固醇药物的治疗。
总蛋白质的摄入量,标准体重成人-每天0.8~1g/ Kg,每日总量为50~70g,消瘦者每日摄入量需达1~1.2g/Kg,孕妇、乳母则应达到1.5g/Kg,儿童为2~3g/Kg。植物来源的蛋白质,尤其是大豆,不含胆固醇,相比动物蛋白更有助于降低血脂水平。故动物类蛋白与植物类蛋白可以各占50%。当然,根据患者口味,选择低脂、优质蛋白的肉类为主也是可以的。近年来研究表明乳清蛋白可促进肠促胰素的分泌,提高胰岛素敏感性。尤其是它所含亮氨酸及其代谢产物能减少肌肉蛋白的分解。系统回顾研究显示,膳食中增加乳清蛋白的摄入有助改善糖代谢,减轻体重。故建议每天一交换份的奶制品。一般豆类每25g为一交换份,水产品100g为一交换份,其他瘦肉类50g为一交换份,奶类150g为一交换份。
目前,没有明确的证据显示糖尿病人群予以抗氧化剂、维生素或矿物质的补充是有益的(如果没有缺乏),故不建议常规补充。
每日喝水量极为重要但却常常被忽略。糖尿病患者对水的依赖性比健康人更强,如果饮水不足,很容易使血糖升高,甚至引起严重的急性并发症。有些患者为了控制多尿的症状,就采取少饮水的方法,这样既不科学,又非常危险。正确的做法恰恰相反。建议每天喝水1.5~2L。
钠盐限制在6~8g/天以内,如并发高血压应<5g/天。
(4)健康的烹调方式和饮食的次序:烹调多采用清蒸、水煮、凉拌、涮、烤、烧、炖、卤等方式,少吃油煎、炸、油酥。
合理进食的次序对控制餐后血糖有一定的帮助,饭前喝汤可增加饱腹感,先吃小部分蔬菜和肉类再吃米饭,可以减慢食物的排空和吸收。
特殊类型糖尿病患者的饮食控制
(1)对于合并高尿酸血症的患者,要避免高嘌呤的食物,如海鲜、肉类、豆类、菇类。如果因为低嘌呤饮食限制了蛋白质的摄入量,就要适当地提高碳水化合物的比例。
(2)对于合并肾功能不全的患者,蛋白的质和量对肾功能可能有影响,以白肉(鱼和鸡肉类)、蔬菜和奶类为主要来源的低蛋白质饮食,可能有改善蛋白尿的作用。出现显性蛋白尿的患者可适量限制饮食蛋白,我国指南推荐蛋白摄入量0.8g/(kg·d)。慢性肾病3期患者建议实施低蛋白饮食配合酮酸饮食,推荐蛋白摄入0.6g/ (kg·d),并补充复方α-酮酸制剂0.12g/(kg·d)。而2015年美国糖尿病协会医学诊疗标准则提出,对于糖尿病肾病患者并不建议蛋白质摄入量低于每天0.8g/kg以下(基于理想体重),因为这并不能改变血糖控制、心血管危险因素控制或GFR下降的过程。透析患者蛋白质推荐量与非糖尿病透析患者相似:血液透析患者为1.1~1.2g/ (kg·d);腹膜透析患者为1.2~1.3g/(kg·d)。实施低蛋白饮食治疗,能量摄入应基本与非糖尿病肾病者相似(30~35kcal/kg)。但是,肥胖患者需适当限制能量(可减少250~500kcal/d),直至达到理想体重。推荐膳食脂肪摄入量:总脂肪供能比低于30%,饱和脂肪低于10%,胆固醇低于200mg/d。慢性肾病4期的糖尿病患者中普遍存在维生素D缺乏,而充足的骨化醇有助于糖尿病肾病者的血糖控制。部分血液透析患者肉碱代谢存在异常,给予静脉注射左旋肉碱后,可能改善其生活质量。
(3)戒烟酒。建议所有患者不要吸烟或使用烟草产品。2015年美国糖尿病协会的糖尿病诊疗指南[5]新增建议,戒烟咨询应纳入糖尿病治疗的一个常规组成部分。酒的乙醇能量很高,1g乙醇产生7kcal热量,并给肝脏带来了负担。成年糖尿病患者如果想饮酒,每日饮酒量应适度(成年女性每天≤1份,成年男性≤2份),尽量选用酒精浓度低的酒类。饮酒或许使糖尿病患者迟发低血糖的风险增加,尤其在空腹饮酒,或接受胰岛素及促胰岛素分泌剂治疗的患者中。服用二甲双胍的患者如果酗酒容易产生乳酸酸中毒。
糖尿病患者的运动
2012年由中华医学会糖尿病学分会发布了《中国糖尿病运动治疗指南》[6]。根据指南,运动治疗应在指导下进行。运动前要进行必要的评估,特别是心肺功能和运动功能的医学评估(如运动负荷试验等)。空腹血糖>16.7mmol/L、反复低血糖或血糖波动较大、有糖尿病酮症酸中毒等急性代谢并发症、合并急性感染、增殖性视网膜病、严重肾病、严重心脑血管疾病(不稳定性心绞痛、严重心律失常、一过性脑缺血发作)等情况下禁忌运动,病情控制稳定后方可逐步恢复运动。
运动项目要与患者的年龄、病情及身体承受能力相适应,并定期评估,适时调整运动计划。成年糖尿病患者每周至少进行150分钟中等强度有氧运动(达最大心率的50%~70%),每周至少3天,每次不低于20分钟,尽量避免连续超过2天不运动。中等强度的体育运动包括:快步走、太极拳、自行车、乒乓球和羽毛球等。较强体育运动为舞蹈、有氧健身操、慢跑、游泳、骑车上坡。鼓励所有人(包括糖尿病患者)减少静坐时间,尤其是避免长时间的静坐(>90分钟)。如无禁忌证,每周最好进行2~3次阻力为轻或中度的抗阻运动。交替进行抗阻运动和有氧运动可得到进一步的代谢改善。
运动前后要加强血糖监测,以免发生低血糖,高强度运动前应临时调整饮食及药物治疗方案。
糖尿病的情绪管理与睡眠
糖尿病与抑郁症有着密切的联系。严重抑郁会影响糖尿病治疗中患者的依从性和自我管理等。2015 ADA标准新增建议,需要关注糖尿病伴抑郁症患者,对老年糖尿病患者(年龄≥65岁)更应优先考虑抑郁症的筛查和治疗。确诊抑郁症的糖尿病患者应接受阶梯式协作治疗方法治疗抑郁症。
睡眠时间与2型糖尿病的关系是近年的研究热点。2015年上半年,《Diabetes Care》上发表了两篇关于糖尿病与睡眠相关的文章。Ferrie JE等进行了持续20年的大样本跟踪性研究,相对于平均每日睡眠时间7小时,每日9小时睡眠会增加2型糖尿病发病风险65%,每日5.5小时睡眠则增加2型糖尿病患病风险35%[7]。Shan Z进行了一项meta分析得到相似的结果,睡眠时间跟糖尿病呈U型曲线关系,每日7~8小时睡眠的人群的2型糖尿病患病率最低[8]。故建议2型糖尿病患者每天睡7~8小时。慢性失眠患者需要到神经心理等相关专科进行专业治疗。
结语
就目前来说,糖尿病是一个终身疾病,所以良好的生活方式干预是一辈子的事,不能说血糖高了就严格点,血糖低了就放松,这样会造成血糖长期的不稳定,也是糖尿病慢性并发症的主要危险因素。只要医患共同努力,坚持合理的生活方式干预,将会长期、稳健地控制血糖。
1 Li G, Zhang P, Wang J, et al. The long-term effect of lifestyle interventions to prevent diabetes in the China Da Qing Diabetes Prevention Study: a 20-year follow-up study. Lancet, 371(9626):1783-1789.
2 Li G, Zhang P, Wang J, et al. Cardiovascular mortality, all-cause mortality, and diabetes incidence after lifestyle intervention for people with impaired glucose tolerance in the Da Qing Diabetes Prevention Study: a 23-year follow-up study. Lancet Diabetes Endocrinol,2014,2(6):474-480.
3 Chen A, Huang Z, Wan X, et al. Attitudes toward diabetes affect maintenance of drug-free remission in patients with newly diagnosed type 2 diabetes after short-term continuous subcutaneous insulin infusion treatment. Diabetes Care,2012,35(3):474-481.
4 中华医学会糖尿病学分会中国医师协会营养医师专业委员会. 《中国糖尿病医学营养治疗指南》. 中华糖尿病杂志,2015,7(2):73-88.
5 The American Diabetes Association. Standards of Medical Care in Diabetes. Diabetes Care,38(Supplement 1):S1-S87.
6 中华医学会糖尿病学分会. 《中国糖尿病运动治疗指南》[M]. 北京:中华医学电子音像出版社,2012.
7 Ferrie JE, Kivim☒ki M, Akbaraly TN, et al. Change in Sleep Duration and Type 2 Diabetes: The Whitehall II Study. Diabetes Care,2015,Jun 11.[Epub ahead of print]
8 Shan Z, Ma H, Xie M, et al. Sleep duration and risk of type 2 diabetes: a meta-analysis of prospective studies. Diabetes Care,38(3):529-537.
10.3969/j.issn.1672-7851.2015.06.010
