923例新的和严重的药品不良反应报告分析
2015-02-25刘小玉张若良赣州市食品药品检验所江西赣州341000
★ 刘小玉 张若良 (赣州市食品药品检验所 江西 赣州 341000)
923例新的和严重的药品不良反应报告分析
★刘小玉张若良(赣州市食品药品检验所江西 赣州 341000)
摘要:目的:分析赣州市新的和严重的药品不良反应报告情况, 为临床合理用药提供参考。方法:对赣州市2013年上报国家药品不良反应监测平台的923 例新的和严重的不良反应病例进行回顾性研究分析。结果:引起新的和严重的药品不良反应涉及的药品以抗感染药物最多,以注射剂为主要剂型,以注射给药为主要途径,表现主要为全身性损害、呼吸系统损害和胃肠系统损害。结论:在临床用药中应重点关注抗感染药和注射剂型,加强合理用药,减少和避免不良反应的发生。
关键词:药品不良反应;抗感染药物;注射剂;注射给药
1资料与方法
1.1资料来源数据来源于国家药品不良反应监测平台2013年收集的赣州市例不良反应报告,根据国家ADR级别判断标准,共有923 例新的和严重的不良反应报告,严重(包含新的严重)病例252例次,新的一般病例671例次。
1.2方法采用回顾性分析方法,对上报数据进行整理,按品种分布情况、剂型、给药途径、损害系统情况等进行统计分析。根据《药品不良反应报告和监测管理办法》中的分类办法,将不良反应类型分为一般的、严重的、新的一般的、新的严重的不良反应4类[1],本文重点对新的一般、严重的、新的严重的不良反应报告进行分析。
2结果
2.1报告基本信息情况2013年赣州市药品不良反应共5495例次,其中新的和严重的不良反应报告923例,占总数的16.8%,离世界卫生组织的标准(>30%)还有一定的差距。
2.2药品情况
2.2.1引起新的和严重的ADR药品品种情况引起新的和严重的ADR最多的药品为头孢曲松(41例次),见表1。
2.2.2引起新的和严重的ADR药品种类情况引起新的和严重的ADR药品种类以抗感染药最多,中药成方次之,分别为315例次和150例次,见表2。
2.2.3引起新的和严重的ADR抗感染药情况引起新的和严重的ADR抗感染药以抗生素最多,合成抗菌药次之,分别为221例次和64例次,见表3。
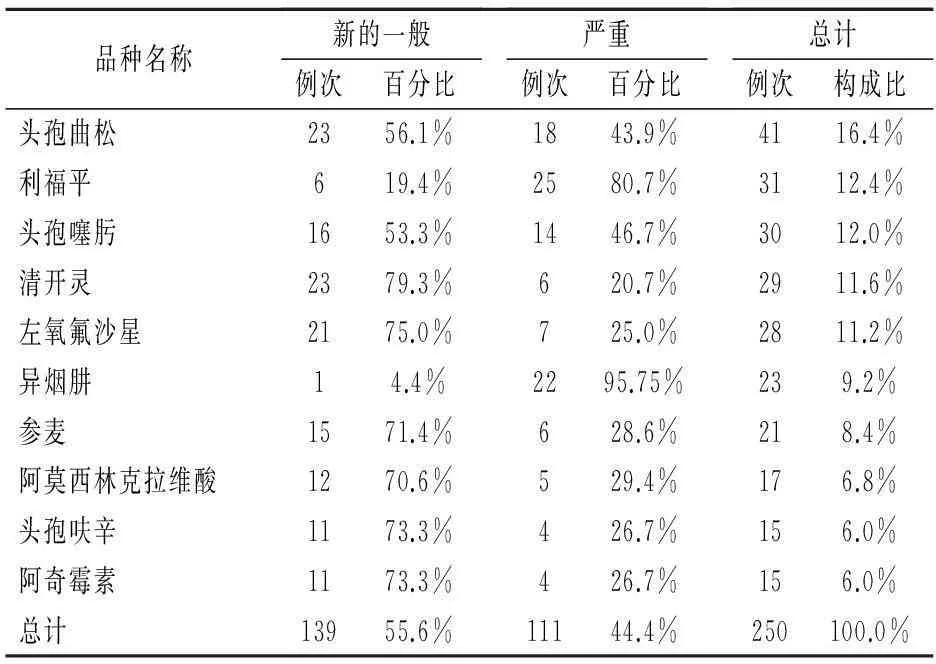
表1 新的和严重的ADR药品品种前10位分布情况表
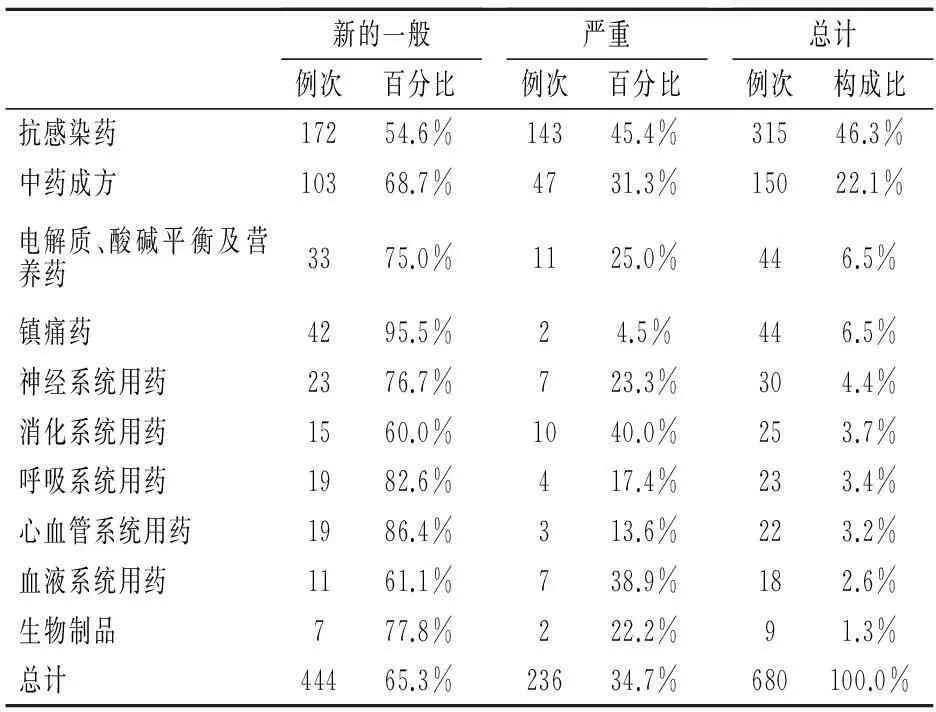
表2 新的和严重的ADR药品种类前10位分布情况表

表3 新的和严重的ADR抗感染药前10位分布情况表
2.3剂型情况统计2013年发生在赣州市新的和严重的ADR药品剂型情况,主要剂型为注射剂、胶囊剂和片剂,见表4。
2.4给药途径新的和严重的ADR给药途径主要以静脉滴注途径最多,为525例次,口服和肌肉注射次之,见表5。
2.5不良反应名称排位情况统计2013年发生在赣州市新的和严重的ADR不良反应名称前10位情况,严重的(包括新的严重的)主要不良反应为过敏样反应、高热、寒战,新的一般的主要不良反应为过敏反应,见表6。

表4 新的和严重的ADR药品剂型前10位分布情况表
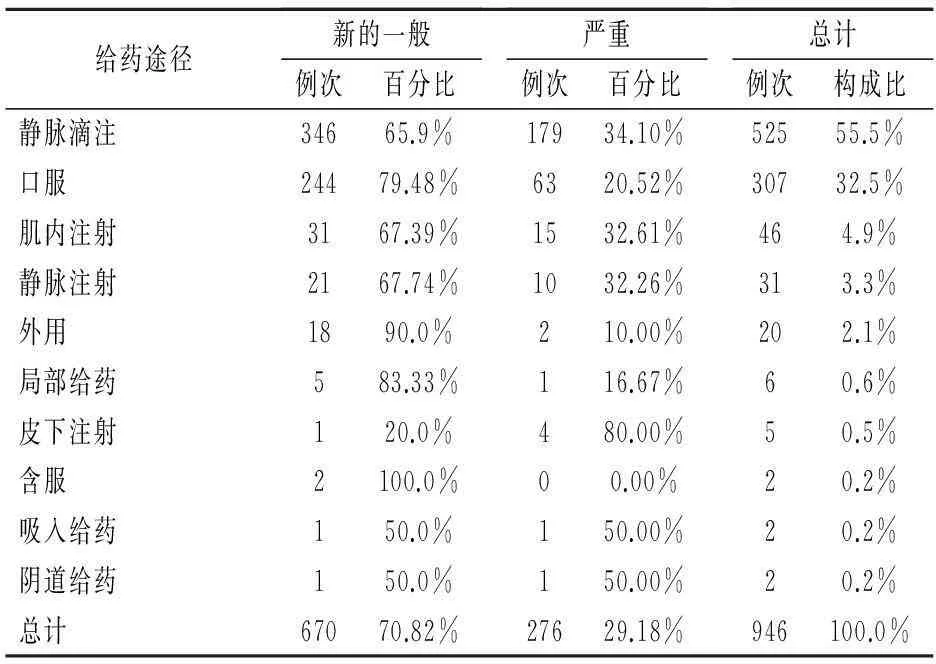
表5 新的和严重的ADR给药途径前10位分布情况表
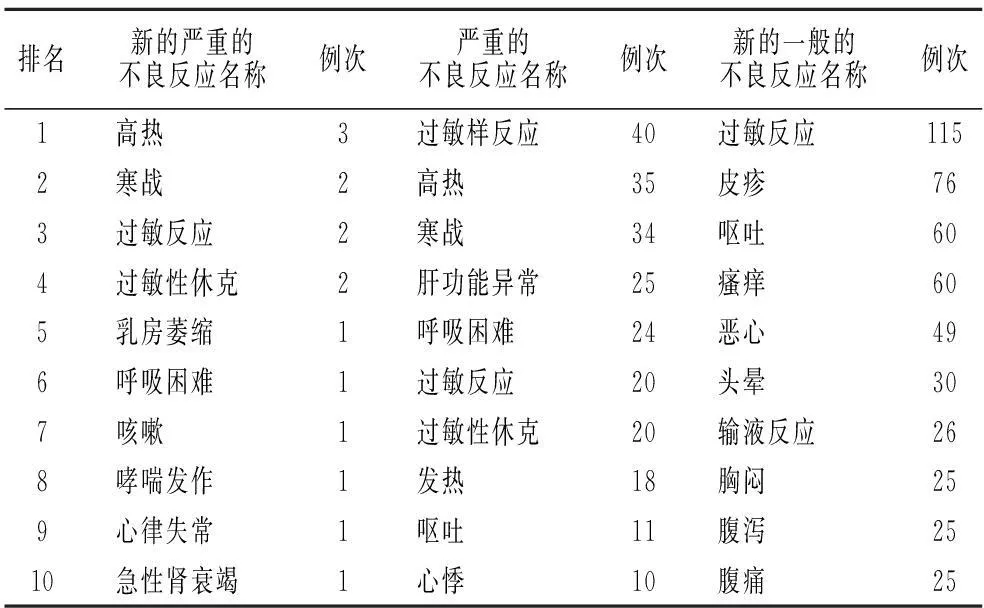
表6 新的和严重的ADR不良反应名称前10位情况表
2.6损害系统情况统计2013年发生在赣州市新的和严重的ADR损害系统情况,严重的(包括新的严重的)不良反应主要为全身性损害及呼吸系统损害,新的一般的不良反应主要为胃肠系统损害及全身性损害。
2.6.1严重的不良反应损害系统情况见表7。
2.6.2新的严重的不良反应损害系统情况见表8。
2.6.3新的一般的不良反应损害系统情况见表9。
3讨论
ADR报告是进行ADR分析评价的基础,其中新的和严重的报告数量及比例是影响ADR报告系统敏感度的重要指标之一。药品上市后,某些未知或严重的ADR不容易被发现,其对人体生命健康的威胁更大。一旦发现这类新的和严重的药品安全隐患,便需要重新对药品的风险和效益进行综合、定性或定量评价,以确定采取何种控制措施。往往都是因为在ADR 监测中发现了新的、严重的不良反应,因此这类报告是ADR监测中最需要关注的。笔者就2013年赣州市收集的新的和严重的ADR进行分析,提取出一些有价值的信息[2]。
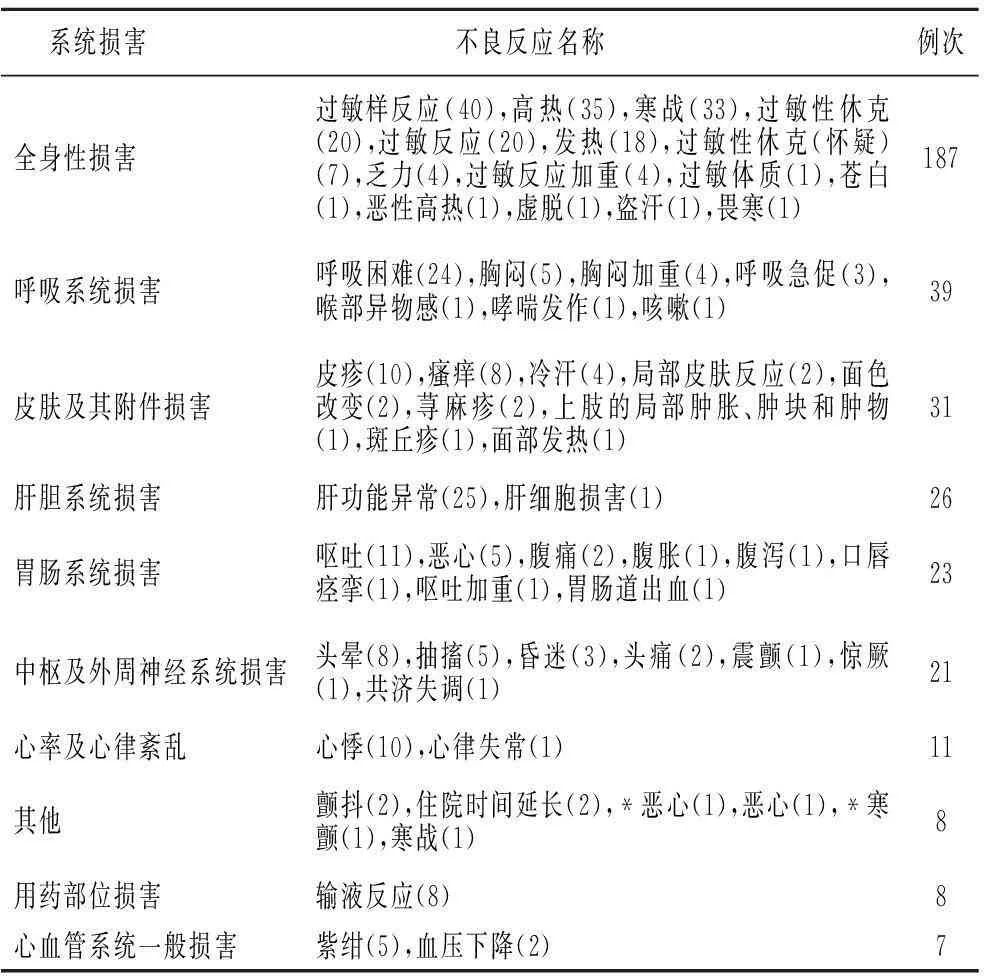
表7 严重的不良反应损害系统前10位情况表

表8 新的严重的不良反应损害系统前10位情况表
3.1ADR与药品品种的关系从表1-3可以看出,引起新的和严重的ADR 以抗感染药物为首,具体分类又以抗生素和合成抗菌药为最多,喹诺酮类、头孢菌素类发生的又最多,这与许多文献报道的一致,说明赣州市不良反应报告数据有一定的代表性。产生这一现象的原因,除了与抗感染药物种类多、使用频率高有关外,临床不合理用药甚至滥用也是不可忽视的因素。主要表现为无指征的预防用药,不必要的联合用药或重复用药,用药剂量过大、用药时间过长或不足、无原则的使用新药与价格昂贵的药物等。
引起新的和严重的ADR 以中药注射剂次之,这与中药注射剂成分复杂,纯度质量低,有效成分不明确,还混杂大量未知安全性成分,药理、毒理、疗效等机制尚未完全明确,缺乏统一的质量控制标准,在制备工艺上质量很难控制有关。另外在注射剂的生产过程中,为了提高药物的溶解度和稳定性,加入了过量的助溶剂、稳定剂等添加剂,加大了中药注射剂ADR 的发生率[3]。

表9 新的一般的不良反应损害系统前10位情况表
3.2从剂型和给药途径看ADR注射剂最易引起新的和严重的ADR,特别是静脉给药,一方面是因为临床上使用非常广泛,还因为静脉给药可使药物直接进入血液循环,在迅速发挥疗效的同时也增加了不良反应发生的可能性。并且静脉注射剂的ADR诱因很多,如内毒素、PH值、渗透压、热源、低温输液等[3]。静脉给药要掌握正确的配置方法,注意药品之间的配伍关系和药品的滴注速度。药品配伍发生作用、溶剂选择不当、药品浓度过高、滴速过快、配置液体保存时间过长等都易引起ADR。临床用药应根据患者的病情,合理选择给药途径,能口服和局部用药的尽量不要选择静脉给药。
3.3ADR与系统损害ADR涉及到全身各个系统,很多不良反应可涉及多系统受累,其中以全身性损害,呼吸系统、胃肠系统受累,皮肤及其附件损害最多,主要表现为高热、寒战、皮疹、瘙痒、恶心、呕吐。这与上述表现容易被临床发现有关。因此要加强对其他系统表现的临床症状的重视,尤其是产期用药患者,更应关注ADR对血液系统、肝、肾功能的影响。
预防和降低药品不良反应的发生率,尤其是严重的药品不良反应,对减轻患者伤害和经济负担,以及减少医疗卫生支出,具有十分重要的意义[4]。
参考文献
[1]药品不良反应报告和监测管理办法[S].卫生部令第81号,2011.
[2]王文沛,邵蓉.我国新的和严重的药品不良反应报告现状及障碍分析[J].中国药事,2011,25(3):227-230.
[3]林晓莲,罗海金,吴杨冰.注射剂致不良反应报告分析[J].中国医院用药评价与分析,2009,9(4):313-315.
The Report Analysis of 923 Cases of New and Serious Adverse Drug
LIU Xiao-yu, ZHANG Ruo-liang
TheFoodandDrugInspectionofGanzhouCity,Ganzhou341000,China.
Abstract:Objective: To analyze the reporting of new and severe adverse drug reaction in Ganzhou city and so as to provide a scientific basis for clinical rational drug use. Methods: Have a retrospective analysis in 923 new and severe adverse drug reports, which were reported to the national adverse drug reaction monitoring platform by the Institute for Food and Drug Control of Ganzhou in 2013. Results: Most of these new and severe adverse drug reactions were caused by anti-infection drugs. They take injection as the main dosage form and take injection as the main route of administration, and mostly caused systemic damage、respiratory system injury and the gastrointestinal system damage. Conclusion: Anti-infection drugs and injection should be given specific focus in clinical to reduce and avoid the occurrence of adverse reactions.
Key words:Adverse Drug Reactions; Anti-infective Drugs; Injection; Injection Treatment
收稿日期:(2014-10-31)编辑:万崇毅
中图分类号:R969.3
文献标识码:A
