HPLC法测定泡囊中蛇床子素的含量
2015-02-23游国叶熊大维李会娜
游国叶,熊大维,李会娜
(1.信阳职业技术学院药学院,信阳 464000; 2.杭州民生药业有限公司,杭州 311100)
HPLC法测定泡囊中蛇床子素的含量
游国叶1,熊大维1,李会娜2
(1.信阳职业技术学院药学院,信阳 464000; 2.杭州民生药业有限公司,杭州 311100)
目的:建立HPLC法测定非离子型表面活性剂泡囊中蛇床子素的含量。方法:采用Luna C18(250 mm×4.6 mm, 5 μm)色谱柱,以甲醇-水(85∶15)为流动相,流速1.0 ml/min, 320 nm处检测。结果:蛇床子素在浓度0.4~50 μg/ml范围内线性关系良好,回归方程为A=93 807C+18 201(r=0.999 9),平均回收率为98.09%,RSD为0.03%。结论:本法快速、准确,结果可靠,重现性好,适于蛇床子素制剂的质量控制。
蛇床子素,非离子表面活性剂泡囊,含量测定,HPLC
蛇床子素(osthole或osthol)是从伞形科植物蛇床的干燥成熟果实蛇床子中提取的一种强脂溶性化合物,又称作甲氧基欧芹酚,其易溶于碱溶液及某些有机溶剂如甲醇、乙醇、氯仿等,不溶于水,口服生物利用度差,临床具有抗菌、抗病毒、抗变态及补肾壮阳性激素样作用,还可用于抗心律失常、哮喘的治疗,对多种实验肿瘤有明显的抑制活性[1,2]。泡囊组成和结构类似于脂质体,主要由非离子型表面活性剂组成,药物不易泄漏,比脂质体稳定,具有多种优势,其载体材料不含磷脂,避免了磷脂的氧化降解[3]。近年来非离子表面活性剂泡囊包封技术已经成为化学、药学和生命科学研究领域中的热点课题之一。本试验采用HPLC法测定蛇床子素非离子表面活性剂泡囊中蛇床子素的含量,结果可靠,适于该制剂的质量控制。
1 仪器和试药
BP211D型半微量电子天平、Waters2695高效液相色谱仪,Waters2996紫外检测器 (美国Waters公司);100 μl进样针(江苏汉邦科技有限公司)。 蛇床子素原料药(上海纯优生物科技有限公司,批号P0086),蛇床子素对照品(中国药品生物制品检定所,批号110822-201308),甲醇为分析纯。
2 试验方法与结果
2.1 色谱条件 色谱柱:Luna C18(250 mm×4.6 mm,5 μm);流动相:甲醇-水(85∶15);流速:1.0 ml/min;检测波长:320 nm;柱温:室温;进样量:20 μl[4]。
2.2 溶液制备
2.2.1 对照品溶液制备 取蛇床子素对照品适量,用流动相溶解并稀释至刻度,准确配制浓度为200 μg/ml的蛇床子素对照品贮备液,备用。精密量取对照品贮备液0.5 ml置于10 ml量瓶中,流动相定容至刻度,摇匀,即得10 μg/ml的蛇床子素对照品溶液。
2.2.2 供试品溶液制备 按既定处方工艺制备本品,取本品(含蛇床子素泡囊混悬液)1 ml于100 ml的量瓶中,流动相定容,即得10 μg/ml的供试品溶液。
2.2.3 阴性对照溶液 另按处方量取不含药的泡囊混悬液1 ml于100 ml的量瓶中,流动相定容,得相当于含10 μg/ml的阴性对照液蛇床子素空白泡囊。
2.3 干扰试验 分别取对照品、供试品和阴性样品溶液20 μl按“2.1”项下色谱条件进样测定,色谱图见图1。试验可见在该色谱条件下,蛇床子素能达到基线分离且峰形稳定,保留时间约为8.5 min,非离子表面活性剂泡囊辅料及破乳剂不干扰蛇床子素的测定。

1.蛇床子素
2.4 蛇床子素标准曲线的绘制 精密称取蛇床子素对照品适量,以流动相定容至刻度,准确配制200 μg/ml的贮备液。分别精密吸取贮备液0.02、0.05、0.1、0.5、1、1.5和2.5 ml置10 ml量瓶中,以甲醇定容至刻度,摇匀,得浓度分别为0.4、1、2、10、20、30和50 μg/ml的系列溶液,进样测定,以峰面积A对浓度C作线性回归,得标准曲线方程:A=93 807C+18 201(r=0.999 9),即蛇床子素在浓度0.4~50 μg/ml范围内,峰面积与测定浓度呈良好的线性关系。
2.5 重复性试验 取本品(批号为20130304)的样品共6份,按照“2.2.2”项下供试品溶液的方法制备,依照“2.1”项下色谱条件分析,测定每份样品溶液中蛇床子素含量。结果显示样品中蛇床子素浓度含量平均为9.86 μg/ml,RSD为1.7 %。表明供试品溶液重复性良好。
2.6 稳定性试验 取重复性试验中的1份样品,分别在0、4、8、12、16、20和24 h按“2.1”项下色谱条件分析,测得供试品溶液中蛇床子素浓度,RSD为0.99%。结果表明,供试品溶液在24 h内基本稳定。
2.7 精密度试验 精密量取蛇床子素储备液适量配制浓度分别为2、20和50 μg/ml的RES溶液3份,按“2.1”项下色谱条件进样,每份样品每隔4 h测定1次,共测5次;每份样品每日测1次,连续测定5 d。分别计算RES的日内及日间精密度。精密度试验结果可知,精密度良好。见表1。
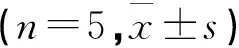
表1 蛇床子素精密度试验结果
2.8 回收率测定 精密量取100 mg含量为99.9%的蛇床子素9份, 分别置于量瓶中,分别加入50、100和200 μg/ml对照品溶液10 ml,各3份,依“2.1”项下色谱条件测定,计算回收率,结果平均回收率为98.09%,RSD为0.03%,表明用HPLC测定蛇床子素的含量准确度良好,见表2。

表2 回收率试验结果
2.9 蛇床子素非离子表面活性剂泡囊含量测定 按照制备方法平行制备3批含药制剂(批号20130304、20130305、20130306),分别精密吸取蛇床子素非离子表面活性剂泡囊1 ml置50 ml量瓶中,以流动相定容至刻度,摇匀,过滤,进样分析,记录色谱图并将峰面积带入标准曲线中计算主药含量,结果见表3。

表3 蛇床子素泡囊含量测定结果(n=3)
3 讨论
3.1 流动相的选择 通过文献查阅和反复预试验,在紫外扫描的基础上确定了主药的测定波长。对不同比例的甲醇- 水、乙腈- 水进行预试验, 结合所得色谱图及实验室现有条件,最终根据既保证药峰与杂质峰分离度及理论塔板数符合《中国药典》规定又保证经济实惠的原则,选择了甲醇-水(85∶15)为流动相,室温条件下测定非离子表面活性剂泡囊中蛇床子素的体外含量分析方法,以HPLC测定蛇床子素的含量,试验条件下线性关系良好,精密度、回收率均符合《中国药典》规定,重现性好,方法学考查表明此法可用来进行含蛇床子素制剂的含量测定。
3.2 波长的选择 在文献查阅基础上,取处方量蛇床子素标准品和不含药的空白辅料混合物,分别置于25 ml量瓶中,流动相溶解定容,备用。以流动相为空白,分别取上两溶液进行紫外扫描,由试验可知在320 nm处标准品有最大吸收峰,不含药的空白辅料混合液无吸收,故选择320 nm为最佳波长。
1 张泽君,张欣.蛇床子素化学成分及药理学研究进展[J].黑龙江医药,2011,24(2):275-276
2 刘慧英,杜晓丹.骨筋丸质量标准提高[J].黑龙江医药,2013,26(2):310-312
3 张林华,何颖娜,马桂磊,等.叶酸靶向紫杉醇聚合物纳米泡囊的制备及其抗肿瘤活性的研究[J].中国药学杂志,2010,45(22):1742-1748
4 陆春宁,梁艺坚,曹耘,等. HPLC测定花蛇解痒胶囊中蛇床子素的含量[J]. 中国实验方剂学杂志,2013,19(12):98-100
Determination of Osthole in Nonionic Surfactant Vesicles by HPLC
You Guoye1, Xiong Dawei1, Li Huina2
(1. School of Pharmacy in Xinyang Vocational and Technical College Xinyang,Xinyang 464000; 2. Hangzhou Minsheng Pharmaceutical Co Ltd, Hangzhou 311100)
Objective: To establish an HPLC method for the determination of osthole in nonionic surfactant vesicles. Methods: A Luna C18(250 mm×4.6 mm,5 μm) column was used as stationary phase,and methanol-water (85∶15) as mobile phase with a flow rate of 1.0 ml/min. The wavelength was set at 320 nm. Results: The linear range of osthole was 0.4~50 μg/ml, the regression equation was expressed byA=93 807C+18 201 (r=0.999 9), the average recovery was 98.09%,and RSD 0.03%. Conclusion: this method is rapid, accurate, reliable, reproducible, suitable for the quality control of osthole preparation.
osthole,nonionic surfactant vesicles,determination,HPLC
2014-02-17
R927.2
A
1006-5687(2015)01-0019-03
