微波辐射下槲皮素硅胶表面印迹聚合物的制备及其吸附性能分析*
2015-02-22丁妍华,刘文琴,白文婷等
微波辐射下槲皮素硅胶表面印迹聚合物的制备及其吸附性能分析*
★丁妍华*刘文琴白文婷谢一辉*
(江西中医药大学药学院南昌 330004)
摘要:目的:微波辐射下制备槲皮素硅胶表面印迹聚合物,并考察其吸附性能。方法:以槲皮素为模板分子,KH-570为硅烷化试剂,微波辅助条件下在硅胶表面合成了分子印迹聚合物。用正交试验优化了硅胶表面改性以及硅胶表面分子印迹的制备工艺。结合高效液相色谱法对制备得到的分子印迹聚合物特异性吸附进行验证。结果:利用微波辐射将反应时间缩短了十几倍。Scatchard模型分析得到其平衡常数Kd=4.44mg/L,最大吸附量Qmax=2.87μmol/g。结论:确定了微波辐射下硅胶表面分子印记聚合物的制备工艺,吸附性能良好。
关键词:表面分子印迹聚合物;槲皮素;微波辅助;正交试验
经典的植化分离分析模式需要多次过柱,耗费大量的时间以及人力物力。分子印迹聚合物(Molecular Imprinted Polymers,MIPs )具有与模板分子相匹配的空穴和由功能单体形成的特定识别位点[1],能够特异性的吸附模板分子,而且环境适应能力强、稳定性好、可重复使用、灵敏度高[2],广泛应用于固相萃取、传感器、色谱、模拟酶催化等领域[3],在中药有效成分分离富集方面优势显著。本课题组在商品硅胶表面进行印迹,其颗粒大,可作为中压柱的固定相,目标成分与母液可实现快速分离。本研究以覆盆子乙酸乙酯部位的有效成分槲皮素为模板分子,重点考察了微波辅助下硅胶表面硅烷化以及表面印迹的制备工艺,探索出硅胶表面印迹聚合物的制备方法。
1仪器和试剂
4-乙烯吡啶,乙二醇二甲基丙烯酸甲酯,硅烷偶联剂KH-570(均购自阿拉丁试剂有限公司);偶氮二异丁腈(天津市光复精细化工研究所);硅胶(300~400目)(青岛鼎康硅胶有限公司);甲醇乙腈均为色谱纯,其余试剂均为分析纯。
槲皮素对照品(自制,纯度为99.11%)。Agilent 1260 高效液相色谱仪(美国安捷伦科技有限公司);微波萃取仪(上海新仪微波化学科技有限公司);Sartorius BS214-D天平(赛多利斯科学仪器有限公司);KQ3200超声波清洗器(昆山超声仪器厂);自动三重蒸馏水器(上海亚荣生化仪器有限公司);FT-IR Spectrometer(Spectrum Two PerkinElmer UATR Two);UV-1750紫外分光光度计(岛津科技有限公司)。
2方法
2.1硅胶酸活化300~400目硅胶200g过筛,选取粒径40μm左右的硅胶,加入50%(V/V)的硝酸回流6h,冷却静置,用蒸馏水洗涤至中性,自然沉降12h,加入50%(V/V)的浓盐酸,室温浸泡6h,蒸馏水洗至中性,硝酸银溶液检验后无氯离子,80℃真空干燥12h,保存于棕色试剂瓶中备用。
2.2硅胶表面硅烷化以硅胶表面硅烷化的得率为指标,考察微波时间、KH-570用量和合成温度对硅烷化实验的影响。
取酸活化后的硅胶16份,每份50g,按表1条件,依次加入无水甲苯250mL,一定量的KH-570,置于微波萃取仪中,三颈烧瓶上方分别连接冷凝管,装有搅拌棒的玻璃管,氮气管路。设置温度为规定温度,以300r/min速度搅拌,氮气保护下,用100w微波功率加热回流至规定时间。抽滤,转入索氏提取器中用无水乙醇抽提12h洗去杂质。于80℃真空干燥12h,得到KH-570硅烷化硅胶。

表1 硅胶表面硅烷化正交试验条件
2.3槲皮素硅胶表面印迹聚合物制备结合覆盆子乙酸乙酯部位的指纹图谱,以槲皮素硅胶表面印迹聚合物特异性吸附槲皮素等黄酮类成分的量为优化指标,考察微波时间,乙二醇二甲基丙烯酸酯用量,4-乙烯吡啶用量,致孔剂氯仿用量,甲醇用量对槲皮素硅胶表面印迹聚合物合成效果的影响。
取3.2中表面硅烷化的硅胶16份,每份5g,分别加入槲皮素的丙酮溶液10mL(4 mg/mL),充分搅拌,按表2条件分别加入4-乙烯基吡啶氯仿溶液、乙二醇二甲基丙烯酸酯氯仿溶液、偶氮二异丁腈甲苯溶液3mL(13.5 mg/mL)、甲醇,用30mL四氯化碳转移至三颈烧瓶。设置微波萃取仪功率100W,温度60℃加热回流至规定时间,无水乙醇洗涤数次,滤过,转入索氏提取器中,甲醇乙酸(9∶1)抽提模板分子,直至抽提液在200~400nm范围内紫外吸收均小于0.01。 再用甲醇洗至中性,80℃真空干燥即得到槲皮素硅胶表面印迹聚合物。

表2 槲皮素分子印迹聚合物正交试验条件
2.4样品制备取覆盆子乙酸乙酯提取浸膏0.3g,加乙醇13mL溶解,加入1.75g槲皮素硅胶表面印迹聚合物,振摇1h。转入色谱柱中,分别用17.5mL三蒸水、17.5mL 30%甲醇洗涤,再用27.5mL色谱甲醇洗脱。甲醇洗脱液氮吹水浴蒸干,加甲醇定容至2mL。
2.5紫外测定取最后的抽提液,以甲醇乙酸(9∶1)为空白对照液,在200~400nm范围内紫外扫描,记录紫外吸收。
2.6红外测定取过筛后的硅胶和槲皮素硅胶表面印迹聚合物分别进行红外测定。
2.7HPLC法测定色谱条件:迪马C18色谱柱,流动相为乙腈(A)∶0.1%甲酸溶液(B):(0~70min,A 3%~22%;70~90min,A 22%~30%;90~105min,A 30%~45%;105~115min,A 45%~100%),检测波长266nm,柱温30℃,流速1mL/min,进样量20μL。
2.8吸附性能测试取浓度分别为0.5,1,1.5,2,2.5mg/100mL的槲皮素乙腈溶液各100mL,精密称取1.00g印迹聚合物5份分别混悬于上述槲皮素乙腈溶液中,室温下混悬1h后静置,取上清液373nm处测定吸光度。静态饱和吸附量公式为Qe=(C0-Ce)V/M,其中Qe为吸附量(mg/g)即每克印迹聚合物吸附槲皮素的量;C0、Ce(mg/mL)分别为吸附前后槲皮素溶液的浓度,V(mL)为溶液的体积;M(g)为加入印迹聚合物的质量。
根据Scatchard方程Q/Ce=(Qmax-Q)/Kd推算出结合平衡常数Kd及最大吸附量Qmax。式中Q和Qmax分别为平衡吸附量和最大吸附量,Ce为平衡时溶液中槲皮素的浓度;Kd为平衡时结合位点的平衡解离常数,以Q/Ce对Q作图,公式转换成Q/Ce= (-1/Kd)Q+Qmax/Kd,根据线性关系斜率和截距可以求得Kd和Qmax两个参数。
3结果和讨论
3.1硅胶表面硅烷化实验结果分析以硅烷化后增加的重量除以加入的硅烷化试剂量为得率,计算各实验条件下产物得率。结果见表3。实验结果用SPSS19.0分析,结果见表4。由表4可知,考察的3个因素中,微波辅助时间和硅烷化试剂用量有显著性差异,反应温度没有显著性差异。影响因素顺序为:微波反应时间>硅烷化试剂用量>反应温度。各因素水平均值显示最佳条件为:微波辅助时间2h,硅烷化试剂用量20mg,反应温度95℃。以该条件重复合成3次,得率分别为:89.02%、88.08%和88.37%。
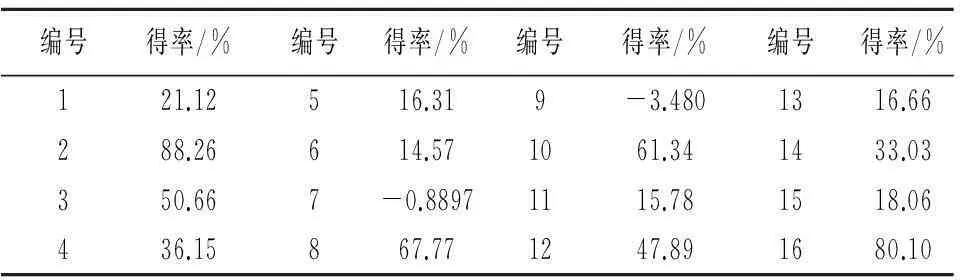
表3 硅胶表面硅烷化正交试验结果
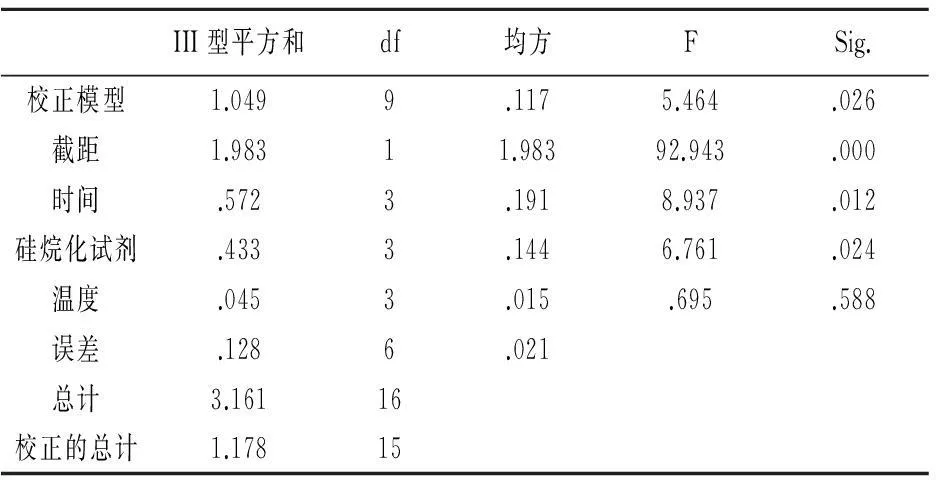
表4 正交试验各因素显著性分析结果
3.2FT-IR结果图1虚线部分放大后显示,硅烷化硅胶:在1635.52 cm-1处有一吸收峰,为硅烷化支链上烯烃的碳碳双键伸缩振动吸收。在1059.43 cm-1处硅烷化硅胶和槲皮素硅胶表面印迹聚合物均有的硅氧键伸缩振动吸收峰。槲皮素硅胶表面印迹聚合物在1717.25 cm-1有羰基吸收峰,为交联剂分子中的酯键。MIPs中1637.30 cm-1吸收峰较硅烷硅胶的1635.05 cm-1明显减小,几乎不可见,说明硅烷化硅胶的双键与功能单体及交联剂中的双键已基本聚合。而且聚合后形成的脂肪链的碳氢面内弯曲振动吸收在MIPs图谱中可见于1454.05 cm-1。MIPs中754.50 cm-1和666.72 cm-1双峰,为苯环单取代吸收峰,说明功能单体4-乙烯吡啶已聚合于MIPs分子中。上述红外光谱提示槲皮素硅胶表面印迹聚合物合成成功。
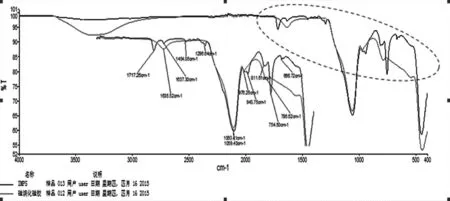
图1 红外图谱对比
3.3HPLC分离效果取条件优化实验中所得每份槲皮素硅胶表面印迹聚合物,分别按2.4样品制备方法分离覆盆子乙酸乙酯提取液中槲皮素,各洗脱液分别按指纹图谱条件进行分析。结果显示(图2):槲皮素硅胶表面印迹聚合物能有效地从覆盆子乙酸乙酯提取液中分离出槲皮素。同时被分离的少量其它成分,经检测初步鉴定为黄酮类成分。
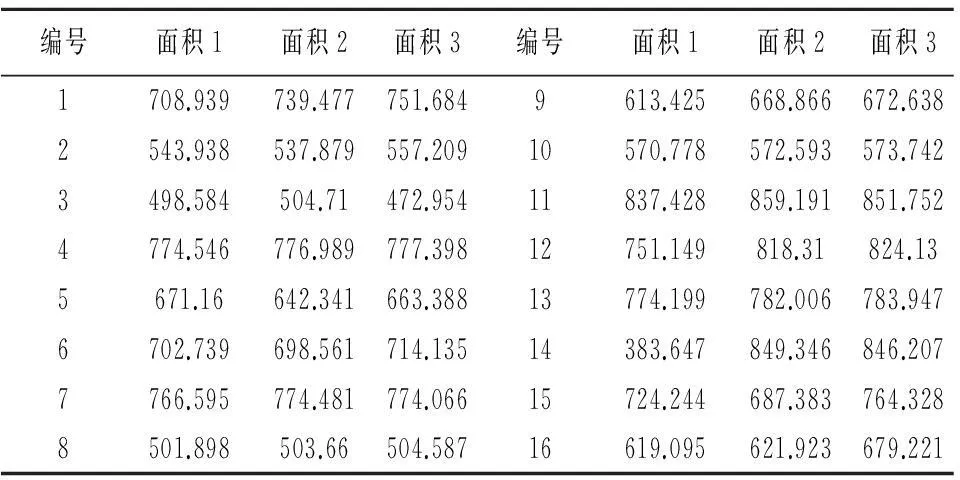
3.4槲皮素硅胶表面印迹聚合物正交实验的结果与分析根据指纹图谱分析结果,分别累计黄酮类成分的峰面积,作为槲皮素硅胶表面印迹聚合物吸附黄酮成分总量。以黄酮成分总量为优化指标,用SPSS19.0进行分析。分析结果(表5-6)显示:考察的各因素均有非常显著的差异,影响因素顺序为:甲醇用量>氯仿用量>4-乙烯吡啶>交联剂>反应时间。各因素水平均值显示最佳条件为:甲醇用量1 mL,氯仿用量6mL,4-乙烯吡啶28mg,交联剂23.6mg,微波辅助时间1.5h。以最优条件合成槲皮素硅胶表面印迹聚合物,按样品分离方法分离覆盆子乙酸乙酯提取液中黄酮类成分,经HPLC检测,峰面积分别为837.428, 798.584, 853.938,表明该工艺基本稳定。
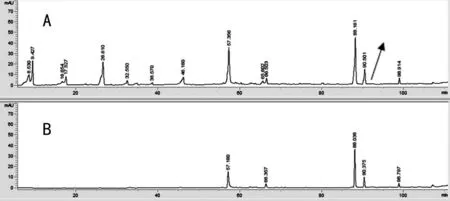
图2 槲皮素印迹聚合物分离效果指纹图谱比较
编号面积1面积2面积3编号面积1面积2面积31708.939739.477751.6849613.425668.866672.6382543.938537.879557.20910570.778572.593573.7423498.584504.71472.95411837.428859.191851.7524774.546776.989777.39812751.149818.31824.135671.16642.341663.38813774.199782.006783.9476702.739698.561714.13514383.647849.346846.2077766.595774.481774.06615724.244687.383764.3288501.898503.66504.58716619.095621.923679.221
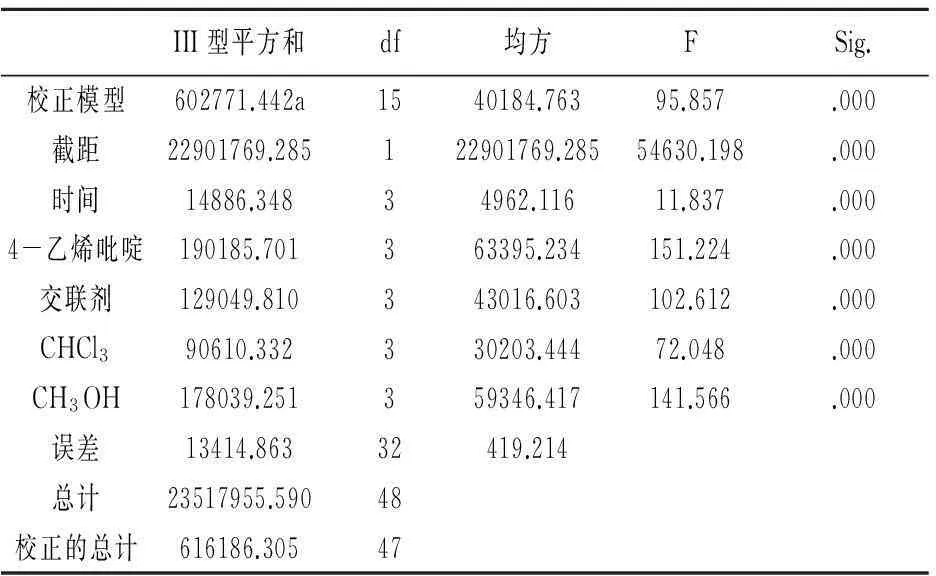
表6 正交实验各因素显著性分析结果
3.5吸附性能分析根据2.8实验步骤得出吸附等温线见图3,线性关系良好。Scatchard分析图见图4。由图4可见,槲皮素硅胶表面印迹聚合物的Scatchard吸附曲线基本上是一条直线,表明在该浓度范围内硅胶表面印迹聚合物对模板分子槲皮素存在特异的结合位点。线性方程为:Y=-0.2251X+0.1953,r=0.9992。根据方程可以算出平衡解离常数Kd=4.44mg/L 最大吸附量Qmax=2.87μmol/g。
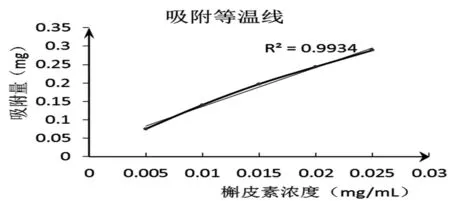
图3 吸附等温线图
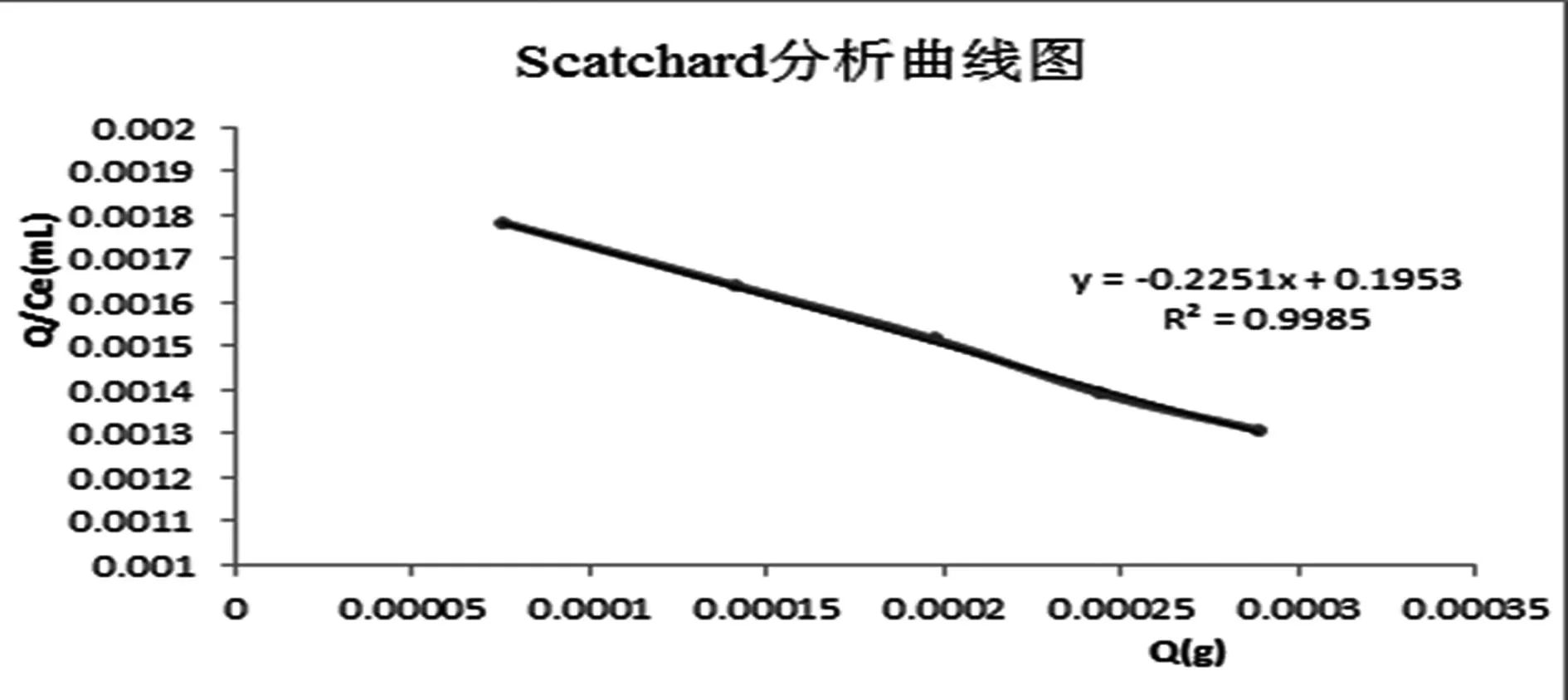
图4 Scatchard分析曲线图
4结论
聚合反应中,微波辐射大大缩短了反应时间,提高了反应效率,为工业化生产进行了有益探索。微
波辅助的非热效应可有效的降低有机化合物反应的温度。一般硅胶表面硅烷化需要在较高的温度进行。该研究表明,温度对硅烷化效率无显著性影响,而且温度在95℃最佳。这可能是微波改变了反应动力学,降低了反应活化能即微波辅助的非热效应所致。前期没有微波辐射下的硅胶表面改性以及表面印迹实验往往需要反应12 h以上,尤其硅烷化实验需要油浴110℃加热才能完成,最大吸附量也只达到0.6μmol/g,微波辐射大大缩短了反应时间,使最佳制备工艺的考察成为可能。
溶剂系统对硅胶表面印迹聚合物的合成有决定性的影响,适宜的溶剂系统,有利于印迹聚合反应在硅胶表面进行,当溶剂对模板分子的溶解度过大、交联剂过量,均有可能使印迹聚合物在溶液中进行,而不是聚合在硅胶表面。
参考文献
[1]盖青青,刘秋叶,何锡文,等.分子印迹技术用于蛋白质的识别[J].化学进展,2008, 20(6):957-968.
[2]赵晨,贾光锋,陆文总,等.表面分子印迹法制备棉酚印迹聚合物及其性能检测[J].科学技术与工程,2014,14(16):88-93.
[3]李小红,曹玉华,高婀娜.分子印迹固相萃取牛奶中甲胺磷[J].分析实验室,2009,28(6):5-8.
收稿日期:(2015-05-18)编辑:曾文雪
中图分类号:TQ317.5
文献标识码:A
通信作者:谢一辉(1958—),男,教授。研究方向:中药有效成分分析。E-mail:243619851@qq.com。
基金项目:第一作者:丁妍华(1990—),女,在读硕士研究生。研究方向:中药有效成分分离与富集。E-mail:dyh1107@126.com。
