放疗联合EGFR-TKIs治疗非小细胞肺癌新进展
2015-02-20吴侃王冰夏冰张仕蓉马胜林
吴侃 王冰 夏冰 张仕蓉 马胜林
·特约综述·
放疗联合EGFR-TKIs治疗非小细胞肺癌新进展
吴侃 王冰 夏冰 张仕蓉 马胜林

马胜林,教授,主任医师,博士研究生导师。现任杭州市第一人民医院集团院长,中华医学会肿瘤放疗分会热疗学组组长,亚洲肿瘤热疗学会副理事长,中国抗癌协会肿瘤放射治疗专业委员会副主任委员、抗癌药物专业委员会副主任委员、临床肿瘤协作中心脑转移肿瘤专家委员会副主任委员、肺癌专业委员会委员,中国药理学会肿瘤药理学与化疗专业委员会副主任委员,主持国家"863"计划子课题、国家卫计委重大行业专项子课题、国家新药创制、国家自然科学基金、省自然基金重点、省部共建基金等10余项科研项目,获省、市科技进步奖10余项,发明专利5项等。入选浙江省首批卫生高层次创新人才、浙江省“新世纪151人才工程”第一层次,获浙江省有突出贡献中青年专家荣誉称号及获国务院特殊津贴。担任LUNG CANCER中文版、Journal of Thoracic Oncoloyg中文版、中华放射肿瘤学等多家杂志编委,作为编委起草了国家卫计委印发的《原发性肺癌、肝癌诊疗规范》。在国内外学术刊物上发表论文100余篇,SCI收录30余篇。主编专著6部,参编著作2部。
在全球范围内,肺癌是造成癌症死亡的最主要原因。非小细胞肺癌(non-small cell lung cancer,NSCLC)约占肺癌的80%,由于缺乏早期诊断的有效手段,临床上首诊NSCLC患者仅25%~30%可选择根治性手术。对于不能手术切除的局部晚期及晚期NSCLC,单纯放射治疗或放化疗综合治疗是主要治疗手段,但总体疗效并不理想。近年来,靶向药物开创了NSCLC个体化治疗时代,越来越多的证据提示以表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine kinase inhibitors,EG⁃FR-TKIs)为代表的靶向药物联合放疗或放化疗治疗NSCLC具有一定的前景。本文就EGFR-TKIs联合放疗治疗不可手术的局部晚期及晚期NSCLC的新进展做一综述。
NSCLC 放射治疗 EGFR-TKI
随着肺癌驱动基因研究的逐步深入,肺癌靶向治疗取得了较大进展,表皮生长因子受体酪氨酸激酶抑制剂(epidermal growth factor receptor tyrosine ki⁃ nase inhibitors,EGFR-TKIs)已广泛应用于晚期非小细胞肺癌(non-small cell lung cancer,NSCLC)的治疗。EGFR-TKIs主要通过竞争性结合三磷酸腺苷的酪氨酸激酶结构域,破坏EGFR活性,阻断其信号传递,从而阻滞癌细胞的增殖、生长和存活等。近年来研究发现,EGFR-TKIs还具有放射增敏作用,其机制包括阻滞细胞周期、诱导细胞凋亡、抑制DNA损伤修复[1-2]等,而基于其毒副作用低、患者耐受性好的特点,EGFR-TKIs有望成为理想的放射增敏剂。本文就EGFR-TKIs与放疗联合治疗不可手术的局部晚期及晚期NSCLC的临床研究进行综述。
1 放疗联合EGFR-TKIs治疗局部晚期NSCLC
临床上超过1/3的NSCLC为不可手术的局部晚期NSCLC。目前NCCN指南推荐对于不可手术的局部晚期NSCLC患者,如体力状态良好且预计生存期较长者应接受根治性同步化放疗。然而同步放化疗总体疗效仍然不尽如人意,且耐受性较差,因此同步放化疗联合靶向治疗能否提高疗效成为近年来的研究热点。
同步放化疗联合靶向药物的Ⅰ、Ⅱ期临床试验较多,然而疗效提高并不明显。2008年Journal of Thoracic Oncology(JTO)报道的一项Ⅰ期临床试验[3]将34例不可切除的Ⅲ期NSCLC患者平均分入A、B两组,A组接受erlotinib联合EP方案化疗同步胸部放疗,B组则接受erlotinib联合PC方案化疗同步放疗的治疗方案,两组耐受性均良好,但中位总生存期并不乐观(10.2个月vs.13.7个月)。该研究入组患者均为突变状态未明的患者,由于总体人群中EGFR突变的患者仅约1/3,可能疗效的提高不能显著影响总的生存,提示后续研究应根据突变情况选择入组人群。其后的一项Ⅱ期临床试验CALGB30106[4]入组63例Ⅲ期NSCLC患者,行PC方案诱导化疗联合gefitinib 2周治疗,根据患者一般情况分成good-risk组和poorrisk组,good-risk组继续采用PC方案化疗加gefitinib同时联合放疗(66 Gy/33 f/7 w),poor-risk组仅采用ge⁃fitinib联合放疗,完成7周治疗后单用gefitinib维持直至肿瘤进展或毒性不可耐受。该研究结果显示,poorrisk组中位总生存期(19.0个月vs.13.0个月)和无进展生存期(13.4个月vs.9.2个月)均优于good-risk组,且超过试验预设的中位总生存期(13个月),然而EGFR突变患者未见无进展生存期及总生存期的额外获益。该研究显示在同步放化疗期间接受EGFR-TKIs治疗的Ⅲ期NSCLC患者较接受单纯放疗联合EGFR-TKIs治疗者总生存期短,阴性结果可能与化疗联合靶向不能增加疗效(INTACT1、INTACT2、TRIBUTE、TAL⁃ENT)有关,TKIs使肿瘤细胞停止增殖、细胞周期停滞,从而可能减少肿瘤细胞对细胞毒性药物的敏感性。
基于上述研究,研究者尝试TKIs联合单纯放疗治疗局部晚期NSCLC,RTOG0972[5]入组75例未经选择、一般情况较差的Ⅲ期NSCLC患者接受化疗诱导后erlotinib同步放疗的治疗方案,取得了可喜的结果,治疗后中位无进展生存期和总生存期分别为11个月和17个月,1年总生存率为57%,高出试验预设的50%。此外,根据EGFR突变状态选择入组人群可能带来更好的生存获益,一项gefitinib同步放疗治疗局部晚期EGFR突变阳性NSCLC的小样本研究[6]中,入组的9例患者中2例携带19Del者获得了PR并长期生存达到5年以上。上述研究提示TKIs同步放疗对EGFR敏感突变的患者是有希望的治疗方案,当然该结果仍需要大样本研究进一步证实。目前放疗联合靶向药物的应用模式(包括联合方式、TKIs治疗时间、突变类型的选择等)尚存在许多疑问,国内已开展多项TKIs联合单纯胸部放疗治疗EGFR突变的局部晚期NSCLC的临床研究,如评估同步erlotinib对比同步EP方案治疗EGFR敏感突变的局部晚期NSCLC的疗效及安全性的前瞻性多中心临床研究等,期待这些研究为临床治疗模式的确立提供更多依据。
2 放疗联合EGFR-TKIs治疗晚期NSCLC
约50%NSCLC患者首诊时即伴有远处转移,且生存期短,缓解症状和提高生存质量是主要目的。放射治疗是晚期NSCLC姑息治疗的重要手段,姑息性放疗通常采用较低的剂量和较少的分割次数。然而近年来研究显示更高剂量和分割次数的姑息性放疗可能带来生存获益,其中一项Meta分析[7]纳入了13项随机临床研究的3 473例患者,发现胸部高剂量放疗组较低剂量放疗组有更优的1年生存率(26.5%vs. 21.7%,P=0.002),尽管其中只有一项研究[8]采用了50 Gy以上的放疗剂量。随后Chen等[9]回顾性分析了1 574例参加癌症治疗结局研究和监测联盟(CanCORS)的转移性NSCLC患者,在接受胸部放疗的21%患者中,放疗剂量在30 Gy以上的患者为65%,50 Gy以上为33%,42%患者放疗分割次数超过20次,剂量和分割次数均超过目前的姑息治疗模式。上述研究表明放射治疗在晚期NSCLC治疗中地位逐渐提高。
随着EGFR-TKIs的广泛应用,NSCLC生存期较以往明显延长,也为放疗提供了机会。来自美国MSKCC[10]和韩国YONSEI[11]的两项临床研究均提示胸内复发是TKIs治疗后的主要失败模式,复发率在60%左右。在临床研究中,出现T790M突变而导致TKIs获得性耐药的肺癌患者比例为50%并表现出有别于其他耐药机制的临床生物学行为,构成了相对特殊的一类肺癌群体。Oxnard等[12]对93例EGFR敏感型突变肺癌患者出现TKIs获得性耐药后进行了再次活检,发现相对远处转移病灶,T790M突变更多见于原发病灶、胸膜以及纵隔、肺门的淋巴结(P=0.014),而且携带T790M突变的患者预后较好,表现出更为缓慢的临床进展,提示积极的局部治疗有可能会为患者带来额外的临床获益。Yu等[13]在2013年JTO的研究显示,局部治疗(放疗及手术)配合EGFR-TKIs的继续治疗策略对于TKIs耐药患者有效,无进展生存期为10个月,自局部治疗起总生存为41个月。TKIs治疗失败时,加入放疗可能延缓疾病的进展,其潜在益处可能包括消灭非交叉抵抗的肿瘤克隆、与TKIs的协同作用以及最大化TKIs的治疗获益(延长疾病无进展生存期)等,但应选择合适的患者,考虑寡转移、PS评分及合理的照射野等因素。
对于一线化疗后进展的患者,TKIs联合放疗亦极具前景。2014年Journal of Clinical Oncology一项Ⅱ期临床研究[14]入组24例接受以铂类为基础的化疗后出现进展的患者,给予立体定向放射治疗同步erlo⁃tinib靶向治疗,共有52个部位接受了立体定向放射治疗,中位无进展生存期14.7个月,中位总生存期20.4个月,仅6.4%患者疾病进展出现在既往接受过放疗的区域,提示放疗在转移病灶治疗中的价值。一项EGFR-TKIs同步放疗治疗晚期/转移性NSCLC的Ⅱ期临床研究显示[15],胸部肿瘤局部控制率96%,中位PFS为10.2个月,中位TTP为6.3个月,中位生存期为21.8个月。1、2、3年OS分别为57%、45%、30%,且治疗耐受性良好,提示该联合治疗模式安全有效。
3 放疗联合EGFR-TKIs治疗NSCLC脑转移
脑转移是影响NSCLC患者预后的关键因素,文献报道首诊NSCLC患者中16.3%~19.9%[16]伴有脑转移,40%~55%[17-18]NSCLC患者在整个病程的某个阶段会出现脑转移,而EGFR突变的肺腺癌患者更容易发生脑转移(OR=3.83,95%CI为1.72~8.55,P=0.001)[19]。
3.1 多发脑转移的治疗
NSCLC脑转移的主要治疗方法包括全脑放疗、外科手术治疗、立体定向放射治疗、化疗等综合治疗模式,但疗效始终不尽人意,近年来TKIs由于其小分子靶向药物的特性,能一定比例透过血脑屏障,对NSCLC脑转移呈现出一定的疗效。早期小样本研究[20-23]已表明TKI联合放疗是NSCLC患者颅内转移的有效治疗手段(表1),Ma等[23]报道的一项Ⅱ期临床研究中,21例亚裔NSCLC脑转移患者接受了全脑放疗(40 Gy/20 f/4 w)联合gefitinib(250 mg/d)治疗,并以gefitinib 250 mg/d直到患者肿瘤进展或因gefitinib毒副作用不能耐受或其他原因中止治疗,结果显示中位生存期13.0个月,中位无进展生存期10.0个月,1年累积生存率58.7%,该研究表明TKIs联合全脑放疗有较好的初步疗效。
目前认为脑转移病灶的分子靶向治疗同样需要进行个体化的筛选。一项来自美国MD安德森癌症中心的Ⅱ期临床研究[24]显示erlotinib同步全脑放疗治疗NSCLC脑转移的中位总生存期为11.8个月,其中EGFR突变阳性患者长达19.1个月,而EGFR野生型患者为9.3个月,提示erlotinib联合全脑放疗在EGFR突变阳性的患者中更有意义。西班牙学者Porta等[25]通过回顾性分析69例经erlotinib单药或者全脑放疗后erlotinib巩固治疗的NSCLC脑转移患者,发现EGFR突变阳性患者客观缓解率(82.4%vs.0,P<0.001)、平均疾病进展时间(11.7个月vs.5.8个月,P<0.05)、总生存(12.9个月vs.3.1个月,P<0.001)均较突变状况未知患者明显改善。因此,对NSCLC脑转移患者应行EGFR基因检测,以利于获益人群的筛选。
尽管全脑放疗是NSCLC脑转移治疗的基石,但其神经系统不良反应一直饱受质疑,2015年ASCO会议上一项研究显示辅助性全脑放疗对1~3个脑转移病灶患者的治疗风险大于收益[26],基于此,TKIs单药治疗对TKIs联合全脑放疗提出了挑战,尤其对EGFR敏感突变的人群。一项荟萃分析[27]纳入16项研究的464例NSCLC患者(102例EGFR敏感突变、362例EGFR突变状态未明),其中358例患者接受单药TKIs治疗,70例患者接受TKIs同步全脑放疗,亚组分析结果显示未经选择的患者接受联合治疗较单药治疗有更好的ORR(66.2%vs.45.2%)和DCR(94.4%vs.73.1%);而对于敏感突变的患者,联合治疗的优势并不明显。Park等[28]报道了一项TKIs单药治疗EGFR阳性突变的NSCLC脑转移患者的Ⅱ期临床研究,结果显示总体有效率达到83%,无疾病生存期7个月,总生存期16个月。Iuchi等[29]研究认为敏感突变人群接受gefitinib单药治疗有效率(87.8%)高,并可避免全脑放疗带来的神经系统不良反应。
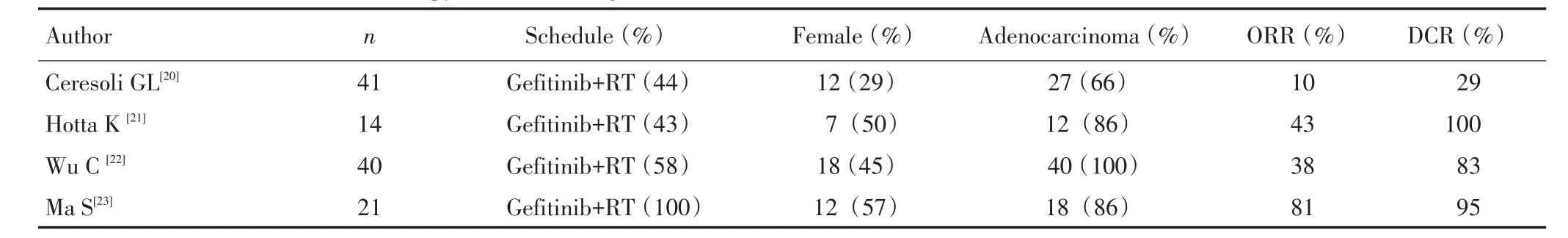
表1 放疗联合gefitinib治疗非小细胞肺癌脑转移的临床研究Table 1 Clinical research on radiotherapy combined with gefitinib in NSCLC-related brain metastasis
同样CTONG0803研究[30]显示对于一线化疗后出现无症状脑转移的腺癌或EGFR突变阳性NSCLC患者,单药erlotinib治疗的颅内疾病中位无进展生存期为10.1个月,其中EGFR突变阳性患者的无进展生存期可达15.2个月,提示了TKIs在该类人群中的应用价值。尽管TKIs对EGFR突变阳性的NSCLC脑转移疗效显著,但并不能否定放射治疗的地位,2015年世界肺癌大会一项[31]回顾性研究分析了132例EGFR敏感突变的肺腺癌脑转移患者,其中79例患者接受一线TKIs单药治疗,53例患者接受TKIs同步脑部放疗,在颅内无进展生存期上联合治疗具有明显的优势(24.7个月vs.19.0个月,P=0.005),尽管OS在组间差异未见统计学意义,但在颅内无进展生存期>22个月的患者中明显提高。而对于无症状脑转移这一独立预后因素,Kim等[31]研究认为给予积极的脑部放疗可以增加临床获益。
3.2 孤立脑转移的治疗
在NSCLC脑转移患者中约1/3是单发病灶的脑转移,局部治疗(脑转移瘤切除/立体定向放射治疗)联合全脑放疗是主要的治疗手段,但其利弊一样颇具争议。近期的几项临床研究[32-33]显示联合全脑放疗可以进一步提高局部控制,但未带来生存获益,而全脑放疗不可避免地会出现神经系统毒性,Chang等[33]的研究显示在SRS后给予全脑放疗可导致生存质量和神经认知功能的下降。日本的一项研究[34]中入组的17例NSCLC患者,在接受EGFR-TKIs治疗达到疾病部分缓解或稳定6个月以上后出现孤立性脑转移,给予继续TKIs治疗联合放射治疗(立体定向放射治疗/全脑放疗),结果显示有效率和疾病控制率分别为41%和76%,中位总生存时间403天,急性毒性反应可控,且无明显的晚期并发症。该研究为孤立性脑转移的治疗提供了新思路,以EGFR-TKIs替代全脑放疗/立体定向放射治疗二者之一,或许可以减少2种放疗手段联用造成的神经系统损伤,但仅为小样本研究,有待大样本随机对照研究进一步提供局部控制和生存获益的证据。
3.3 EGFR-TKIs治疗失败后脑转移的治疗
颅内进展是晚期NSCLC-TKIs治疗失败的重要原因之一,文献报道TKIs治疗后颅内失败发生率为22%~33%[10-11,13,35]。基础研究表明TKIs对放射治疗有增敏作用,Weickhardt等[36]对TKI治疗后颅内失败的患者给予全脑放疗和/或立体定向放射手术治疗,同时继续使用TKIs,从首次疾病进展到二次疾病进展的中位时间为7.1个月。目前认为对于TKIs治疗后颅内失败的患者,在颅外疾病控制稳定的情况下可以继续使用TKIs,同时对颅内病灶给予全脑放疗和/或立体定向放射手术治疗,这不仅能充分消灭非交叉抵抗的肿瘤克隆,还能够最大化TKIs治疗获益。
4 小结
目前已有许多基础及临床研究探索了EGFRTKIs联合放疗的疗效和安全性,特别针对局部晚期NSCLC,EGFR-TKIs同步放疗的治疗策略在EGFR敏感性突变的患者或可带来更大获益。由于TKIs的广泛应用,晚期NSCLC患者生存期明显延长,为放疗的参与提供了更多的机会,当病灶比较局限、进展缓慢时在继续使用TKIs同时可考虑给予局部放疗,并应考虑寡转移、PS评分及照射野等因素。而对于EGFR突变阳性的NSCLC脑转移人群,TKIs联合脑部放疗及TKIs单药治疗对既定的脑转移治疗模式提出了挑战,新的治疗模式有待进一步研究。
[1]Kriegs M,Gurtner K,Can Y,et al.Radiosensitization of NSCLC cells by EGFR inhibition is the result of an enhanced p53-depen⁃dent G1arrest[J].Radiother Oncol,2015,115(1):120-127.
[2]Sato Y,Ebara T,Sunaga N,et al.Interaction of radiation and gefi⁃tinib on a human lung cancer cell line with mutant EGFR gene in vitro[J].Anticancer Res,2012,32(11):4877-4881.
[3]Choong NW,Mauer AM,Haraf DJ,et al.Phase I trial of erlo⁃tinib-basedmultimodality therapy for inoperable stageⅢnonsmall cell lung cancer[J].J Thorac Oncol,2008,3(9):1003-1011.
[4]Ready N,Jänne PA,Bogart J,et al.Chemoradiotherapy and gefi⁃tinib in stageⅢnon-small cell lung cancer with epidermal growth factor receptor and KRAS mutation analysis:cancer and leukemia group B(CALEB)30106,a CALGB-stratified phaseⅡtrial[J].J ThoracOncol,2010,5(9):1382-1390.
[5]Lilenbaum R,Samuels M,Wang X,et al.A phaseⅡstudy of in⁃duction chemotherapy followed by thoracic radiotherapy and er⁃lotinib in poor-risk stageⅢnon-small-cell lung cancer:results of CALGB 30605(Alliance)/RTOG 0972(NRG)[J].J Thorac On⁃col,2015,10(1):143-147.
[6]Okamoto I,Takahashi T,Okamoto H,et al.Single-agent gefi⁃tinib with concurrent radiotherapy for locally advanced nonsmall cell lung cancer harboring mutations of the epidermal growth factor receptor[J].Lung Cancer,2011,72(2):199-204.
[7]Fairchild A,Harris K,Barnes E,et al.Palliative thoracic radiother⁃apy for lung cancer:A systematic review[J].J Clin Oncol,2008, 26(24):4001-4011.
[8]Nestle U,Nieder C,Walter K,et al.A palliative accelerated irradi⁃ation regimen for advanced nonsmall-cell lung cancer vs.con⁃ventionally fractionated 60 GY:Results of a randomized equiva⁃lence study[J].Int J Radiat Oncol Biol Phys,2000,48(1):95-103.
[9]Chen AB,Cronin A,Weeks JC,et al.Palliative radiation therapy practice in patients with metastatic non-small-cell lung cancer:a Cancer Care Outcomes Research and Surveillance Consortium (CanCORS)Study[J].J Clin Oncol,2013,31(5):558-564.
[10]Omuro AM,Kris MG,Miller VA,et al.High incidence of disease recurrence in the brain and leptomeninges in patients with nons⁃mall cell lung carcinoma after response to gefitinib[J].Cancer,2005,103(11):2344-2348.
[11]Lee YJ,Choi HJ,Kim SK,et al.Frequent central nervous system failure after clinical benefit with epidermal growth factor receptor tyrosine kinase inhibitors in Korean patients with nonsmall-cell lung cancer[J].Cancer,2010,116(5):1336-1343.
HY-82型油炸锅:双缸双筛电热炸炉;C21-SDHC15K型电磁炉:浙江绍兴苏泊尔生活电器有限公司;ACS-30型电子计价秤:赛多利斯科学仪器(北京)有限公司;BCD-196KDA型冰箱:海尔集团股份有限公司;其他设备:由食品工程学院实验室提供。
[12]Oxnard GR,Arcila ME,Sima CS,et al.Acquired resistance to EGFR tyrosine kinase inhibitors in EGFR-mutant lung cancer: distinct natural history of patients with tumors harboring the T790M mutation[J].Clin Cancer Res,2011,17(6):1616-1622.
[13]Yu HA,Sima CS,Huang J,et al.Local therapy with continued EGFR tyrosine kinase inhibitor therapy as a treatment strategy in EGFR-mutant advanced lung cancers that have developed ac⁃quired resistance to EGFR tyrosine kinase inhibitors[J].J Thorac Oncol,2013,8(3):346-351.
[14]Iyengar P,Kavanagh BD,Wardak Z,et al.PhaseⅡtrial of stereo⁃tactic body radiation therapy combined with erlotinib for patients with limited but progressive metastatic non-small-cell lung can⁃cer[J].J ClinOncol,2014,32(34):3824-3830.
[15]Wang J,Xia TY,Wang YJ,et al.Prospective study of epidermal growth factor receptor tyrosine kinase inhibitors concurrent with individualized radiotherapy for patients with locally advanced or metastatic non-small-cell lung cancer[J].Int J Radiat Oncol Biol Phys,2011,81(3):e59-e65.
[16]Bamholtz-Sloan JS,Sloan AE,Davis FG,et al.Incidence propor⁃tions of brain metastases in patients diagnosed(1973to2001)in the⁃Metropolitan Detroit Surveillance System[J].J Clin Oncol,2004, 22(14):2865-2872.
[17]Chen AM,Jahan TM,Jablons DM,et al.Risk of cerebral metasta⁃ses and neurological death after pathological complete response to neoadjuvant therapy for locally advanced nonsmall-cell lung cancer:clinical implications for the subsequent management of the brain[J].Cancer,2007,109(8):1668-1675.
[18]Ceresoli GL,Reni M,Chiesa G,et al.Brain metastases in locally advanced nonsmall cell lung carcinoma after multimodality treat⁃ment:risk factors analysis[J].Cancer,2002,95(3):605-612.
[19]Shin DY,Na II,Kim CH,et al.EGFR mutation and brain metas⁃tasis in pulmonary adenocarcinomas[J].J Thorac Oncol,2014,9 (2):195-199.
[20]Ceresoli GL,Cappuzzo F,Gregorc V,et al.Gefitinib in patients with brain metastases from non-small-cell lung cancer:a prospective trial [J].Ann Oncol,2004,15(7):1042-1047.
[21]Hotta K,Kiura K,Ueoka H,et al.Effect of gefitinib('Iressa', ZD1839)on brain metastases in patients with advanced non-smallcell lung cancer[J].Lung Cancer,2004,46(2):255-261.
[22]Wu C,Li YL,Wang ZM,et al.Gefitinib as palliative therapy for lung adenocarcinoma metastatic to the brain[J].Lung Cancer,2007,57(3): 359-364.
[23]Ma S,Xu Y,Deng Q,et al.Treatment of brain metastasis from nonsmall cell lung cancer with whole brain radiotherapy and Gefitinib in a Chinese population[J].Lung Cancer,2009,65(2):198-203.
[24]Welsh JW,Komaki R,Amini A,et al.PhaseⅡtrial of erlotinib plus concurrent whole-brain radiation therapy for patients with brain metastases from non-small-cell lung cancer[J].J Clin On⁃col,2013,31(7):895-902.
[25]Porta R,Sánchez-Torres JM,Paz-Ares L,et al.Brain metastases from lung cancer responding to erlotinib:the importance of EG⁃FR mutation[J].Eur Respir J,2011,37(3):624-631.
[26]Brown PD,Asher AL,Ballman KV,et al.NCCTG N0574(Alli⁃ance):A phaseⅢrandomized trial of whole brain radiation thera⁃py(WBRT)in addition to radiosurgery(SRS)in patients with 1 to 3 brain metastases[J].J Clin Oncol,2015,33(Suppl):LBA4.
[27]Fan Y,Xu X,Xie C,et al.EGFR-TKI therapy for patients with brain metastases from non-small-cell lung cancer:a pooled anal⁃ysis of published data[J].Onco Targets Ther,2014,7:2075-2084.
[28]Park SJ,Kim HT,Lee DH,et al.Efficacy of epidermal growth fac⁃tor receptor tyrosine kinase inhibitors for brain metastasis in nons⁃mall cell lung cancer patients harboring either exon 19 or 21 mu⁃tation[J].Lung Cancer,2012,77(3):556-560.
[29]Iuchi T,Shingyoji M,Sakaida T,et al.PhaseⅡtrial of gefitinib alone without radiation therapy for Japanese patients with brain metastases from EGFR-mutant lung adenocarcinoma[J].Lung Cancer,2013, 82(2):282-287.
[30]Wu YL,Zhou C,Cheng Y,et al.Erlotinib as second-line treatment in patients with advanced non-small-cell lung cancer and asymp⁃tomatic brain metastases:a phaseⅡstudy(CTONG-0803)[J].Ann Oncol,2013,24(4):993-999.
[31]Kim KH,Lee J,Lee JI,et al.Can upfront systemic chemotherapy replace stereotactic radiosurgery or whole brain radiotherapy in the treatment of non-small cell lung cancer patients with asymp⁃tomatic brain metastases[J]?Lung Cancer,2010,68(2):258-263.
[32]Aoyama H,Shirato H,Tago M,et al.Stereotactic radiosurgery pluswhole-brain radiation therapy vs stereotactic radiosurgery alone for treatment ofbrain metastases:A randomized controlled trial[J].JAMA,2006,295(21):2483-2491.
[33]Chang EL,Wefel JS,Hess KR,et al.Neurocognition in patients with brainmetastases treated with radiosurgery or radiosurgery plus whole-brain irradiation:Arandomised controlled trial[J].Lan⁃cet Oncol,2009,10(11):1037-1044.
[34]Shukuya T,Takahashi T,Naito T,et al.Continuous EGFRTKI administration following radiotherapy for non-small cell lung cancer patients with isolated CNS failure[J].Lung Cancer, 2011,74(3):457-461.
[35]Ma S,Xu Y,Deng Q,et al.Clinical features of gefitinib-responders with non-small cell lung cancer[J].J ClinOncol,2008,26(15S):19136.
[36]Weickhardt AJ,Scheier B,Burke JM,et al.Local ablative therapy of oligoprogressive disease prolongs disease control by tyrosine ki⁃nase inhibitors in oncogene-addicted non-small-cell lung cancer [J].J Thorac Oncol,2012,7(12):1807-1814.
(2015-08-03收稿)
(2015-11-18修回)
(编辑:杨红欣)
Advances in radiotherapy combined with EGFR-TKIs for non-small cell lung cancer
Kan WU,Bing WANG,Bing XIA,Shirong ZHANG,Shenglin MA
Correspondence to:Shenglin MA;E-mail:mashenglin@medmail.com.cn
Department of Radiation Oncology,Hangzhou First People's Hospital,Hangzhou Cancer Hospital,Hangzhou 310006,China
This work was supported by the National Natural Science Foundation of China(No.81272611,81301927),Zhejiang Provincial Natural
Science Foundation(No.LY13H160023),and the Medical and Scientific Research Projects of Hangzhou City(No.20150633B42).
Lung cancer is the main cause of cancer-related death worldwide.Non-small cell lung cancer(NSCLC)accounts for about 80%of lung cancer cases,but only 25%-30%of initially diagnosed patients have the option of radical surgery because of the lack of effective measures for early diagnosis.For locally advanced and advanced NSCLC,radiotherapy alone or comprehensive treatment with chemoradiotherapy is the main treatment method;however,the curative effect is unsatisfactory.Recently,increasing evidence suggests that targeted drugs,such as epidermal growth factor receptor tyrosine kinase inhibitors(EGFR-TKIs),combined with radiotherapy/ chemoradiotherapy represent a promising treatment modality for NSCLC.This review will discuss the research status of EGFR-TKIs and radiotherapy for locally advanced and advanced NSCLC.
NSCLC,radiotherapy,EGFR-TKI
10.3969/j.issn.1000-8179.2015.23.846

杭州市第一人民医院,杭州市肿瘤医院放疗科(杭州市310006)
马胜林 mashenglin@medmail.com.cn
吴侃 专业方向为胸部肿瘤的放射治疗。
E-mail:wukanwukan@126.com
