自乳化系统联合液固压缩技术运用于难溶性药物的初探
2015-02-14罗开沛李小芳周维向志芸杨露林浩刘海霞
罗开沛,李小芳,周维,向志芸,杨露,林浩,刘海霞
·炮制制剂·
自乳化系统联合液固压缩技术运用于难溶性药物的初探
罗开沛,李小芳,周维,向志芸,杨露,林浩,刘海霞
近年来,许多新技术、新方法运用于难溶性药物的增溶,但在实际应用中会遇到一定的局限性。本文通过查阅国内外文献,介绍自乳化系统和液固压缩技术及各自的的优缺点,探讨将自乳化系统和液固压缩技术结合,既发挥两项技术的优势,又起到互补作用,并形成一套完备的工艺体系,为增溶技术提供了新思路。
自乳化系统;液固压缩技术;难溶性药物;溶解度
作为最常用的口服给药形式,固体制剂中的活性药物成分必须良好的崩解溶出,才能被胃肠道顺利吸收。固体药物在胃肠道中的溶解速度和程度决定了其被吸收的速度和程度,在水溶性差的情况下药物的溶解快慢作为药物被吸收的控制步骤,影响吸收速率[1-2]。因此,当今的一个主要挑战是增加难溶性药物的溶解度。据文献报道[3-7],大约40%的所开发的新药是难溶或不溶于水的。此外,高达50%的口服药物由于低溶解度和高亲脂性使其制备和使用受到阻碍。
随着科学技术的发展,已经运用了各项技术以增加难溶性药物的溶解性,从而提高生物利用度,如纳米混悬剂[8]、自乳化系统[9]、固体分散体[10]、固体脂质纳米粒[11]、液固压缩技术[12-13]等,考虑到机械设备和制药技术相对简单、成本较低、适合工业化生产等因素,本文对自乳化系统和液固压缩技术进行简单的综述,并对两项技术联合应用于难溶性药物进行探讨与展望。
1 自乳化系统(SEDDS)
1.1 组成
自乳化药物给药系统[9]是由药物、油相、表面活性剂和助表面活性剂等组成的均匀油状混合物,在体外轻微震荡或胃肠道的蠕动下能够自发形成一种热力学稳定的O/W型乳滴,其粒径在100~500nm之间,这种乳剂称为自乳化系统(SEDDS)。有些SEDDS系统中加入了一些被称作为过饱和辅料的羟丙甲纤维素(HPMC)、聚乙烯吡咯烷酮 (PVP)、甲基纤维素等,其目的在于增强液体粘度;提高载药量;防止药物在体内析出以及减小对胃肠道刺激性[14]。
1.2 应用
自乳化系统的提出推动了药剂学领域增溶技术
的进一步发展,由于能够增加难溶性药物的溶解度,使其受到了国内外研究学者的广泛关注,因此,做了相关方面的大量尝试和研究,取得了相应的进展。比如:刘楠等[15]将靛玉红制备成自乳化释药系统,并用星点设计优化处方,结果发现,优化后的自乳化制剂将靛玉红的溶解度提高了4000倍,良好的达到了增溶的目的。阮越勇等[16]以丙二醇单月桂酸甘油酯为油相,聚氧乙烯蓖麻油为表面活性剂,二乙二醇单乙醚为助表面活性剂,制备姜黄素自乳化释药系统,经考察其自乳化制剂稳定性良好,显著地提高姜黄素在水中的溶解度。 此外,国内外申请的自乳化系统专利不在少数,例如,何仲贵等[17]以油酸乙酯为油相、聚山梨酯80为表面活性剂、丙二醇作为助表面活性剂,将葛根黄酮提取物制成SEDDS软胶囊,提高了药物的水溶性和生物利用度,增强了药物的疗效。Lambert, Karel J等[18]研制出了以脂肪酸丙二醇酯为油相的难溶性药物的自乳化组合物,并提出溶解亲脂性药物油相载体的有效量。同时,目前国外上市的SEDDS制剂有4种[19],分别是瑞士诺华的山地明和环孢素A,雅培公司的利托那韦以及罗氏制药的沙奎那韦,这些药物已经被证实具有良好的溶解度和临床疗效。
1.3 优势
自乳化系统得到有力的发展,与其本身的优势是分不开的。(1)将难溶性药物制成自乳化制剂,能有效增加溶解度,提高生物利用度。(2)与传统的胶囊剂和片剂等相比,自乳化制剂能够均匀、快速地把药物传递至吸收的部位[20]。(3)在人体正常体温条件下,自乳化制剂遇到水液可以在胃肠道轻微蠕动下自发形成一种O/W型乳剂,产生较大的表面积[21]。(4)将药物溶解于油相中,在口服后自发形成乳剂,可以有效地避免乳剂容易出现分层的问题,有助于制剂的贮藏和运输。
1.4 缺点[20,22]
尽管SEDDS具有增加难溶性药物的溶解度的优点,但是在生产实际操作中也出现了一些难以避免的问题,(1)表面活性剂在系统中有较大的用量,而较多表面活性剂能对胃肠道产生刺激性,并且长期服用会出现慢性毒性。(2)在制备软胶囊时,对滴头的大小、药液温度和滴速等仪器设备条件有较高的要求,因此制剂成本和设备控制难以达到。(3)由于助表面活性剂多为挥发性溶剂,可能会迁移到胶囊囊壳,发生共同作用,甚至透过囊壳挥发,以致药物沉淀,从而影响载药量,达不到应有的疗效。(4)在系统中加入固体辅料制成固体制剂,在加热干燥过程中,会导致部分具有挥发性助表面活性剂挥发而造成损失,影响药物的增溶性。
2 液固压缩技术
2.1 组成
液固压缩技术[12]首次由Spireas等提出,它是由难溶性药物、非挥发性溶剂、载体和涂层材料组成。该技术是将难溶性药物溶解于非挥发性的溶剂中,形成溶液或混悬液,然后加入具有多孔性质的载体材料进行吸附,搅拌,再加入具有更强吸附能力的涂层材料,制成一种干燥的,非粘壁的,并且具有良好自由流动性和可压性的固体粉末。根据制剂的需要,可以加入一些崩解剂,润滑剂,分散剂等,制成缓释片,速释片等。
2.2 运用
国外对液固压缩技术研究较多,也有很多报道,Patel, V.P.等[23]以格列吡嗪为模型药物运用液固压缩技术,以微晶纤维素为载体、二氧化硅为涂层材料、聚乙二醇-400为液体赋形剂将其制成液固压缩片,在评估崩解时限时,60min内,经测定超过90 %的释放度,由此得出,液固压缩制剂有效的提高了格列吡嗪溶解度和溶出速率。Nokhodchia A等[24]以丙烯酸树脂为载体,硅土为涂层材料制备成茶碱缓释液固压缩片,并以不同的赋形剂考察对释药速率的影响,结果显示不同的赋形剂,释药速率不同;同时,增强了HPMC的缓释效应。而国内在此方面起步较晚,到目前对液固压缩技术研究尚少,赵许杰等[25]以水飞蓟素为模型药物制备液固压缩片,溶解15 min时,溶出率达到80%以上,持续到45min时,溶出度已达到90%以上,崩解时限也具有明显优势,可在100 s内达到完全崩解。
2.3 优势[22,26]
液固压缩技术是近年来国外药剂学及生物药剂学领域研究的重点,其主要优势概括为如下几个方面:(1)制备工艺简单,设备技术要求低,适合产业化生产。(2)运用液固压缩制剂制备成片剂,颗粒剂,硬胶囊剂等,尽管呈固体状态,但药物始终以液体分子形式存在,增强了药物的溶解性。(3)不溶于水的固体药物和亲脂性的液体药物均可运用液固压缩技术,制成液固压缩制剂,提高难溶性药物溶解性。(4)液固压缩缓控释制剂相比通过渗透泵技术以及激光微孔技术制得的胶囊剂具有更恒定的溶出速率。(5)涉及到的载体和涂层材料,如微
晶纤维素、微粉硅胶、淀粉、乳糖等为一般性传统辅料,经济易得。
2.4 缺点[35]
液固压缩技术虽然能提高难溶性药物的溶解度,是一个比较可行的办法,但存在以下缺点:(1)载药量小是液固压缩制剂最大的障碍,导致患者服用剂量大,次数多等问题,若制成片剂,片重超过1g,会造成难以吞服的现象。(2) 在工业大生产中,大量的载体材料和涂层材料与少量的溶液均匀混合存在一定困难。
3 自乳化系统联合液固压缩技术共同应用
3.1 辅料选择
3.1.1 油相 所选的油相应遵从以下原则,较少量的油相能够溶解处方量的药物,并且在低温条件下,不能有药物溶出,容易被同处方中的表面活性剂乳化。目前多用经改造后的植物油类和具有不同饱和度的长链、中链甘油三酯油类。中链脂肪酸甘油酯也常被优先作为油相,因为其拥有良好的流动性和自乳化性[27]。
3.1.2 表面活性剂 表面活性剂为非离子型表面活性剂,其毒性小于离子型表面活性剂,具有较高的HLB值。主要的亲水性非离子表面活性剂有脂肪酸甘油酯、脂肪酸山梨酯等[28]。常用的有Tween80以及乙氧基聚乙二醇甘油酯等,其使用量一般为30%~60%。
3.1.3 助表面活性剂 助表面活性剂能有效改变表面活性剂的表面活性,降低界面的表面张力,增强表面活性剂的溶解;也可以改变亲水亲油平衡性,调节HLB值。一般选用中长链的醇类如乙二醇,聚乙二醇,丙二醇,乙二醇单乙基醚(Transcutol)等。
3.1.4 载体材料 载体材料具有多孔的性质,才能确保足够的吸附性能。常用的载体材料有微晶纤维素,乳糖,淀粉,硅酸镁铝等,其中微晶纤维素包括Avicel PH-101、AvicelPH-102以及 Avicel PH-200三类。若制备成缓释制剂,一般选择丙烯酸树脂类做载体材料。由于不同载体对不同的溶液或混悬液负载能力不同,所以应对具体用的载体进行筛选[29]。
3.1.5 涂层材料 涂层材料是一种细而多孔,具有高吸附能力的辅料,大多数是多微孔无机化合物,其作用是将载体材料吸附液体所形成的湿颗粒转变为干燥的,具有流动性的固体粉末。如微粉硅胶,氢氧化镁,滑石等。一般而言,无定形微粉硅胶是较为理想的涂层材料[30]。
3.1.6 添加剂 在处方中加入一些润滑剂,崩解剂等,增强固体粉末的流动性,也缩短了崩解时间,有利于药物的溶出。部分添加剂如羟丙甲纤维素、聚维酮、和聚乙二醇( PEG 35000)可以提高载药量。Javadzadeh Y等[31]制备卡马西平液压片时就添加并对比以上三种添加剂,结果显示明显提高了载药量。
3.2 制备方法
自乳化系统联合液固压缩技术运用于难溶性药物增溶实为两项技术的结合,首先制备成乳液,其次,制成液固压缩制剂,具体操作步骤如下[32,36]:
1、配备一系列油相,表面活性剂,助表面活性剂作为供选,将难溶性药物分别溶解于以上三种辅料中,测得各自的溶解度。
2、根据难溶性药物溶解的最大量,优选出油相,表面活性剂,助表面活性剂。
3、根据所优选出的辅料,以不同的比例混合,观察混合溶液的乳化性质,绘制空白伪三元相图,确定自乳化区域。若辅料有多种选择,则根据处方的不同,绘制各自的伪三元相图,选取并确定自乳化面积最大的处方。
4、以选出的处方,根据空白伪三元相图的不同比例将油相,表面活性剂,助表面活性剂混合,然后加入难溶性药物,绘制含药伪三元相图,确定乳化区域面积。
5、以微乳粒径或载药量为指标,设计正交试验优选出辅料的最佳比例,制得乳液。
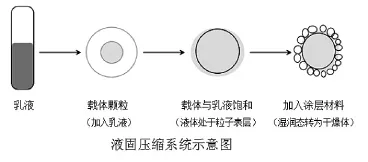
6、在乳液中加入适量的载体和涂层材料,以及添加剂,混合均匀,制备成液固压缩制剂,如下图所示。为保证载体和涂层材料对液体最佳吸附并且具有良好的流动性和可压性,Spireas等[33]提出了液固压缩技术的数学模型,其中涉及到几个定义,R值表示所用重量载体材料(Q)和涂层材料(q)的比值,负载指数(Lf)表示载体材料(Q)对溶剂(W)吸附的最大量。溶剂重量(W)表示药物和液体赋形剂的质量之和。即有:

此外,Ф值表示辅料在保持良好的流动性时所固定非挥发性溶剂所需要的最大保留势能,Ф值可以用测试辅料的滑动角(Angle of slide)的方法而确定。ФCA 表示载体材料对非挥发性溶剂所保留的最大势能,ФCO 表示涂层材料对非挥发性溶剂所保留的最大势能。ФCA和ФCO值根据实验而测得。即存在如下关系:

综上所述,由实验测得ФCA和ФCO值,设定R值,即可求出负载指数(Lf),称定制备的乳液重量为W,将Lf与W带入方程(1)、(2)中求出载体材料(Q)和涂层材料(q)的重量。
3.3 自乳化系统联合液固压缩技术共同应用的优势
自乳化系统运用在难溶性药物方面取得了较大的进展,国内外的研究也很广泛,包括应用于西药制剂和中药制剂的增溶。目前也有上市的自乳化制剂,突出了自乳化系统在增溶方面起到的作用与贡献。然而,自乳化系统以液体形式多制备成硬胶囊或软胶囊,由于[20,22]助表面活性剂多为挥发性溶剂,可能会迁移到胶囊囊壳,甚至透过囊壳挥发,以致药物沉淀,从而影响载药量。其次,在制备软胶囊时,滴头的大小、药液温度和滴速等仪器设备条件有较高的要求,制剂成本和设备控制难以达到。而且在系统中加入固体辅料制成固体制剂,在加热干燥过程中,会导致部分具有挥发性辅料挥发而造成损失,影响药物的增溶性等等。这些一系列问题暴露出的自乳化系统的缺陷,所以目前将液体药物固体化成为了研究的热点,加入微晶纤维素,可溶性淀粉,甘露醇,乳糖等[32,34]固体辅料,采用喷雾干燥技术,纳米技术和熔融挤压技术等[35]制成片剂或颗粒剂等其他剂型。但是这些辅料却没有统一的规律性,包括辅料的选择和用量,要通过大量筛选才能得到优化结果。至此,引入液固压缩技术,优势在于虽然制剂呈固体状态而药物以液体形式存在,能有效提高溶解度,也具有完备的数学模型体系,对固体辅料的具体用量和吸附的最大能力进行了充分解释,保证了固体粉末良好的流动性和可压性,既简化了工艺,又具有可靠性。相反,自乳化系统的加入也解决了液固压缩技术在工业化放大过程中,要使大量的载体材料与很小量的液体溶液均匀混合,存在一定困难[22]的缺点。
4 前景展望
自乳化系统与液固压缩技术均有各自的理论,也比较成熟,将两项技术联合运用于难溶性药物的增溶,既发挥两项技术的优势,又起到互补作用,并形成一套完备的工艺体系,为增溶技术提供了新思路。赵霞等[36]以环孢霉素A为模型药物,丙二醇月桂酸为油相,蓖麻油聚乙二醇-35为表面活性剂,PEG-400为助表面活性剂,微晶纤维素为载体材料,微粉硅胶为涂层材料,交联羧甲基纤维素钠为崩解剂运用自乳化系统和液固压缩技术联合开发制备了环孢霉素A液固压缩片,在考察厚度,片重,硬度,均一性等均合格,崩解时限小于15min。同时,体外释放实验以去离子水,模拟胃液,模拟肠液测试溶解度,与传统片相比,溶解度显著增加。
自乳化系统联合液固压缩技术运用于难溶性药物理论与实际可行,不过才刚刚起步,还需要进行大量的实验研究。目前液固压缩制剂载药量小是一个非常突出的问题,有待于开发比表面积更大的新型辅料,减少固体辅料的用量,提高载药量。其次,自乳化系统和液固压缩技术增溶的机制还尚未解决,一直处于探索阶段,而两技术相结合用于难溶性药物增溶的机制随着新技术,新设备的创新还要继续研究和考证,所以在运用与研究初期还有很长的路要走,随着对新型辅料,新型技术地不断深入,自乳化系统联合液固压缩技术运用于难溶性药物拥有广阔的应用前景。
[1] Javadzadeh Y, Siahi-Shadbad M R, Barzegar-Jalali M, et al.Enhancement of dissolution rate of piroxicam using liquisolid compacts[J]. Il Farmaco,2005,60(4):361.
[2] kumar Nagabandi V, Ramarao T, Jayaveera K N. Liquisolid compacts: A novel approach to enhance bioavailability of poorly soluble drugs[J]. Int J Pharm Bio Sci, 2011,1(3): 89.
[3] Naseem A, Olliff C J, Martini L G, et al. Effects of plasma irradiation on the wettability and dissolution of compacts of griseofulvin[J]. Int. J. Pharm, 2004,269(2):443.
[4] Shailesh T, Hitesh H, Dashrath M. Formulation and Evaluation of Liquisolid Compacts for Olmesartan Medoxomil[J]. Journal of Drug Delivery,2013:1.
[5] Kavitha K, Kotha N S, Raja L, et al. Effect of dissolution rate by liquisolid compact approach: An overview[J]. Der Pharma Lettre, 2011, 3: 71.
[6] Boghra R, Patel A, Desai H, et al. Formulation and evaluation of irbesartan liquisolid tablets[J]. Int. J. Pharm. Sci. Rev, 2011,
9(2): 32.
[7] Gursoy R N, Benita S. Self-emulsifying drug delivery systems (SEDDS) for improved oral delivery of lipophilic drug[J]. Biomed. Pharmacother,2004,58:173.
[8] 朱建芬,吴祥根.纳米混悬剂的制备方法及在药剂学中应用的研究进展[J].中国医药工业杂志, 2006, 37 (3) : 196.
[9] 程玉钏,周建平,吕慧侠.固体自乳化药物传递系统的研究概况[J].药学进展,2008,32 (2) : 68.
[10] 刘娱姗,高署,柯学,等. 难溶性药物固体分散体研究新进展[J].药学进展, 2013,37(4): 166.
[11] 朴林美,尹寿玉,崔艳琳.固体脂质纳米粒的研究概述[J]. 药物与人,2014,5(27):26.
[12] Spireas S, Sadu S, Grover R. In vitro evaluation of hydrocortisone liquisolid tablets [J]. J Pharm Sci, 1998, 87(7): 867.
[13] Spireas S, Sadu S. Enhancement of prednisolone dissolution properties using liquisolid compacts [J]. Int J Pharm, 1998, 166(2): 177.
[14] Wei YH, Ye XL, Shang XG,et al. Enhanced oral bioavailability of silybin by a supersaturatable selfemulsifying drug delivery system(S-SEDDS)[J]. Colloids and Surfaces A:Physicochemical and Engineerin Aspects,2012,396 (20): 22.
[15] 刘楠,王云红,张传辉,等. 靛玉红自乳化释药系统的制备[J].中成药,2014,04:734.
[16] 阮越勇,牟晓崟,高缘,等.姜黄素自乳化释药系统处方研究及体外溶出评价[J].海峡药学,2014,05:54.
[17] 何仲贵,崔升淼.葛根黄酮自微乳化软胶囊及其制备方法:中国,CN1457795A[P]. 2003-11-26.
[18] Lambert K J, Constantinides P P, Quay S C. Emulsion vehicle for poorly soluble drugs: U.S. Patent 20,040,202,712[P]. 2004-10-14.
[19] Cursory RN, Benita S. Self-emulsifying drug delivery systems (SEDDS) for improved oral delivery of lipophilic drugs[J]. Biomedecine&Pharmacotherapy,2004,58(3):173.
[20] 王科燕,张永军.自乳化释药系统及其新剂型的研究概况[J].中国药业,2009,08:63.
[21] Gershanik T, Benita S. Self-dispersing lipid formulations for improving oral absorption of lipophhilic drugs[J]. Eur J Pharm Bio,2000,50(1-2):179.
[22] 赵霞,孙会敏.自乳化释药系统与液固压缩技术联合开发难溶性药物新剂型的进展[J]. 药物分析杂志,2012,09:1697.
[23] Patel V P, Patel N M. Dissolution enhancement of glipizide using Liquisolid tablet technology[J]. Indian Drugs,2008,45 (4) :318.
[24] Nokhodchia A, Aliakbara R, Desaia S,et al. Liquisolid compacts: The effect of cosolvent and HPMC on theophylline release [J]. Biointerfaces, 2010, 79: 262.
[25] 赵许杰,闫雪生,袁敏,等.液固压缩技术在水飞蓟素制剂方面的应用[J].药学研究,2013,11:641.
[26] Sambasiva R A, Naga Aparna T. Liquisolid technology: An overview [J]. Int J Res Pharm Biomed Sci,2011,2(2):401.
[27] 周庆辉,平其能.自乳化药物传递系统的应用与前景[J].药学进展,2001,03:134.
[28] 陈伶俐.自乳化药物传递系统的研究进展[J]. 黑龙江医药,2010,01:55.
[29] Javadzadeh Y, Musaalrezaei L, Nokhodchi A. Liquisolid technique as a new approach to sustain propranolol hydrochloride release from tablet matrices[J]. Int J Pharm, 2008,362(1):102.
[30] Tayel S A, Soliman I I, Louis D. Improvement of dissolution properties of carbamazepine through application of the liquisolid tablet technique[J]. Eur J Pharm Biopharm, 2008, 69(1): 342.
[31] Javadzadeh Y, Jafari-Navimipour B, Nokhodchi A. Liquisolid technique for dissolution rate enhancement of a high dose water-insoluble drug (carbamazepine) [J]. Int J Pharm, 2007, 341: 26.
[32] 高永艳,陈海文,梁超峰.黄芩苷固体自乳化颗粒剂的制备[J].中国医药导报,2014,19:96.
[33] Spireas S. Liquisolid systems and methods of preparing same: US,US6423339B1[P]. 2002-07-23.
[34] 张建,叶珍珍,崔升淼.山楂叶总黄酮固体自乳化颗粒的处方优化和评价[J].中国实验方剂学杂志,2012,04:15.
[35] Tang B, Cheng G, Gu J C, et al. Development of solid selfemulsifying drug delivery systems: preparation techniques and dosage form[J]. Drug Discovery Today, 2008, 13 (13-14):606.
[36] Zhao X, Zhou Y Q, Potharaju S, et al. Development of a self micro-emulsifying tablet of cyclosporine-A by the liquisolid compact technique[J]. Int J Pharm Sci Res, 2011, 2(9) : 2299.
(责任编辑:胡慧玲)
A preliminary study of the application of self micro-emulsifying system combined liquisolid compression techniques in insoluble drugs/
LUO Kai-pei, LI Xiao-fang, ZHOU Wei, XIANG Zhi-yun, YANG Lu, LIN Hao, LIU Hai-xia//(Pharmacy College, Chengdu University of Traditional Chinese Medicine; The Ministry of Education Key Laboratory of Standardization of Chinese Herbal Medicine; Key laboratory of Systematic Research, Development and Utilization of Chinese Medicine Resources in Sichuan Province—Key Laboratory Breeding Base of Co-founded by Sichuan Province and MOST, Chengdu 611137, Sichuan)
In recent years, many new technologies and methods have been used in the solubilization of insoluble drugs, but they have encountered some limitations in practical applications. In this paper, through referring to the domestic and foreign literature, the advantages and disadvantages of self-emulsifying system and the liquisolid compacts technology are presented. And the possibility of the combination of self emulsifying system and liquisolid compacts technologies is explored not only to play the advantages of both technologies, but also play a complementary role. Therefore, a set of complete process system is formed to provide a new idea for the solubilization technology.
Self-emulsifying system; liquisolid compacts technology; insoluble drug; solubility
R 283
A
1674-926X(2015)02-012-05
成都中医药大学药学院 中药材标准化教育部重点实验室 四川省中药资源系统研究与开发利用重点实验室—省部共建国家重点实验室培育基地,四川 成都 611137
罗开沛,男,硕士研究生,从事中药新剂型及中新技术研究
Tel:15351218131 Email:574503164@qq.com
李小芳,女,教授,博士生导师,从事中药新剂型及新技术研究 Email:lixiaofang918@163.com
2014-11-10
