非诺贝特降低生活方式干预无效的脂肪肝患者LDL的疗效
2015-01-12吴玉华李春明武谦虎朱孝雷花长松镇江市第三人民医院镇江212000
吴玉华,李春明,武谦虎,朱孝雷,花长松(镇江市第三人民医院,镇江 212000)
非诺贝特降低生活方式干预无效的脂肪肝患者LDL的疗效
吴玉华,李春明,武谦虎,朱孝雷,花长松(镇江市第三人民医院,镇江 212000)
目的 调查单用生活方式干预治疗与同时口服非诺贝特治疗非酒精性脂肪肝患者脂代谢紊乱的疗效。方法 纳入经6个月的生活方式干预治疗后仍具有脂代谢紊乱的非酒精性脂肪肝患者,口服非诺贝特每日100mg,同时继续进行生活方式干预治疗。结果 在52例参加了6个月的生活方式干预治疗的非酒精性脂肪肝患者中,21例仍有脂代谢紊乱的患者被纳入临床研究。纳入患者年龄58(27~75)岁,体质量63.0(39.4~109.0)kg,体质量指数25.4(18.2~37.1)kg·m-2,ALT 23(14~73)IU·L-1,TG 105(92~216)mg·dL-1,HDL 58(37~93)mg·dL-1,LDL 153(66~209)mg·dL-1。21例患者在使用非诺贝特治疗6月后,20例患者中15例(15/20,75%,P=0.001 5)血LDL水平得到改善,5例患者血LDL水平未见明显下降。1例患者口服非诺贝特后出现皮肤瘙痒及皮疹,退出了研究。结论 对伴脂代谢紊乱的非酒精性脂肪肝患者,经生活方式干预治疗后脂代谢紊乱未见改善,在联合使用降血脂药物非诺贝特后,脂代谢紊乱可得到改善。
非诺贝特;脂代谢紊乱;生活方式干预;低密度脂蛋白
非酒精性脂肪肝(NAFLD)是患者在无酒精滥用及其他损肝病因的情况下发生的渐进性慢性肝病状态,其肝病谱包括预后较好的单纯性脂肪肝、具有炎症和纤维化的非酒精性脂肪性肝炎、肝硬化和肝细胞癌[1]。NAFLD的发生与脂质代谢紊乱密切相关。NAFLD患者脂质代谢紊乱的特征表现在血三酰甘油(TG)、低密度脂蛋白(LDL)升高及高密度脂蛋白(HDL)水平下降[2]。Oza等研究报道,对伴有脂代谢紊乱的非酒精性脂肪肝患者,进行为期6个月的生活方式干预后,患者体质量下降,腹部脂肪堆积减少,肝功能指标、TG水平、胰岛素抵抗及人口学参数得到了改善,但总胆固醇(TC)、HDL、LDL水平未见明显改善[3]。在本研究中,我们调查了NAFLD患者经6个月的生活方式干预后脂肪代谢紊乱仍无明显改善而加用非诺贝特的疗效。
1 资料与方法
1.1 研究对象及纳入标准 对2012年8月至2013年8月在镇江市第三人民医院肝病科门诊就诊的伴有脂肪代谢紊乱的NAFLD患者,进行为期6个月的生活方式干预,纳入了仍具有脂肪代谢紊乱的NAFLD患者,加用非诺贝特口服,进行前瞻性的队列研究。所有患者均进行了腹部超声检查。
NAFLD的超声诊断遵循如下标准[4]:(1)肝区近场回声弥漫性增强(强于肾脏和脾脏),远场回声逐渐衰减,肝内管道结构显示不清。(2)肝脏轻度至中度肿大,边缘圆钝。(3)肝内血管回声减少,管腔变细或不清晰。(4)彩色多普勒血流显像提示,肝内彩色血流信号减少或不易显示,但肝内血管走向正常。研究对象(病人)的纳入标准如下:(1)所有肝炎病毒血清标志物均阴性;(2)未见已知慢性肝病的临床表现;(3)未使用过引起肝细胞脂肪变性的药物;(4)未使用过胰岛素增敏剂治疗。脂代谢紊乱定义为[5]:血LDL水平≥140mg·dL-1,或HDL水平<40mg·dL-1,和(或)TG水平≥150mg·dL-1。
1.2 干预措施的实施
1.2.1 生活方式干预 包括饮食和体育活动2个方面。生活方式干预在患者各自家庭进行,患者根据自己的情况自主选择体育活动的方式,在家自主进食。纳入对象均需完成连续3d的基线饮食摄入记录,在纳入研究后的1周内参加由本院营养专家指导的饮食健康教育,患者进食参考营养专家建议的卡里路摄入标准,饮食卡里路的摄入量依据患者实际体质量、在家进行的体育活动的类型等因素按照Mifflin-St Jeor公式计算[6],个体化进行。目标饮食摄入所含的能量定义为:标准体质量×25~30kcal。受试者均需提供基线时的活动习惯并接受减体质量的健康教育。受试者按照要求进行规则的体育活动,每日活动30min,中等强度,每周进行4~7d,体育活动的方式包括快走、慢跑、骑自行车、使用跑步机等。要求患者每天记录生活方式干预实施日志,以明确自己体质量控制情况和每日锻炼的效果。
1.2.2 药物干预 在完成6个月的生活方式干预后仍具有脂代谢紊乱的NAFLD患者,开始每日口服降血脂药物非诺贝特100mg,并继续同前坚持生活方式干预6个月。
1.3 临床、实验室及影像学评价 对所有患者每月进行一次人口学和血生化评价,测量身高、体质量,计算体质量指数(BMI)。患者经12h禁食后,在09:00左右抽取静脉血标本,通过标准生化检测技术测定丙氨酸氨基转移酶(ALT)、草氨酸氨基转移酶(AST)、碱性磷酸酶(ALP)、谷氨酰转肽酶(GGT)、空腹血糖(FBS)、糖化血红蛋白(HbAc1)、尿酸(UA)、TC(总胆固醇)、TG(三酰甘油)、LDL(低密度脂蛋白)、HDL(高密度脂蛋白)等指标。利用Homeostasis评价模型计算胰岛素抵抗指数(HOMA-IR),计算公式如下:HOMA-IR=空腹血胰岛素(μU·mL-1)×空腹血糖(mg·dL-1)/405。
1.4 统计学分析 数据分析均用统计软件SPSS 19.0进行,计数资料用中位数表达,双项有序列联表计数资料的比较用Wilcoxon秩和检验进行比较,P<0.05表示差异有统计学意义。
2 结果
2.1 病人人口学及生化特征 2012年8月至2013年1月在本院肝病门诊接受生活方式干预治疗的52例伴脂代谢紊乱的NAFLD患者中,21例患者完成6个月生活方式干预后脂代谢紊乱无改善。纳入此临床研究21例患者,其中男性9例,女性12例。患者在基线状态和在使用非诺贝特治疗开始时的特征包括人口学特征BW、BMI、HOMA-IR及生化学特征肝功能指标、血脂指标、尿酸等。纳入患者的特征资料如表1所示。
2.2 用非诺贝特治疗6个月后的疗效 在完成6个月(第6至12月)的非诺贝特联合生活方式干预治疗后,21例患者中,有20例完成临床研究,1例患者在口服非诺贝特后出现皮疹和皮肤瘙痒,停止服用非诺贝特而退出临床研究。与先行6个月的单独生活方式干预结束时相比,在继续6个月的生活方式干预联合口服非诺贝特治疗结束时的12个月后,患者LDL水平明显下降,153(66~209)(mg·dL-1)vs 138(60~168)(mg·dL-1),P=0.001 5,而ALT水平有所升高,23(15~126)(IU·L-1)vs 28(9~175)(IU·L-1),P=0.037 3;与生活方式干预前的基线状态时相比,生活方式干预联合口服非诺贝特治疗12个月后,患者LDL水平明显下降,156(85~184)(mg·dL-1)vs 138(60~168)(mg·dL-1),P=0.002 4,BMI、HbA1c、TC等也均降低,*P分别为0.049 4,0.043 1,0.002 4;而且ALT水平也有所下降,为36(15~131)(IU·L-1)vs 28(9~175)(IU·L-1),但未显示统计学差异,P=0.073 1。实施不同干预措施时患者的生化指标比较见表1。
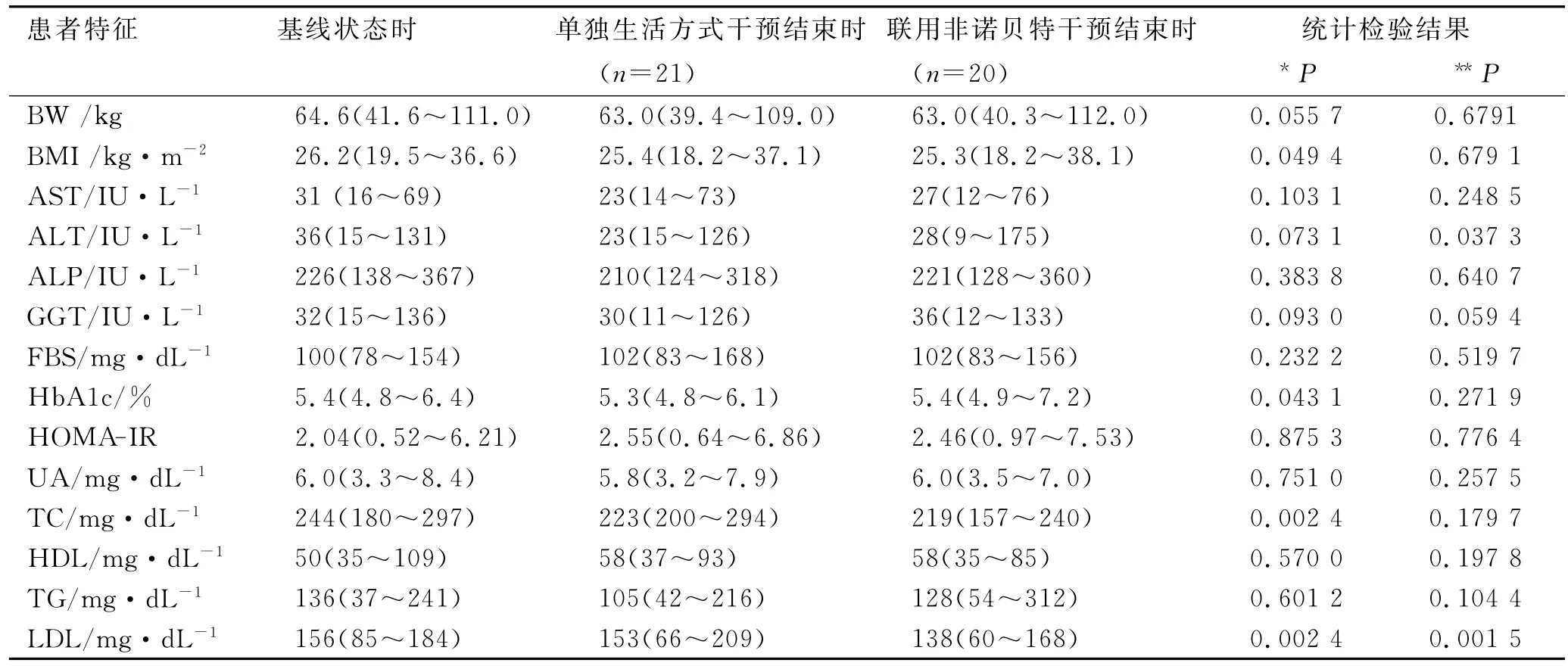
表1 NAFLD患者生活方式干预与联用非诺贝特的人口学和生化特征的比较Tab.1 The comparison of demographic and biochemical characteristics between lifestyle intervention alone and combination lifestyle intervention with fenofibrate in patients with NAFLD
3 讨论
本研究资料显示,对经6个月的生活方式干预后血脂无明显下降的NAFLD患者,联合口服降血脂药物非诺贝特可以显著降低血LDL水平。但仅从纠正脂代谢紊乱这一点看,只进行生活方式干预,对伴有脂代谢紊乱的NAFLD患者未产生满意的结果。在伴有脂代谢紊乱的NAFLD患者肝脏中,尽管胆固醇产生过多,但其合成过程仍处于活跃状态[7],提示在有脂代谢紊乱的NAFLD患者中胆固醇代谢失调。据研究报道,有胰岛素抵抗的肥胖男性体质量下降仅10kg,LDL受体结合能力的提高并不足以降低体内升高的乳糜微粒残留物,但是实施更明显的减体质量措施可使血中乳糜微粒水平降低[8];考虑到饮食对脂代谢的影响,低脂肪、高多糖饮食显示,能使TC水平下降,而高纤维、低蛋白、低脂肪、低碳水化合物的饮食可降低血TC和LDL水平[9]。据此推测,生活方式干预使患者体质量下降的程度不足以引起血中乳糜微粒的下降,而且生活方式干预中对饮食的要求没有限制能量的摄入,没有严格限制饮食中碳水化合物、饱和脂肪酸及胆固醇含量。综合体质量下降程度和饮食成分的差异,NAFLD特异性的脂代谢异常以及脂代谢紊乱相关的基因多态性等因素,推测或许是NAFLD患者仅经6个月的生活方式干预而脂代谢无明显改善的原因。
对于经生活方式干预仍有脂肪代谢紊乱的NAFLD患者,在生活方式干预的基础上联合使用降血脂药物以期改善脂代谢紊乱很有必要。贝特类调节血脂药物是一类人工合成的PPARα(过氧化物增殖物激活受体)的配体[10],研究报道,在NAFLD患者中使用非诺贝特,不仅可以改善脂代谢紊乱,也可改善生化参数如ALT、CRP水平以及肝组织学参数NAS积分与肝细胞脂肪变性分级[11],表明非诺贝特是治疗NAFLD患者脂代谢紊乱的可靠药物[12]。本研究显示,与生活方式干预前基线状态时相比,NAFLD患者LDL水平在单用生活方式干预后有所下降,生活方式干预联合使用非诺贝特后明显下降,BMI、HbA1c、TC等也下降,ALT水平与基线状态时相比未见统计学差异,提示生活方式干预联合使用非诺贝特干预,可有效改善NAFLD患者的脂肪代谢紊乱,降低LDL水平而不引起肝功能损伤。本文显示,NAFLD患者ALT水平在使用非诺贝特后与使用前相比有所升高,但与基线状态时相比略有下降(未显示统计学差异)。在13例使用非诺贝特后血ALT水平有升高的患者中,有10例患者体质量与使用非诺贝特前相比有所增加,因此,推测使用非诺贝特后ALT水平的升高,可能是患者体质量增加后NAFLD肝细胞炎症短暂加剧所致,但不能排除非诺贝特对肝细胞的直接损伤,也不明确其相关作用机制。
本研究中1例患者因出现皮疹和皮肤瘙痒停止用药而退出临床研究,此外未发现其他不良反应,这反映出使用非诺贝特有较好的安全性。本研究的局限性在于,没有对纳入的患者进行肝穿刺,因此,未能明确干预措施实施前、后肝脏组织学变化。今后的研究将对伴LDL水平升高、脂代谢紊乱的NAFLD患者,开展大样本的肝组织学评价,以比较使用非诺贝特联合生活方式干预与单用生活方式干预降低NAFLD患者LDL水平的效果。
总之,本研究结果显示,对血LDL水平升高的NAFLD患者,如果仅用生活方式干预不能使血脂紊乱得到改善,LDL水平仍然较高,在生活方式干预的同时,联合口服降血脂药物非诺贝特可有效地降低LDL水平,而且具有较好的安全性。同时,降低包括TC、LDL在内的血脂水平,对预防和治疗冠心病具有非常重要的意义[13]。
[1]Bugianesi E,Leone N,Vanni E,et al.Expanding the natural history of nonalcoholic steatohepatitis:from cryptogenic cirrhosis to hepatocellular carcinoma[J].Gatroenterology,2002,123(1):134-140.
[2]Speliotes E K,Massaro J M,Hoffmann U,et al.Fatty liver is associated with dyslipidemia and dysglycemia independent of visceral fat:the framingham heart study[J].Hepatology,2010,51(6):1979-1987.
[3]Oza N,Eguchi Y,Mizuta T,et al.A pilot trial of body weight reduction for nonalcoholic fatty liver disease with a home-based lifestyle modification intervention delivered in collaboration with interdisciplinary medical staff[J].J Gastroenterol,2009,44(12):1203-1208.
[4]Saadeh S,Younossi Z M,Remer E M,et al.The utility of radiological imaging in nonalcoholic fatty liver disease[J].Gastroenterology,2002,123(3):745-750.
[5]Teramoto T,Sasaki J,Ueshima H,et al.Executive summary of Japan Atherosclerosis Society(JAS)guideline for diagnosis and prevention of atherosclerotic cardiovascular diseases for Japanese[J].J Atheroscler Thromb,2007,14(2):45-50.
[6]Seagle H,Strain G,Makris A,et al.Position of the A-merican Dietetic Association:weight management[J].J Am Diet Assoc,2009,109(2):330-346.
[7]Tobin K A,Steineger H H,Alberti S,et al.Crosstalk between fatty acid and cholesterol metabolism mediated by liver X receptor-alpha[J].Mol Endocrinol,2000,14(5):741-752.
[8]James A P,Watts G F,Barrett P H,et al.Effect of weight loss on postprandial lipemia and low-density lipoprotein receptor binding in overweight men[J].Metabolism,2003,52(2):136-141.
[9]周峰,华春,李建梅,等.非酒精性脂肪肝的发病机制及其饮食干预[J].中国老年学杂志,2013,33(21):5482-5484.
[10]王谊,吕昊宇,蒋建勤,等.药物治疗高脂血症的作用机制[J].西北药学杂志,2012,27(2):188-190.
[11]Dam-Larsen S,Becker U,Franzmann M B,et al.Final results of a long-term,clinical follow-up in fatty liver patients[J].Scand J Gastroenterol,2009,44(10):1236-1243.
[12]Fernández-Miranda C,Pérez-Carreras M,Colina F,et al.A pilot trial of fenofibrate for the treatment of nonalcoholic fatty liver disease[J].Dig Liver Dis,2008,40(3):200-205.
[13]王艳丽,于晓原,张璐璐.阿托伐他汀钙治疗老年冠心病合并高脂血症的疗效观察[J].西北药学杂志,2013,28(6):630-631.
Efficacy of fenofibrate for reducing serum low-density lipoprotein cholesterol levels resistant to lifestyle intervention in patients with non-alcoholic fatty liver disease
WU Yuhua,LI Chunming,WU Qianhu,ZHU Xiaolei,HUA Changsong(The Third People′s Hospital of Zhenjiang,Zhenjiang 212000,China)
Objective To investigate the efficacy of fenofibrate and lifestyle intervention for treating patients with non-alcoholic fatty liver disease(NAFLD)and residual dyslipidemia via a combination of fenofibrate and lifestyle intervention.Methods Patients with NAFLD with residual dyslipidemia after a 6-month lifestyle intervention program were included and analyzed.After completion of the 6-month program,the patients received po administration of fenofibrate at 100mg·d-1,in addition to lifestyle intervention,for 6months.Results 52patients with NAFLD who had participated in the 6-month lifestyle intervention program between 2012and 2013,21with residual dyslipidemia(10males and 11females)were enrolled.Median age was 58years(range,27-75),median body weight was 63.0kg(range,39.4-109.0),median body mass index was 25.4kg·m-2(range,18.2-37.1),median alanine aminotransferase was 23IU·L-1(14-73),median high-density lipoprotein(HDL)was 58mg·dL-1(range,37-93),median triglycerides(TG)was 105mg·dL-1(range,92-216)and median low-density lipoprotein(LDL)was 153(66-209)mg·dL-1.After 6months of treatment,serum LDL levels were improved in 15of 20(75%)patients(P=0.001 5),while no improvement was observed in the remaining five patients(25%).Fenofibrate was discontinued in one patient who developed skin rash.Conclusion Fenofibrate is effective for treating residual dyslipidemia after lifestyle intervention in patients with NAFLD.
fenofibrate;dyslipidemia;lifestyle intervention;low-density lipoprotein
10.3969/j.issn.1004-2407.2015.01.020
R97
A
1004-2407(2015)01-0073-04
2014-07-01)
