HPLC法测定抗结核病药物四味抗痨丸中巴豆苷的含量
2015-01-12邱远金朱国强贾晓光陈书强李忠民新疆维吾尔自治区中药民族药研究所乌鲁木齐83000上海苍龙生物科技发展有限公司上海00063
邱远金,朱国强*,贾晓光,陈书强,李忠民(.新疆维吾尔自治区中药民族药研究所,乌鲁木齐 83000;.上海苍龙生物科技发展有限公司,上海 00063)
HPLC法测定抗结核病药物四味抗痨丸中巴豆苷的含量
邱远金1,朱国强1*,贾晓光1,陈书强2,李忠民2(1.新疆维吾尔自治区中药民族药研究所,乌鲁木齐 830002;2.上海苍龙生物科技发展有限公司,上海 200063)
目的 建立高效液相色谱法测定四味抗痨丸中巴豆苷含量。方法 采用高效液相色谱法测定四味抗痨丸中巴豆苷的含量。色谱柱为Luna C18柱,流动相为乙腈-甲醇-水(1∶4∶95),检测波长为292nm,流速为1.0mL·min-1。结果 巴豆苷在6.195×10-2~1.239μg范围内与峰面积有良好的线性关系,r=0.999 9(n=7),平均回收率为98.4%,RSD为1.0%,经测定供试品中巴豆苷平均含量为0.207 3mg·g-1。结论 该方法简便、准确、重复性好,可用于四味抗痨丸中巴豆苷含量测定。
四味抗痨丸;巴豆苷;高效液相色谱法;结核病
中国是全球22个肺结核高负担国家之一,肺结核患者数量居世界第1位;据全国法定传染病报告,结核病报告发病人数始终位居法定报告甲、乙类传染病前列,卫生部将结核病列为全国重点控制的重大疾病之一[1]。目前主要采用西药治疗结核病,常伴随对患者肝脏及其他脏器损伤的不良反应和毒副作用,也出现耐药性,在一定程度和范围内西药失去其已有的治疗效果[2-4],因此,抗结核病新药研发尤其从中药中筛选抗结核病药物具有重要意义。四味抗痨丸是在传统药方的基础上研制开发的医疗机构制剂(批准文号:新药制字Z20120005),属纯中药复方,由巴豆霜等四味中药组成,具有滋阴清火、养血敛阴、消肿生肌功效,用于治疗肺结核、骨与关节结核、淋巴结核、结核性胸膜炎等结核病。其中巴豆霜性辛、热,归胃、大肠经,有峻下冷积、逐水退肿、豁痰利咽、抗结核杆菌的功效[5];主要用于泻下寒积、逐水消肿、祛痰利咽及外用蚀疮、恶疮疥癣。本研究采用高效液相色谱法测定四味抗痨丸中巴豆苷的含量,为有效控制制剂质量和保障用药安全提供依据。
1 仪器与试药
1.1 仪器 SK5200HP超声仪(59Hz,200W);Metter EL104电子分析天平;LC-2010CHT型高效液相色谱仪(岛津)。
1.2 试药 巴豆苷对照品(批号111856-201001)购自中国食品药品检定研究院。四味抗痨丸(每10丸质量1g,批号20120412,20120413,20120414)。色谱乙腈、色谱甲醇、乙醚、纯化水。
2 方法与结果
2.1 色谱条件 色谱柱:Luna C18柱(250mm×4.6mm,5μm);流动相:乙腈-甲醇-水(1∶4∶95);检测波长:292nm;柱温:30℃;流速:1.0mL·min-1;进样量:20μL。
2.2 系统适用性 分别取对照品溶液、供试品溶液,缺巴豆霜的阴性供试品溶液,各取10μL注入液相色谱仪,记录色谱图,见图1。结果表明,巴豆苷对照品与四味抗痨丸中巴豆苷的保留时间一致,阴性供试品溶液在相应位置处未出现巴豆苷吸收峰,且巴豆苷色谱峰与其他组分色谱峰分离完全。理论板数按巴豆苷峰计算不低于5 000。
2.3 对照品溶液制备 精密称取巴豆苷对照品适量,置于10mL量瓶中,加水溶解,定容至刻度,得质量浓度61.95μg·mL-1对照品溶液。
2.4 供试品溶液制备 取四味抗痨丸样品粉末(过三号筛)约3g,精密称定,置于索氏提取器中,加乙醚50mL,加热回流3h,弃去乙醚液,药渣挥干溶剂,连同滤纸筒移入具塞锥形瓶中,精密加水50mL,称定质量,超声处理20min,放冷,再称定质量,用水补足减失的质量,摇匀,滤过,即得。
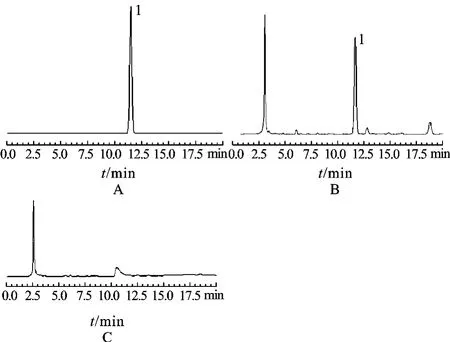
图1 HPLC图A.对照品;B.样品;C.阴性样品;1.巴豆苷Fig.1 HPLC chromatogramsA.reference substance;B.sample;C.negative sample;1.crotonside
2.5 阴性样品 除巴豆霜以外,其余药按四味抗痨丸处方与制法制成阴性样品,再按2.4项下方法制成阴性对照溶液。吸取对照品、供试品及阴性对照溶液注入色谱仪,照上述色谱条件进样测定。结果,阴性对照溶液中在巴豆苷峰的出峰位置处未出现吸收峰,表明处方中其他药材对巴豆苷的含量测定无干扰。
2.6 标准曲线制作 分别精密吸取上述对照品溶液1,2,4,8,10,12和20μL注入色谱仪,在上述色谱条件下测定,以峰面积为纵坐标、巴豆苷质量为横坐标,进行线性回归,得回归方程:Y=2×106X+413.7(r=0.999 9),线性范围:6.195×10-2~1.239μg。
2.7 精密度 吸取对照品溶液10μL,重复进样6次,按上述色谱条件操作,测其峰面积,以峰面积计算RSD值,结果RSD为0.05%,表明此方法精密度良好。
2.8 稳定性 精密吸取供试品溶液10μL,按上述色谱条件,在0,2,4,8,16和24h测定巴豆苷峰面积,计算RSD,结果RSD为0.82%。结果表明,此方法稳定性较好。
2.9 重复性 准确称取同批次供试品6份,按2.4项下方法操作制备供试品溶液,并测定巴豆苷含量,结果平均含量为0.208 1mg·g-1,RSD为1.74%(n=6),实验结果表明,此方法重复性较好。
2.10 回收率 采用加样回收法。称取同一批次样品5份,按照2.4项下方法操作,取样品溶液1mL,分别置于测试瓶中,分别加入质量浓度为61.95μg·mL-1对照品溶液0.2mL,按照标准曲线制作中峰面积测定方法进行操作,计算,平均回收率为98.4%,RSD为1.0%,结果表明此方法回收率良好。
2.11 样品含量测定 取3批样品,按上述色谱条件和方法测定巴豆苷的含量。结果3批样品(批号分别为20120412,20120413,20120414)的含量分别为0.206 2,0.209 6和0.205 9mg·g-1,平均含量为0.207 3mg·g-1。
根据上述测定结果,1g样品含巴豆霜以巴豆苷(C10H13N5O5)计,不得少于0.14mg。
3 讨论
结核病是严重危害人类健康的慢性传染病,已成为全球重大的公共卫生问题和社会问题[6]。根据2011年全国第五次结核病流行病学调查报告及新疆结核病监测报告结果显示,新疆结核病发病形势呈现出复杂、耐药、难治性结核病人增多、结核病合并艾滋病双重感染病人增多等特点,结核病对新疆社会稳定和经济发展造成了重大影响[7]。四味抗痨丸作为医疗机构制剂在新疆多所医院使用,在治疗和控制新疆结核病方面起到了较好的作用。
从处方组成看,巴豆霜作为处方主要组成成分之一,主要含有:脂肪油(即巴豆油,为棕榈酸、硬脂酸、油酸、巴豆油酸、巴克酸等的甘油酯),蛋白质(含巴克毒素crotin),巴克树脂(为泻下成分,是巴克豆醇phorbol、甲酸、丁酸、巴克油酸等结合而成的酯),生物碱,巴豆苷等[8],巴豆苷是巴豆霜中典型成分之一,具有多种生物活性和药理活性,具有抗结核杆菌的作用[5,910];因此,测定有效成分巴豆苷含量对控制四味抗痨丸质量具有重要意义,选择巴豆苷为定量测定指标。本研究采用HPLC法对3批供试品中巴豆苷含量进行测定,3批样品的含量分别为0.206 2,0.209 6和0.205 9mg·g-1,平均含量为0.207 3mg·g-1。根据测定结果,1g样品含巴豆霜以巴豆苷(C10H13N5O5)计,不得少于0.14mg。高效液相色谱法常用于测定药物中有效成分[11-12],具有方法简便、准确、重复性好的特点,该方法可用于四味抗痨丸中巴豆苷含量测定。
[1]肖东楼,赵明刚.中国结核病防治规划实施工作指南[M].北京:中国协和医科大学出版社,2009:25-26.
[2]肖和平,顾瑾.抗结核药物性肝损伤的临床特点[J].中国防痨杂志,2013,35(7):485-487.
[3]冯红云,陈易新.4 750例抗结核药品不良反应分析[J].中国药物警戒,2010,7(12):751-754.
[4]高星,欧阳松,林鸳.453例抗结核药物引起副作用的临床分析[J].江西医药,2010,45(4):334-335.
[5]胡林峰,韩会娟,朱红霞,等.巴豆提取物抑菌活性初步研究[J].湖南农林科学,2011,(7):78-79,84.
[6]WHO.Global tuberculosis control:surveillance,planning,financing[M].Geneva:World Health Organization,2007:9-11.
[7]杨津明,杰恩斯·斯马胡勒,邰新蓉,等.新疆维吾尔自治区2010-2011年结核病流行病学抽样调查结果分析[J].中国防痨杂志,2013,35(12):960-964.
[8]金锋,张振凌,任玉珍,等.巴豆的化学成分和药理活性研究进展[J].中国现代中药,2013,15(5):372-375.
[9]陈蓓华,王哲人.单味巴豆治疗骨结核[J].中国民间疗法,1998,6(6):46-47.
[10]赵中夫,赵正保.巴豆油各分离组份体外抗结核分枝杆菌实验研究[J].长治医学院学报,2006,20(1):1-3.
[11]那海秋,高广慧,赵飞,等.高效液相色谱法测定多维元素片中泛酸的含量[J].西北药学杂志,2014,29(2):145-146.
[12]侯鸿军,王莉.HPLC法测定余甘降脂片中没食子酸的含量[J].西北药学杂志,2014,29(1):22-24.
Determination of crotonside in the anti-tuberculosis drug Siweikanglao Pills by HPLC
QIU Yuanjin1,ZHU Guoqiang1*,JIA Xiaoguang1,CHEN Shuqiang2,LI Zhongmin2(1.Xinjiang Institutes of Traditional Chinese Medica and National Medica,Urumqi 830002,China;2.Biological Technology Development Limited Company of Shanghai Canglong,Shanghai 200063,China)
Objective To establish an HPLC method for the determination of crotonside in Siweikanglao Pills.Methods HPLC analysis was carried out on a Luna C18column and a mixture of acetonitrile-methanol-water(1∶4∶95)was used as the mobile phase,with the detection wavelength at 292nm,and the flow rate at 1.0mL·min-1.Results The linear range of crotonside was from 6.195×10-2to 1.239μg.The correlation coefficient of the calibration curves was 0.999 9.The average recovery rate was 98.4% with relative standard deviation of 1.0%.The average content in Siweikanglao Pills was 0.207 3mg·g-1.Conclusion The results showed that the method is simple,accurate and repeatable,and it is suitable for the quality control of Siweikanglao Pills.
Siweikanglao Pills;crotonside;HPLC;anti-tuberculosis
10.3969/j.issn.1004-2407.2015.01.009
R282
A
1004-2407(2015)01-0028-03
2014-07-22)
新疆维吾尔自治区科技支撑计划项目(编号:201233137)
邱远金,男,助理研究员
*通信作者:朱国强,男,研究员
