西南远志中一个新的三萜皂苷
2015-01-08耿圆圆黄艳杰王军民
耿圆圆,黄艳杰,王军民,周 俊,华 燕*
1 西南林业大学,昆明 650224;2中国科学院昆明植物研究所,昆明 650201
西南远志(Polygala crotalarioides Buch.Ham.)为远志科远志属植物,别名地花生、翻转红、猪大肠(四川),娘母良(云南佤族语)[1]。该植物是云南佤族民间流传的一种珍奇中药,长期服用能使眉须秀长,有颜容光泽和痣斑消退等功效[2]。作为一种民间中药,西南远志主要用于活血止痛、安神补心、顺气化痰[3-5];此外,药理学实验表明,西南远志还具有抗缺氧、抗疲劳、抗低温、提高机体对不良环境的适应能力等功效[6]。在前期工作中已报道了6 个新的口山酮[7-9]和两个新的三萜皂苷类化合物[10]的分离和结构鉴定,为从该植物中寻找更多的活性单体成分,本实验对采自云南云县的西南远志进行了进一步的化学成分研究,分离得到3 个齐墩果酸型皂苷类化合物,分别为3-O-β-D-葡萄糖基presenegenin 28-O-α-L-阿拉伯糖基-(1→3)-β-D-木糖基-(1→4)-[β-D-芹糖基-(1→3)]-α-L-鼠李糖基-(1→2)-[β-D-葡萄糖基-(1→3)]-[4-O-(E/Z)-3″,4″,5″-三甲氧基肉桂酰基]-β-D-岩藻糖基酯(1)、3-O-β-D-葡萄糖基presenegenin 28-O-β-D-木糖基-(1 →4)-α-L-鼠李糖基-(1→2)-[α-L-鼠李糖基-(1→3)]-[4-O-(E/Z)-对甲氧基肉桂酰基]-β-D-岩藻糖基酯(2)和3-O-β-D-葡萄糖基presenegenin 28-O-α-L-阿拉伯糖基-(1→4)-β-D-木糖基-(1→4)-[β-D-芹糖基-(1→3)]-α-L-鼠李糖基-(1→2)-[4-O-(E/Z)-对甲氧基肉桂酰基]-[α-L-鼠李糖基-(1→3)]-β-D-岩藻糖基酯(3),命名为(E/Z)-crotalarioside G(1),(E/Z)-Onjisaponin Y(2)和(E/Z)-polygalasaponin XXXII(3)。化合物结构式见图1。
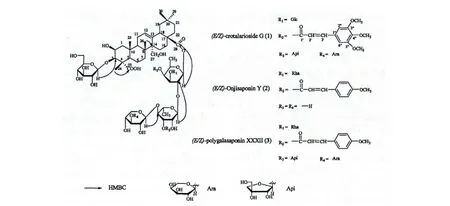
图1 化合物1~3 的化学结构及主要HMBC 相关Fig.1 Chemical structures and key HMBC correlations of compounds 1-3
1 仪器与材料
HPD100 大孔树脂;薄层层析硅胶;柱层析硅胶(80~100 目、200~300 目和300~400 目);Sephadex LH-20;反相填充材料Rp-18(40~60 μm);HPLC 分析柱(Agilent,ZORBAX SB-C18,4.6 ×150 mm,5 μm);HPLC 半制备柱(Agilent,ZORBAX SBC18,9.4 ×250 mm,5 μm);Bruker DRX-500 核磁共振仪,TMS 作内标,化学位移δ 用ppm 表示,偶合常数J 用Hz 表示;Bio-Rad FTS-135 型红外光谱测定仪(KBr 压片);UV2401 PC 紫外可见分光光度计;Finnigan MAT90 质谱仪;Bruker HTC/Esquire 液相-离子阱色谱质谱联用仪;Waters AutoSpec Premier P776 质谱仪;显色剂:5%H2SO4乙醇溶液。
西南远志1 kg,采自云南省云县,由昆明植物所陈书坤研究员鉴定,标本现保存在昆明植物所植物化学与西部植物资源持续利用国家重点实验室。
2 提取与分离
西南远志根1 kg,粉碎后用75%乙醇提取4次,第一次4 h,之后三次各2 h,合并提取液,减压浓缩回收乙醇。水溶液通过HPD100 树脂,用水、75%乙醇、95%乙醇依次洗脱。75%洗脱部分减压浓缩得浸膏96 g,以200 g 硅胶(80~100 目)拌样,1.5 kg 硅胶(200~300 目)干柱柱层析,用氯仿-甲醇-水(7∶4∶1)洗脱,得到10 个组分(1~10)。
组分1~4(75.8 g),经硅胶(氯仿-甲醇-水7∶3∶0.5 和7∶5∶1)和Sephadex LH-20(甲醇)柱层析,得到总皂苷(15 g)。经RP-18 反相柱(甲醇-水5∶5→7∶3)柱层析,把总皂苷分为4 个组分(A~D)。每个组分所含皂苷结构类似,结合的糖基又较多,常规反相柱分离难度很大,故采用制备、半制备HPLC 分离。
组分B 用HPLC 半制备,乙腈-0.1%醋酸水溶液(39∶61)为流动相,得到化合物2(36 mg)和3(35 mg)。组分C 用HPLC 半制备,乙腈-0.1%醋酸水溶液(34∶66)为流动相,得到化合物1(61 mg)。
3 结构鉴定
化合物1 白色粉末;高分辨质谱HR-TOF-MS给出分子离子峰1749.7378[M-H]-(计算值1749.7383),分子式C81H122O41,质谱ESI-MS m/z:1749.2[M-H]-。IR (KBr):3430、2931、1721、1635、1260、1076 cm-1,表明有羟基、羰基和烯基官能团。在13C NMR 谱上可看到苷元部分有30 个碳信号,其中有二个羰基碳信号[δC181.4 (s),176.8 (s)],二个双键碳信号[δC139.3 (s),127.9 (d)],五个甲基信号[δC33.1 (s),24.1 (s),18.8 (s),17.5 (s),14.3(s)],一个氧亚甲基信号[δC64.5 (t)]。另外,在1H 和13C NMR 谱上还可观察到七个糖基端基碳及相应氢质子的信号[δC111.3 (d),105.6 (d),105.2 (d),105.2 (d),104.6 (d),101.8 (d),94.9(d);δH6.01 (1H,d,J=4.0 Hz),5.01 (1H,d,J=7.5 Hz)/5.02*,5.04 (1H,d,J=7.8 Hz),5.15(1H,d,J=6.5 Hz),6.30/6.41 (1H,br s),6.14/6.16 (1H,d,J=8.0 Hz)]和一对对3″,4″,5″-三甲氧基肉桂酰基顺反异构体信号(见表1 和2),提示可能为三萜皂苷。其苷元部分的1H 和13C NMR 数据与已知苷元presenegenin[11]比较发现,两者基本相同,说明化合物1 的苷元为presenegenin。继续分析发现,由于这对3″,4″,5″-三甲氧基肉桂酰基顺反异构取代基的存在,使糖基部分出双峰或细微裂分现象,苷元部分由于距离较远,影响不大,但也有一些氢谱信号出现裂分。
糖基部分的化学位移由HMQC、HMBC、HMQCTOCSY 谱得到归属。其碳、氢信号及端基氢的偶合常数与所报道文献[11]中化合物polygalasaponin XXXI 糖基部分几乎一致,故推断化合物1 的糖基种类及构型与polygalasaponin XXXI 中的相同,为β-D-葡萄糖,β-D-木糖,α-L-鼠李糖,β-D-岩藻糖,β-D-芹糖和α-L-阿拉伯糖。不同的是岩藻糖基3 位上增加了一个葡萄糖基,可由岩藻糖基3 位的碳化学位移向低场移至δC82.5/82.7,且增加的葡萄糖基的H-1″″'与其HMBC 相关所证实。其它糖基连接次序与polygalasaponin XXXI 中的相同,可通过HMBC 谱来进一步确定。在HMBC 谱上可看出以下远程相关:葡萄糖基的H-1'与苷元C-3 相关,岩藻糖基的H-1″与苷元C-28 相关,鼠李糖基的H-1″与岩藻糖基的C-2″相关,木糖基的H-1″″与鼠李糖基的C-4'″相关,另外一个葡萄糖基的H-1″″'与岩藻糖基的C-3″″相关,芹糖基的H-1″″''与鼠李糖基的C-3″'相关,阿拉伯糖基的H-1″″''与木糖基的C-3″″,并且岩藻糖基H-4″与(E/Z)-3″,4″,5″-三甲氧基肉桂酰基羰基碳相关。在HPLC 上分析时,化合物1 表现为两个峰,以乙腈-0.1%醋酸水溶液(34∶66)为流动相,用RP-18柱HPLC 制备分离,结果发现两个化合物之间互变,无法使其分离,最后只能以立体异构混合体形式得到。综上所述,其结构可鉴定为3-O-β-D-葡萄糖基presenegenin 28-O-α-L-阿拉伯糖基-(1→3)-β-D-木糖基-(1→4)-[β-D-芹糖基-(1→3)]-α-L-鼠李糖基-(1→2)-[β-D-葡萄糖基-(1 →3)]-[4-O-(E/Z)-3″,4″,5″-三甲氧基肉桂酰基]-β-D-岩藻糖基酯,命名为(E/Z)-crotalarioside G。
化合物2 白色粉末,质谱FAB-MS m/z:1410[M]-。结合13C 核磁共振数据确定该化合物分子式为C69H102O30。IR (KBr):3455、2931、1719、1615、1258、1069 cm-1。仔细比较化合物2 和1 的1H 和13C NMR 数据发现,两者结构非常相似,只是苷元C-28上糖基的种类和数量不一样。化合物2 中无芹糖和阿拉伯糖,原连接在岩藻糖基上的葡萄糖基和(E/Z)-3″,4″,5″-三甲氧基肉桂酰基消失,取而代之的是另一鼠李糖基和一个(E/Z)-对甲氧基肉桂酰基,由于对甲氧基肉桂酰基顺反异构体的存在,与化合物1 情况相同,用RP-18 柱HPLC 制备分离,发现两个化合物之间也存在互变,无法使其分离。所以,化合物2 最终也只能以立体异构混合物形式得到,结构鉴定为3-O-β-D-葡萄糖基presenegenin 28-O-β-D-木糖基-(1 →4)-α-L-鼠李糖基-(1 →2)-[α-L-鼠李糖基-(1→3)]-[4-O-(E/Z)-对甲氧基肉桂酰基]-β-D-岩藻糖基酯。通过与文献[12]比较,发现化合物2 与Onjisaponin Y 的结构相同,但文献没有对该化合物的立体构型进行阐述。最终命名为(E/Z)-Onjisaponin Y。
化合物3 白色粉末,质谱FAB-MS m/z:1674[M]-,结合13C 核磁共振数据确定该化合物分子式为C79H118O38。通过与文献[11]比较,发现化合物3与polygalasaponin XXXII 的13C 和1H NMR 数据基本一致,但文献没有对该化合物的立体构型进行阐述。与化合物1 和2 情况相同,化合物3 出现图谱双峰或细微裂分现象,归结其原因是由于(E/Z)-对甲氧基肉桂酰基的存在。用RP-18 柱HPLC 制备分离,发现两个化合物之间也存在互变,无法使其分离。所以,化合物3 最终也是以立体异构混合物形式得到,结构鉴定为3-O-β-D-葡萄糖基presenegenin 28-O-α-L-阿拉伯糖基-(1→4)-β-D-木糖基-(1→4)-[β-D-芹糖基-(1 →3)]-α-L-鼠李糖 基-(1 →2)-[4-O-(E/Z)-对甲氧基肉桂酰基]-[α-L-鼠李糖基-(1 →3)]-β-D-岩藻糖基酯,命名为(E/Z)-polygalasaponin XXXII。
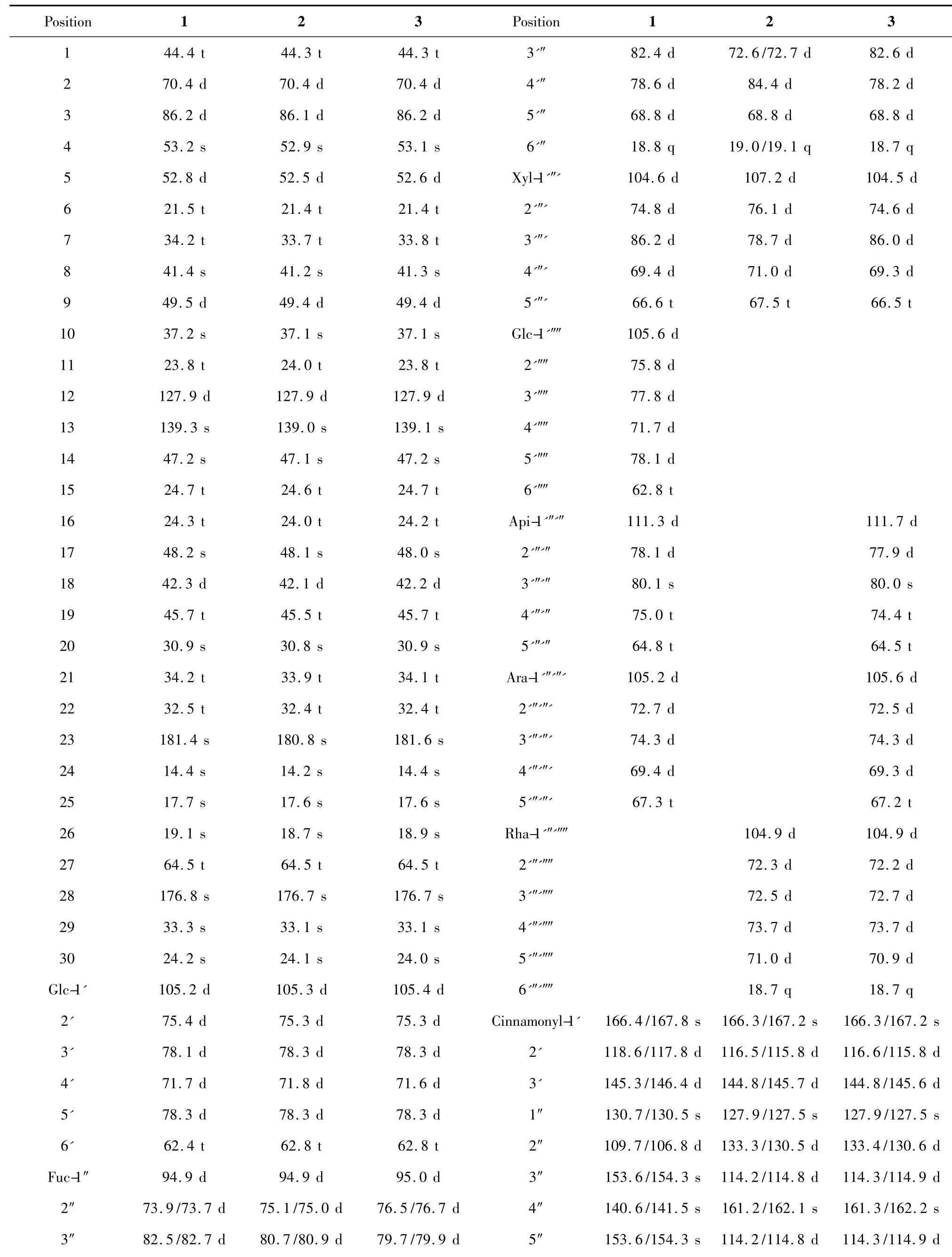
表1 化合物1~3 的碳谱数据(125 MHz,C5D5N,δ)Table 1 13C NMR spectral data of 1-3 (125 MHz,C5D5N,δ)


表2 化合物1~3 的氢谱数据(500 MHz,C5D5N,δ)Table 2 1H NMR spectral data of 1-3 (500 MHz,C5D5N,δ)
1 Delectis Florae Reipublicae Popularis Sinicae,Agendae Academiae Sinicae Edita (中国植物志编委会).Flora Reipublicae Popularis Sinicae (中国植物志).Beijing:Science Press,1997.182-183.
2 Xiang BX (向碧霞),Zhang PF (张平夫),Xiang YH (向应海).The investigation of Wa herbs“Ya mo niang”and their resouses.Guizhou Sci (贵州科学),1995,13:24-28.
3 Wu ZY (吴征镒).Xinhua Outline of Materia Medica,1st Ed (新华本草纲要,第1 版).Shanghai:Shanghai Science and Technology Press,1985.283-284.
4 Sichuan Institute of Chinese Medicine (四川省中药研究所).Sichuan Chinese Herbal Medicine (四川常用中草药).Chengdu:Sichuan People's Publishing House,1971.511-512.
5 Jiangsu New Medical College (江苏新医学院).Dictionary of Chinese Medicine,Vol.1 (中药大辞典,上册).Shanghai:Shanghai People's Publishing House,1977.815.
6 Zhang PF (张平夫),Li MJ (李明炬),Sun XH (孙学惠).Pharmacological studies on the strong effects of“Ya mo niang”.Guizhou Sci (贵州科学),1995,13:35-38.
7 Hua Y,Chen CX,Liu YQ,et al.Three new xanthones from Polygala crotalarioides.Chin Chem Lett,2006,17:773-775.
8 Hua Y,Chen CX,Liu YQ,et al.Two new xanthones from Polygala crotalarioides.J Asian Nat Prod Res,2007,9:273-275.
9 Zhou LY (周凌云),Zhou FR (周凡蕊),Hua Y(华燕).One new xanthone from Polygala crotalarioides.China Tradit Herb Drugs (中草药),2011,42:1261-1263.
10 Hua Y,Chen CX,Zhou J.Two new triterpenoid saponins from Polygala crotalarioides.Chin Chem Lett,2010,21:1107-1110.
11 Zhang DM,Miyase T,Kuroyanagi M,et al.Five new triterpene saponins,polygalasaponins XXVIII-XXXII from the root of Polygala japonica Houtt.Chem Pharm Bull,1996,44:810-815.
12 Li CJ,Yang JZ,Yu SS,et al.Triterpenoid saponins with neuroprotective effects from the roots of Polygala tenuifolia.Planta Med,2008,74:133-141.
