大孔树脂对红枣汁吸附脱色的动力学和热力学研究
2015-01-01吕新刚王毕妮
李 丹,吕新刚,程 妮,王毕妮,曹 炜
(西北大学化工学院,陕西西安 710069)
红枣,又名大枣,为鼠李科植物枣的成熟果实。红枣不仅富含多种营养素和生物活性物质,而且有多种保健功能。我国是世界红枣主产国[1],但红枣加工产品以干枣、枣酱、枣脯等传统产品居多,精深加工产品较少[2],红枣资源优势尚未得到充分利用。因而,生产高附加值的红枣精深产品成为提高红枣产业国内外竞争力的有效途径。近年来,色泽自然、澄清透明的红枣汁饮料倍受青睐,但是由于红枣富含酚类、多糖及氨基酸等褐变前体物质[3],在加工过程中极易发生褐变,严重影响了红枣汁的质量,因而脱除红枣汁在加工过程中产生的褐变物质,改善红枣汁的色泽对提高其质量尤为重要。
目前,提高果汁色值多用吸附技术。常用的吸附材料有活性炭、膨润土、聚乙烯吡咯烷酮(PVPP)和大孔树脂。其中,大孔树脂不仅克服了活性炭吸附选择性差、膨润土易堵塞超滤膜、PVPP难回收的缺点,而且相比传统吸附剂,大孔树脂还具有吸附量大、再生性好、稳定性强、成本低、操作简单及易于实现自动化等优点[4]。
本文选用HYA-602大孔吸附树脂对红枣汁进行吸附脱色,研究吸附脱色过程的动力学和热力学性质,为大孔吸附树脂在红枣汁脱色中的应用提供依据。
1 材料与方法
1.1 材料与试剂
红枣,陕西佳县红枣;果浆酶(Mzyme PL),食品级,诺维信酶制剂有限公司;HYA-602大孔树脂,西安瀚宇树脂科技有限公司;无水乙醇为国产分析纯。
1.2 仪器与设备
HH-2型电热恒温水浴锅,北京科伟永兴仪器有限公司;JM-B5002电子秤,余姚市纪铭称重校验设备有限公司;LXJ-Ⅱ型低速大容量多管离心机,上海安亭科学仪器厂;TGL-16G高速台式离心机,上海安亭科学仪器厂;JB90-D型强力电动搅拌,上海标本模型厂;722G可见分光光度计,上海仪电分析仪器有限公司;WYT-4型手持糖量仪,吴州中友光学仪器有限公司;打浆机,美国ACA公司。
1.3 指标测定方法
可溶性固形物测定:采用手持糖量仪。色值A420的测定[5]采用分光光度计法,方法如下:取2mL样品,加入等体积95%(体积分数)乙醇,混匀,静置10min;于5 000r/min条件下离心10min后,取上层清液于1cm比色皿中,以蒸馏水为对照,在波长420nm处测定其吸光度;重复测定3次,取平均值。
1.4 实验方法
1.4.1 红枣汁的制备 称取完整无霉烂的红枣适量,清洗后加入4倍体积的纯净水,于70℃加热软化20min。软化后冷却至室温,手工去核后打浆。枣浆于50℃酶解2h,然后以4 800r/min离心10min,取上层清液即得红枣原汁。
1.4.2 树脂的预处理 将新树脂加3倍树脂体积的95%(体积分数)乙醇浸泡3 h,然后用蒸馏水以1~2BV/h的速度淋洗至流出液没有乙醇味,倒出备用。
1.4.3 动力学吸附实验 取适量红枣汁稀释至12Brix。将300mL稀释后的红枣汁置于500mL烧杯中,加入30g树脂,置于25℃下搅拌。每隔10min取样测定吸光值A420,按照式(1)计算即时吸附量qt,绘制吸附动力学曲线,确定吸附平衡时间。

式中:qt为时间t时树脂的即时吸附量,g-1;A为初始吸光值;At为时间t时的吸光值;m为树脂的添加量,g。
1.4.4 热力学吸附实验 分别取300mL稀释后的红枣汁(12Brix)置于5个烧杯中,准确加入6,12,18,24,30g 树脂在 298,313,328K 条件下搅拌至达吸附平衡状态,测定吸光值A420。绘制吸附等温线,计算热力学参数。以上所有实验均以未加树脂的红枣汁作为空白对照,对所测吸光值进行校正,以消除温度等环境因素对其的影响。
1.5 数据处理与分析
本研究中所有数据均采用Microsoft Office Excel进行处理并借助OriginLab公司的Origin 8.0进行绘图和拟合,采用SPSS19进行误差分析。
2 结果与分析
2.1 吸附动力学
2.1.1 吸附动力学曲线 吸附动力学曲线是反映吸附量与吸附作用时间关系的曲线。当吸附量不再增加(在本实验中表现为吸光值A420不再减少)时,认为吸附反应达到表观吸附平衡。HYA-602树脂的吸附动力学曲线见图1。
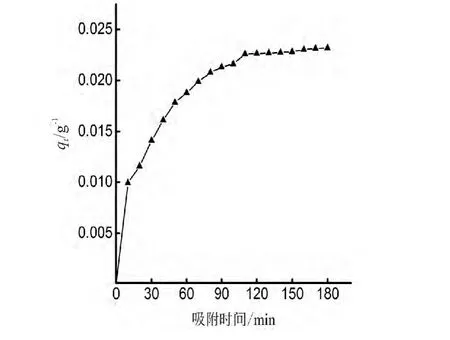
图1 298K条件下,HYA-602树脂的吸附动力学曲线(树脂浓度=100g/L)Fig.1 Adsorption kinetic curve of HYA-602 resin at 298K(resin concentration=100g/L)
可以看出,吸附反应开始后,红枣汁中褐变物质在HYA-602树脂上的吸附量在最初10min内急剧增加,随后吸附量的增加趋于缓和,直到110min时吸附反应进入平台期。鉴于此,可将红枣汁中褐变物质在HYA-602树脂上的吸附过程分为快速吸附阶段、慢吸附阶段和吸附平衡阶段。吸附反应开始的最初10min为快速吸附阶段,吸附量达到了表观平衡吸附量(110min时的吸附量)的43%,此阶段反应的推动力可能是固液两相中吸附质的浓度差以及吸附剂表面大量空余的吸附位点;10min至100min为慢速吸附阶段,吸附量占表观平衡吸附量的52%,此阶段固液两相中吸附质的浓度差逐渐缩小,吸附剂表面的吸附位点趋于饱和;110min至180min为吸附平衡阶段,瞬时吸附速率(dqt/dt)逐渐减小到零。
2.1.2 吸附动力学模型与吸附机理 本研究采用Pseudo一级速率方程[6]、Pseudo二级速率方程[7]、Elovich 动力学模型[8]、Weber&Morris 颗粒内扩散模型和Boyd液膜扩散模型对298K下红枣汁中褐变物质在HYA-602树脂上的吸附过程进行描述。
1)吸附反应模型
Pseudo一级速率方程、Pseudo二级速率方程和Elovich动力学模型非线性拟合的各参数见表1。从表中各参数可以看出,3种动力学模型对于描述红枣汁中褐变物质在HYA-602树脂上的吸附过程都有较好的适用性。从决定系数r2来看,相较于Pseudo一级速率方程和Pseudo二级速率方程,Elovich动力学模型的拟合度最佳(r2在0.99以上);从误差分析角度,Elovich动力学模型的RSS,ARS,χ2均小于前两者。所以,Elovich动力学模型能够更准确地描述HYA-602树脂对于红枣汁的吸附脱色过程。这表明红枣汁中褐变物质在HYA-602树脂上的吸附过程可能是发生在不均匀吸附表面的化学吸附过程,并且吸附反应过程中活化能的变化较大,吸附速率随着吸附剂表面吸附量的增加呈指数下降。
2)吸附机理
吸附反应的速率是由吸附机理和反应限速步骤决定的。普遍认为树脂对于底物的吸附过程主要包括以下3步:①吸附质穿过紧贴在树脂表面的边界层到达树脂表面,即液膜扩散;②吸附质通过树脂外表面的微孔向其颗粒内部扩散,到达树脂内表面,即颗粒内扩散;③吸附质在树脂内表面上的吸附位点被吸附,即发生吸附反应。一般情况下,第3步反应的速度非常快,所以液膜扩散或(和)颗粒内扩散是整个吸附反应的控制步骤[10]。
Weber&Morris颗粒内扩散模型是最常报道的用于揭示吸附反应机理的模型,其表达式如下:

式中:qt为时间t时树脂的吸附量,g-1;kip为第p阶段反应速率常数,g-1·min-1/2;Ci为图线中第i阶段的截距,g-1。
根据动力学实验数据绘制qt-t1/2图(图2),图线不经过原点,说明吸附液膜扩散不是反应的唯一限速步骤[11]。并且,动力学曲线分为3部分,分别可用来描述吸附过程对应的3个步骤:液膜扩散阶段、颗粒内扩散阶段、吸附平衡阶段[12]。线性拟合得第一阶段的截距为0.001 1,说明边界层效应对于整个吸附反应速率的影响较小[13]。
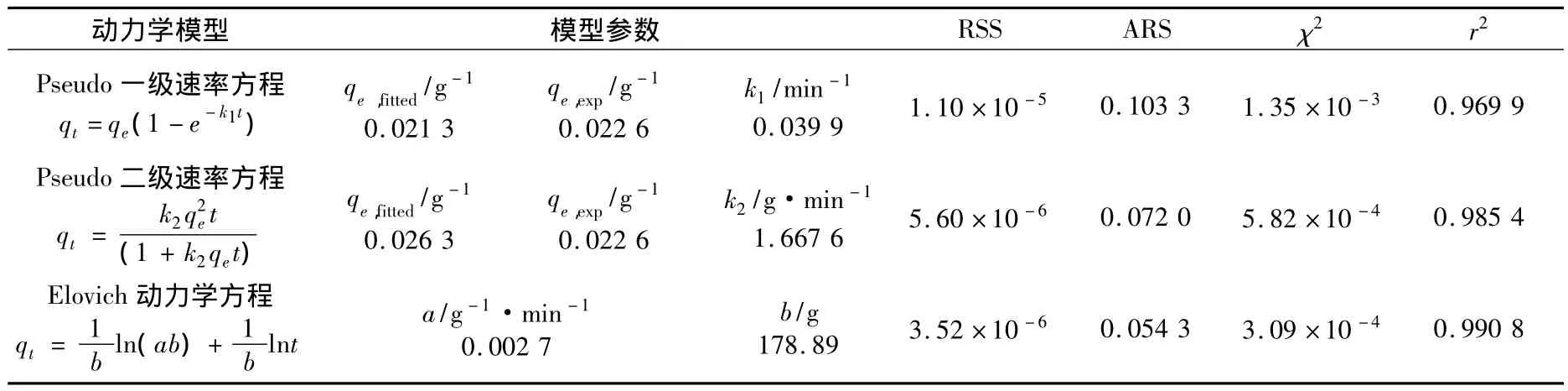
表1 不同动力学模型的非线性拟合参数和误差分析Tab.1 Parameters and error analysis of different kinetic models(non-linear regression method)

图2 Weber&Morris颗粒内扩散模型图(T=298K,树脂浓度=100g/L)Fig.2 Plot of Weber&Morris intraparticle diffusion model(T=298K,resin concentration=100g/L)
为了进一步揭示HYA-602树脂对红枣汁吸附脱色反应达平衡前的控制步骤,本文采用Boyd模型(见式(3))对0~100min的动力学实验数据进行剖析。

式中:F为时间t时的平衡分数,Bt为F的数学函数。吸附反应达平衡时可表示为F=qt/qe,则上式经简化变形后为Bt=-ln(1-F)-0.497 7。
Bt-t呈良好的线性(r2=0.980 6),但不经过原点,表明HYA-602树脂对红枣汁吸附脱色过程的反应速率受液膜扩散的控制[14]。同时,液膜扩散虽为整个吸附反应的限速步骤,但其对于控制反应速率的贡献只占很小一部分;相反,颗粒内扩散对于反应的限速效应不容忽视。
2.2 吸附等温线
固液吸附是发生在固液两相界面上的表面效应。当吸附达到表观平衡时,吸附与解吸速率相等。在恒温条件下,通过固相中溶质的浓度Q对液相中溶质的浓度C作图,便得到吸附等温线。本研究中 Q= [(A-Ae)/Ae]/m,C=Ae/A。用不同的等温吸附模型对等温线进行拟合,可以揭示吸附剂的吸附特性,并且近一步了解吸附热力学特性。常用的等温吸附模型有Langmuir型、Freundlich型、Temkin型、Dubinin-Radushkevich(DR)型、Toth型、BET型、Redlich-Peterson(R-P)型等[15]。
298,313,328K条件下HYA-602树脂对红枣汁吸附脱色反应的吸附等温线见图3。可以看出,随着温度的升高,同一树脂浓度下的吸附量呈增加趋势,说明升温有利于吸附反应的进行。

图3 不同温度下吸附等温线Fig.3 Plot of adsorption isotherms at different temperature
采用 Langmuir型、Freundlich型、Redlich-Peterson(R-P)型和Temkin吸附模型对吸附等温线进行拟合,各模型参数和误差分析见表2。结果显示,在本实验条件下,以上4种吸附模型对于3个温度下的吸附等温线均有较高的拟合度(r2大于0.92)。但是,结合误差分析值知,Langmuir模型对红枣汁中褐变物质在HYA-602树脂上的等温吸附行为描述最佳,其次是Temkin模型和Redlich-Peterson(R-P)模型,而Freundlich模型稍差。从Langmuir模型的角度,单分子层饱和吸附量Qm和吸附常数KL随反应温度的升高而增大,表明HYA-602树脂对红枣汁中褐变物质的吸附能力和结合能力随温度升高而增加。从Freundlich模型给出的参数n可知,3个反应温度下1/n的值分别为0.34,0.33,0.32,均小于 0.5,说明红枣汁中褐变物质易吸附于HYA-602树脂[16];并且随着温度的升高,吸附强度n和吸附容量KF均增加,表现出化学吸附的特征[17]。Redlich-Peterson(R-P)模型是结合了 Langmuir模型和Freundlich模型的3参数经验方程[18],本研究中298,313,328K条件下的R-P经验常数β均接近于1,表明等温吸附过程接近于Langmuir模型的描述。红枣汁中褐变物质在HYA-602树脂上的吸附并非理想的均匀表面吸附,这可能跟HYA-602树脂的表面特性、红枣汁中褐变物质结构的复杂性以及多元食品体系中或许存在的多组分竞争吸附有关。
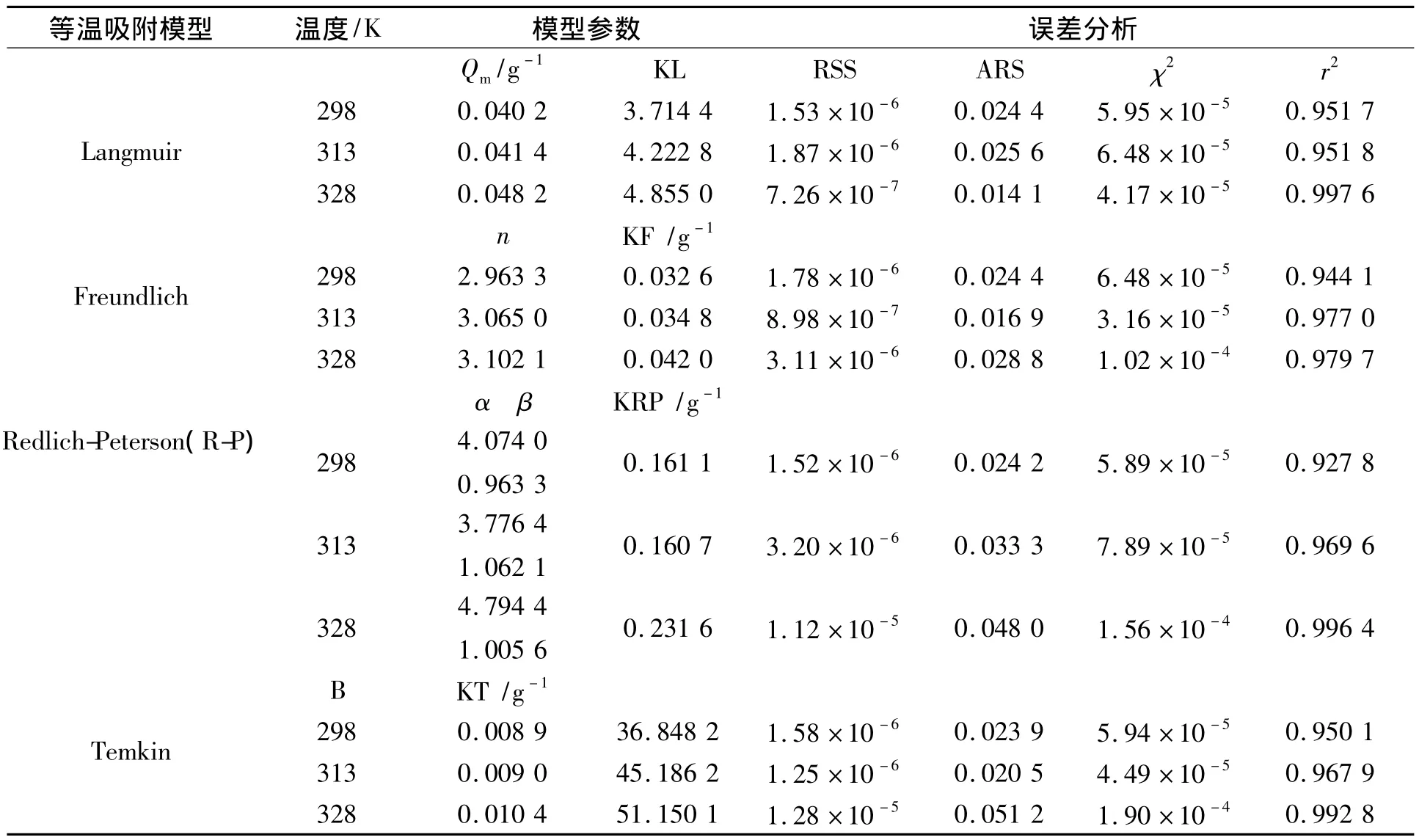
表2 不同等温吸附模型非线性拟合参数及误差分析Tab.2 Parameters and error analysis of different isotherm models(non-linear regression method)
2.3 吸附热力学
为了揭示HYA-602树脂对红枣汁吸附脱色的热力学特征,本研究采用吉布斯方程(式4)和范特霍夫方程(Van't Hoff)(式5)给出该吸附过程的热力学参数:Gibbs自由能变(ΔG)、熵变(ΔS)和焓变(ΔH)。
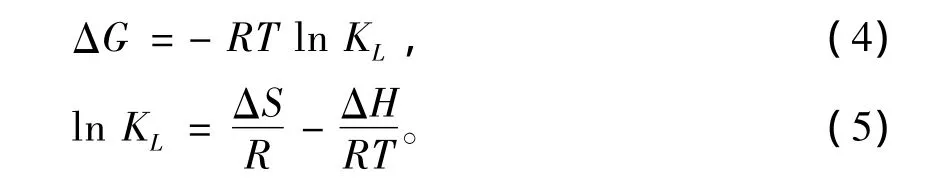
式中:R为摩尔气体常数,R=8.314J/mol·K;T为绝对温度,K;KL为Langmuir吸附平衡常数。
HYA-602树脂对红枣汁吸附脱色过程的热力学参数见表3。由此可知,该吸附过程的ΔG<0,ΔH>0,说明吸附过程是吸热的并且是自发进行的,升温有利于反应的进行,这与上文得到的结论相同。同时,吸附焓变ΔH<20kJ/mol,结合前述动力学和等温模型研究结果,可以判断物理吸附和化学吸附同时存在于HYA-602树脂对于红枣汁的吸附脱色过程中,并且该吸附过程以物理吸附为主,符合“果汁生产过程只能采用物理方法”的规定[19],说明该种树脂可以用于果汁脱色。
3 结论
1)在298K,树脂浓度100g/L条件下,HYA-602树脂对红枣汁的吸附脱色过程能够在较短的时间内达到平衡(110min);并且Elovich动力学方程对该吸附过程的拟合度较高(r2大于0.99),表明该吸附过程表现出化学吸附的特性。同时,该吸附反应受液膜扩散和颗粒内扩散的共同控制,且液膜扩散对反应速率的控制更显著。

表3 红枣汁中色素物质在HYA-602树脂上吸附的热力学参数Tab.3 Thermodynamic parameters for dark colored compounds adsorption onto HYA-602 resin
2)红枣汁中褐变物质在HYA-602树脂上的吸附并非理想的均匀表面吸附,这可能跟HYA-602树脂的表面特性、红枣汁中褐变物质结构的复杂性以及多元食品体系中或许存在的多组分竞争吸附有关。
3)热力学研究中 ΔG <0,0< ΔH <20kJ/mol,S>0。这表明HYA-602树脂对红枣汁的吸附脱色过程是吸热的、自发的,并且以物理吸附为主,该树脂可用于红枣汁的脱色。
[1] 柳永晶,张茹,吴昊轩,等.红枣的加工利用与产业发展现状[J].科技经济市场,2014(1):52-53.
[2] 周禹含,毕金峰,陈芊芊,等.中国红枣加工及产业发展现状[J]. 食品与机械,2011,29(4):214-217.
[3] 徐辉艳.红枣汁非酶褐变及其控制研究[D].西安:陕西师范大学,2009:17.
[4] 乐爱山,付兴隆,姚秉华,等.树脂吸附技术在果汁加工中的应用进展[J]. 食品科技,2010,35(4):88-92.
[5] ZHU Da-zhou,JI Bao-ping,EUM H L,et al.Evaluation of the non-enzymatic browning in thermally processed apple juice by front-face fluorescence spectroscopy[J].Food Chemistry,2009,113(1):272-279.
[6] TSENG Ru-ling,WU Feng-chin,JUANG Ruey-shin.Characteristics and applications of the Lagergren's first-order equation for adsorption kinetics[J].Journal of the Taiwan Institute of Chemical Engineers,2010,41(6):661-669.
[7] KUMAR D B,SMAIL K,MOSTEFA K,et al.Adsorption kinetics of some textile dyes onto granular activated carbon[J].Journal of Environmental Chemical Engineering,2013,1(3):496-503.
[8] WU Feng-chin,TSENG Ru-ling,JUANG Ruey-shin.Characteristics of Elovich equation used for the analysis of adsorption kineticsin dye-chitosan systems[J].Chemical Engineering Journal,2009,158:366-373.
[9] CHENG C W,PPRTER J F,MCKAY G.Sorption kinetics for the removal of copper and zinc from effluents using bone char[J].Separation and Purification Technologh,2000,12(1-2):55-64.
[10] GAO Zhen-peng,YU Zhi-fang,YUE Tian-li,et al.Adsorption isotherm,thermodynamics and kinetics studies of polyphenols separation from kiwifruit juice using adsorbent resin[J].Journal of Food Engineering,2013,116(1):195-201.
[11] MAHMOOD T,DIN S U,NAEEM A,et al.Kinetics,equilibrium and thermodynamics studies of arsenate adsorption from aqueous solutions onto iron hydroxide[J].Journal of Industrial and Engineering Chemistry,2014,20(5):3234-3242.
[12] MOHD A A,NUR A A P,OLUGBENGA S B.Kinetic,equilibrium and thermodynamic studies of synthetic dye removal using pomegranate peel activated carbon prepared by microwave-induced KOU activation[J].Water Resources and industry,2014,6:18-35.
[13] LIU Wen-xia,GUAN Bao-hong,YU Jie.Adsorption characteristics of carbon tetrachloride from aqueous solution onto polyacrylonitrile-based activated carbon fiber[J].Journal of Central South University of Technology,2010,17(5):972-978.
[14] MARIANA P T,SVETLANA D G,VELYANA G,et al.Kinetic study of brilliant green adsorption from aqueous solution onto white rice husk ash[J].Journal of Colloid and Interface Science,2013,409:112-122.
[15]傅正强.靖远凹凸棒吸附水溶液中Cd(Ⅱ)性能的研究[D].兰州:兰州交通大学,2013:16.
[16]周琦.白腐真菌培养废弃物吸附阳离子染料的研究[D].武汉:武汉理工大学,2012:92.
[17]李新杰,蒋丹丹,张跃军.粉末活性炭吸附水中ClO2的热力学与动力学研究[N].南京:南京理工大学学报,2013,37(1):156-163.
[18]高帅鹏.氢氧化镁改性沸石对水体中甲基橙、亮绿和镉离子的吸附研究[D].郑州:郑州大学,2013:13.
[19] QIU Non-gxue,GUO Shan-guang,CHANG Yu-hua.Study upon kinetic process of apple juice adsorption de-coloration by using adsorbent resin[J].Journal of Food Engineering,2007,81(1):243-249.
