同位素稀释气相色谱-质谱联用法测定白酒中16种邻苯二甲酸酯
2014-12-16杜娟许华苗宏健
杜娟,许华,苗宏健
1(北京市海淀区产品质量监督检验所,北京,100094)
2(卫生部食品安全风险评估重点实验室,国家食品安全风险评估中心,北京,100021)
邻苯二甲酸酯(phthalate esters,PAEs)又称酞酸酯,一般为无色透明黏稠液体,难溶于水,不易挥发,凝固点低,易溶于甲醇、乙醇、乙醚等有机溶剂。PAEs作为一种改性剂广泛应用于塑料工业中能起到软化作用,同时也被用作润滑剂、去污剂、颜料、化妆品、农药载体等的生产原料[1]。PAEs作为塑料生产的一种助剂,可以增强产品的可塑性和提高产品的强度,添加量约占20% ~50%。由于PAEs与聚烯烃类塑料分子之间仅仅由氢键或范德华力链接,所以很容易从塑料中扩散到外环境。研究表明,PAEs是一类环境激素,属于内分泌干扰物[2]。进入人体后可通过多种途径影响机体内分泌系统,进而影响分泌系统的正常功能,导致人体生殖功能障碍、发育行为障碍及其他与雌激素调节失衡有关的恶性肿瘤[3]。此外,PAEs还具有三致“致畸、致癌、致突变”作用[4-5]。
PAEs可以通过饮水、进食、皮肤接触和呼吸等途径进入人体[6-7]。PAEs已普遍存在于大气飘尘、工业废水、河流和土壤中。在食品、饮用水,甚至人体的体液(血清、尿液和母乳)中也检测到PAEs,酞酸酯类已经成为一种普遍污染物[8-9]。LIU等首次在调查了全国范围内地表水中6种PAEs(DEP、DMP、DBP、BBP、DEHP、DNO)的污染情况,其中 DBP和 DEHP检出率最高,检出浓度分别在ND~1.52 μg/L和ND~6.35 μg/L 的范围[10]。欧盟及美日等国均将 PAEs列为优先控制污染物[11]。
自从2012年,白酒中塑化剂事件后,引起了人们对白酒中塑化剂的重视。根据现有白酒检测结果分析,主要检出的PAEs有DIBP、DBP、DEHP以及少量的DMP和DEP。有文献报道,白酒中塑化剂主要来源于输送过程以及包装运输等环节与塑料制品的接触[12]。国标中对食品中塑化剂的分析主要是采用外标法[13]。酒类样品中含有大量的乙醇,因而使用正己烷直接提取酒类中的PAEs有一定的困难,而文献对食品样品中塑化剂的分析方法有气相色谱-质谱法[14]、液相色谱-串联质谱法[11]、气相色谱法[4]等。因为酒类样品基质较为简单,本实验拟采用正己烷直接提取,同位素稀释气相色谱-质谱联用法测定白酒中16种PAEs。实验结果表明,方法的线性范围、精密度和准确性,加标回收率等各项验证指标均满足要求,且本方法简便、快速、准确度高。
1 材料与方法
1.1 材料
白酒为随机选取市售酒类样品,于4℃冰箱中保存。
1.2 试剂与仪器
邻苯二甲酸酯标准品:邻苯二甲酸二甲酯(DMP)、邻苯二甲酸二乙酯(DEP)、邻苯二甲酸二异丁酯(DIBP)、邻苯二甲酸二丁酯(DBP)、邻苯二甲酸二(2-甲氧基)乙酯(DMEP)、邻苯二甲酸二(4-甲基-2戊基)酯(BMPP)、邻苯二甲酸二(2-乙氧基)乙酯(DEEP)、邻苯二甲酸二戊酯(DPP)、邻苯二甲酸二己酯(DHXP)、邻苯二甲酸丁基苄基酯(BBP)、邻苯二甲酸二(2-丁氧基)乙酯(DBEP)、邻苯二甲酸二环己酯(DCHP)、邻苯二甲酸二(2-乙基)己酯(DEHP)、邻苯二甲酸二正辛酯(DNOP)、邻苯二甲酸二壬酯(DNP),所有标准品的纯度均大于99%,溶剂为正己烷,Accustandard公司。邻苯二甲酸二苯酯(DPhP)(99.9%),德国Sigma公司,于冰箱中避光保存。
氘代同位素的邻苯二甲酸酯标准品:D4-邻苯二甲酸二甲酯(D4-DMP)、D4-邻苯二甲酸二乙酯(D4-DEP)、D4-邻苯二甲酸二异丁酯(D4-DIBP)、D4-邻苯二甲酸二丁酯(D4-DBP)、D4-邻苯二甲酸(2-甲氧基)乙酯(D4-DMEP)、D4-邻苯二甲酸二(4-甲基-2-戊基)酯(D4-BMPP)、D4-邻苯二甲酸二(2-乙氧基)乙酯(D4-DEEP)、D4-邻苯二甲酸二戊酯(D4-DPP)、D4-邻苯二甲酸二己酯(D4-DHXP)、D4-邻苯二甲酸丁基苄基酯(D4-BBP)、D4-邻苯二甲酸二(2-丁氧基)乙酯(D4-DBEP)、D4-邻苯二甲酸二环己酯(D4-DCHP)、D4-邻苯二甲酸二(2-乙基)己酯(D4-DEHP)、D4-邻苯二甲酸二苯酯(D4-DPhP)、D4-邻苯二甲酸二正辛酯(D4-DNOP)、D4-邻苯二甲酸二壬酯(D4-DNP)(纯度均≥95.0%),加拿大CDN Isotones公司。
甲苯、正己烷(均为色谱纯),美国Honeywell公司,水为去离子水。
气相色谱质谱联用仪(7890A-5975C,配有电子轰击源(EI)、美国Agilent公司);分析天平(BS224 s,德国Sartorius);离心机(80-2,江苏省金壇市融化仪器制造有限公司);涡旋混匀器(Vortex-Genie2,美国Scientific Industries)。
1.3 标准溶液的配制
混合标准溶液的配制:分别准确称取标准品(精确至0.1 mg),用正己烷溶解,配置成质量浓度为10 mg/L的标准储备液,置于-18℃冰箱中冷藏避光保存,待用。
混合D4内标标准溶液的配制:分别准确称取D4-邻苯二甲酸酯标准品(精确至0.1 mg)配制成质量浓度为10 mg/L的内标标准储备液,置于-18℃冰箱中冷藏避光保存,待用。
1.4 样品前处理
准确移取酒样1.0 mL,于10 mL玻璃离心管中,加 20 μL D4-标准中间液(10 μg/mL),加入提取溶剂正己烷2.0 mL,涡旋振荡1 min,在3 000 r/min下离心3 min,取上清液,待测。
1.5 仪器分析条件
1.5.1 气相色谱条件
色谱柱为HP-5ms石英毛细管柱(30 mm×0.25 mm × 0.25 μm,美国 Agilent公司),载气为氦气(纯度 >99.999%),流速为 1.0 mL/min,采用柱上不分流模式进样,进样量 1 μL,溶剂延迟7.0 min;柱升温程序:初始温度60℃,保持1 min,40℃ /min升至160℃,5℃/min升至200℃,保持5 min,8℃/min升至240℃,5℃ /min升至290℃,保持3 min。
1.5.2 质谱条件
电子轰击源(EI)电离方式;电离能量70 eV;传输线温度280℃;离子源温度230℃;四级杆温度150℃;检测方式为选择离子监测(SIM)。16种PAEs及其同位素内标的保留时间和SIM扫描离子见表1和表2。
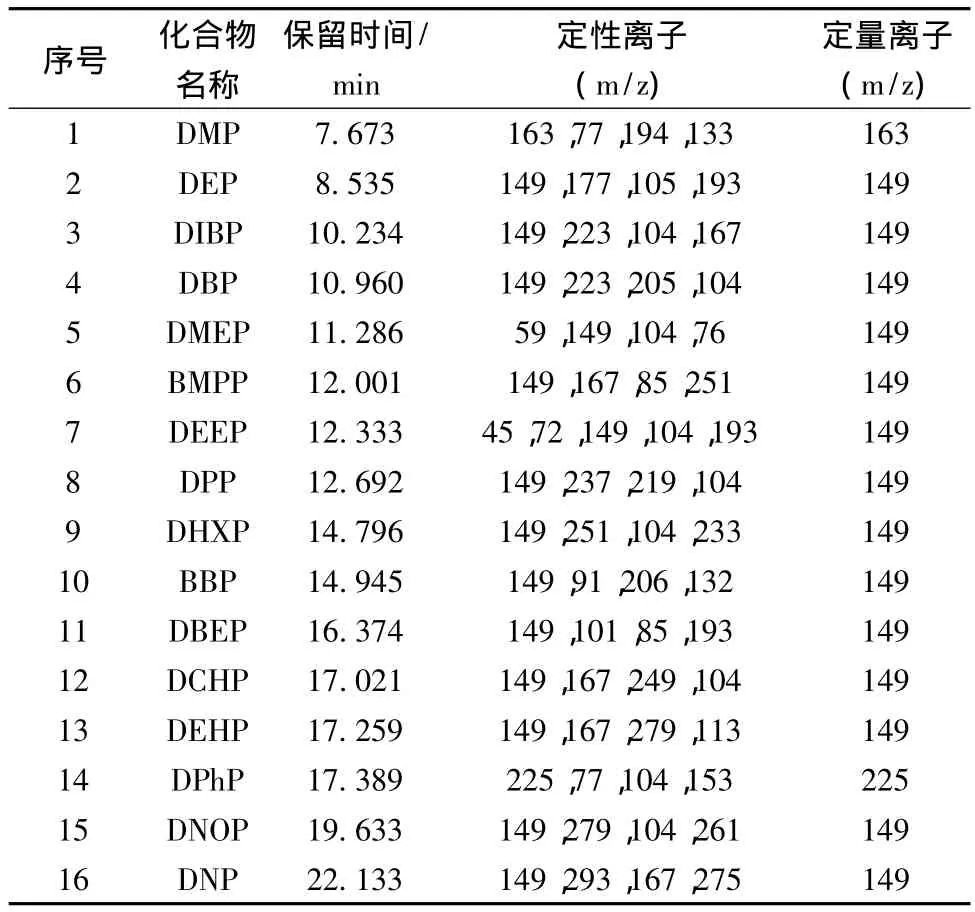
表1 16种PAEs保留时间和质谱碎片离子Table1 Retention time and target ions of 16 PAEs
2 结果与讨论
2.1 质谱方法的确定及总离子流色谱图
按照步骤1.5仪器分析条件在质谱全扫描条件下对16种PAEs标准溶液及其D4内标混合溶液进行分析,全扫描范围为50~400amu,在16种PAEs质谱图中,根据丰度及特征性强的原则对每个化合物选择1个定量离子及4~5个定性离子,选择结果见表1和表2。
按照步骤1.5对16种0.1 mg/L PAEs标准溶液(含内标0.1 mg/L)进行分析,分析结果的色谱图见图1。从图1可看出,16种目标化合物能有效分开,峰型对称,各峰间隔适宜,说明本实验的色谱检测条件适合。

表2 16种PAEs氘代同位素内标保留时间和质谱碎片离子Table 1 Retention time and target ions of 16 PAEs’internal standards

图1 16种0.1 mg/L PAEs的总离子流色谱图(内标 0.1 mg/L)Fig.1 Total ion chromatogram of 16 PAEs of 0.1 mg/L(0.1 mg/L Isotopic internal standards)
2.2 提取溶剂的选择
食品中PAEs的提取溶剂主要有正己烷,甲苯,乙腈,二氯甲烷等,通过初步试验表明,由于乙腈与水能部分互溶,不适合提取酒类样品;二氯甲烷密度较大,提取酒样时在样液的下层,不方便将二氯甲烷层取出,因此本方法选择甲苯和正己烷进行试验。
分别采用甲苯和正己烷按照步骤1.4对白酒样品中16种PAEs加标样品进行提取,加标水平为0.15 mg/L(内标0.10 mg/L),提取液均使用步骤1.5进行分析。结果表明,在扣除基质空白的基础上,白酒样品中甲苯提取回收率为88.01% ~114.95%,正己烷提取回收率87.78% ~110.75%。因此,利用同位素内标稀释法,甲苯和正己烷的提取效果没有差别。而由于甲苯的毒性较大,故本试验选用正己烷作为提取溶剂。
2.3 白酒样品去除乙醇对回收率的影响
本研究主要考察白酒中的乙醇对回收率的影响。准确量取1.0 mL白酒样品于10 mL具塞玻璃离心管中,加入16种 PAEs,加标水平为 0.25 mg/L(内标0.10 mg/L),在沸水浴中加热15 min除去样品中的乙醇,冷却至室温后加入2.0 mL正己烷,涡旋震荡1 min,在3000 r/min下离心3 min,取上清液,待测。另外准确量取1.0 mL白酒样品于10 mL具塞玻璃离心管中,加入相同水平的16种PAEs标样及内标,直接采用步骤1.4进行提取,取上清液,待测。
试验结果表明,均扣除基质空白后,沸水浴除乙醇方法的16种PAEs回收率为91.92% ~102.95%,不去除乙醇的回收率为90.42% ~102.88%。因此,去除乙醇对16种PAEs的回收率没有影响。为了简便样品的前处理方法,选用正己烷直接提取的前处理方法。
2.4 方法的线性相关性
采用步骤1.5分析方法,对16种PAEs标准系列溶液(16种D4-邻苯二甲酸酯浓度均为0.1 mg/L),浓度为 0、0.05、0.1、0.2、0.5、1.0 和 2.0 mg/L 进行分析。以标准溶液与内标浓度的比为横坐标,色谱峰面积的比为纵坐标绘制标准曲线见表4。由标准曲线可见,各目标化合物的线性相关系数r>0.999,说明在0.05~2.0 mg/L范围内有良好的线性关系。按最低添加量计算,16种PAEs的定量限均能达到0.05 mg/L。
2.5 方法的精密度和准确度
选取本底值较低的白酒样品,分别添加16种PAEs混和标准溶液进行加标回收实验。添加浓度分别为1 ×LOQ,3 ×LOQ 和5 ×LOQ 即 0.05、0.15、0.25 mg/L。按照步骤1.4和1.5对加标样品进行分析,每个加标浓度做6个平行试验,结果见表4和表5。
结果表明,白酒低水平(0.05 mg/L)的添加回收的回收率在80.6% ~117.7%之间,相对标准偏差RSD≤14.4%;中水平(0.15 mg/L)添加回收的回收率在81.7% ~108.7%之间,相对标准偏差 RSD≤10.7%;高水平添加回收的回收率在 80.6% ~108.0%之间,相对标准偏差RSD≤10.4%。以上试验结果表明,本方法的准确度和精密度均较好。

表3 16种邻苯二甲酸酯的线性方程、相关系数及定量限Table 3 Linear equations,correlation coefficient(r)and limit of quantitation(LOQ)of 16 Phthalate Esters
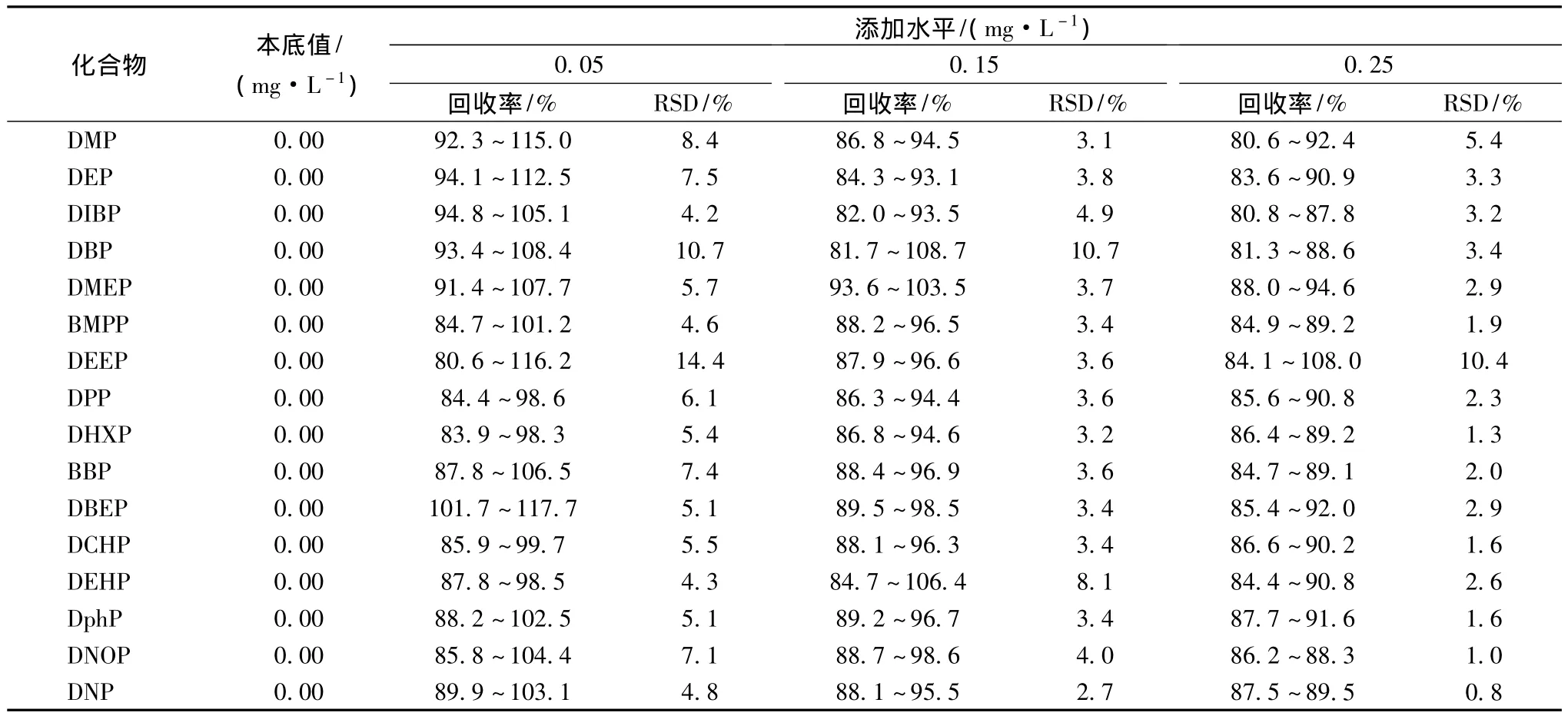
表4 白酒低、中、高三水平(0.05、0.15、0.25 mg/L)添加回收率试验及RSD结果(n=6)Table 4 Recovery and relative standard deviation(RSDs)of each pesticide at three spiked Level(0.05、0.15、0.25 mg/L)in Chinese spirits,n=6
2.6 实际样品的检测
采用所建立的方法对市售50个白酒样品(酱香型、浓香型、清香型、米香型和兼香型)中的16种PAEs进行定量检测。结果表明,白酒中DMP、DIBP、DBP和DEHP均有检出,与文献报道相符。其检出率和检出范围见表5。
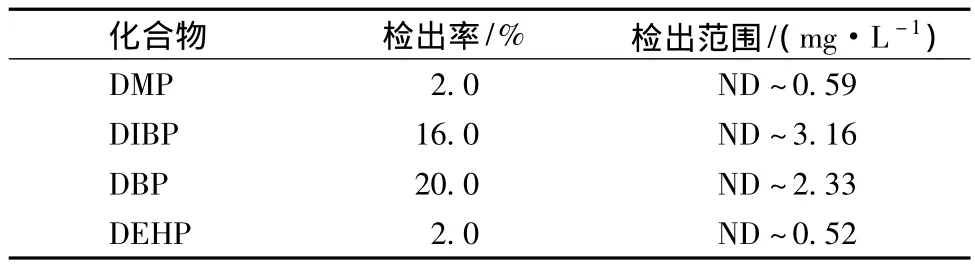
表5 50个白酒样品检测结果Table 5 Results obtained for determination of 17 phthalates in 50 Chinese spirits samples
3 结论
本文建立了白酒样品中16种PAEs的同位素内标稀释法气相色谱-质谱联用检测方法。方法分析步骤简便、快速;样品取样量较小,提取溶剂用量少,检测成本和对环境的污染均较低;前处理步骤简单,且稀释倍数小,能有效降低系统误差。采用同位素稀释内标法定量,准确性较高;本方法具有良好的线性关系、方法精密度和准确度等。本方法能很好得用在实际样品的分析中。
[1] 彭丽英,王卫国,王新,等.离子迁移谱快速筛查白酒中痕量邻苯二甲酸酯的研究[J].分析化学,2014,42(2):278-282.
[2] 熊含鸿,曾玩娴.白酒中17中邻苯二甲酸酯测定方法初探[J].酿酒,2013,40(3):93-96.
[3] 曹国洲,肖道清,朱晓艳.食品接触制品中邻苯二甲酸酯类增塑剂的风险评估[J].食品科学,2010,31(5):325-327.
[4] 徐希柱,于晓旭,洒荣波.邻苯二甲酸酯的研究进展[J].现代预防医学,2012,39(4):822-824.
[5] 柴丽月,辛志宏,蔡晶.食品中邻苯二甲酸酯类增塑剂含量的测定[J].食品科学,2008,29(7):362-365.
[6] 王琦,贾润礼.聚氯乙烯增塑剂的研究[J].绝缘材料,2007,40(5):38-41.
[7] http://www.sciencedaily.com/releases/2012/05/120523102142.htm.
[8] Suzuki Y,Niwa M,Yoshinaga J,et al.Prenatal exposure to phthalate esters and PAHs and birth outcomes[J].Environment International,2010,36(7):699-704.
[9] Lee M R,Lai F Y,Dou J P,et al.Determination of trace leaching phthalate esters in water and urine from plastic containers by solid-phase microextraction and gas chromatography-mass spectrometry[J].Analytical Letters,2011,44(4):676-686.
[10] LIU Xiaowei,SHI Jianghong,BO Ting,et al.Occurrence of phthalic acid esters in source waters:a nationwide survey in China during the period of 2009-2012[J].Environmental pollution,2014.184:262-270.
[11] 刘红河,黄晓群,王晖.高效液相色谱-串联质谱法测定食品中邻苯二甲酸酯[J].现代预防医学,2008,35(1):119-121.
[12] 陈勇,李开雁.气质联用(GC-MS)分析蒸馏白酒中塑化剂[J].酿酒,2013,40(5):76-79.
[13] GB 21911-2008.食品中邻苯二甲酸酶的测定[S].
[14] 王鹏功,高明星,程刚.气相色谱-质谱法对食用油中17种邻苯二甲酸酯的测定[J].食品科学,2012,18(33):246-249.
