多奈哌齐治疗痴呆的系统评价
2014-11-17杨南竹贠相华周玉颖吴玉秋王宏艳
杨南竹, 贠相华, 周玉颖, 吴玉秋, 王宏艳
痴呆是由多种中枢神经系统变性或缺血过程所引起的、影响患者社会或职业能力的认知功能缺陷综合征。痴呆影响患者的认知、行为和功能,并造成看护负担,迄今为止尚无根治方法,目前的药物干预只能延缓其进展和改善症状。多奈哌齐(donepezil)是一种胆碱酯酶抑制剂[1],它可有效选择性抑制中枢神经系统中乙酰胆碱的降解,增加神经细胞突触间隙乙酰胆碱的浓度,改善痴呆患者的记忆和智能状态。过去常用于AD的治疗。
近年来逐渐用于治疗VD、PD、LBD等其他病因造成的认知障碍。通过对文献报道的多奈哌齐治疗痴呆的对照研究进行Meta分析,进一步评价多奈哌齐治疗痴呆的临床疗效。
1 资料与方法
1.1 资料 检索策略检索的数据库 Medline、EMBASE、Ovid、CNKI及万方数据库。检索词:多奈派齐、痴呆、Donepezil、Dementia等。均选取建库至2013年9月所收录文献。排除综述、信件、评论等类型的文章。
1.1.1 纳入标准 (1)研究设计为随机对照实验(RCT);(2)所有受试者均为痴呆患者,包括PD、AD、LBD、VD 等,诊断标准符合 NINDS-AIREN[2]或 DSM-IV[3]诊断标准;(3)干预措施:多奈哌齐不同剂量口服,治疗周期为12~24 w,具体方法(见表1);(4)各试验组间比较在人群性别、年龄、评分基线水平均无显著差异;(5)研究对象在研究前未应用其他抗痴呆药物治疗;(6)为避免剔除脱落数据所造成的偏倚,统计采用末次观测结转法(LOCF)等填补缺失值。
1.1.2 排除标准 (1)原文非中文或英文的文献;(2)重复报告;(3)动物实验;(4)多奈哌齐与其他胆碱酯酶抑制剂配对的随机对照试验、未设置安慰剂对照组的试验;(5)摘要或会议汇编;(6)Jadad量表评分<5分者。
1.2 评定方法 从整体功能、认知功能、精神状态、行为4方面选取不同量表评价疗效。整体功能评价包括CIBIC+、CDR-SB;认知功能评价包括 ADAS-cog、MMSE;精神状态评价以NPI为评定标准;行为评价包括ADL和ADFACS。比较不同剂量多奈哌齐或安慰剂治疗前后不同量表差值变化。初始剂量5 mg,28~30 d改为10 mg,维持12~24 w的患者归入10 mg组。
1.3 纳入文献的质量评价 纳入研究的方法学质量评价采用Jadad质量评分法,包括:(1)随机方法是否正确;(2)是否做到分配隐藏,方法是否正确;(3)是否采用盲法;(4)有无失访或退出,如有失访或退出时,原因是否描述清楚,是否采用意向性治疗分析方法(ITT)。
1.4 纳入文献的资料提取 从文献中提取下列信息:受试者例数、干预情况(干预措施、剂量、疗程)、结局测量指标、不良事件发生率等。2名评价员对纳入试验按照上述标准独立进行质量评价和资料提取,然后交叉核对,对有分歧而难以确定其是否纳入的试验通过讨论或由第3位研究者决定其是否纳入。
1.5 统计学方法 统计分析软件采用Cochrane协作网提供的Rev Man 5.2软件进行Meta分析。计数资料采用RR值为疗效分析统计量,计量资料采用加权均数差或标准化均数差为疗效分析统计量,各效应量均以95%CI表示。各纳入研究结果间的异质性采用χ2检验。当各研究间有统计学异质(P>0.1,I2<50%)时,采用固定效应模型进行Meta分析;如各研究间存在统计学异质性(P<0.1,I2>50%),分析其异质性来源,对可能导致异质性的因素进行亚组分析。若亚组之间存在统计学异质性而无临床异质性时,采用随机效应模型分析。异质性源于低质量研究,进行敏感性分析。如两组间异质性过大或无法找寻数据来源时,采用描述性分析。
2 结果
2.1 文献入选情况 共检索到198篇文献。初步阅读文章内容,入选21篇。其中4篇选用量表与本次分析不符,2篇未设计安慰剂对照组,1篇无具体数据,1篇为另外3篇的总结。因此本研究共纳入13篇RCT文献,患者共6146人,其中 AD2118人,VD3373人,PD550人,LBD105人。Jadad评分均为5分(见表1)。
2.2 多奈哌齐治疗前后评分差值的影响 不同剂量多奈哌齐对整体功能(CIBIC+,CDR-SB)认知功能(ADAS-cog、MMSE)的疗效优于安慰剂组(P<0.00001):不同剂量多奈哌齐对精神状态(NPI)的影响与安慰剂无差异(P=0.12)。评价多奈哌齐对行为的影响有不同结果:应用ADL评分显示多奈哌齐与安慰剂疗效无差异(P=0.55);而应用ADFACS评分显示多奈哌齐更有效(P=0.0009)(见表2)。
2.3 不同剂量多奈哌齐治疗前后评分差值的影响Meta分析结果显示,5 mg与10 mg多奈哌齐在改善整体功能、认知功能、精神状态、行为等几方面评分差异均无统计学意义(见表3)。
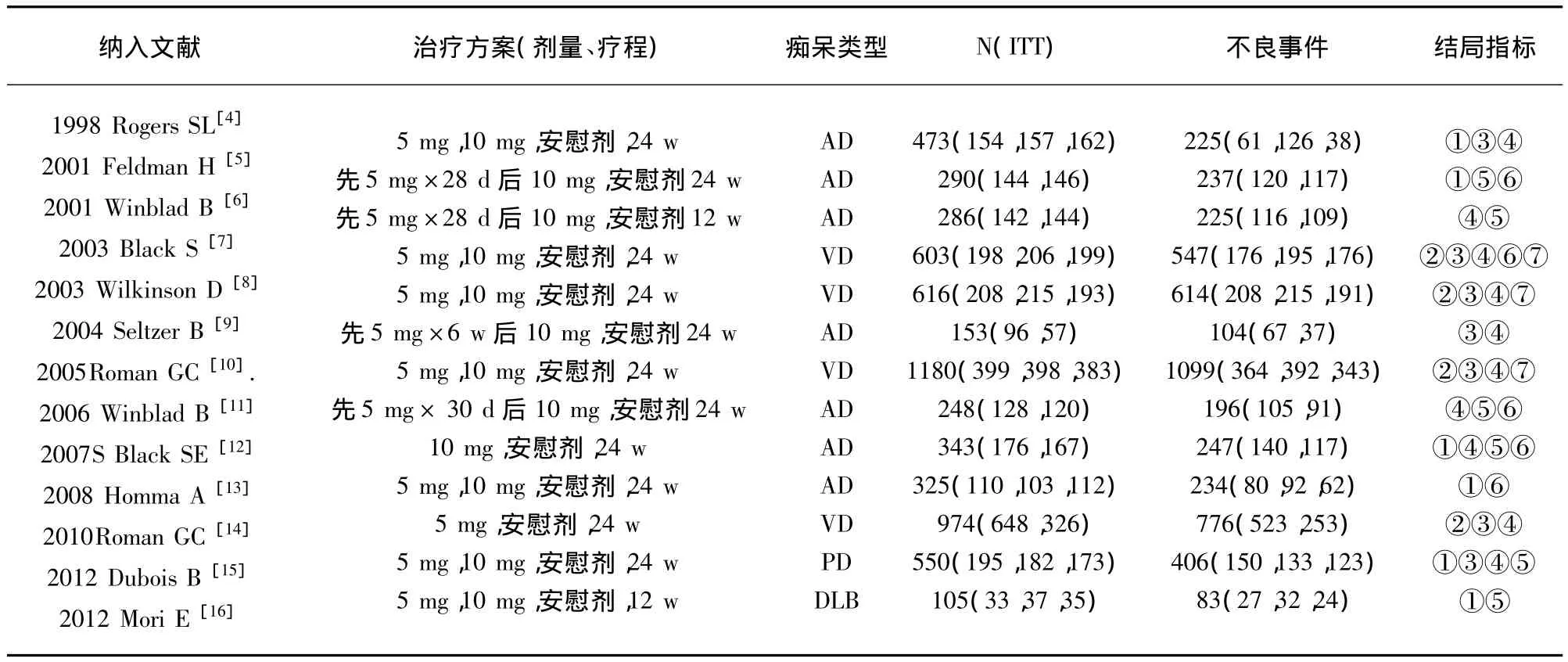
表1 纳入文献的基本信息

表2 多奈哌齐治疗前后评分差值的Meta分析

表3 不同剂量多奈哌齐治疗前后评分差值的Meta分析
3 讨论
本研究纳入了有关比较不同剂量多奈哌齐和安慰剂治疗痴呆的13篇文献进行系统评价。Meta分析结果显示:不同剂量多奈哌齐的疗效整体优于安慰剂组。这与以往研究结果一致[17]。对于不同剂量多奈哌齐的疗效,5 mg与10 mg在改善整体功能、认知功能、精神状态、行为等几方面评分差异均无统计学意义,提示多奈哌齐疗效并不存在剂量依赖性。但目前有研究[18]观察高剂量(23 mg/d)与标准剂量(10 mg/d),多奈哌齐中度至重度AD时发现,虽然高剂量多奈哌齐对整体功能评价无显著改善,但可显著改善认知状态,因此对不同剂量多奈哌齐疗效的评估需要更多的临床观察。
出现偏倚的可能:(1)对痴呆患者的选择上虽然都是按照一定的标准,但不同地域、人种、年龄、性别患者的标准存在一定差异,可能导致异质性,同时在量表的选择、疗效的判定上存在一定差异。一些研究将ADAS-cog变化≥4分作为轻-中度痴呆的临床的重要改善标准,而对于MMSE≥3分变化亦认为具有临床重要意义,CIBIC+量表评分的任何变化均视为具有临床改善,导致一定的临床异质性的存在。以上因素难以量化。(2)本研究比较治疗前后疗效,均选择评分变化差值比较,但入选患者基线MMSE评分差异较大,包括部分中重度痴呆患者,亦可能对评价结果造成偏倚。(3)此外对于中重度患者,应用药物治疗后疗效不显著、出现其他合并症加重病情或出现不良反应可能性较大,出现失访、退出、或更换其他药物治疗的可能性亦较大,均可能对结果造成偏倚。(4)入选痴呆患者中AD、VD患者所占比重较大,各占34.46%、54.44%,有关其他类型痴呆的临床试验相对较少,还需进一步完善资料。有研究[19]通过对22个自身对照或安慰剂对照的独立临床试验(国外7篇,国内15篇)进行的Meta分析,评估多奈哌齐治疗VD的有效性,发现国外试验设计,随机方法、盲法设计更加恰当严谨,失访、退出原因及不良反应均有详细报道,Jadad评分均为5分;国内试验普遍质量偏低,Jadad 1~3分。国外试验设计更为合理,疗程更长;纳入研究的人数更多;结局指标较多,且多报道治疗前后的评分,变化差值对疗效评价更加全面。本次Meta通过筛选未纳入国内试验,建议国内的多奈哌齐临床试验研究借鉴国外研究。在今后的临床研究应注意设计更加严谨的试验方法,以减少各种偏倚;同时应开展大样本、多中心、具有统一结局指标的随机对照试验。
[1]Qaseem A,Snow V,Cross JT JR,et al.Current pharmacologic treatment of dementia:a clinical practice guideline from the American college of physicians and the American academy of family physicians[J].Ann Intern Med,2008,148(5):370-378.
[2]Roman GC,Tatemichi TK,Erkinjuntti T,et al.Vascular dementia:diagnostic criteria for research studies:report of the NINDS-AIREN International Workshop[J].Neurology,1993,43:250-260.
[3]American Psychiatric Association.Diagnostic and statistical manual of mental disorders,4th ed.Washington,DC:American Psychiatric Association,1994.
[4]Rogers SL,Farlow MR,Doody RS.et al.A 24-week,double-blind,placebo-controlled trial of donepezil in patients with Alzheimer’s disease.Donepezil Study Group[J].Neurology,1998,50(1):136-145.
[5]Feldman H,Gauthier S,Hecker J.et al.A 24-week,randomized,double-blind study of donepezil in moderate to severe Alzheimer’s disease[J].Neurology,2001,57(4):613-620.
[6]Winblad B,Engedal K,Soininen H,et al.A 1-year,randomized,placebo-controlled study of donepezil in patients with mild to moderate AD[J].Neurology,2001,57(3):489-495.
[7]Black S,Roman GC,Geldmacher DS,et al.Efficacy and tolerability of donepezil in vascular dementia:positive results of a 24-week,multicenter,international,randomized,placebo-controlled clinical trial[J].Stroke,2003,34(10):2323-2330.
[8]Wilkinson D,Doody R,Helme R,et al.Donepezil in vascular dementia:a randomized,placebo-controlled study[J].Neurology,2003,61(4):479-86.
[9]Seltzer B,Zolnouni P,Nunez M,et al.Efficacy of donepezil in earlystage Alzheimer disease:a randomized placebo-controlled trial[J].Arch Neurol,2004,61(12):1852-1856.
[10]Roman GC,Wilkinson DG,Doody RS,et al.Donepezil in vascular dementia:combined analysis of two large-scale clinical trials[J].Dement Geriatr Cogn Disord,2005,20(6):338-344.
[11]Winblad B,Kilander L,Eriksson S,et al.Donepezil in patients with severe Alzheimer’s disease:double-blind,parallel-group,placebocontrolled study[J].Lancet,2006,367(9516):1057-1065.
[12]Black SE,Doody R,Li H,et al.Donepezil preserves cognition and global function in patients with severe Alzheimer disease[J].Neurology,2007,69(5):459-469.
[13]Homma A,Imai Y,Tago H,et al.Donepezil treatment of patients with severe Alzheimer’s disease in a Japanese population:results from a 24-week,double-blind,placebo-controlled,randomized trial[J].Dement Geriatr Cogn Disord,2008,25(5):399-407.
[14]Romna GC,Salloway S,Black SE,et al.Randomized,placebo-controlled,clinical trial of donepezil in vascular dementia:differential effects by hippocampal size[J].Stroke,2010,41(6):1213-1221.
[15]Dubois B,Tolosa E,Katzenschlager R,et al.Donepezil in Parkinson’s disease dementia:a randomized,double-blind efficacy and safety study[J].Mov Disord,2012,27(10):1230-1238.
[16]Mori E,Ikeda M,Kosaka K,et al.Donepezil for dementia with Lewy bodies:a randomized,placebo-controlled trial[J].Ann Neurol,2012,72(1):41-52.
[17]Krista L,Lanctt NH.Efficacy and safety of cholinesterase inhibitors in Alzheimer’s disease:a meta-analysis[J].CMAJ,2003,169(6):557-564.
[18]Martin R,Farlow MD.Effectiveness and tolerability of high-dose(23 mg/d)versus standard-dose(10 mg/d)donepezil in moderate to severe Alzheimer’s disease:A 24-Week,randomized,souble-blind atudy[J].Clin Ther,2010,32(7):1234-1251.
[19]马 卓,陈 月,冯婉玉,等.多奈哌齐治疗血管性痴呆临床疗效的系统评价[J].中国新药杂志,2013,22(5):569-576.
[20]Cousineau N,McDowell I,Hotz S,et al.Measuring chronic patients'feelings of beinga burden to their caregivers:development and preliminary validation of a scale[J].Med Care,2003,41(1):110-118.
[21]Kowal J,Wilson KG,McWilliams LA,et al.Self-perceived burden in chronic pain:relevance,prevalence,and predictors[J].Pain,2012,153(8):1735-1741.
[22]Van Orden KA,Lynam ME,Hollar D,et al.Perceived burdensomeness as an indicator of suicidal symptoms[J].Cognitive Therapy and Research,2006,30(4):457-467.
[23]Carota A,Bogousslavsky J.Mood disorders after stroke[J].Front Neurol Neurosci,2012,30:70-74.
[24]George MG,Tong X,Kuklina EV,et al.Trends in stroke hospitalizations and associated risk factors among children and young adults,1995-2008[J].Ann Neurol,2011,70(5):713-721.
[25]肖水源.社会支持评定量表的理论基础与研究应用[J].临床精神医学杂志,1999,4(2):98-100.
[26]McPherson CJ,Wilson KG,Chyurlia L,et al.The balance of give and take in care giver-partner relationships:An examination of selfperceived burden,relationship equity,and quality of life from the perspective of care recipients following stroke[J].Rehabil Psychol.2010,55(2):194-203.
[27]Campbell P,Wynne-Jones G,Dunn KM.The influence of informal social support on risk and prognosis in spinal pain:a systematic review[J].Eur J Pain,2011,15(5):1-14.
[28]刘 燕,金 奕,赵 岳,等.青年脑卒中患者健康行为及影响因素分析[J].中华护理杂志,2012,47(1):58-61.
[29]Kruithof WJ,van Mierlo ML,Visser-Meily JM,et al.Associations between social support and stroke survivors health-related quality of life-a systematic review[J].Patient Educ Couns,2013,93(2):169-176.
[30]Levada OA,Slivko EI.Post-stroke depression[J].Zh Nevrol Psikhiatr Im SSKorsakova,2006,16:73-79.
