复方车前子滴丸制备工艺及其含量测定
2014-11-08张雪峰薛桂蓬
张雪峰,欧 燕,薛桂蓬
(1.新疆生产建设兵团总医院,新疆 乌鲁木齐 830002;2.新疆药物研究所,新疆 乌鲁木齐 830004)
复方车前子滴丸由车前子、甘草、熟地3味药组方,具有清热化瘀、补肾通淋,主治慢性前列腺炎。方中君药车前子[1]为车前科植物车前草 Plantago asiatica L.或平车前草 Plantago depressa Willd.的干燥成熟种子,具有清热利尿、渗湿通淋、明目祛痰的功效。车前子中含大量黏液质(多糖类化合物)及车前子酸、胆碱、腺嘌呤、琥珀酸、蛋白质、微量元素、桃叶珊瑚苷等黄酮类成分。现代医学研究表明,黄酮类化合物具有明显的抗溃疡、解痉、抗炎、抗菌、抗氧化、抗衰老、增强机体免疫力、软化血管、降血糖、调血脂等生理活性。滴丸剂具有生产周期短、溶出快、生物利用度高等特点。本试验采用单因素及正交试验设计对其成型工艺进行研究[2],并对滴丸中毛蕊花糖苷的含量进行测定。
1 仪器与试药
DWJ-2000S型自动滴丸机(烟台百药泰中药科技发展有限公司);ZB-1C型智能崩解仪(天津大学精密仪器厂);LibrorAEG-200型电子天平电子恒温水浴锅(北京永光明医疗器械厂);LC-20A型高效液相色谱仪(日本岛津);SPD-20A型紫外检测器;Shimadzu LC-Solution数据工作站;Water Purifier超纯水机(四川沃特尔水处理设备有限公司);KQ-100DE型数控超声波清洗器(昆山市超声仪有限公司)。复方车前子滴丸提取物(新疆生产建设兵团总医院,批号为20100609);毛蕊花糖苷对照品(中国药品生物制品检定所,批号为111530-200303);聚乙二醇4000(PEG 4000)、聚乙二醇6000(PEG 6000)(北京海淀会友精细化工有限公司,批号分别为090416,090222);液体石蜡(北京海淀会友精细化工有限公司,批号为091124);二甲基硅油100(天津大茂化学试剂厂)。
2 方法与结果
2.1 滴丸制备
称取药粉与基质(PEG 4000或PEG 6000)适量,混匀,置烧杯中水浴加热,并不断搅拌使熔融,然后将药液加入滴灌,保温10min。待冷凝温度、药液温度等达到要求时,进行滴制。用滤纸吸去丸表面的冷却液,即得复方车前子滴丸。
2.2 制备工艺优选
基质种类及药物与基质配比的考察[3]:采用不同的基质与药粉配比(2.5∶1),制备滴丸,以滴制情况、硬度、圆整度、溶散时限为评价指标,考察基质种类,结果见表1。可见,采用PEG 4000物料的流动性要比用PEG 6000的流动性要好,但由于中药药粉特殊性质结合试验结果最终选择PEG 6000为基质。在此基础上进一步对药物与基质的配比进行筛选。结果见表2,可见,当药液与基质配比为1∶25和1∶3.0时,均较易滴制,从减少服用量和节约成本的角度考虑,选用药物与基质配比为1∶2.5。

表1 不同基质与药物配比对滴丸成型的影响

表2 药物与基质不同配比对滴丸成型的影响
正交试验优选料液温度、滴速和滴距[4-5]:通过上述试验确定了药粉∶PEG 6000为1∶2.5,在此基础上,对影响滴丸成型的料液温度(因素A)、滴速(因素B)和滴距(因素C)3个因素安排正交试验,每个因素选取3个水平,以丸重变异系数[参照2010年版《中国药典(一部)》附录ⅠK滴丸剂项下质量差异检查法检查]和外观质量(大小均匀、色泽一致、圆整,丸与丸之间不粘连,常温下不软化,满分为10分)为评价指标。优选最佳制备条件。按照表3所列的因素水平进行正交试验安排,选择 L9(34)正交试验表,结果见表4。方差分析结果见表5和表6。由直观分析可见,影响丸重变异系数效果的因素顺序为A>B>C,以药液温度影响最大,由于丸重变异系数越小越好,故结果为A2B2C1。经方差分析可见,药液温度对丸重变异系数有显著性影响,滴速和滴距无显著性差异,故选择A2B3C1;影响丸外观质量的因素顺序为A>C>B,以药液温度影响最大,结果为A2B2C3。经方差分析可见,药液温度对外观质量有显著性影响,滴速和滴距无显著性差异,故选择A2B3C1。确定最优滴丸成型工艺为药粉与PEG 6000配比为1∶2.5,药液温度为90℃,滴速为每分钟55滴,滴距为6 cm。

表3 因素水平表
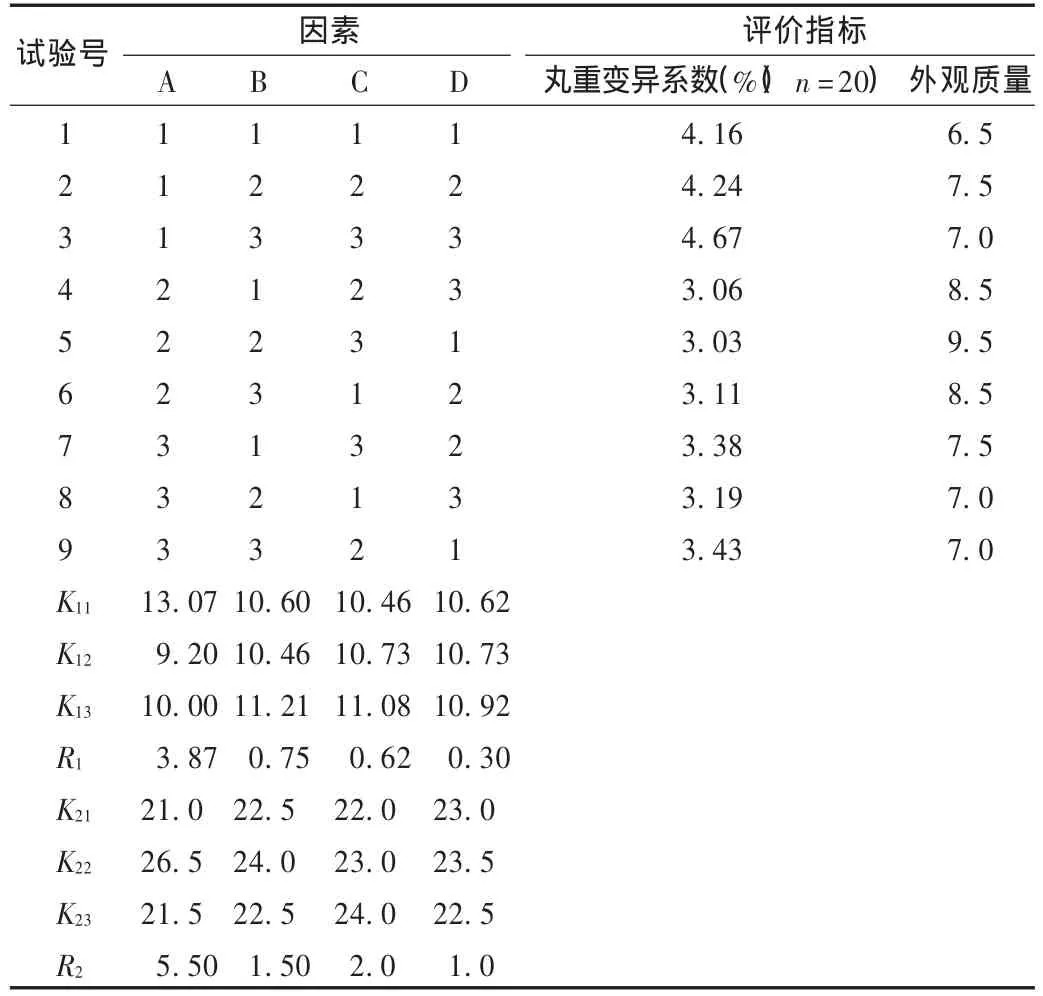
表4 正交试验方案与结果 L9(34)
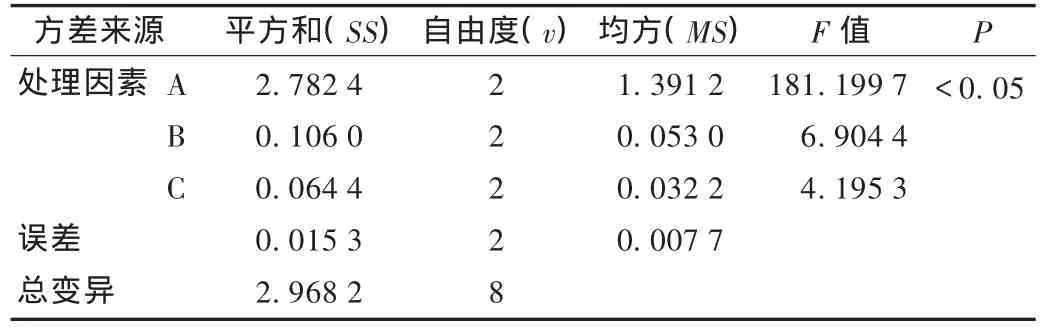
表5 丸重变异系数方差分析结果
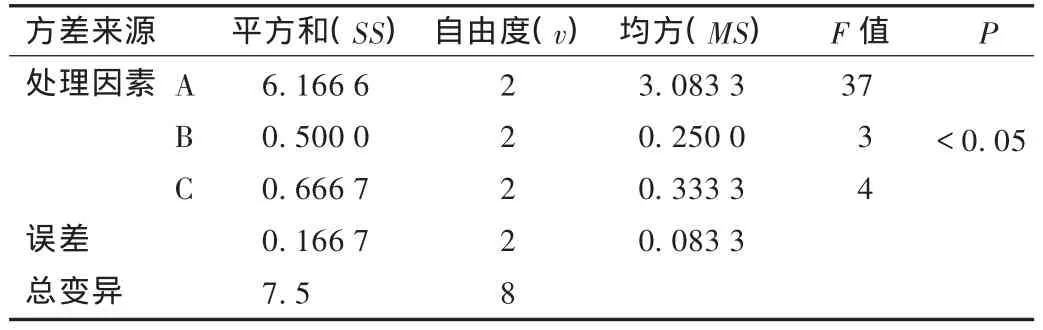
表6 外观质量方差分析结果
2.3 最佳工艺验证试验
按照优选出的工艺条件,进行验证试验,所得滴丸圆整度好,溶散时限和丸重差异符合2010年版《中国药典(一部)》附录ⅠK滴丸剂项下规定,验证试验结果见表7。
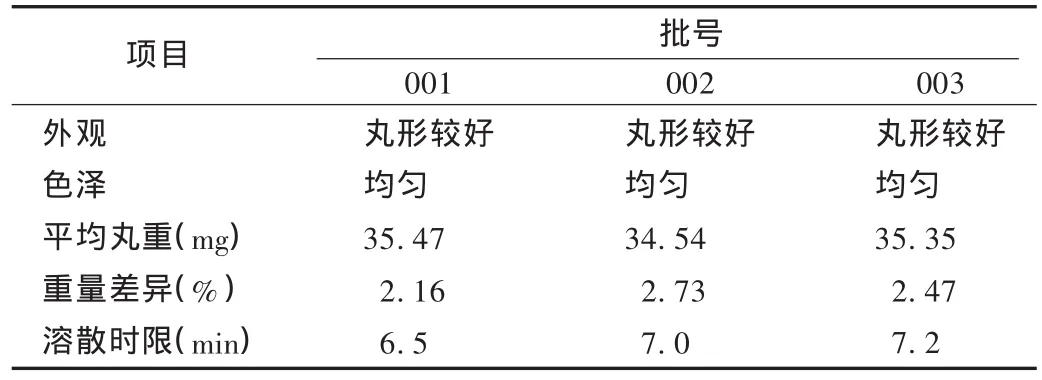
表7 验证试验结果
2.4滴丸含量测定[6-7]
2.4.1 色谱条件与系统适用性试验
色谱柱:Agilent C18柱(250 mm ×4.6 mm,5 μm);流动相:乙腈-0.2%醋酸溶液(25∶75)圆1位;检测波长:334nm;柱温:35℃;流速:1.0 μg/mL;进样量:10 μL。取对照品溶液、供试品溶液、阴性对照品溶液按拟订色谱条件进样,色谱图见图1。
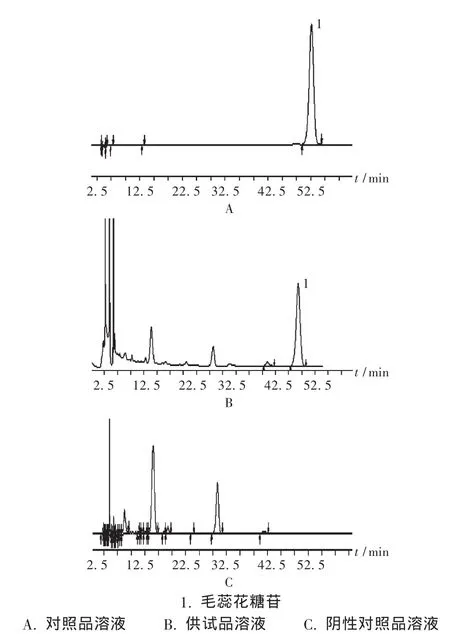
图1 高效液相色谱图
2.4.2 溶液制备
取毛蕊花糖苷对照品适量,精密称定,加60%甲醇制成每1 mL含348 μg的溶液,即得对照品贮备液。再精密量取4 mL贮备液,置10 mL容量瓶中,加60%甲醇至刻度,摇匀,制成每1 mL含139.2 μg的溶液,即得对照品溶液。取本品20丸,精密称定,研细,取0.3 g置25 mL容量瓶中,加无水乙醇稀释至刻度,超声处理30 min,滤过,滤液作为供试品溶液。取缺车前子的滴丸样品20丸,精密称定,研细,取0.3 g置25 mL容量瓶中,加无水乙醇稀释至刻度,超声处理30 min,滤过,滤液作为阴性对照品溶液。
2.4.3 方法学考察
标准曲线制备[8]:精密吸取上述毛蕊花糖苷对照品液(348 μg/mL)0.5,1.0,1.5,2.0,4.0 mL 置 10 mL 容量瓶中,加甲醇稀释至刻度,摇匀,制成含毛蕊花糖苷为 17.4,34.8,52.2,69.6,139.2 μg/mL 的对照品溶液。分别精密吸取 10 μL,注入高效液相色谱仪,记录峰面积,以质量浓度(C,μg/mL)为横坐标、峰面积(A)为纵坐标进行线性回归,得标准曲线方程 A=11 355C+10 120,r=0.999 5(n=5)。结果表明,毛蕊花糖苷质量浓度在17.4~139.2 μg/mL范围内与峰面积呈良好线性关系。
稳定性试验:依法制备供试品溶液,分别于 0,2,4,6,8,10 h时进样,测定峰面积,计算毛蕊花糖苷的含量。结果的 RSD为1.89%(n=6),表明供试品溶液在10 h内稳定。
精密度试验:取上述毛蕊花糖苷对照品溶液(348 μg/mL)1.0 mL置10 mL容量瓶中,加甲醇稀释至刻度,摇匀,重复进样6次。结果的 RSD为0.46%,表明仪器精密度良好。
重复性试验:取同一批样品6份,依法制备供试品溶液并测定峰面积,计算毛蕊花糖苷的含量。结果的 RSD为1.36%,表明方法重复性良好。
加样回收试验:精密称取已知毛蕊花糖苷含量的样品粉末10份,第1份为空白,其余分3组,各3份,精密加入一定量毛蕊花糖苷对照品,制成高、中、低3个质量浓度,依法制备供试品溶液,测定峰面积,计算回收率。结果毛蕊花糖苷的平均加样回收率为 98.78% ,RSD 为 1.25%(n=9)。
3 讨论
PEG4000,PEG6000是制备固体分散体的常用基质,由于其相对分子质量的不同而使其与药物混合溶融后状态不同,黏度不同,以致滴制过程中难易程度不同。本研究采用可量化指标的丸重变异系数,以及对包括滴制圆整度、硬度、拖尾在内的外观质量来评定工艺的优劣,使用PEG 6000可使滴丸硬度增加,并使黏性适中,容易滴制。冷却液也是影响滴丸制备的重要因素之一,不同冷却液黏度不同,使丸下降速度不同,黏度小的丸下降快就可能产生粘连,黏度太大,丸下降太慢则滴制周期长,效率低;并且冷却液的温度是影响滴丸丸型是否圆整的重要因素,温度太低丸未来得及收缩即凝固定型使丸呈扁型,温度太高丸未凝固完全会产生丸与丸粘连。
车前子在2010年版《中国药典(一部)》中含量测定项下,采用HPLC法(梯度洗脱)测定毛蕊花糖苷和京尼平苷的含量[9],由于未买到京尼平苷对照品,因此本试验只对车前子中毛蕊花糖苷的含量进行测定。预试验中,曾先后比较了甲醇-0.5%醋酸溶液(40 ∶60)、甲醇 -0.3% 醋酸溶液(35 ∶65)、甲醇 -0.2%醋酸溶液(35∶65,25∶75)、甲醇-0.1%醋酸溶液(15∶85)等。结果在甲醇 -0.2%醋酸溶液(25∶75)条件下测定毛蕊花糖苷,取得了较好效果。
本试验筛选出的复方车前子滴丸工艺简便、可行,评价指标可靠、合理,符合2010年版《中国药典(一部)》对滴丸制剂的要求。
[1]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2010:63.
[2]夏忠玉,孙国兵.小儿咳喘灵滴丸工艺研究[J].中国药业,2012,21(24):69-70.
[3]张望刚,王 俏,陈国神,等.盐酸丙卡特罗舌下滴丸的研制及其稳定性考察[J].中国现代应用药学,2011,28(6)∶542 -545.
[4]谭桂莲,武 佳.槐米滴丸制备工艺及其含量测定[J].中国实验方剂志,2011,17(5)∶49 - 51.
[5]薛桂蓬,顾政一,张 洁,等.金蒿抗流感滴丸制备工艺及其含量测定[J].中国药业,2012,21(13)∶39 -41.
[6]万 茵,谢明勇,何彦林.反相高效液相色谱法同时测定车前子中的毛蕊花苷和异毛蕊花苷[J].天然产物研究与开发,2008(20)∶474-476.
[7]燕宪海,张爱丽,田友清.葛花滴丸的制备工艺及葛根素的含量测定[J].安徽农业科学,2011,39(36)∶22 319 -22 321.
[8]习志刚,董海松,任冬冬,等.大豆异黄酮苷元滴丸的制备和含量测定[J].药学与临床研究,2009,17(3)∶168 - 171.
[9]王 颖 .宁心滴丸制备工艺研究[J].中国药业,2012,21(18)∶52-54.
