磁珠法试剂与Trizol试剂检测肠道病毒核酸的效果观察
2014-09-28王述莲邓中平呼建民钟礼立
王述莲,邓中平,呼建民,钟礼立,黄 河
肠道病毒属于RNA病毒,是引起手足口病的主要病原体。该病毒感染性强、致病率高[1-3]。快速检测肠道病毒是治疗手足口病的重要基础。目前,国内外常规检测肠道病毒的核酸提取方法是Trizol法,该方法需多次离心、洗涤、吸弃废液等开放操作,过程中易造成污染和核酸丢失,也易导致检测结果重复性和稳定性不理想;而磁珠法是近年来研发的一种较为先进的肠道病毒核酸提取方法,该方法为常温裂解释放核酸,无需使用水浴或干浴设备,不必反复高速离心,操作方便,且节约成本。本文将肠道病毒核酸的磁珠法提取试剂与常规Trizol法提取试剂进行对比观察,即以“新型的”磁珠法肠道病毒核酸提取试剂为观察试剂,以“常规的”Trizol法提取试剂为对照试剂,旨在探讨磁珠法试剂的临床检测效果。
1 资料与方法
1.1 一般资料 收集临床诊断为手足口病患者的咽拭子标本412例,其中男240例,女172例;年龄1~12岁,平均4.5岁。所有病例确诊均严格按照国家卫生部颁布的《手足口病诊疗指南》(2010年版)执行[4]。以“新型的”磁珠法肠道病毒核酸提取试剂为观察试剂,以“常规的”Trizol法提取试剂为对照试剂。
1.2 主要试剂和仪器 “新型”肠道病毒核酸检测试剂购自湖南圣湘生物科技有限公司,采用磁珠法提取肠道病毒核酸,最低检测限为400 copies/mL;对照试剂购自美国Invitrogen公司,采用Trizol法提取肠道病毒核酸,采用已上市的检测试剂盒进行检测。按照试剂盒说明书,提取试剂和反应试剂均在检测过程中配套使用。磁珠法和Trizol法提取的肠道病毒核酸,均采用美国Stratagene公司的Mx3000P实时荧光定量PCR仪进行检测。
1.3 方法
1.3.1 磁珠法操作步骤 ①在1.5 mL灭菌离心管中依次加入600μL RNA提取“溶液1”、200μL待测样本、100 μL RNA提取“溶液2”,震荡混匀10 s后,室温静置10 min;②瞬时离心后,将离心管置于分离器上,3 min后吸弃废液;③向离心管中加入600 μL RNA提取“溶液3”,加入200 μL RNA提取“溶液4”,震荡混匀5 s,瞬时离心后将离心管再次置于分离器上,3 min后,将废液全部吸弃;④向离心管中加入30 μL RNA洗脱液,将离心管壁上磁珠洗脱到管底,室温静置10 min后,将离心管再次置于分离器上,静置3 min,然后将RNA洗脱液移入新的1.5 mL灭菌离心管中。
1.3.2 Trizol法操作步骤 ①在1.5 mL的灭菌离心管中依次加入样本 500 μL、Trizol试剂 500 μL,充分混匀,室温放置10 min;②加入200 μL氯仿,拧紧盖,用力震荡,直至溶液充分乳化、成乳白状、无分相现象,室温静置10 min;③于4℃、13 000 r/min离心15 min,吸取上层液相移入另一离心管;④加入等体积异丙醇,轻轻颠倒离心管,充分混匀液体,室温放置10 min;⑤于4℃、13 000 r/min离心15 min,弃上清;⑥向离心管内加入75%乙醇1 mL,震荡混匀,于4℃、13000 r/min离心10 min,弃上清,在超净台中干燥5 min;⑦向离心管内加入试剂盒中的DEPC水 50 μL,充分混匀。
1.3.3 临床样本检测 分别采用磁珠法试剂和Trizol法试剂,对412例咽拭子标本进行临床样本核酸提取。①磁珠法提取样本,是经样本裂解、核酸吸附、杂质洗脱后获得核酸。②Trizol法提取样本,是经样本裂解,氯仿去杂质,离心获得液相后,采用异丙醇析出核酸,乙醇漂洗,室温干燥,加水复溶后获得核酸。本组412例标本均按照上述2种方法的操作步骤,分别提取核酸。尔后,再分别采用各自的检测试剂,采用美国Stratagene公司的Mx3000P实时荧光定量PCR仪进行核酸检测。
1.4 统计学分析 采用SPSS 15.0软件进行统计分析,应用Kappa评价方法对磁珠法试剂和Trizol法试剂及复核检测结果进行诊断的一致性分析,检验水准为 α=0.05。Kappa值参考评价原则:0.75 < κ≤1,诊断一致性好;0.4 < κ≤0.75,诊断一致性一般;0≤κ≤0.4时,诊断一致性差。以 P≤0.05为差异有统计学意义。
2 结 果
本研究共检测咽栻子临床样本412例,分别采用磁珠法和Trizol法的肠道病毒检测试剂盒说明书,提取样本的肠道病毒核酸后,再采用各自的检测试剂进行检测。2种方法检测得到的阳性和阴例数,经统计学处理,差异无统计学意义(P>0.05)。见表1。
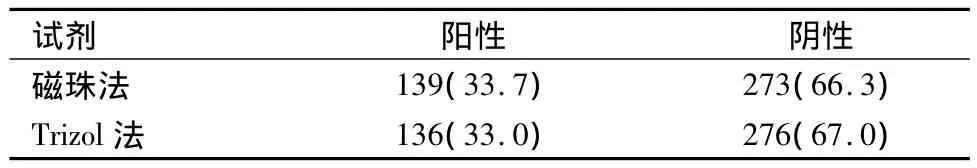
表1 磁珠法试剂与Trizol法试剂检测结果比较[n(%)]
Kappa检验的输出结果为:κ =0.983,P <0.05。磁珠法试剂和Trizol法试剂及复核检测结果的一致性有统计学意义,提示诊断一致性好。
3 讨 论
手足口病患者肠道病毒的核酸检测步骤,一般是先要提取肠道病毒核酸,尔后再采用荧光定量PCR方法进行核酸检测。由于荧光定量PCR方法具有高敏感性、高精确性等特点,所以,该方法可用于肠道病毒感染的早期诊断和无症状病毒携带者的检测[5-7]。但肠道病毒核酸提取方法不同,可导致病毒核酸提取效果的差异,进而会影响该病毒检测结果的准确性。本研究采用磁珠法和Trizol法检测同一批412例样本,虽然磁珠法试剂盒检测结果的阳性率(33.7%)高于 Trizol试剂盒阳性率(33.0%),但差异无统计学意义。提示,磁珠法试剂盒与市面常见试剂盒的检测结果一致性较高。
在样本核酸的提取过程中,Trizol法需反复高速离心,提取步骤比较繁琐;需使用氯仿、异丙醇等有毒副作用的试剂;需转移液相到新的离心管,该步骤是提取成败的关键,受到操作人员手法和经验等因素的影响,易吸取到中间层和下层的杂质,影响到提取效率;在转移样本的过程中还易出现样本间的交叉污染,影响到检测结果的准确性。而磁珠法通过核酸的释放、磁珠吸附核酸、一步洗涤杂质,去除了杂质的干扰,可获得高质量的核酸;同时,磁珠法无需加热、转移上清等操作,较易将核酸完整地提取出来,操作简便;提取过程在一个封闭的离心管内完成,无需转移液体,可有效防止样本间的交叉污染,使该方法的准确性、灵敏度大大提高,降低了对操作人员的技术要求,节省了检验时间,可更好地指导医师进行临床诊断和治疗,在临床上具有较高的应用价值。
[1]Lo CW,Wu KG,Lin MC,et al.Application of a molecular method for the classification of human enteroviruses and its correlation with clinical manifestations[J].J Microbiol Immunol Infect,2010,43(5):354-359.
[2]Oberste M,Schnurr D,Maher K,et al.Molecular identification of new picornaviruses and characterization of a proposed enterovirus 73 serotype[J].J Gen Virol,2001,82(2):409-416.
[3]Caro V,Guillot S,Delpeyroux F,et al.Molecular strategy for'serotyping'of human enteroviruses[J].J Gen Virol,2001,82(1):79-91.
[4]卫生部.手足口病诊疗指南(2010年版)[J].柳州医学,2012,25(2):140-143.
[5]Hamilton MS,Jackson MA,Abel D.Clinical utility of polymerase chain reaction testing for enteroviral meningitis[J].Pediatr Infect Dis J,1999,18(6):533-537.
[6]Nijhuis M,van Maarseveen N,Schuurman R,et al.Rapid and sensitive routine detection of all members of the genus enterovirus in different clinical specimens by real-time PCR[J].J Clin Microbiol,2002,40(10):3666-3670.
[7]尤俊斌,苏郑明,陈玮莹.肠道病毒71型引起手足口病的发病机制[J].医学研究生学报,2012,25(8):876-878.
