经胸小切口封堵术与外科手术治疗膜部室间隔缺损的对比研究
2014-09-15杨新超柳德斌王炜
杨新超 柳德斌 王炜
临床研究
经胸小切口封堵术与外科手术治疗膜部室间隔缺损的对比研究
杨新超 柳德斌 王炜
作者单位:730000 甘肃省兰州市,兰州大学第一医院心外科(杨新超);兰州大学第二医院心外科(柳德斌、王炜)
目的 探讨经胸小切口封堵术治疗膜部室间隔缺损(VSD)的优势及临床应用价值。方法 自2011年9月至2013年2月,选择40例经胸小切口封堵术治疗膜部VSD的患者,另外选40例经传统外科修补术治疗膜部 VSD 的患者。两组患者年龄 1~32(15.5±3.5)岁,体重 10.8~58.0(24.2±7.5)kg,膜部室间隔缺损大小为2~14(5.6±0.5)mm。分别依据两种不同的方法完成手术,比较两组的疗效、并发症及其他相关因素,评估经胸小切口封堵术的可行性及优越性。结果 经胸小切口封堵术组有1例患者封堵失败,行开胸手术治疗,成功率97.5%;外科手术组除1例因急性感染死亡外,余全部手术成功。两组治疗成功率相似,但在术后并发症及其他相关因素方面有明显差别。术后3~12个月随访,经胸小切口组无新并发症出现,而外科组新出现一系列并发症。结论 尽管经胸小切口膜部VSD封堵术较外科手术治疗效果相当,但具有术后并发症较少、恢复快、创伤小、患者易于接受等优点。目前该技术是可行的,且临床应用价值高。
食管超声心动图; 小切口; 膜部室间隔缺损
室间隔缺损(VSD)的治疗先后经过体外循环下开胸手术及导管介入封堵术[1-3]的发展历程。近年来,随着技术的不断进步,经食管超声(TEE)引导右心室穿刺封堵治疗VSD技术在我国已成功应用于临床[4,5],逐渐代替外科手术治疗部分VSD。自2011年9月至2013年2月,我科选择经胸小切口膜部VSD封堵术与外科手术患者各40例,进行临床对比,具体方法如下。
1 资料与方法
1.1 一般资料 入选标准:所有患者按照以下入选标准进行选择,包括:①两组所有患者年龄在1~32(15.5±3.5)岁,体重 10.8~58.0(24.2±7.5)kg;②有明显左向右分流的膜部室间隔缺损(2~14 mm),不伴有重度肺动脉高压;③除了动脉导管未闭、房间隔缺损等外,任何伴有其他可以给术后增加风险因素的疾病不适宜入选。患者中2例合并动脉导管未闭,4例合并房间隔缺损,6例有轻度肺动脉高压,2例合并轻度三尖瓣反流。
1.2 手术基本方法 ①经胸小切口封堵术组:患者仰卧位全麻,于胸骨中下段正中切开皮肤3~5 cm,进胸剪开心包并悬吊,右室壁定位,缝荷包并穿刺,在TEE指导下插入导引钢丝,并穿过膜部VSD进入左室腔内,沿导丝引入鞘管至左室,确认鞘管置入左室后,退出导丝,将带有适宜大小(一般可选择比测量VSD范围大1~2 mm)封堵器的导管沿鞘管置入至左室(如图1),顺序释放左室面伞盘,TEE证实膜部室间隔缺损无残余分流,心内结构未受影响,特别是主动脉瓣的启闭正常(图2),于右室腔内释放右室面伞盘,轻行推拉实验证实无移位(如图3),撤出输送装置后缝线打结,依常规逐层关胸。②外科手术组:所有患者均依常规在全麻下采用胸骨正中切口,浅低温、体外循环下利用自体心包完成膜部VSD修补,对于伴随病症给予对症处理,术后心包、纵隔内置管引流,进监护病房。
1.3 统计学方法 所有资料采用Stata 10.0统计软件进行处理。计量资料以±s表示,计数资料用χ2检验和Fisher检验比较,部分组间资料的比较采用简单t检验。P<0.05为差异有统计学意义。
2 结果
2.1 疗效及并发症比较 ①经胸小切口封堵术组:本组所选40例膜部VSD患者的缺损大小均为3~7 mm,治疗后除1例术后2 d出现Ⅲ度传导阻滞(给予激素治疗及抗凝治疗后尚未恢复)行二次开胸手术治疗外,余均获封堵成功,成功率达97.5%。术后5例出现微量残余分流(均<2 mm),轻度传导及心律异常7例,给予对症治疗后恢复较可,2例出现轻度主动脉瓣和三尖瓣反流,患者无症状,未给予治疗。左室舒张末压(IVEDP)由术前平均(10.8±3.0)mm Hg(1 mm Hg=0.133 kPa)降至术后的(7.1±2.6)mm Hg(P<0.05);心胸比率(C/T)由术前的0.48±0.05减小至术后的0.46±0.05(P<0.05)。②外科组:本组治疗40例膜部VSD患者的缺损相对较大,均为2~14 mm,治疗后除1例因急性感染死亡外,余全部手术成功。术后2例出现少量残余分流(3 mm),2例出现心包积液后行穿刺引流术,2例术后伤口出血行二次开胸缝合止血治疗,少量胸腔积液2例,部分性肺膨胀不全3例,心包少量积气1例,轻度主动脉瓣反流1例,轻度左前分支阻滞1例。以上并发症均经对症治疗后相应改善或治愈。左室舒张末径(LVEDD)由术前的(38.9±5.6)mm 降至术后的 (36.8±5.4)mm (P<0.05);胸心比率(C/T)值由术前的 0.50±0.06 减小至术后的 0.43±0.05(P<0.05)。③其他指标比较:经胸小切口封堵术组在手术耗时、术后ICU监护时间、总住院天数、术后恢复时间等方面均显著少于外科组,但在器材费及治疗总费用上要明显高于外科组。封堵术组无患者输血,外科组共40人次需要输血液制品,其中输全血22人次(400~1200 ml)、输血浆8人次(200~400 ml)、输红细胞 10人次(2~8 U)。余指标如左室射血分数(LVEF)、左室收缩末内径(LVESD)、左室舒张末容量(LVEDV)及左室收缩末容量(LVESV)等术后两组比较差异无统计学意义。见表 1~3。
2.2 随访 经胸小切口封堵术组患者术后3~12个月随访查TTE示:仍见3例1~2 mm的微量残余分流,1例中度三尖瓣反流,2例传导阻滞;余封堵器回声清晰,位置正常稳固,未发现移位与脱落,心功能各项评价指标正常。外科组出院后3~17个月复查心脏彩超示:残余分流及反流情况消失,轻度传导阻滞及主动脉瓣关闭不全未消失,另外新出现心包积液和三尖瓣反流各2例,1例伤口红肿、发炎,1例心功能衰竭,1例因与手术无关的急性胃肠炎死亡,分别给予心包引流、消炎等对症治疗后症状有所缓解。
3 讨论
经胸小切口右心室穿刺膜部VSD封堵术是一项新开展的微创杂交技术。该技术的临床应用体现了VSD治疗策略的转变。目前,临床上不断有关此技术成功应用的报道[6-8],其技术越来越成熟。相比而言,经胸小切口封堵这一新技术避免了外科手术所带来的不利因素,在临床上具有明显的优势。本研究是通过临床对比来发现其优缺点,充分发挥临床优势,同时解决不足之处。我们观察两组治疗结果发现,两组疗效(成功率及相关心功能变化)近似(如表1)。但经胸小切口封堵术较外科手术在术后并发症及其他相关因素方面明显具有并发症少、手术时间短、操作简单、安全有效[4,9]、美容效果好[10]和短期结果可接受[11]等优点(如表2、3),更重要的是目前这项技术可以有效代替外科手术应用于其他简单的先天性心脏病,如经右房的房间隔缺损封堵术[12-14]和动脉导管未闭封堵术[15,16],所以其治疗范围也在不断扩大。但这毕竟是一项全新技术,仍有局限性,我们应该注意到其术后残余漏发生率高、费用高及易导致传导阻滞[17]等不足之处。同时,该项新技术应用前景广泛,但临床技能尚不成熟,其应用范围相对较局限,目前仅适用于选择简单且缺损相对较小的VSD,所以要使该技术能够成熟而且更广泛地用于临床,还需不断地进行临床研究和技术改进。当然,这就要求医师必须具有良好的超声基础和专业知识,能够结合临床经验筛选更广泛的适应证,合理选择封堵器大小,这是预防和有效避免术后并发症的关键。同时更多中心参与的长期随访研究将进一步为该术式提供循证支持,以确保新技术的有效性。
总体来说,采用这种新型微创封堵技术治疗膜部VSD是有效、可行的。相信随着国产VSD封堵器的研发、临床研究的不断进步,其术后分流率高、传导阻滞严重、器材费用高等缺点会得到相应的解决,同时适应证也会越来越广。经胸小切口封堵技术将逐步替代外科手术成为治疗VSD的首选方法。
表1 两组术后结果比较(±s)
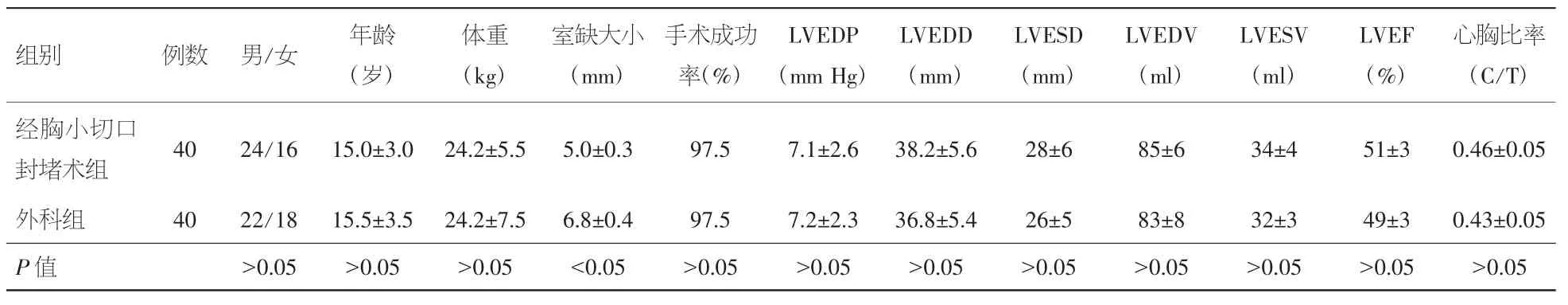
表1 两组术后结果比较(±s)
组别 例数 男/女 年龄(岁)心胸比率(C/T)经胸小切口封堵术组 40 24/16 15.0±3.0 24.2±5.5 5.0±0.3 97.5 7.1±2.6 38.2±5.6 28±6 85±6 34±4 51±3 0.46±0.05体重(kg)室缺大小(mm)手术成功率(%)LVEDP(mm Hg)LVEDD(mm)LVESD(mm)LVEDV(ml)LVESV(ml)LVEF(%)外科组 40 22/18 15.5±3.5 24.2±7.5 6.8±0.4 97.5 7.2±2.3 36.8±5.4 26±5 83±8 32±3 49±3 0.43±0.05 P 值 >0.05 >0.05 >0.05 <0.05 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05 >0.05
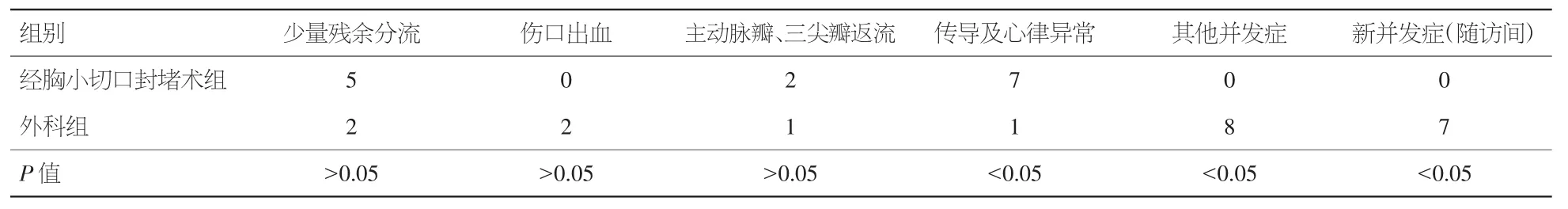
表2 两组并发症发生情况(例)
表3 两组其他指标比较(±s)

表3 两组其他指标比较(±s)
组别 室缺位置 手术创伤总费用(万元)经胸小切口封堵术组 膜周部 胸骨中下段 无需 无需 48±21 1~2 4~7 3~7 2.5~4.5 3.5~7.0情况 体外循环 输血量(ml)手术时间(min)术后ICU监护(d)总住院天数(d)术后恢复时间(d)器材费(万元)外科组 膜周部 胸骨正中 需 400~1200 145±26 1~15 8~32 80~160 0.2~0.9 2.5~4.0 P 值 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05 <0.05
(本文图片第383页)
[1]Hijazi ZM,Hakim F,Haweleh AA,et al.Catheter closure of perimembranous ventricular septal defects using the new Amplatzer membranous VSD occluder∶initial clinical experience.Catheterization and cardiovascular interventions,2002,56:508-515.
[2]Bass JL,Kalra G,Arora R,et al.Initial human experience with the Amplatzer perimembranous ventricular septal occluder device.Catheterization and Cardiovascular Interventions,2003,58:238-245.
[3]Arora R,Trehan V,Kumar A,et al.Transcatheter closure of congenital ventricular septal defects:experience with various devices.J Interv Cardiol,2003,16:83-91.
[4] Li F,Chen M,Qiu Z,et al.A new minimally invasive technique to occlude ventricular septal defect using an occluder device.Ann Thoracic Surg,2008,85:1067-1071.
[5]吴勤.超声心动图引导经胸小切口室间隔缺损封堵术.中南大学学报(医学版),2011,37:699-705.
[6]Bacha EA,Cao QL,Starr JP,et al.Perventricular device closure of muscular ventricular septal defects on the beating heart∶technique and results.J Thoracic Cardiovascular Surg,2003,126:1718-1723.
[7]Maheshwari S,Suresh P,Bansal M,et al.Perventricular device closure of muscular ventricular septal defects on the beating heart.Indian Heart J,2004,56:333-335.
[8] ZengXJ, SunSQ, ChenXF, etal.Deviceclosureof perimembranousventricularseptaldefectswith a minimally invasive technique in 12 patients.Ann Thoracic Surg,2008,85:192.
[9]Xing Q,Pan S,An Q,et al.Minimally invasive perventricular device closure of perimembranous ventricular septal defect without cardiopulmonary bypass∶multicenter experience and mid-term follow-up.J Thoracic Cardiovascular surg,2010,139:1409.
[10]Pan S,Xing Q,Cao Q,et al.Perventricular device closure of doubly committed subarterial ventral septal defect through left anterior minithoracotomy on beating hearts.Ann Thoracic surg,2012,94:2070-2075.
[11]Gan C,Lin K,An Q,et al.Perventricular device closure of muscular ventricular septal defects on beating hearts∶initial experience in eight children.J Thoracic Cardiovascular Surg,2009,137:929-933.
[12]Majunke N,Bialkowski J,Wilson N,et al.Closure of atrial septal defect with the Amplatzer septal occluder in adults.Am J Cardio,2009,103:550-554.
[13] Vaidyanathan B,Simpson JM,Kumar RK.Transesophageal echocardiography for device closure of atrial septal defects case selection, planning, and procedural guidance. JACC:Cardiovascular Imaging,2009,2:1238-1242.
[14]Seca L,Cacao R,Silva J,et al Intracardiac echocardiography imaging for device closure of atrial septal defects-A singlecenter experience.Revista Portuguesa de Cardiologia(English Edition),2012,31:407-412.
[15]Hongxin L,Wenbin G,Zhu M,et al.New minimally invasive technique of perpulmonary device closure of patentductus arteriosus through a parasternal approach.Ann Thoracic Surgery,2012,93:862-868.
[16]Tao K,Zhu D,An Q,et al.Perventricular device closure of patent ductus arteriosus: A secondary chance.An Thoracic Surg,2012,93:1007-1009.
[17]Predescu D,Chaturvedi RR,Friedberg MK,et al.Complete heart block associated with device closure of perimembranous ventricularseptaldefects.JThoracic CardiovascularSurg,2008,136:1223-1228.
Comparative study on treatment of perimembrane ventricular septal defects by the chest small incision closure of VSD and by surgical repair
YANG Xin-chao*,LIU De-bin,WANG Wei.*Department of Cardiovascular Surgery,the First Hospital Lanzhou University,Lanzhou 730000,China
Objective To discuss the advantages of device closure via a small lower sternal incision of perimembrane VSD and the clinical application value,constantly summarize the clinical experiences.Methods Between September 2011 and February 2013,40 patients who underwent closure via a small lower sternal incision and another 40 patients who underwent the conventional surgical repair of perimembrane VSD were collected,aged 12 months to 32 years(15.5±3.5)years old with a body weight of 10.8-58.0(24.2±7.5)kg,the size of perimembrane VSD was 2-14(5.6±0.5)mm.Assessing the superiority and feasibility of closure via a small lower sternal incision by comparing with each other.Results The small incision group was successful in all patients,except for 1 patient who required immediate surgical conversion after the operation failed (97.5%).The surgical group∶all patients are successful in 40 patients except one patient died of acute infection.The success rate of device closure was similar to the surgical repair.However,there were many significant differences in complications and other related factors.In a follow-up period of 3 to 12 months there was no new complications in the small incision group,but surgical group appeared lots of new complications.Conclusion Though the success rate of device closure is similar to the surgical repair,but the recovery time, complications,trauma to the vessels and other relevant factors decrease.At present,this technique is feasible,its clinical application value is quite high and the patients are easy to accept it.
Transesophageal echocardiography; Small incision; Perimembrane ventricular septal defects
LIU De-bin,E-mail:ldebin@yahoo.com.cn
柳德斌,E-mail:ldebin@yahoo.com.cn
10.3969/j.issn.1672-5301.2014.04.011
R654.2
B
1672-5301(2014)04-0323-04
2013-10-09)
