无创正压通气治疗肥胖低通气综合征并发心力衰竭的探讨
2014-09-04宋琼珠欧阳松云孙培宗陈瑞英郑州大学第一附属医院呼吸睡眠科河南郑州450052
宋琼珠,欧阳松云,孙培宗,陈瑞英(郑州大学第一附属医院呼吸睡眠科,河南 郑州 450052)
·论著·
无创正压通气治疗肥胖低通气综合征并发心力衰竭的探讨
宋琼珠,欧阳松云*,孙培宗,陈瑞英
(郑州大学第一附属医院呼吸睡眠科,河南 郑州 450052)
目的探讨肥胖低通气综合征(obesity hypoventilation syndrome,OHS)并发心力衰竭的有效治疗方法。方法回顾性分析120例OHS合并心力衰竭患者,无创正压通气(noninvasive positive pressure ventilation,NPPV)组60例采用NPPV加常规抗心力衰竭药物治疗,对照组60例常规抗心力衰竭药物治疗,比较2组治疗前、治疗6个月后相关指标。结果对照组治疗后动脉血气分析、脑利钠肽(brain natriuretic peptide,BNP)、心脏彩超、多导睡眠监测(polysomnography,PSG)均恶化(P<0.05或<0.01)。NPPV组治疗后体质量指数(body mass index,BMI)下降,动脉血气分析、BNP、心脏彩超、PSG均明显好转(P<0.01)。治疗后与对照组比较,NPPV组BMI、动脉血气分析、BNP、心脏彩超、PSG均明显好转(P<0.01)。结论OHS并发心力衰竭常规抗心力衰竭疗效不佳,及早行NPPV治疗预后良好。
肥胖低通气综合征;心力衰竭;连续气道正压通气
10.3969/j.issn.1007-3205.2014.07.002
肥胖低通气综合征(obesityhypoventilationsyndrome,OHS)是由肥胖导致的日间慢性通气不足,并可引起心脑血管、内分泌等全身多系统损害,导致日常生活和社会活动减少,有住院和死亡的高风险。发病机制包括睡眠呼吸紊乱、呼吸驱动力减低以及与肥胖相关的呼吸系统受损等[1]。其临床表现多样,变化急骤,易致猝死。早期行无创正压通气(noninvasivepositivepressureventilation,NPPV)治疗则可改善预后,降低病死率。目前关于OHS的研究尚少,且临床工作中易忽视NPPV治疗。本研究观察对OHS并发心力衰竭患者行NPPV为主的综合治疗效果,旨在提高对OHS并发心力衰竭的诊治水平。
1 资料与方法
1.1 一般资料:选取2005年1月—2013年8月郑州大学第一附属医院收治的符合肥胖低通气综合征诊断标准[2]及Framingham心力衰竭诊断标准确诊的OHS并发心力衰竭患者120例,随机分为2组。对照组60例,男性32 例,女性28例,年龄48~69岁,平均(59.50±5.68)岁;NPPV组60例,男性26 例,女性34例,年龄45~68岁,平均(58.30±4.75)岁。2组患者性别、年龄差异均无统计学意义(P>0.05),具有可比性。
1.2 排除标准:经询问病史、体检及相关检查排除可能导致肺泡通气不足的其他疾病如重度阻塞性或限制性肺疾病、胸壁疾病、脊柱侧后凸畸形、神经肌肉疾病、严重的甲状腺功能减退、先天性中枢性低通气综合征[3],以及心、肺、血液系统和脑血管疾病等。
1.3 方法:①记录所有研究对象身高、体质量,计算体质量指数(bodymassindex,BMI),检查动脉血气分析,记录动脉血氧分压(arterialpartialpressureofoxygen,PaO2)、动脉血二氧化碳分压(arterialpartialpressureofcarbondioxide,PaCO2)。②BNP测定,采集外周静脉血1mL,EDTA抗凝,使用美国Biosite公司生产的Triagemeterplus免疫荧光定量心肌梗死和心力衰竭诊断仪器及配套试剂卡,定量检测BNP,检测范围5~5 000ng/L。③心脏彩超,仪器为MYLAB50,频率3.5mHz。记录反映心功能的左心室射血分数(leftventricularejectionfraction,LVEF)和反映心脏结构的肺动脉压(pulmonaryarterypressure,PAP)。④多导睡眠监测(polysomnography,PSG),行7h夜间PSG,应用澳大利亚产的Compumedic型多导睡眠监测仪,记录呼吸暂停低通气指数(apneahypoventilationindex,AHI)、低通气指数(hypoventilationindex,HI)、最低指脉氧饱和度(lowestpulseoxygensaturation,L-SpO2)。所有资料均经电脑同步记录储存,自动分析处理后再手动复核修正。治疗6个月后重复以上内容。
1.4 治疗:对照组仅给予常规抗心力衰竭药物治疗(包括抗感染药物,利尿剂、血管紧张素转换酶抑制剂、血管紧张素Ⅱ受体拮抗剂、β受体阻滞剂、硝酸酯类等),NPPV组在常规抗心力衰竭药物治疗的基础上加NPPV治疗,其压力滴定均由专业睡眠技师按照“阻塞性睡眠呼吸暂停低通气综合征诊治指南(2011年修订版)”和“阻塞性睡眠呼吸暂停低通气综合征患者持续气道正压通气临床应用专家共识(草案)”[4-5]进行。本研究NPPV治疗根据症状及实验室检查选取不同方案,先设置初始呼气压力为5~7cmH2O,逐步上调至消除低通气。入院时昏迷或PaCO2过高的患者,吸气压力调至患者能耐受的最大压力(18~24cmH2O),保证潮气量(8~10mL/kg);症状较轻的患者吸气压力初设为8~10cmH2O,逐渐上调以保证上气道开放。

2 结 果
2.1 2组治疗前后BMI、PaO2和PaCO2变化: 治疗前2组BMI、PaO2和PaCO2差异均无统计学意义(P>0.05);治疗后对照组BMI无明显变化,PaO2下降、PaCO2上升(P<0.05或<0.01);治疗后NPPV组BMI和PaCO2下降,PaO2上升(P<0.01)。NPPV组治疗后BMI和PaCO2低于对照组、PaO2高于对照组(P<0.01)。见表1。

GroupsBMIBeforetreatmentAftertreatmentPaO2(mmHg)BeforetreatmentAftertreatmentPaCO2(mmHg)BeforetreatmentAftertreatmentControl38.7±4.137.6±7.260.4±7.256.7±10.4∗74.5±67.186.2±11.5#NPPV38.8±3.923.9±3.7#60.1±8.290.5±5.8#73.9±8.541.1±5.2#t0.0013.6720.0035.3670.1025.823P>0.05<0.01>0.05<0.01>0.05<0.01
*P<0.05 #P<0.01vsbefore treatment by pairedttest
BMI:body mass index;PaO2:arterial partial pressure of oxygen;PaCO2:arterial partial pressure of carbon dioxide;NPPV:noninvasive positive pressure ventilation
2.2 2组治疗前后BNP、PAP和LVEF变化: 治疗前2组BNP、PAP和LVEF差异均无统计学意义(P>0.05)。治疗后对照组BNP和PAP上升,LVEF下降(P<0.05);治疗后NPPV组BNP和PAP下降,LVEF上升(P<0.01)。NPPV组治疗后BNP和PAP低于对照组,LVEF高于对照组(P<0.01)。见表2。
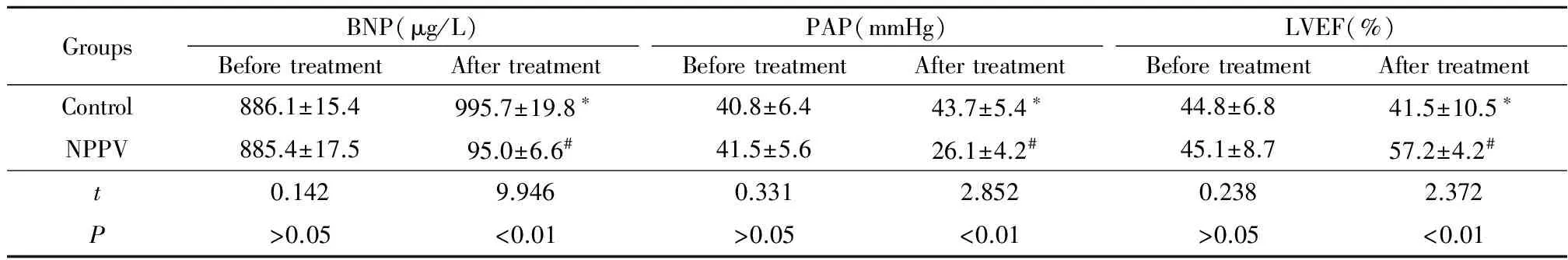
GroupsBNP(μg/L)BeforetreatmentAftertreatmentPAP(mmHg)BeforetreatmentAftertreatmentLVEF(%)BeforetreatmentAftertreatmentControl886.1±15.4995.7±19.8∗40.8±6.443.7±5.4∗44.8±6.841.5±10.5∗NPPV885.4±17.595.0±6.6#41.5±5.626.1±4.2#45.1±8.757.2±4.2#t0.1429.9460.3312.8520.2382.372P>0.05<0.01>0.05<0.01>0.05<0.01
*P<0.05 #P<0.01vsbefore treatment by pairedttest
BNP:brain natriuretic peptide;PAP:pulmonary artery pressure;LVEF:left ventricular ejection fraction;NPPV:noninvasive positive pressure ventilation
2.3 2组治疗前后PSG指标变化: 治疗前2组的AHI、HI、L-SpO2差异均无统计学意义。治疗后对照组AHI和HI上升,L-SpO2下降(P<0.05);治疗后NPPV组AHI和HI下降,L-SpO2上升(P<0.01)。NPPV组治疗后AHI和HI低于对照组,L-SpO2高于对照组(P<0.01)。见表3。
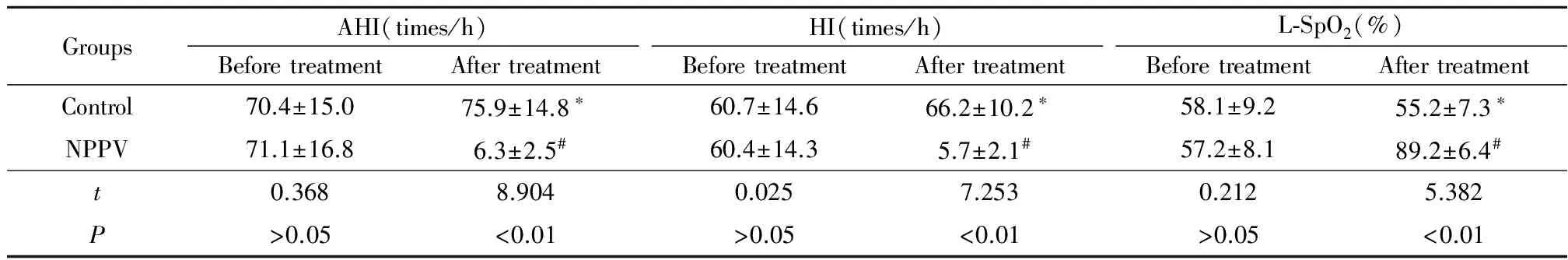
GroupsAHI(times/h)BeforetreatmentAftertreatmentHI(times/h)BeforetreatmentAftertreatmentL⁃SpO2(%)BeforetreatmentAftertreatmentControl70.4±15.075.9±14.8∗60.7±14.666.2±10.2∗58.1±9.255.2±7.3∗NPPV71.1±16.86.3±2.5#60.4±14.35.7±2.1#57.2±8.189.2±6.4#t0.3688.9040.0257.2530.2125.382P>0.05<0.01>0.05<0.01>0.05<0.01
*P<0.05 #P<0.01vsbefore treatment by pairedttest
AHI:apnea hypoventilation index;HI: hypoventilation index;L-SpO2:lowest pulse oxygen saturation;NPPV:noninvasive positive pressure ventilation
2.4 临床转归及随访:本研究随访时间8年,NPPV组治疗3~4d患者嗜睡状态、呼吸困难、下肢水肿等症状即有好转,51例均长期家庭NPPV治疗,病情无反复,9例未坚持治疗病情加重,其中2例已死亡。对照组患者心力衰竭症状日益加重,15例曾反复有创机械通气,生活质量极差,18例已死亡,其中11例为猝死。
3 讨 论
OHS是病理性肥胖的一种特殊表现,是一种睡眠、呼吸、代谢和心血管功能障碍导致活动减少,缺乏社会参与和有较高病死率的疾病。主要特点为病态肥胖、白天嗜睡、呼吸困难,清醒状态下低氧血症、高碳酸血症,肺循环及体循环血压升高,代谢综合征,继发性红细胞增多等,易并发呼吸衰竭、心力衰竭[6],若仅常规抗心力衰竭治疗往往效果不佳,其主要原因为对OHS合并心力衰竭认识不足。
OHS合并心力衰竭患者有以下临床特点:①心力衰竭往往为右心衰竭,长期缺氧致低氧性肺血管收缩,高碳酸血症使血管对缺氧的收缩敏感性增强,易形成肺动脉高压[7]致右心衰竭。心力衰竭加重较快,变化急骤,处理不当可致猝死。本研究随访对照组18例死亡患者中有11例为猝死。②由于OHS病程长,易反复下呼吸道感染出现咳嗽、咳痰,加重低氧血症、高碳酸血症,从而诱发或加重心力衰竭,易误诊为慢性阻塞性肺疾病急性加重致心力衰竭。故需详细询问病史且注意肥胖、限制性通气功能障碍、肺泡低通气等OHS的特点。③OHS合并心力衰竭患者入院时多病情危重,本研究即有15例曾出现意识障碍。意识障碍可能与OHS所致肺性脑病有关,易误诊为脑血管疾病等,延误治疗。④OHS患者经常因过度肥胖首诊入内分泌科,本研究60%OHS患者首诊入内分泌科,后经会诊转入呼吸科救治。⑤因对OHS认识不足及不重视NPPV治疗,单纯用抗心力衰竭药物不能从病因上纠正低通气导致的病理生理过程对心脏的损害。本研究对照组治疗6个月后心脏功能明显下降,结构指标恶化。
OHS合并心力衰竭的发病机制为:OHS患者多表现为较大的颈围和更高的腰臀比,上气道阻力增加,胸腹腔内脂肪堆积致肺及胸廓顺应性和弹性回缩下降,膈肌上抬且运动受限,造成限制性通气功能障碍且增加呼吸功[8]。因瘦素抵抗等内分泌因素及长期存在低氧、高碳酸血症致呼吸中枢受损,呼吸驱动力降低,加之肥胖致通气不足[9],通过刺激外周及中枢化学感受器使交感神经活性增高,并通过增加炎症因子、氧化应激致血管内皮功能障碍,心肌损伤、重构及肺循环血管阻力增加[9-10],肺动脉高压,右心负荷加重诱发右心衰竭。过度肥胖,膈肌活动受限,回心血量减少致心脏搏出量减少,氧供减少,而交感神经系统活性增强致高血压及心率增快均增加心肌耗氧量,氧供不足和耗氧增加损害心肌并形成恶性循环,最终导致全心衰竭[9-10]。双水平NPPV治疗是通过分别对吸气相和呼气相提供不同水平的正压,增加潮气量,减少呼吸功和耗氧量,防止气道塌陷,扩张上气道,改善中枢神经系统对低氧和高二氧化碳的敏感性,使通气驱动增强,肺泡通气量增加,从而改善低氧血症和高碳酸血症[11],降低交感神经兴奋性,同时减少炎症因子、氧化应激及内皮源性缩血管因子释放,增加内皮源性一氧化氮,改善血管舒张功能,降低肺循环及体循环压力,减轻心脏损害[12]。本研究结果显示NPPV治疗6个月后动脉血气分析明显改善,BNP、PAP下降,LVEF上升,心脏功能改善。与Nakayama等[13-14]报道一致。
本研究NPPV组治疗3~4d患者嗜睡状态、呼吸困难、下肢水肿等症状即有好转,治疗6个月后BMI下降,动脉血气分析明显好转,心脏功能及结构改善,PSG明显好转。NPPV组51例患者均长期坚持家庭NPPV治疗,病情无反复,9例未坚持治疗患者病情加重。对照组患者心力衰竭症状日益加重,15例曾反复行有创机械通气,生活质量极差,18例已死亡。表明以NPPV为基础的综合治疗对OHS并发心力衰竭短期疗效显著,长期治疗可防止心力衰竭再发生,明显改善生活质量,降低病死率。
OHS易致呼吸衰竭、心力衰竭、代谢综合征等,病情重,且易漏诊、误诊。在临床工作中,对肥胖的心力衰竭患者,应注意OHS的存在,对OHS所致心力衰竭应及早并维持NPPV为主的综合治疗。
[1] BOREL JC,BOREL AL,Monneret D,et al.Obesity hypoventilation syndrome: from sleep-disordered breathing to systemic comorbidities and the need to offer combined treatment strategies[J].Respirology,2012,17(4):601-610.
[2] 谢芳,韩芳.肥胖低通气综合征的诊治进展[J].国际呼吸杂志,2007,27(14):1117-1120.
[3] MOKHLESI B.Obesity hypoventilation syndrome: a state-of-the-art review[J].Respir Care,2010,55(10):1347-1365.
[4] 中华医学会呼吸病学分会睡眠呼吸疾病学组.阻塞性睡眠呼吸暂停低通气综合征诊治指南(2011年修订版)[J].中华结核和呼吸杂志,2012,35(1):9-12.
[5] 中华医学会呼吸病学分会睡眠呼吸障碍学组,李庆云.阻塞性睡眠呼吸暂停低通气综合征患者持续气道正压通气临床应用专家共识(草案)[J].中华结核和呼吸杂志,2012,35(1):13-18.
[6] 王小亚,周光耀.肥胖低通气综合征[J].华西医学,2007,22(1):178-179.
[7] 翟振国,谢万木,王辰.肺动脉高压的概念和临床分类[J].中华结核和呼吸杂志,2007,30(9):651-653.
[8] 焦俊,张睢扬,宋云熙.肥胖低通气综合征[J].国际呼吸杂志,2012,32(1):72-78.
[9] CHAU EH,LAM D,WONG J,et al.Obesity hypoventilation syndrome: a review of epidemiology,pathophysiology,and perioperative considerations[J].Anesthesiology,2012,117(1):188-205.
[10] MARIK PE.The malignant obesity hypoventilation syndrome (MOHS)[J].Obes Rev,2012,13(10):902-909.
[11] JANSSENS JP,METZGER M,SFORZA E.Impact of volume targeting on efficacy of bi-level non-invasive ventilation and sleep in obesity-hypoventilation[J].Respir med,2009,103(2):165-172.
[12] 黄志坚,韩烨,杨运旗,等.心力衰竭合并阻塞性睡眠呼吸暂停低通气综合征的病例分析[J/CD].中华肺部疾病杂志:电子版,2010,3(1):30-33.
[13] NAKAYAMA H.Sleep-disordered breathing[J].Nihon Rinsho,2013,71(2):286-290.
[14] WEITZENBLUM E,KESSLER R,CANUET M,et al.Obesity-hypoventilation syndrome[J].Rev Mal Respir,2008,25(4):391-403.
(本文编辑:许卓文)
NONINVASIVEPOSITIVEPRESSUREVENTILATIONONPATIENTSWITHOBESITYHYPOVENTILATIONSYNDROMECOMPLICATEDBYHEARTFAILURE
SONGQiongzhu,OUYANGSongyun*,SUNPeizong,CHENRuiying
(DivisionofRespiratorySleep,theFirstAffiliatedHospitalofZhengzhouUniversity,Zhengzhou450052,China)
CT:ObjectiveToexploreeffectivetreatmentsforpatientswithobesityhypoventilationsyndromecomplicatedbyheartfailure.MethodsRetrospectiveanalysiswasperformedon120patientswithobesityhypoventilationsyndromecomplicatedbyheartfailure.Noninvasivepositivepressureventilation(NPPV)group(60cases)wastreatedwithNPPVandmedications,andthecontrolgroup(60cases)onlywithmedications.Therelatedindicatorsandcurativeeffectsbeforetreatment,6monthsaftertreatmentwerecomparedbetweentwogroups.ResultsArterialbloodgasanalysis,brainnatriureticpeptide(BNP),echocardiographyandpolysomnography(PSG)thecontrolgroupaftertreatmentallworsened(P<0.05or<0.01).Bodymassindex(BMI)decreased,arterialbloodgasanalysis,BNP,echocardiographyandPSGofNPPVgroupaftertreatmentallimprovedsignificantly(P<0.01).Comparedwithcontrolgroupaftertreatment,NPPVgroupimprovedsignificantlyinBMI,arterialbloodgasanalysis,BNP,echocardiographyandPSG(P<0.01).ConclusionNPPVisaneffectivemethodforpatientswithobesityhypoventilationsyndromecomplicatedbyheartfailure.
obesityhypoventilationsyndrome;heartfailure;continuouspositiveairwaypressure
2014-04-02;
2014-05-07
河南省科技厅重点攻关项目(122102310218)
宋琼珠(1988-),女 河南漯河人,郑州大学第一附属医院医学硕士研究生,从事睡眠呼吸障碍疾病诊治研究。
*通讯作者
R459.9
A
1007-3205(2014)07-0749-04
