海洋生物碱2,3-二羟基-10-溴吲哚[3,2-a]咔唑的简易合成
2014-09-02梁大伟王悦秋
梁大伟,王悦秋
(雅安职业技术学院 药学检验系,四川 雅安 625000)
海洋生物碱2,3-二羟基-10-溴吲哚[3,2-a]咔唑的简易合成
梁大伟*,王悦秋
(雅安职业技术学院 药学检验系,四川 雅安 625000)
2,3-二羟基-10-溴吲哚[3,2-a]咔唑(1)是一种从海绵体中提取的具有多种潜在生物活性的天然海洋生物碱. 本文作者以3,6-二溴吲哚(2)与5,6-二乙酰氧基吲哚(3)为原料,经过酸催化偶联、分子间成环两步关键反应构建吲哚[3,2-a]咔唑母核;所构建的吲哚[3,2-a]咔唑母核在碱性条件下水解脱去酚羟基上的酯基,即得到目标化合物1,总收率为48%.
海洋生物碱;吲哚;咔唑;合成
海洋有机生物体已经成为天然产物的主要来源之一,其中孕育着大量结构新颖且活性广泛的有机分子[1-2]. 而海洋生物碱作为其中一类研究较多的活性分子,近年来受到了合成化学家与药物化学家们的广泛关注[3],它们具有抗感染[4]、抗抑郁与焦虑[5]、抗病毒、抗炎、抗寄生虫药及中枢神经系统治疗等多种生物活性[6]. 2,3-二羟基-10-溴吲哚[3,2-a]咔唑 (1) 是WRIGHT课题组[7]于2013年从深海植物Asteropus的海绵体中提取分离的一种天然海洋生物碱,它对病原真菌白色念珠菌与耐甲氧西林金黄色葡萄球菌的最小抑制浓度分别为25与50 mg/L;同时,在测试PANC1人胰腺癌与NCI/ADR-RES卵巢癌细胞株时,没有显示出毒副作用,具有潜在的开发应用价值.
本文作者在相关吲哚[3,2-a]咔唑衍生物的合成文献基础上,设计了一条三步简易法合成1,其中以3,6-二溴吲哚(2)与5,6-二乙酰氧基吲哚(3)为原料,经过酸催化偶联、分子间成环两步关键反应构建吲哚[3,2-a]咔唑母核,最后,在碱性条件下水解脱去酚羟基上的酯基即可合成目标化合物1(图1).
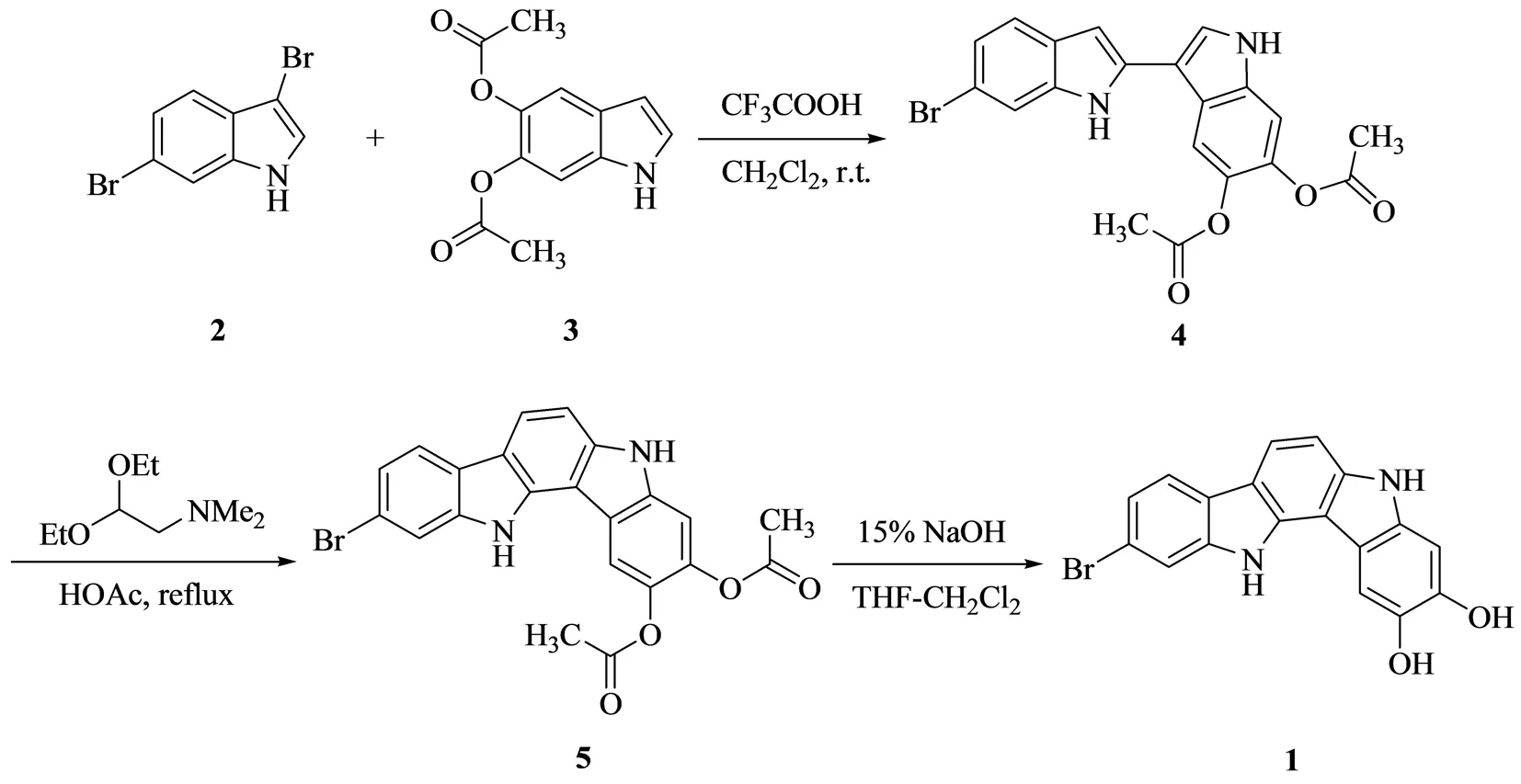
图1 2,3-二羟基-10-溴吲哚[3,2-a]咔唑(1)的合成路线Fig.1 Synthesis of 2,3-dihydroxy-10-bromoindolo[3,2-a]carbazole (1)
1 实验部分
1.1 仪器与试剂
原料购于Sigma公司与韶远化学试剂有限公司,分析纯;溶剂为市售分析纯,常规干燥剂干燥,未经过进一步处理,直接使用. 反应均采用薄层层析 (TLC) 跟踪反应进程,显色剂采用碘熏;产物分离所用柱层析硅胶 (300~400目)、薄层层析硅胶 (GF254) 均为青岛海洋化工厂产品. 熔点仪为Thomas-Hoover型,温度计未加校正;核磁采用Bruker ARX-400型核磁共振仪测定,DMSO-d6为溶剂,TMS为内标;质谱采用Agilent-6 120 LC/MS测定,ESI离子源.
1.2 合成方法
1.2.1 6-溴-2-(5′,6′-二乙酰氧基-3′-吲哚基)吲哚(4)的合成
将3,6-二溴吲哚 (2) (546 mg,2 mmol) 与5,6-二乙酰氧基吲哚(3) (466 mg,2 mmol) 溶于20 mL的无水二氯甲烷溶液,然后向其中加入0.06 mL的三氟乙酸,氮气保护下常温搅拌反应约1 h. 反应完毕,向反应液中滴加氨水中和反应溶液至pH=7,分出有机相,用饱和氯化钠溶液洗涤,无水硫酸镁干燥,并经减压浓缩得粗品,进一步采用硅胶柱层析(乙酸乙酯和石油醚的体积比为1∶3) 纯化得571 mg的淡棕色固体6-溴-2-(5′,6′-二乙酰氧基-3′-吲哚基)吲哚(4),收率为67%. m.p.: 217~219 ℃,ESI-MS (m/z): 427.1 (M+1)+,1H NMR (400 MHz, DMSO-d6)δ: 11.63(br s, 1H, NH), 10.95 (br s, 1H, NH), 8.01 (s, 1H, pyrrole-H), 6.87~7.65 (m, 6H, indole-H), 2.10 (s, 3H, CH3), 2.03 (s, 3H, CH3).
1.2.2 2,3-二乙酰氧基-10-溴吲哚[3,2-a]咔唑(5)的合成
将6-溴-2-(5′,6′-二乙酰氧基-3′-吲哚基)吲哚(4) (426 mg,1 mmol) 与二甲氨基乙醛缩二乙醇(177 mg,1.1 mmol) 溶解于10 mL的醋酸中,升温回流8 h. 反应完毕,将反应液倒入适量水中,用二氯甲烷萃取 (3 × 15 mL),合并有机相,依次用饱和碳酸氢钠、饱和氯化钠洗涤,无水硫酸镁干燥,减压浓缩得粗品,进一步采用硅胶柱层析 (乙酸乙酯和石油醚的体积比为1∶3) 纯化得351 mg棕色固体2,3-二乙酰氧基-10-溴吲哚[3,2-a]咔唑(5),收率为78%. m.p. > 250 ℃,ESI-MS (m/z): 451.1 (M+1)+,1H NMR (400 MHz, DMSO-d6)δ: 11.61 (br s, 1H, NH), 10.93 (br s, 1H, NH), 7.93 (d, 1H,J= 5.2 Hz, Ar-H), 7.89 (s, 1H, Ar-H), 7.82 (d, 1H,J= 5.6 Hz, Ar-H), 7.61 (d, 1H,J= 1.2 Hz, Ar-H), 7.18 (dd, 1H,J= 1.2, 5.2 Hz, Ar-H), 7.13 (d, 1H,J= 5.6 Hz, Ar-H), 6.87 (s, 1H, Ar-H), 2.10 (s, 3H, CH3), 2.03 (s, 3H, CH3).
1.2.3 2,3-二羟基-10-溴吲哚[3,2-a]咔唑(1)的合成
将2,3-二乙酰氧基-10-溴吲哚[3,2-a]咔唑(5) (351 mg,0.78 mmol) 溶于10 mL的四氢呋喃与二氯甲烷 (1∶1, 体积比) 的混合溶液中,加入15%的氢氧化钠溶液 (3.12 mmol),升温回流1 h. 反应完毕,减压浓缩除去大部分溶剂,向残余物中加入适量的水,并用5%稀盐酸调pH=7,用二氯甲烷萃取 (3 × 15 mL),合并有机相,依次用饱和碳酸氢钠、饱和氯化钠洗涤,无水硫酸镁干燥,减压浓缩得粗品,进一步硅胶柱层析 (乙酸乙酯和石油醚的体积比为1∶2) 纯化得263 mg棕色固体2,3-二羟基-10-溴吲哚[3,2-a]咔唑(1),收率为92%. m.p. > 250 ℃,ESI-MS (m/z): 367.0 (M+1)+,1H NMR (400 MHz, DMSO-d6)δ: 11.63 (br s, 1H, NH), 10.94 (br s, 1H, NH), 9.31 (br s, 1H, OH), 9.20 (br s, 1H, OH), 7.96 (d, 1H,J= 5.2 Hz, Ar-H), 7.88 (s, 1H, Ar-H), 7.86 (d, 1H,J= 5.6 Hz, Ar-H), 7.62 (d, 1H,J= 1.2 Hz, Ar-H), 7.19 (dd, 1H,J= 1.2, 5.2 Hz, Ar-H), 7.12 (d, 1H,J= 5.6 Hz, Ar-H), 6.88 (s, 1H, Ar-H).
2 结果与讨论
2,3′-二吲哚化合物的构建方法很多,如卤代吲哚在铜催化下偶联[8],硒催化两分子吲哚偶联[9],路易酸(SnCl4)及质子酸(CF3COOH、HCl、HBr)催化偶联反应[10]. 本文作者选择质子酸CF3COOH催化3,6-二溴吲哚(2)与5,6-二乙酰氧基吲哚(3)偶联反应合成6-溴-2-(5′,6′-二乙酰氧基-3′-吲哚基)吲哚(4),收率为67%. 进一步与二甲氨基乙醛缩二乙醇在醋酸体系中回流发生成环反应[11]生成2,3-二乙酰氧基-10-溴吲哚[3,2-a]咔唑(5),收率为78%. 最后,化合物5在碱性条件下2与3-位酯基水解,较高收率(92%)的生成目标化合物2,3-二羟基-10-溴吲哚[3,2-a]咔唑(1).
3 结论
本文作者以3,6-二溴吲哚(2)与5,6-二乙酰氧基吲哚(3)为原料,经过三氟乙酸催化偶联反应,以及与二甲氨基乙醛缩二乙醇分子间成环两步关键反应构建吲哚[3,2-a]咔唑母核,最后在碱性条件下水解脱去酚羟基上的酯基合成了具有多种潜在生物活性的天然海洋生物碱化合物2,3-二羟基-10-溴吲哚[3,2-a]咔唑(1). 反应步骤较短,易于操作.
[1] TAN L T. Bioactive natural products from marine cyanobacteria for drug discovery [J]. Phytochemistry, 2007, 68(7): 954-979.
[2] BLUNT J W, COPP B R, HU W P, et al. Marine natural products [J]. Nat Prod Rep, 2008, 25(1): 35-94.
[3] KURAMOTO M, ARIMOTO H, UEMURA D. Bioactive alkaloids from the sea: A review [J]. Mar Drugs, 2004, 2(1): 39-54.
[4] DONIA M, HAMANN M T. Marine natural products and their potential applications as anti-infective agents [J]. Lancet Infect Dis, 2003, 3(6): 338-348.
[5] KOCHANOWSKA-KARAMYAN A J, HAMANN M T. Marine indole alkaloids: Potential new drug leads for the control of depression and anxiety [J]. Chem Rev, 2010, 110(8): 4489-4497.
[6] GUL W, HAMANN M T. Indole alkaloid marine natural products: An established source of cancer drug leads with considerable promise for the control of parasitic, neurological and other diseases [J]. Life Sci, 2005, 78(5): 442-453.
[7] RUSSELL F, HARMODY D, MCCARTHY P J, et al. Indolo[3,2-a]carbazoles from a deep-water sponge of theGenusAsteropus[J]. J Nat Prod, 2013, 76(10): 1989-1992.
[8] BERGMAN J, EKLUND N. Synthesis of 2,2′-biindolyls by coupling reactions [J]. Tetrahedron, 1980, 36(10): 1439-1443.
[9] BERGMAN J. Synthesis of 2,3′-biindolyl from indole in one-step reactions [J]. J Heterocycl Chem, 1973, 10(1): 121-122.
[10] BOCCHI V, PALLA G. Synthesis and spectroscopic characteristics of 2,3′-biindolyl and 2,2′-indolylpyrroles [J]. Tetrahedron, 1984, 40(17): 3251-3256.
[11] JANOSIK T, BERGMAN J. Reactions of 2,3′-biindolyl: Synthesis of indolo[3,2-a]carbazoles [J]. Tetrahedron, 1999, 55(8): 2371-2380.
[责任编辑:任铁钢]
Facilesynthesisofmarinealkaloid2,3-dihydroxyl-
10-bromoindolo[3,2-a]carbazole
LIANG Dawei*, WANG Yueqiu
(DepartmentofPharmacy&Laboratory,Ya′anVacationalCollege,Ya′an625000,Sichuan,China)
2,3-dihydroxy-10-bromoindolo[3,2-a]carbazole (1) is a natural marine alkaloid isolated from a marine sponge possessing a variety of potent biological activities. With 3,6-dibromoindole (2) and 5,6-diacetoxyindole (3) as the starting materials, indolo[3,2-a]carbazole framework is constructed through acid promoted coupling reaction and intermolecular cyclization, the two key steps for construction of the framework. Resultant indolo[3,2-a]carbazole framework is hydrolyzed under alkaline condition to eliminate the ester group in phenolic hydroxyl group affording the target compound1with an overall yield of 48%.
marine alkaloid; indolo; carbazole; synthesis
2014-06-16.
梁大伟 (1985-),男,博士,主要从事药物及药物中间体的合成研究.*
,E-mail:ldawei@yahoo.com.
O 626. 2
A
1008-1011(2014)05-0453-03
10.14002/j.hxya.2014.05.004
猜你喜欢
杂志排行
化学研究的其它文章
- 三种席夫碱-Ni(II)配合物的电子结构和吸收光谱的理论计算
- 共混硫化丁腈橡胶-氯丁橡胶的物理性能
- 不同消解方法分析污泥中重金属含量的比较
- Synthesis and characterization of a dysprosium-organic framework incorporating 2-hydroxyl-6-methyl-isonicotinic acid and oxalate mixed ligands
- Crystal structure and proton-conductivity of a complex based on phosphomolybdic acid and 2-(2-hydroxybenzene)benzimidazole
- 利用高浓度秸秆废弃物发酵产氢
