重金属离子对致癌性NDMA形成影响的实验与理论研究
2014-09-01刘雅萌刘永东
曾 婷,刘雅萌,刘永东
(北京工业大学生命科学与生物工程学院,北京 100124)
重金属离子对致癌性NDMA形成影响的实验与理论研究
曾 婷,刘雅萌,刘永东*
(北京工业大学生命科学与生物工程学院,北京 100124)
重金属污染对环境和人体健康已造成严重威胁,N-亚硝基二甲胺(NDMA)作为具有强致癌性的环境污染物也引起了广泛的关注.本论文探讨了重金属离子Cd(Ⅱ)、Hg(Ⅱ)和Pb(Ⅱ)在模拟胃液中,对NDMA形成的影响;并运用密度泛函理论(DFT)计算方法研究了重金属离子的可能作用机理.实验研究中发现3种重金属离子均能促进NDMA的形成,而理论计算结果表明重金属离子与二甲胺之间的相互作用强于与亚硝酸之间的相互作用,而且重金属离子与二甲胺形成的中间体通过先失去氢质子,再与亚硝酸作用可以生成NDMA.此反应是一个放热过程,而且反应的能垒较低,由此推测重金属离子很可能是通过与二甲胺作用而促进NDMA的形成.
重金属离子;NDMA形成;促进作用;密度泛函理论
重金属污染物对环境以及人体造成了严重的威胁,尤其是在发展中国家,比如中国.重金属对人体健康造成的威胁主要与镉、汞、铅的暴露相关.镉能毒害肾脏、骨骼系统、呼吸系统[1].汞高度危害人体健康,尤其是对胚胎早期的发育造成严重威胁[2].铅是一个累积性的有毒物,能影响包括神经系统,血液系统,胃肠道,心血管和肾脏等多种人体系统.工业“三废”和生活污水的排放严重污染了土壤和水体[3].重金属通过土壤/水/空气-粮食/蔬菜/牲畜-食物的途径进入人体[4].表1列举了此3种重金属在我国的不同体系中的限量值[5-6].
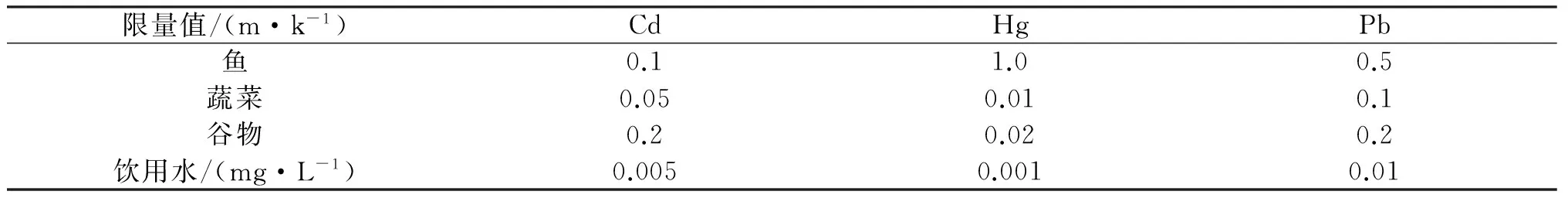
表1 鱼类、蔬菜、谷物、饮用水中重金属的限量标准
由于大部分的N-亚硝基化合物(NOC)是人类潜在的致癌物,因此引起了人们的广泛关注[7].N-亚硝基二甲胺(NDMA)是NOC中结构最简单,但致癌性最强的物质之一.国际癌症研究机构(IARC)已将NDMA及其他3种NOC归类为2A类致癌物[8].美国环境保护署(U.S. EPA)公布,饮用水中0.7 ng·L-1的NDMA将会产生10-6的致癌风险[9].研究发现人体暴露于NDMA有外源性和内源性两种途径,而且其中在人体内胃、肠和膀胱等器官形成的内源性途径约占总暴露的60%以上[10].因此,有关内源性NDMA形成的研究已成为保护人体健康的重要研究内容和被关注的领域.
如上所述,重金属和NDMA都对人体健康具有很大威胁.尤其是发展中国家粮食、蔬菜中重金属的浓度常常高于限量值,因此,研究重金属对体内NDMA形成的影响很有必要.但迄今为止,重金属离子对内源性NDMA形成的研究非常缺乏[11].因此,本研究着重对3种重金属离子对模拟胃液中NDMA形成的影响及其作用机理进行研究.
1 材料与方法
1.1 主要试剂与仪器
NDMA及NDMA-d6标准溶液,由Dr. Ehrenstorfer GmbH提供;Cd(Ⅱ)、Hg(Ⅱ)和Pb(Ⅱ)标准溶液,国家有色金属及电子材料分析测试中心;二氯甲烷、正己烷、甲醇为色谱纯,天津福晨;二甲胺盐酸盐、亚硝酸钠、氯化钠为分析纯,国药集团;胃蛋白酶,Sigma公司;水由Milli Q超纯水机制备.
气相色谱-质谱联用仪(GC/MS):Trace DSQ (Thermo);色谱柱:DB-1701(30 m×0.25 mm×0.25 μm,Agilent J&W).
1.2 实验方法
1.2.1 NDMA检测的GC/MS条件[12]进样口温度:200 ℃;离子源温度:250 ℃;传输线温度:230 ℃;载气流速:1.0 mL·min-1;进样模式:不分流;程序升温方法:初始温度为45 ℃,保持5 min,再以10 ℃·min-1速率升高至200 ℃,保持5 min.溶剂延迟时间:3.50 min;Full Scan扫描范围:20~300;SIM碎片离子选择:74,42,28,80;进样量:1 μL;EI源电子轰击能量:70 eV.
1.2.2 NDMA形成的反应过程 空白组:向试管中加入6 mL pH 2.0的盐酸,浓度为20 g·L-1的氯化钠溶液1 mL,浓度为32 g·L-1的胃蛋白酶溶液1 mL,50 mmol·L-1的DMA溶液1 mL,50 mmol·L-1的亚硝酸钠溶液1 mL,用4 mol·L-1盐酸调节溶液至pH 2;实验组:向试管中依次加入5 mL pH 2.0的盐酸,浓度为20 g·L-1的氯化钠溶液1 mL,浓度为32 g·L-1的胃蛋白酶溶液1 mL,50 mmol·L-1的DMA溶液1 mL,50 mmol·L-1的亚硝酸钠溶液1 mL,重金属溶液1 mL,用4 mol·L-1盐酸调节至pH 2.将空白体系和实验体系置于37 ℃水浴中反应2 h.
1.2.3 样品处理 反应结束后,取出样品,加入内标.将其上样于预先用甲醇活化好的固相萃取柱,上样完毕后,彻底抽干;用正己烷淋洗一遍;最后用二氯甲烷洗脱并定容至3 mL,待测.
1.3 理论计算方法
本文运用密度泛函理论(DFT), 在B3LYP/6-311+G(d,p)/LANL2DZ水平上[13-15]分别对重金属离子与亚硝酸以及重金属离子与DMA反应中的反应物、中间体、过渡态和产物进行了几何结构的全优化,同时在此水平上计算了各驻点的振动频率,确认所得到的构型是无虚频的稳定点或有且仅有一个虚频的过渡态;并通过内禀反应坐标(IRC)的计算,确定了过渡态是连接反应物和产物的最低能量途径.本文所有计算均利用Gaussian A03[16]程序完成.
2 结果与讨论
2.1 重金属离子对NDMA形成的影响
对不同浓度的重金属离子(0.005、0.01、0.1和1.0 mg·L-1)对模拟胃液中5 mmol·L-1二甲胺和5 mmol·L-1亚硝酸钠形成NDMA的影响进行了研究,所得数据如表2和图1所示.

表2 重金属Cd、Hg、Pb离子与NDMA的促进率
从表2可以看出,当体系中加入Cd(Ⅱ)、Hg(Ⅱ)和Pb(Ⅱ)溶液时,NDMA的生成量较空白实验有一定的增加,这表明上述3种重金属离子均对NDMA的形成具有促进作用.当Cd(Ⅱ)浓度为0.005、0.01、0.1和1.0 mg·L-1时,NDMA的促进率分别为3.8%、8.0%、12.7%和19.9%,表明随Cd(Ⅱ)浓度的增加,其对NDMA的促进率也明显增大,由此可见Cd(Ⅱ)的浓度与其对NDMA促进率间存在着正相关.

图1 不同浓度下的3种重金属离子对于模拟胃液中NDMA形成的影响Fig.1 The effect of three different concentration heavy metal ions on NDMA formation in SGF
如图1所示,Hg(Ⅱ)与Cd(Ⅱ)呈现相同的趋势,Hg(Ⅱ)的浓度同样与NDMA形成的促进率呈现正相关的关系.1.0 mg·L-1的Hg(Ⅱ)促进NDMA形成的促进率最大,为27.90%.比较相同浓度下Cd(Ⅱ)和Hg(Ⅱ)对NDMA形成的促进率发现,Hg(Ⅱ)的促进率比Cd的高.而Pb(Ⅱ)与Cd(Ⅱ)和Hg(Ⅱ)不同,随着体系中Pb(Ⅱ)浓度的升高,NDMA形成的促进率呈现不断降低的趋势.当Pb(Ⅱ)的浓度低至0.005 mg·L-1时,促进率达到最大值13.8%.上述结果表明最大促进率的顺序为Hg(Ⅱ)>Cd(Ⅱ)>Pb(Ⅱ),然而当浓度最低时,3种重金属离子的促进率顺序为Pb(Ⅱ)>Hg(Ⅱ)>Cd(Ⅱ).但其中最大促进率(27.9%)远远小于Schreiber[11]等报道的Cu(Ⅱ)对NHCl2和DMA反应体系中NDMA形成的促进率(80%).
2.2 重金属离子与DMA结合产物的理论研究
本文运用密度泛函理论(DFT)对重金属离子与DMA相互作用的产物M-DMA及重金属离子与亚硝酸相互作用的产物M-HNO2进行了研究.Herrera[17]等人报道金属离子Cu(Ⅱ) 与Zn(Ⅱ)能与胺分子上氮原子发生配位作用,结合形成金属离子与胺分子的四配位体,Kecht[18]认为金属离子与胺分子能形成稳定的平面正方形和四面体复合物.
2.3重金属离子与DMA/HNO2结合产物结合能的理论研究
为探讨实验中重金属离子的促进作用,首先需要清楚重金属离子是先与DMA还是与HNO2作用.为此,作者研究了重金属离子和DMA分子及亚硝酸分子之间的相互作用.M-DMA和M-HNO2中间体的反应能量和结合能列于表3.考虑到实际溶液体系中多种离子的存在及离子氛的作用,真实的金属离子的键能可能会远低于计算值.

表3 B3LYP/6-311+G(d,p)和LANL2DZ水平上计算得到的金属离子与DMA或HNO2结合反应焓变、自由能变和产物的结合能,单位:kJ·mol-1
由表3可知,重金属离子与DMA和亚硝酸之间相互作用的反应均为放热过程.重金属Cd(Ⅱ), Hg(Ⅱ), Pb(Ⅱ)与DMA分子配位生成的MNH(CH3)2(Ⅱ) 中间体结合能分别为500.4, 569.0和417.1 kJ·mol-1,而重金属与亚硝酸生成的M(ONOH)中间体结合能分别为284.5, 309.2 和248.5 kJ·mol-1.这清楚地表明,M-DMA的焓变和自由能变均比M-NO2相应的焓变和自由能变要低,而重金属离子与DMA中间体结合能比重金属与亚硝酸中间体结合能高出约160 ~ 250 kJ·mol-1.
可见,重金属离子与DMA之间相互作用远比与亚硝酸的作用要强,而且M-DMA中间体的稳定性也远比M-HNO2中间体强.这表明在热力学上,重金属离子更容易与DMA反应而不是亚硝酸.由此,可以推测重金属离子很可能是通过先与二甲胺作用,形成反应活性比二甲胺更强的中间体,更易发生亚硝化反应,从而促进NDMA的形成.
2.4 重金属离子与DMA结合产物与亚硝酸反应生成NDMA的理论研究
基于前面的研究,发现重金属离子更容易与DMA结合生成稳定的中间体,因此,继续研究此中间体如何与亚硝酸反应生成NDMA.研究发现,重金属离子与DMA结合的中间体M-NH(CH3)2可以通过先失去一个氢质子后与亚硝酸反应.反应中的反应物配合物(CP1)、过渡态(TS1)和产物配合物(TM1)的结构如图2所示.MN(CH3)2+与亚硝酸反应过程中的焓变、自由能变和反应能垒的数据列于表4中.
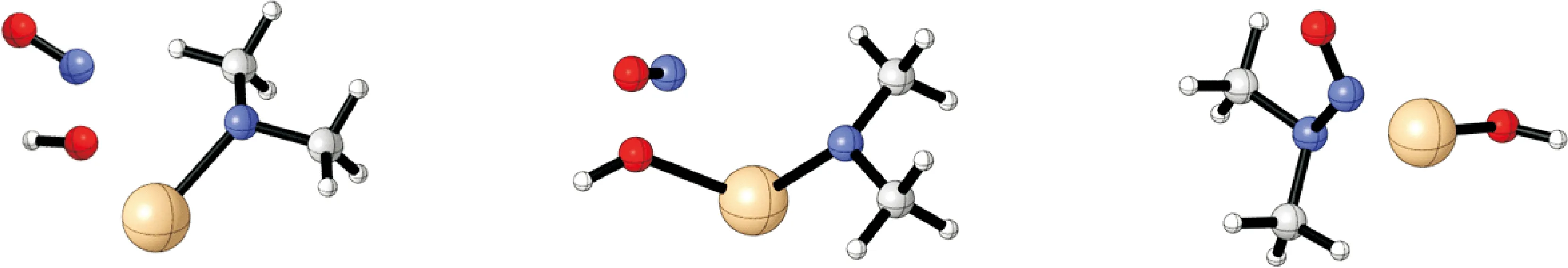
CP1 TS1 TM1
从图2中可看出,反应物配合物(CP1)中亚硝酸中的OH基团通过慢慢接近重金属离子,与其发生键合形成M-OH键,ON基团与MOH中的O原子相互作用,形成如TS1所示的过渡态.此过渡态中的ON基团通过迁移,与M-N(CH3)2中的N原子发生相互作用,进而键合形成NDMA,与此同时M-N键断裂,导致M(OH)+离子生成.

表4 B3LYP/6-311+G(d,p)和LANL2DZ水平上计算得到的与亚硝酸反应的热力学数据 单位:kJ·mol-1
如表4所示,对于Cd,Pb和Hg 3种重金属离子的配合物MN(CH3)2+都能与亚硝酸反应生成NDMA,而且反应都是放热过程,反应热分别为-61.06、-70.72和-34.00 kJ·mol-1,这些反应的自由能变分别为-56.58,-57.46和-26.18 kJ·mol-1,可见此反应在热力学上可自发进行.根据过渡态理论,Cd,Pb和Hg 3种重金属离子的络合物与亚硝酸反应的能垒分别为21.24,14.55和41.40 kJ·mol-1,而反应的自由能活化能为30.44,24.42和53.95 kJ·mol-1.作者课题组以前的计算结果[19]表明,DMA直接与亚硝酸反应的能垒高于130 kJ·mol-1,而本文的计算结果发现,重金属参与后的这些反应的能垒和自由能活化能都明显降低.可见,重金属离子与DMA结合的配合物较容易与亚硝酸反应生成NDMA.因此,可以推测重金属离子很可能是通过与DMA作用,生成活性更强的中间体,更易发生亚硝化反应,从而促进NDMA的形成.
3 结论
本文研究了重金属离子Cd(Ⅱ),Hg(Ⅱ)和Pb(Ⅱ)在模拟胃液中对NDMA形成的影响,研究发现3种重金属离子均能促进NDMA的形成,其最大促进率的顺序为Hg(Ⅱ)>Cd(Ⅱ)>Pb(Ⅱ);但当浓度为0.005 mg·L-1时,Pb(Ⅱ) 表现出最大的促进率(13.8%).运用DFT方法研究了重金属离子与DMA和亚硝酸的作用,结果表明重金属离子与DMA之间存在比亚硝酸更强烈的相互作用,M-DMA中间体的稳定性也远强于M-HNO2中间体.DFT的深入研究发现重金属离子与DMA形成的配合物,较容易与亚硝酸反应,反应的活化能低于42 kJ·mol-1,且为放热反应.由此可以推测,金属离子很可能是通过先与二甲胺作用,形成反应活性比二甲胺更强的中间体,更易发生亚硝化反应,从而促进了NDMA的形成.
[1] 谢黎虹, 许梓荣. 重金属镉对动物及人类的毒性研究进展[J]. 浙江农业学报, 2003,15(6):376-381.
[2] 王志平, 王凤英, 乌日娜. 重金属汞的污染与危害[J]. 集宁师专学报, 2006,28(4):70-71.
[3] 贾广宁. 重金属污染的危害与防治[J]. 有色矿冶, 2004,20(1):39-42.
[4] SHARMA R K, AGRAWAL M, MARSHALL F M. Heavy metals in vegetables collected from production and market sites of a tropical urban area of India[J]. Food Chem Toxicol, 2009,47(3):583-591.
[5] GB 2762-2005. 食品中污染物限量 [S]. 2005.
[6] GB 5749-2006. 生活饮用水卫生标准 [S]. 2006.
[7] 曾瑶池, 胡敏予. 叶黄素、番茄红素与黄斑变性研究进展[J]. 中华肿瘤防治杂志, 2008,15(2):151-155.
[8] IARC monographs on the evaluation of the carcinogenic risk of chemicals to humans. Some N-nitroso compounds[M]. Lyon: IARC Press, 1978.
[9] United States Environmental Protection Agency IRIS database[DB]. 1993. http://www.epa.gov/ncea/iris/subst/0045.htm (accessed May 15, 2012).
[10] TRICKER A R. N-nitroso compounds and man: sources of exposure, endogenous formation and occurrence in body fluids[J]. Eur J Cancer Prev, 1997, 6(3): 226-268.
[11] SCHREIBER I M, MITCH W A. Nitrosamine formation pathway revisited: the importance of chloramines speciation and dissolved oxygen[J]. Environ Sci Technol, 2006,40(19):6007-6014.
[12] 周 全. 几种天然产物及镉、铅、汞离子对N-亚硝基二甲胺形成影响的研究[D]. 北京:北京工业大学, 2012.
[13] BECKE A D. Density-functional thermochemistry. Ⅲ. The role of exact exchange[J]. J Chem Phys, 1993,98(7):5648-5652.
[14] LEE C, YANG W T, PARR R G. Development of the colle-salvetti correlation-energy formula into a functional of the electron-density[J]. Phys Rev B, 1988,37:785-789.
[15] FRISCH M J, POPLE J A, BINKLEY J S. Self-consistent molecular-orbital methods. 25. Supplementary functions for gaussian-basis sets[J]. J Chem Phys, 1984,80(7):3265-3269.
[16] FRISCH M J, TRUCKS G W, SCHLEGEL H B,etal. Gaussian 03[CP].Gaussian, Inc, Pittsburgh PA, 2003.
[17] HERRERA A M, STAPLES R J, KRYATOV S V,etal. Nickel(Ⅱ) and copper(Ⅱ) complexes with pyridine-containing macrocycles bearing an aminopropyl pendant arm: synthesis, characterization, and modifications of the pendant amino group[J]. Dalton Trans, 2003(5):846-856.
[18] KECHT J, MINTOVA S, BEIN T. Nanosized zeolites templated by metal-amine complexes[J]. Chem Mater, 2007,19(6):1203-1205.
[19] 闾春林, 刘永东, 钟儒刚. 二甲胺与亚硝酸反应生成N,N-二甲基亚硝胺的理论研究[J]. 化学学报, 2007,65(16):1568-1572.
(编辑 杨春明)
An Experimental and Theoretical Investigation of Effect of Heavy Metal Ions on Carcinogenic NDMA Formation
ZENGTing,LIUYa-meng,LIUYong-dong*
(College of Life Science and Bioengineering, Beijing University of Technology, Beijing 100124, China)
Heavy metal ion contamination has caused severe threats to environment and human body. N-Nitrosodimethylamine(NDMA), as a potent carcinogen, has drawn much attention. In the present study, the influence of heavy metal ions including Cd(Ⅱ), Hg(Ⅱ), and Pb(Ⅱ) on NDMA formation in simulated gastric fluid and the possible reaction mechanisms were investigated from both experimental and theoretical aspects. The experimental results indicate that NDMA formation can be promoted by above heavy metal ions. DFT calculations indicate that there are much stronger interaction of heavy metal ions with dimethylamine(DMA) than those of heavy meal ions with nitrite. Moreover, the intermediates of heavy metal ions with DMA can first release a proton, and then react with nitrous acid to form NDMA. This reaction is an exothermal process and its energy barrier is relatively low, from which it can be predicted that heavy metal ions are bound to react with DMA to facilitate the formation of NDMA.
heavy metal ions; NDMA formation; promotion effect; DFT
2014-05-19
北京市自然科学基金资助项目(8132015);北京市强教人才拔尖创新人才资助项目(CIT & TCD201304057)
*
,E-mail:ydliu@bjut.edu.cn
O641
A
1000-2537(2014)06-0042-05
