微波合成介孔有机-无机互穿网络材料中金催化中心的构建
2014-12-22彭建兵曹志峰喻宁亚
彭建兵,李 晔,曹志峰,喻宁亚*
(1.顺德职业技术学院,中国顺德 528300;2.湖南师范大学湖南省资源精细化与先进材料重点实验室,中国长沙 410081)
纳米金催化剂在许多重要的选择性氧化反应中显示了优异的催化性能[1-6],然而尺寸极小的金粒子具有较大的表面自由能和较低的熔点[7],在没有空间阻隔的情况下会发生快速的自身聚集使得金粒子尺寸急剧增大,从而失去催化活性.因此,纳米金催化剂中载体的物理化学性质,如结构组成,对金物种的亲和力及金粒子与载体之间的相互作用等对最终纳米金催化剂的催化活性及稳定性起着关键作用.与传统的纳米金催化剂载体,如金属氧化物或活性碳相比,介孔材料具有较规则的孔道结构,而且织构性质高度可控.更为重要的是,介孔材料有可裁剪的表面及结构,可根据需求来合成任务特定型的材料,这为合理设计合成纳米金催化剂载体提供了可能[8-12].作者在此之前合成了一种含离子液体片段和硫醚的桥接有机硅前躯体[13]并将其复合到介孔材料中,由于含硫有机组分在材料中均匀分布,金纳米粒子可以在其中高度分散,所得纳米金催化剂在以双氧水为氧化剂的烯烃环氧化反应中表现出了极高的催化活性和稳定性.然而,上述催化剂中含离子液体片段和硫醚的桥接有机硅前躯体合成十分复杂而且金锚点性质单一[14,15],催化剂的催化活性与催化剂稳定性相互制约.最近,作者结合螯合树脂与介孔材料在贵金属富集分离的优势,合成了一系列新型的三聚氰胺-甲醛-硫脲树脂/SBA-15 复合材料.在30 ℃下,该复合材料对Au(ⅡI)的饱和吸附量达到3.04 mmol·g-1[18],这暗示此类材料可能是很好的纳米金催化剂的载体.
本文利用廉价的三聚氰胺、甲醛、硫脲为原料,合成了含极性基团的三聚氰胺-硫脲树脂低聚物(有机网络),将其与水玻璃(无机网络)缩聚,在模板剂P123 作用下,以微波加热共水解-缩聚一步合成了介孔有机-无机互穿网络材料.利用材料孔道表面的硅羟基为还原剂及三聚氰胺和硫脲上的氮原子和硫原子对金纳米粒子的稳定作用成功制备了相应的负载型纳米金催化剂.研究了所得催化剂在苯乙烯环氧化反应中的催化性能,系统考察了催化剂的用量、反应时间和温度、氧化剂用量等反应条件对苯乙烯环氧化反应的影响,并考察了催化剂的重复使用性能.
1 实验部分
1.1 试剂
实验中所使用的试剂有甲醛(分析纯,湖北奥生新材料科技有限公司),硫脲(分析纯,天津市恒兴化学试剂制造有限公司),冰醋酸(分析纯,天津市恒兴化学试剂制造有限公司),甲醇(分析纯,天津市恒兴化学试剂制造有限公司),三聚氰胺(分析纯,天津市博迪化工有限公司),水玻璃(Sigma-Aldrich),P123(EO20PO70EO20,Aldrich),氢氧化钠(分析纯,天津市化学试剂三厂),苯乙烯(分析纯,国药集团化学试剂有限公司),乙腈(分析纯,天津市大茂化学试剂厂),四水合氯金酸(分析纯,国药集团化学试剂有限公司).
1.2 负载型纳米金催化剂的制备
在60 ℃下,称取6.00 g P123 溶解于60 mL 去离子水形成溶液A.将12.5 mL 质量分数37%的甲醛水溶液与62.5 mL 去离子水混合,以0.5 mol·L-1的氢氧化钠水溶液调整溶液pH 值在8.5~9.0,然后加入3.75 g 三聚氰胺和2.28 g 硫脲,于60 ℃下搅拌2 h.将溶液A 倒入上述溶液,搅拌2.5 h,得到溶液B.在溶液B 搅拌期间,将13.5 g 水玻璃溶于150 mL 去离子水,在室温下搅拌约30 min,得到溶液C.在溶液B中快速倒入2.85 mL 冰醋酸,剧烈搅拌下,马上倒入溶液C,将所得混合液于60 ℃下搅拌1 h 后,再在60℃微波加热6 h,过滤,干燥,乙醇索氏抽提48 h,即得到含氮和硫的介孔有机-无机互穿网络材料.取500 mg 上述制得的样品分散在20 mL 去离子水中,在30 ℃下逐滴加入25 mL 的HAuCl4水溶液(0.24 mol·L-1,用1 mol·L-1NaOH 调节pH 值至7~8),搅拌24 h,过滤,真空干燥,得到含金的样品.
1.3 样品的表征
用Avatar 370 FT-IR 型红外光谱仪测定样品的红外光谱图,选择波数范围在4 000~400 cm-1内,分辨率为4 cm-1.以Micromeritics Tristar 3000 型物理吸附仪测试样品的比表面积及孔径分布,吸附温度为液氮温度-196 ℃,通过BET 方法计算样品比表面积,由等温线吸附支通过BJH 模型计算样品孔径分布.将所合成的催化剂在JEM-2010 型透射电镜上进行观察,以分析催化活性中心金纳米粒子的粒径大小和分散度.用Thermo ICAP 6300 型电感耦合等离子体发射光谱仪测定所合成的催化剂中的金的含量.用Vario EL CUBE 型元素分析仪测定样品中氮和硫元素的含量.
1.4 催化剂性能评价
以100 mL 三颈圆底烧瓶为反应器,准确称取50 mg 催化剂,加入1.04 g(10 mmol)的苯乙烯和5 mL乙腈,然后接上回流冷凝管和pH 计,混合物在磁力搅拌下缓慢加热至60 ℃,然后逐滴加入3.4 mL 30 %的H2O2(30 mmol)与10 mL 甲醇的混合溶液,在滴加混合溶液的同时不断地用1 mol·L-1的氢氧化钠水溶液调节反应溶液的pH 至9.0~9.5.反应8 h 后将溶液冷却至室温然后离心分离.产物经GC-MS(HP 5790)及Agilent Technologies 6890 N 气相色谱分析.使用后的催化剂用无水乙醇洗涤数次,真空干燥后重复使用.
2 结果及讨论
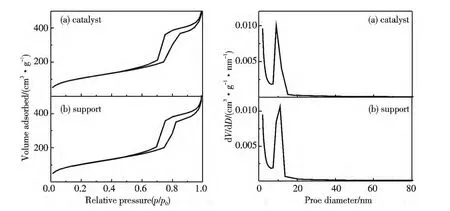
图1 催化剂(a)与载体(b)的N2 吸附-脱附等温线(左)及孔径分布曲线(右)Fig.1 Nitrogen adsorption-desorption isotherm(left)and pore distribution(right)of the catalyst(a)and support(b)
2.1 样品的表征
图1 是负载型纳米金催化剂及其载体的N2吸附-脱附等温线及孔径分布曲线.由图可见,纳米金催化剂和载体都具有典型介孔材料特征的IV 型吸附-脱附等温线,在N2相对压力p/p0=0.7~0.85 处有一个明显的毛细凝聚突跃,并且还具备SBA-15 型介孔材料的H1型滞后环,这些结果表明催化剂和载体具有有序的介孔结构.对比催化剂和载体的织构参数(见表1),催化剂的比表面积和孔体积相对载体有明显的降低,而且,孔径从11.0 nm 减小到10.6 nm.这些结果说明,金纳米粒子已经成功引入载体介孔中.根据ICP 的结果,催化剂中金的质量分数为2.1%.

表1 负载型纳米金催化剂及其载体的物化性质Tab.1 Physicochemical properties of the catalyst and the corresponding support
图2 为三聚氰胺和载体的红外谱图.通过比较可以看出两个谱图都在1 531 cm-1,1 456 cm-1处出现属于 C==N 的伸缩振动峰.三聚氰胺中3 380 cm-1的—NH2吸收峰在载体中消失了,说明载体的合成过程中,三聚氰胺与甲醛发生了缩聚反应,形成了有机网络.此外,载体在3 475 cm-1出现了—OH 的吸收峰,在1 146 cm-1出现了Si—O—Si 的吸收峰.

图2 三聚氰胺及载体的FT-IR 图谱Fig.2 FT-IR spectra of the support and melamine
为了更进一步探究催化剂中有机网络和无机网络是通过何种方式掺杂在一起的,将载体进行了如下处理:称取0.5 g载体于550 ℃在空气气氛下煅烧1 h,从而完全除去催化剂中的有机组分,然后将剩下的无机组分进行N2吸附-脱附测试,所得N2吸附-脱附等温线及孔径分布曲线见图3.载体焙烧后的无机组分具有典型介孔材料特征的IV 型吸附-脱附等温线,在N2相对压力p/p0=0.7~0.9 处有一个明显的毛细凝聚突跃,并具备SBA-15 型介孔材料的H1型滞后环,这些结果表明,载体在去除有机网络后依然具有有序的介孔结构.此外,N2吸附-脱附结果显示,焙烧后载体的比表面积为718 m2·g-1,孔容为1.25 cm3·g-1,相比焙烧前显著地增大.值得指出的是,焙烧后载体的孔径大小为11.0 nm,没有变化.TEM 分析表明负载型纳米金催化剂具有发达的介孔空隙,而且没有观察到有机物的积聚体杂相(见图4a).结合N2吸附-脱附分析中载体焙烧前后载体孔径不变,比表面积和孔容增加的结果,可以推断催化剂中有机网络和无机网络形成了互穿网络.

图3 焙烧后载体的N2 吸附-脱附等温线(左)及孔径分布曲线(右)Fig.3 Nitrogen adsorption-desorption isotherms(left)and pore size distribution(right)of the support after calcination
从图4 还可以看出,负载型纳米金催化剂具有规则的六方孔道结构(图4a 为110 晶面,图4b 为001 晶面),金纳米粒子均匀分布在载体的介孔孔道内(见图4b 白圈处),金纳米粒子的直径为3 nm 左右.这表明合成的介孔有机-无机互穿网络材料是良好的金纳米粒子载体,其中金纳米粒子能在载体上高度分散.

图4 负载型纳米金催化剂的TEM 图Fig.4 TEM images of the supported GNP catalyst
2.2 催化性能研究
2.2.1 反应温度对苯乙烯环氧化反应的影响 表2 为反应温度对苯乙烯环氧化反应的影响.从表中可以看出,反应温度对苯乙烯环氧化反应影响较大.随着温度的上升,苯乙烯的转化率逐渐升高.但是环氧苯乙烷的选择性却先升后降,在60 ℃时达到最高值.因此60 ℃是苯乙烯环氧化反应的最佳温度.

表2 反应温度对苯乙烯环氧化的影响aTab.2 Effect of reaction temperature on epoxidation of styrenea
2.2.2 反应时间对苯乙烯环氧化反应的影响 表3 为反应时间对苯乙烯环氧化反应的影响.可以看出,随着反应时间的延长,苯乙烯的转化率逐渐提高,而环氧苯乙烷的选择性基本无变化.当反应时间超过8 h后,环氧苯乙烷的选择性开始下降.考虑到反应时间为8 h 时苯乙烯转化率已经达到98 %,因而选择8 h为最佳反应时间.
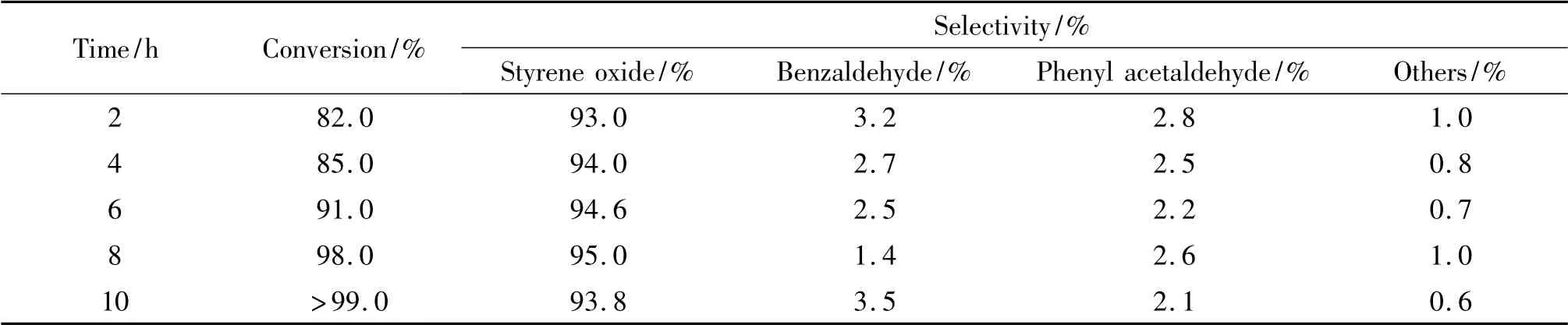
表3 反应时间对苯乙烯环氧化的影响aTab.3 Effect of reaction time on epoxidation of styrenea
2.2.3 催化剂用量的影响 表4 为催化剂用量对苯乙烯环氧化反应的影响.从表中可以看出不加催化剂时,苯乙烯也存在一定程度的转化,苯乙烯转化率为30.0%,环氧苯乙烷的选择性为75.0%,这主要是由于Payne 反应的存在[16].加入纳米金催化剂后,苯乙烯的转化率有了明显提高.当催化剂用量从30 mg 增加到50 mg 时,由于催化氧化活性位的增加,苯乙烯的转化率会相应地升高;但是增加催化剂用量至100 mg,反应活性却出现了一定程度的下降.这是因为金纳米粒子的表面可以促使双氧水的分解[17],以至于双氧水不能充分利用到环氧化反应中,因此过多的催化剂也不利于催化苯乙烯环氧化反应的进行.

表4 催化剂用量对苯乙烯环氧化的影响aTab.4 Effect of catalyst amount on epoxidation of styrenea
2.2.4 氧化剂H2O2用量的影响 表5 为氧化剂用量对苯乙烯环氧化反应的影响.当氧化剂H2O2与苯乙烯摩尔比从1.0 增加到3.0 时,苯乙烯的转化率从38.7 %增加到98.0 %,而环氧苯乙烷产物的选择性也从88.7%增加到95.0%.当进一步增大H2O2的用量时,反应的转化率略有增加,而选择性下降.因而氧化剂H2O2与苯乙烯的优化摩尔比为3.0.

表5 氧化剂用量对苯乙烯环氧化的影响aTab.5 Effect of amounts of oxidant on epoxidation of styrenea
2.2.5 催化剂的重复使用性 催化剂经离心后用无水乙醇洗涤3~4 次室温下真空干燥得到再生催化剂,再进行催化剂重复使用性的考查.从图5 结果可以看到,前5 次随着重复使用的次数的增加苯乙烯的转化率和环氧苯乙烷的选择性基本不变,催化剂使用5 次过后,苯乙烯的转化率和环氧苯乙烷的选择性下降.ICP 结果显示催化剂使用6 次后,催化剂中金的质量分数由2.1%下降到了1.4%,因而金纳米粒子的流失导致了催化剂在使用5 次后催化活性的下降.介孔有机-无机互穿网络载体制备中三聚氰胺与硫脲的物质的量之比为1∶1,而元素分析仪测定的N 和S 元素含量表明最终载体中的三聚氰胺与硫脲的物质的量之比为5∶1.这表明在介孔有机-无机互穿网络载体合成过程中,硫脲进入载体的量较少.由于元素S 相对于元素N 而言,对金物种有更强的亲和力,因而最终载体中较低的S 含量可能是催化剂重复使用5 次后金纳米粒子流失的原因.

图5 催化剂在苯乙烯环氧化反应中的重复使用结果Fig.5 Reuse results of the catalyst in epoxidation of styrene
3 结论
本文利用互穿聚合物网络理念以P123 为模板剂,三聚氰胺、硫脲和水玻璃为原料,采用微波加热共水解-缩聚法一步合成了有机-无机互穿网络介孔材料,并以此为载体制备了纳米金催化剂.以双氧水为氧化剂的苯乙烯环氧化为探针反应,考察了反应时间、反应温度、催化剂用量、氧化剂用量对所得纳米金催化剂催化性能的影响.得出的最佳反应条件为:反应时间8 h、反应温度60 ℃、催化剂用量50 mg、氧化剂用量为底物物质的量比的3 倍.此时,苯乙烯的转化率可达98%,产物环氧苯乙烷的选择性可达95%.且催化剂可重复使用5 次而保持催化效果基本不变.
[1]HUANG J,HARUTA M,TOMOKI A,et al.Propene epoxidation with dioxygen catalyzed by gold clusters[J].Angew Chem Int Ed,2009,48(42):7862-7866.
[2]AJAIKUMAR S,AHLKVIST J,LARSSON W,et al.Oxidation of α-pinene over gold containing bimetallic nanoparticles supported on reducible TiO2by deposition-precipitation method[J].Appl Catal A,2011,392(1-2):11-18.
[3]EDWARDS J K,HUTCHINGS G J,SOLSONA B E,et al.Direct synthesis of hydrogen peroxide from H2and O2using TiO2-supported Au-Pd catalysts[J].J Catal,2005,236(1):69-79.
[4]MIYAMURA H,MATSUBARA R,MIYAZAKI Y,et al.Aerobic oxidation of alcohols at room temperature and atmospheric conditions catalyzed by reusable gold nanoclusters stabilized by the benzene rings of polystyrene derivatives[J].Angew Chem Int Ed,2007,46(22):4151-4154.
[5]CHEN L F,RICHARDS R,HU J C.Intercalation of aggregation-free and well-dispersed gold nanopar-ticles into the walls of mesoporous silica as a robust“green”catalyst for nalkane oxidation[J].J Am Chem Soc,2009,131(3):914-915.
[6]HEREIJGERS B P C,WECKHUYSEN B M.Aerobic oxidation of cyclohexane by gold-based catalysts:New mechanistic insight by thorough product analysis[J].J Catal,2010,270(1):16-25.
[7]BARTHOLOMEW C H.Sintering kinetics of supported metals:new perspectives from a unifying GPLE treatment[J].Appl Catal A,1993,107(1):1-57.
[8]KIMURA T,KURODA K,SUGHARA Y,et al.Esterification of the silanol groups in the mesoporous silica derived from kanemite[J].Porous Mater,1998,5(2):127-132.
[9]BURKETT S L,SIMS S D,MANN S,et al.Synthesis of hybrid inorganic-organic mesoporous silica by co-condensation of siloxane and organosiloxane precursors[J].Chem Commun,1996(11):1367-1368.
[10]SIMS S D,BURKETT S L,MANN S,et al.Direct preparation of organically modified MCM-type materials.Preparation and characterization of aminopropyl-MCM and 2-cyanoethyl-MCM[J].Chem Commun,1996,16:1961-1962.
[11]LIM M H,BLANFORD C F,STEIN A,et al.Synthesis and characterization of a reactive vinyl-functionalized MCM-41:probing the internal pore structure by a bromination reaction[J].J Am Chem Soc,1997,119(17):4090-4091.
[12]BABONNEAU F,LEITE L,FONTLUPT S,et al.Structural characterization of organically-modified porous silicates synthesized using CTA+surfactant and acidic conditions[J].J Mater Chem,1999(9):175-178.
[13]YU N Y,DING Y,LUO A Y,et al.Gold nanoparticles supported on periodic mesoporous organosilicas for epoxidation of olefins:effects of pore architecture and surface modification method of the supports[J].Micropor Mesopor Mater,2011,143(2-3):426-434.
[14]JIN Y,ZHUANG D,YU N,et al.Epoxidation of styrene over gold nanoparticles supported on organic-inorganic hybrid mesoporous silicas with aqueous hydrogen peroxide[J].Micropor Mesopor Mater,2009,126(1-2):159-165.
[15]JIN Y,WANG P,YIN D,et al.Gold nanoparticles stabilized in a novel periodic mesoporous organosilica of SBA-15 for styrene epoxidation[J].Micropor Mesopor Mater,2008,111(1-3):569-576.
[16]PAYNE G B,DEMING P H,WILLAMS P H,et al.Reactions of hydrogen peroxide.VⅡ.alkali-catalyzed epoxidation and oxidation using a nitrile as co-reactant[J].J Org Chem,1961,26(3):659-663.
[17]SUH M,BAGUS P S,PAK S,et al.Reactions of hydroxyl radicals on titania,silica,alumina,and gold surfaces[J].J Phys Chem B,2000,104(12):2736-2742.
[18]黄 毅,廖九英,喻宁亚,等.三聚氰胺-甲醛-硫脲树脂/SBA-15 复合材料的合成及其对水溶液中Au(ⅡI)吸附性能的研究[J].湖南师范大学自然科学学报,2013,36(2):56-63.
