莲心碱固体分散体的制备工艺研究
2014-06-12彭买姣吴婷婷
唐 婷,彭买姣,周 江,吴婷婷,桂 卉*
(湖南省教育厅中药现代化重点实验室,湖南中医药大学药学院,湖南 长沙 410208)
莲心碱固体分散体的制备工艺研究
唐 婷,彭买姣,周 江,吴婷婷,桂 卉*
(湖南省教育厅中药现代化重点实验室,湖南中医药大学药学院,湖南 长沙 410208)
目的 优选莲心碱固体分散体最佳制备工艺并考察其质量。方法 以莲心碱的累积溶出率为评价指标,通过单因素试验优选出制备莲心碱固体分散体的载体及方法;采用正交试验设计,确立固体分散体的最佳制备工艺;采用高效液相测定其载药量,并对其释药特性进行考察。结果 莲心碱固体分散体的最适分散载体为聚乙烯吡咯烷酮(PVP);最佳制备方法为溶剂法;莲心碱固体分散体的最佳制备工艺为:药物与载体比例为1∶1;吸附时间为30 min;溶剂量30 mL。结论 将莲心碱制备成固体分散体能提高其溶解度,为莲心碱相关制剂的研发提供实验依据。
莲心碱;固体分散体;制备工艺;溶解度
莲心碱是从中药莲子心中提取、分离得到的一种双苄基异喹啉类生物碱[1],药理实验证明莲心碱具有降压、抗心律失常、清除自由基、抗氧化、对抗血栓形成、降低血清总胆固醇等多种生理活性,具有良好的开发应用前景[2]。然而莲心碱在水中溶解度差,口服生物利用度较低,已经成为其临床应用的难题之一。已有研究表明,固体分散技术可提高药物的溶解度[3-4]。本实验以莲心碱的累积溶出百分率为评价指标,通过单因素实验筛选出莲心碱固体分散体的制备方法及载体材料;采用正交试验,优选出莲心碱固体分散体的最佳制备工艺,并对其释药特性及载药量进行考察,为莲心碱相关制剂的研发提供实验依据。
1 仪器与试药
1.1 仪器
Agilent HP 1200型高效液相色谱仪(Agilent公司);ZRS-8G型溶出仪 (天津大学无线电厂);756PC型紫外分光光度仪 (上海奥普勒有限公司);DF-101S型集热式恒温加热磁力搅拌器(巩义市予华有限责任有限公司);CP-114型电子分析天平(上海奥豪斯公司)。
1.2 试药
莲心碱原料药(含量为0.8%,批号HK-130121)华康生物技术公司;莲心碱对照品(上海源叶生物有限公司,HPLC≥98%,批号20121122);固体分散体载体材料:PEG 4000、PEG 6000(无锡市民丰试剂厂,批号:HG22-716-67)、聚乙烯吡咯烷酮 (PVP国药集团化学试剂有限公司)、Poloxamer188(上海源叶生物有限公司,批号KF0220Y13D);乙腈(GR,Tedia company);甲醇(GR,Tedia company);其他试剂均为分析纯,水为去离子水。
2 方法与结果
2.1 莲心碱固体分散体的制备
分别以PVP-K30、泊洛沙姆188、PEG4000、PEG6000为载体材料,采用不同的方法制备莲心碱固体分散体,药物与载体的质量之比为1∶3,即称取药物1 g,各载体材料3 g,制备固体分散体,并对其进行溶出度的测定,计算累积溶出百分率并进行比较。
2.1.1 溶剂法 按照以上处方称取莲心碱固体分散体与载体(1∶3),分别溶解于50 mL的甲醇中,超声10 min后混合,在水浴温度为60℃时,磁力搅拌20 min,蒸去多余的甲醇后,在40℃时抽真空干燥,粉碎后过80目筛。
2.1.2 熔融法 称取以上处方量的莲心碱提取物与载体(1∶3),先将载体置于蒸发皿中,水浴或者直火加热至完全熔化后,加入莲心碱提取物,长时间搅拌后,将熔融物倾倒在不锈钢板上成薄层,放置于冰箱中使之骤冷成固体,取出粉碎后过80目筛,40℃抽真空干燥。
2.1.3 研磨法 称取以上处方量的莲心碱提取物与载体(1∶3),将莲心碱提取物与载体混合后,强力持久地研磨1 h,过80目筛。
2.2 固体分散体中莲心碱的含量测定
2.2.1 标准曲线的绘制 在282 nm处[5],测定用pH6.8的缓冲液配置的不同浓度的莲心碱标准品的吸光度值,得标准曲线:Y=13.086X+0.0183,R2= 0.999 2。结果表明莲心碱标准品溶液在 0.005~0.03 mg/mL,浓度范围内线性关系良好。
2.2.2 溶出度测定 取制备的莲心碱固体分散体1 g,粉碎后,过80目筛,置于溶出度测定仪中,以pH6.8的缓冲液作为溶出介质,转速为100 r/min,当药物接触溶出液时开始计时,分别在0、3、8、10、20、30、45 min时取样7 mL,置于10 mL的容量瓶中,同时立即补加等量的溶出介质,于282 nm下测定其吸光度值,计算累积溶出百分率。
2.3 莲心碱固体分散体的工艺研究
2.3.1 固体分散体制备方法的选择 取PVP 3 g、莲心碱提取物1 g,分别采用溶剂法、研磨法、熔融法制备莲心碱固体分散体,以莲心碱的累积溶出百分率为评价指标。优选出莲心碱的制备方法。实验结果见图1。
由图1可知,当条件相同下,以溶剂法制备莲心碱固体分散体,其莲心碱的累积溶出率最大,且对莲心碱的增溶作用最强。
2.3.2 固体分散体载体考察 在相同条件下,取莲心碱提取物 1 g,PVP、Poloxmamer188、PEG4000、PEG6000各3 g,按照“2.1.1”中溶剂法制备固体分散体,通过测定各载体材料制备的固体分散体中莲心碱的溶吸光度值,求得累积溶出百分率,进行比较,优选出制备固体分散体的载体材料。由图2可知,莲心碱提取物与4种载体(PVP、Poloxamer188、PEG4000、PEG4000)制成固体分散体后,溶解度和溶出速率都有提高。相比之下以PVP为载体材料的固体分散体,对莲心碱提取物的体外溶出速率提高最大且较完全。由此可知以PVP为固体分散体的材料是最理想的,对莲心碱的增溶作用最强。

图1 不同方法制备莲心碱固体分散体的累积溶出百分率

图2 不同载体材料的莲心碱固体分散体累积溶出百分率
2.3.3 正交试验 根据上述“2.3.1”及“2.3.2”项单因素考察结果,采用溶剂法,选择PVP为固体分散体载体,以药物与载体比例、搅拌时间、甲醇的量为考察因素,以固体分散体中莲心碱累积溶出度为评价指标,用L9(34)正交表设计试验,所选因素水平及正交实验表见表1、表2,方差分析结果见表3。
由表2可知影响莲心碱固体分散体溶出的各因素的主次顺序为A(药物与载体的比例)>B(吸附时间)>C(甲醇的量),其中甲醇的量不具备统计学意义,考虑其最佳工艺条件为A1B3C3。由表3方差分析可知,其中A、B因素对莲心碱的溶出有显著的影响,具有统计学意义。其中药物与载体的比例对莲心碱的溶出有极显著的影响(P<0.01);药物与载体的吸附时间具有显著影响(P<0.05);甲醇的量对莲心碱的溶出影响不大(P<0.05),综合以上因素,确定莲心碱的最佳制备工艺处方为A1B3C3,即莲心碱与载体比例为1∶1;搅拌时间为30 min;甲醇的量为30 mL。

表1 固体分散体制备工艺因素表

表2 固体分散体正交试验方案与结果

表3 方差分析结果
2.4 验证试验
按照上述最佳优化条件,称取莲心碱1 g,PVP载体1 g,用30 mL甲醇溶解,磁力搅拌30 min后,挥干多余溶剂,40℃真空干燥,粉碎,过80目筛,制备固体分散体,测定其含量及累积溶出度,平行操作3份,结果见表4。
结果表明,优选出的工艺稳定可靠,重现性好。
表4 验证实验
2.5 载药量的测定
2.5.1 对照品溶液的制备 取莲心碱对照品5.5 mg,于25 mL容量瓶中加甲醇定容,配成浓度为0.22 mg/mL。
2.5.2 固体分散体及原料药样品的制备 取固体分散体和原料药材1 g,加入50 mL三氯甲烷回流提取30 min,浓缩回收三氯甲烷,残渣加入适量的甲醇溶解,置于10 mL的容量瓶中,加甲醇定容,用0.45 μm的微孔滤膜过滤。
2.5.3 色谱条件 色谱柱为Macherey-Nagel C18色谱柱 (4.6 mm×250 mm,5 μm);流动相为乙腈-0.015 mol/L十二烷基硫酸钠 (取十二烷基磺酸钠0.41 g加水100 mL使溶解)-冰醋酸 (56∶43∶1);流速为 1.0 mL/min,柱温为 30℃,检测波长为282 nm。色谱图见图3。
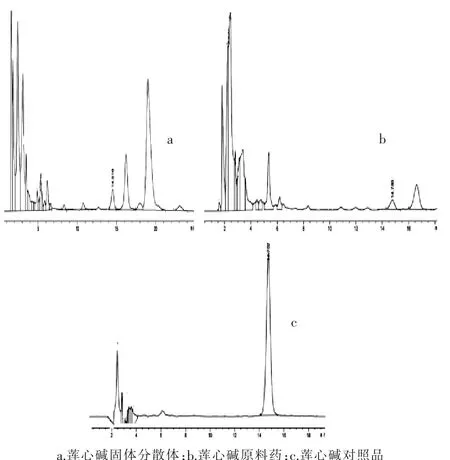
图3 莲心碱及其固体分散体HPLC图
2.5.4 莲心碱的含量测定及 PVP的载药量计算 采用“2.5.2”制备测试样品,按“2.5.3”条件测定莲心碱的含量,按下述公式计算PVP的载药量:载药量=固体分散体中莲心碱的量/载药固体分散体的量。结果3批固体分散体的载药量为 (5.4± 0.3)mg/g。
3 讨论
莲心碱是一种异喹啉生物碱,在水中的溶解度较低。一般来说,药物应根据其在胃肠道的吸收选择合适的的溶出介质,当溶出介质越接近胃肠道生理环境,越有望得到更好的体外相关性。故本实验使用了单因素筛选方法,以累积溶出百分率为指标,从以下几种介质中(人工胃液、水、pH为6.8及7.2的缓冲溶液)优选出最佳溶出介质,结果显示,pH6.8的溶出介质对莲心碱增溶最为明显。
目前尚未报道过将莲心碱制备成固体分散体以增加莲心碱的溶出度和生物利用度。本实验采用PVP为载体材料,使用溶剂法将莲心碱制备成固体分散体,能够显著增加莲心碱的溶出速率。经过预实验发现药物与载体的比例为1∶1时对莲心碱的增溶效果最好,当莲心碱与PVP的质量比为1∶1,吸附时间为30 min,溶剂的量为30 mL时,制备成的莲心碱固体分散体的累积溶出率最大。莲心碱固体分散体的载药性能较好,当载药量越大时,制剂的给药剂量也就越小,安全性也越好,优化处方后其PVP的载药量在(5.4±0.3)mg/g。在固体分散体的制备过程中,推测其载体PVP阻止或者延缓了莲心碱的晶型析出,使莲心碱形成较高能量的无定型物,使莲心碱保持高度分散状态。
[1]许 磊,姚崇舜,陈济明.莲心碱的研究概况[J].中草药,2000,31 (12):955-957.
[2]余万桂,邓德明,陈庭煊,等.莲心碱对大叔脑缺血/在灌注后TNF-a表达的影响[J].中药药理与临床,2009,25(1):16-18.
[3]平其能.现代药剂学[M].北京:中国医药科技出版社,2009:66-74.
[4]马世堂,刘培勋,徐 阳,等.难溶性药物增溶研究进展[J].医药导报,2009,28(8):1 052-1 054.
[5]胡学民,张先洲,蔡鸿生,等.莲心碱在兔体内药物动力学研究[J].中国中药杂志,1992,17(10):622-624.
(本文编辑 杨 瑛)
Optimization of Preparation Technology of Liensinine Solid Dispersions
TANG Ting,PENG Maijiao,ZHOU Jiang,WU Tingting,GUI hui*
(Key Laboratory of Hunan traditional Chinese Medicine modernization,School of Pharmacy,Hunan University of Chinese Medicine,Changsha,Hunan,410208,China)
Objective To optimize the the formulation of liensinine solid dispersions and study the characterization of the liensinine solid dispersions. Methods With the cumulative dissolution percentage of liensinine as the evaluation index.Investigated by single factor to select the best carrier and the best preparation;Orthogonal experiment design was used to establish the best prescription of solid dispersions;The drug loading was determined by HPLC analysis to investigate the drug release characteristics.Results The optimum carrier of liensinine solid dispersant is polyvinyl pyrrolidone(PVP);The best preparation method is the solvent;The best inclusion process is as follows:the ratio of drug and carrier:1:1;adsorption time:30 min; amount of solvent:30 mL.Conclusion The solid dispering can improve the solubility of liensinine. The experimentresearch lay the foundation ofliensinine related preparations and clinical application.
liensinine;solid dispersion;preparation technology;solubility
R943
A
10.3969/j.issn.1674-070X.2014.04.005.013.04
2013-10-23
湖南省科技计划项目(2013SK3100);湖南省教育厅创新平台开放基金科研项目(13K078)。
唐 婷,女,在读硕士研究生,主要从事中药制剂与质量控制研研究。
*桂 卉,女,教授,E-mail:guihui1993@.126.com。
