含银离子烧伤敷料的遗传毒性研究*
2014-06-05李光远祝君梅史梦柔李毅敏
程 鹏,高 萍,程 琳,李光远,祝君梅,史梦柔,李毅敏
(天津市医药科学研究所,天津300020)
实验研究
含银离子烧伤敷料的遗传毒性研究*
程 鹏,高 萍,程 琳,李光远,祝君梅,史梦柔,李毅敏
(天津市医药科学研究所,天津300020)
目的:采用哺乳动物细胞和细菌对含银离子烧伤敷料进行遗传毒性研究。方法:通过鼠伤寒沙门菌回复突变试验(Ames试验)、体外哺乳动物细胞染色体畸变试验和体外哺乳动物细胞基因突变试验,观察该敷料浸提液是否引起细胞的基因突变、染色体结构的改变或DNA和基因的改变。结果:该试样在3.0 cm2/ml(浸提原液剂量)样品的二甲基亚砜(DMSO)浸提液对试验所用鼠伤寒沙门菌有抑制作用,3.0 cm2/ml样品浸提液对中国仓鼠肺成纤维细胞(CHL)具有毒性作用,对体外培养的V79细胞无诱导HGPRT基因突变作用。结论:结果显示在一定的剂量下,该含银离子烧伤敷料未见引起明显的遗传毒性作用,而浸提原液剂量组具有一定的遗传毒性作用。
遗传毒性,银离子,敷料
随着医学的进步和人们对创伤愈合理论认识的进一步深入,人们对医用敷料的要求逐渐提高,载银敷料应运而生,其不仅能够有效抵抗病原菌的侵染,而且对伤口愈合和皮肤再生具有显著疗效[1]。对银离子烧伤敷料进行临床前安全性评价,是其应用于临床前的重要内容。通过对其进行鼠伤寒沙门菌回复突变试验、体外哺乳动物细胞染色体畸变试验和体外哺乳动物细胞基因突变试验,观察其浸提液是否引起细胞的基因突变、染色体结构的改变或DNA和基因的改变,以降低临床研究受试者和新产品上市后使用人群的使用风险。
1 材料与方法:
1.1 材料
1.1.1 试验样品亲水纤维含银烧伤功能性敷料,是一种柔软无菌无纺布水刺敷料,由羧甲基纤维素钠及沿长轴缝合产品的尼龙丝组成,含有1.2%(w/w)的银离子。
1.1.2 试验菌株TA97、TA98、TA100、TA102,由天津市防病中心购入(批号20051108),本实验室传代保存,并经鉴定合格的菌株。
1.1.3 细胞株中国仓鼠肺成纤维细胞(V79),中国仓鼠肺成纤维细胞(CHL),购自中国科学院上海生命科学研究院细胞资源中心。
1.1.4 试药敌克松(Dexon,Sigma公司生产,批号102K0733),2-氨基芴(2AF,Sigma公司生产,批号16F-3451),1,8二羟基蒽醌(Fluka公司生产,批号447068/1),RPMI1640培养液(GIBCO公司生产,批号1047966),甲基磺酸乙酯(EMS)(上海试剂一厂,批号10-01-03),7,12-二甲基苯蒽(DMBA)(Sigma,批号408181000),秋水仙素10 μg/ml(联星生物技术有限公司,进口分装),丝裂霉素(MC,浙江海正药业股份有限公司生产,批号100110),环磷酰胺(CP,江苏恒瑞药业股份有限公司生产,批号10110621),代谢活化系统:S9混合液(本实验室制备)。
1.2 材料的准备Ames试验将样品以3 cm2/ml+吸收量的比例置生理盐水(NS)和二甲基亚砜(DMSO)中,50℃下浸提72 h作为浸提原液;体外哺乳动物细胞染色体畸变试验将样品以同样比例置含10%胎牛血清培养液中,37℃下浸提72 h;哺乳动物细胞体外基因突变试验将样品以同样比例置无血清培养液中,37℃下浸提72 h。
1.3 Ames试验菌株:鼠伤寒沙门菌组氨酸缺陷型TA97、TA98、TA100、TA102。阴性对照:同批号浸提介质。阳性对照:敌克松(500 μg/ml)、2-氨基芴(2 mg/ml)、1,8-二羟基蒽醌(500 μg/ml)。检验方法:平板掺入法。试验设阴性对照、阳性对照、浸提原液组、1/2浸提原液组、1/4浸提原液组。非活化试验;加入0.2 mol/L磷酸缓冲液0.5 ml及受试液、新鲜菌液各0.1 ml。活化试验,加入5%S9mix 0.5 ml及受试液、新鲜菌液各0.1 ml。置37℃培养72 h后统计回变菌落数。同时做S9mix检菌。
1.4 体外哺乳动物细胞染色体畸变试验采用同批浸提介质作为空白对照。含0.25 μg/ml丝裂霉素的同批浸提介质作为非活化系统的阳性对照。含20 μg/ml环磷酰胺的同批浸提介质作为活化系统的阳性对照。
试验所用细胞株为中国仓鼠肺成纤维细胞(CHL)。将生长旺盛的CHL细胞用胰蛋白酶液消化,制备成5×104个/ml的细胞悬液,每个培养皿接种3.0 ml。24 h后吸去培养液,加入试验样品浸提液,共设三个剂量组(浸提原液组、1/2浸提原液组、1/4浸提原液组)、空白对照组和阳性对照组。非活化系统分别培养24 h和48 h,收获细胞。活化系统(加S9混合液)在2.7 ml试验样品浸提液中加入0.3 ml S9混合液,6 h后将液体吸去,用Hanks液洗细胞3次,加入含血清1640培养液,继续培养至24 h,收获细胞。收获前3 h加入秋水仙素,阻断细胞有丝分裂的中期分裂相。每一试验组选择100个分散良好的中期分裂相细胞进行染色体畸变分析,计算畸变率,采用χ2检验对各组畸变率进行统计学分析。
1.5 哺乳动物细胞体外基因突变试验阴性对照为无血清培养液;阳性对照非活化系统为1.0 mg/ml甲基磺酸乙酯溶液(EMS),活化系统为250 μg/ml 7,12-二甲基苯蒽(DMBA)。
取纯化V79细胞,每个50 ml大小的培养瓶接种5.0×105个细胞,培养20 h后,非活化系统分别加入5.0 ml材料浸提液及对照液;活化系统分别加入4.5 ml材料浸提液及对照液后,再加入0.5 ml S9混合液,置于CO2培养箱中培养4 h。弃去含受试物的培养液,D-Hank’s液洗涤,换完全培养液培养20 h。上述细胞经消化液消化、计数,将细胞接种于6孔板中,每孔接种2.0×102个细胞,培养7 d后用甲醇固定,姬姆萨染色,计数形成的集落。另外在50 ml的培养瓶中接种5.0×105个细胞进行表达。中间低密度传代一次。表达结束后,消化计数,6孔板的每孔中接种2.0×102个细胞,7 d后测定细胞克隆形成率。同时在6孔板的孔中接种1.5×105个细胞,2 h后加入含6-TG选择培养液培养,作HGPRT基因突变集落选择,选择期为10 d,计算基因位点突变频率。
2 结果
2.1 Ames试验①在活化和非活化条件下,3.0 cm2/ml样品的生理盐水浸提液对试验所用鼠伤寒沙门菌无诱变性。②在活化下,3.0 cm2/ml样品的DMSO浸提液对试验所用鼠伤寒沙门菌无诱变性。③在非活化下,3.0 cm2/ml(浸提原液剂量)样品的DMSO浸提液对试验所用鼠伤寒沙门菌有抑制作用。在下列试验剂量下对以下试验菌株无诱变性:TA97:1/16,1/32和1/64剂量;TA98:1/2、1/4和1/8剂量;TA100: 1/16、1/32和1/64剂量;TA102:1/8、1/16和1/32剂量。见表1。
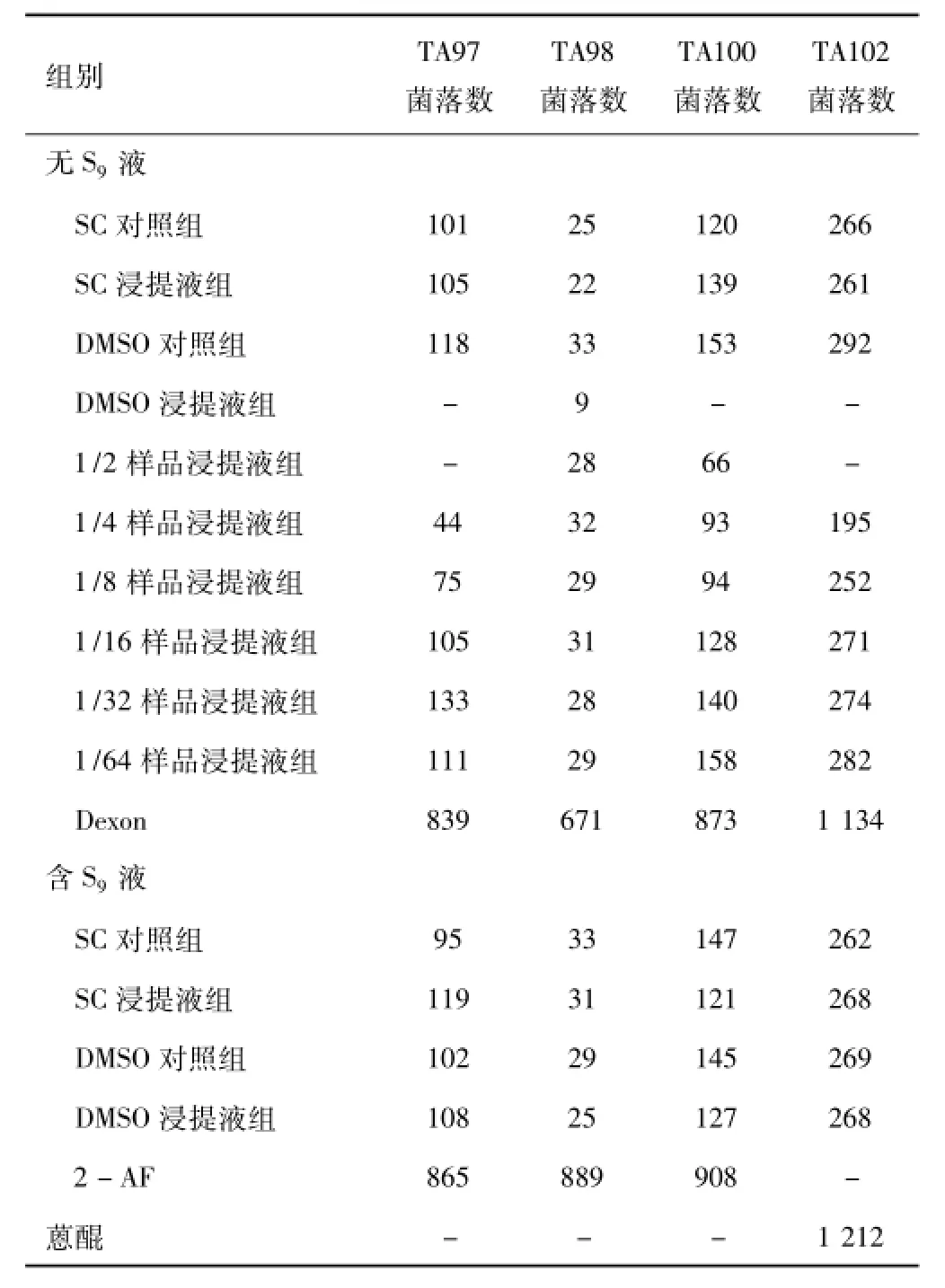
表1 鼠伤寒沙门菌回复_突变试验(Ames试验)结果统计
2.2 体外哺乳动物细胞染色体畸变试验3.0cm2/ml样品浸提液对CHL细胞具有毒性作用,半数生长抑制浓度(IC50)为0.44 cm2/ml。在活化和非活化条件下,0.44、0.22和0.11 cm2/ml样品浸提液与CHL细胞接触后,染色体畸变率均为0%,与空白对照组比较无显著差异(P>0.05)。上述剂量的试验样品浸提液对培养的CHL细胞无诱发染色体畸变作用,见表2和表3。

表2 体外哺乳动物细胞染色体畸变试验细胞毒性测定试验结果
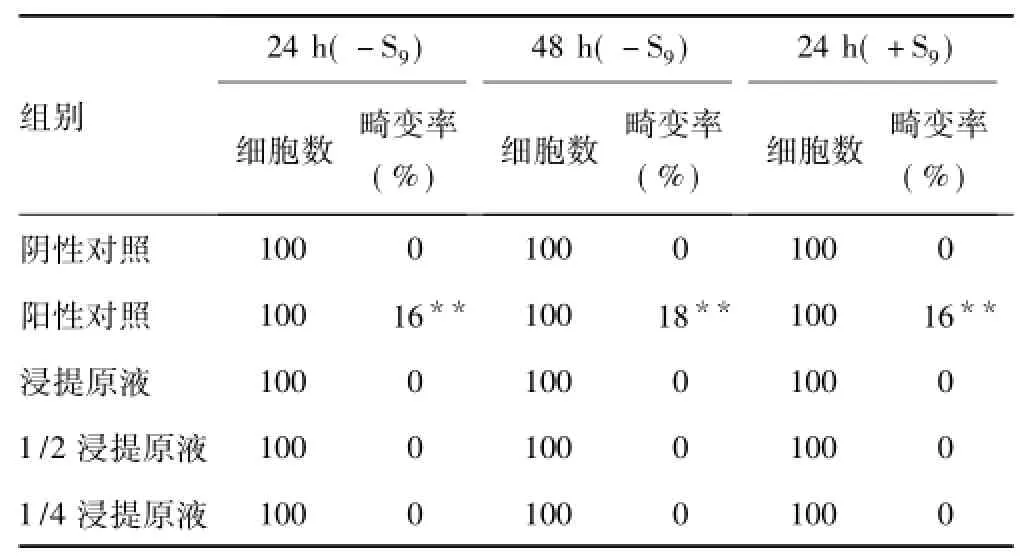
表3 体外哺乳动物细胞染色体畸变试验结果统计
2.3 哺乳动物细胞体外基因突变试验在活化和非活化条件下,3.0、1.5和0.75 cm2/ml样品浸提液对体外培养的V79细胞无诱导HGPRT基因突变作用,见表4。
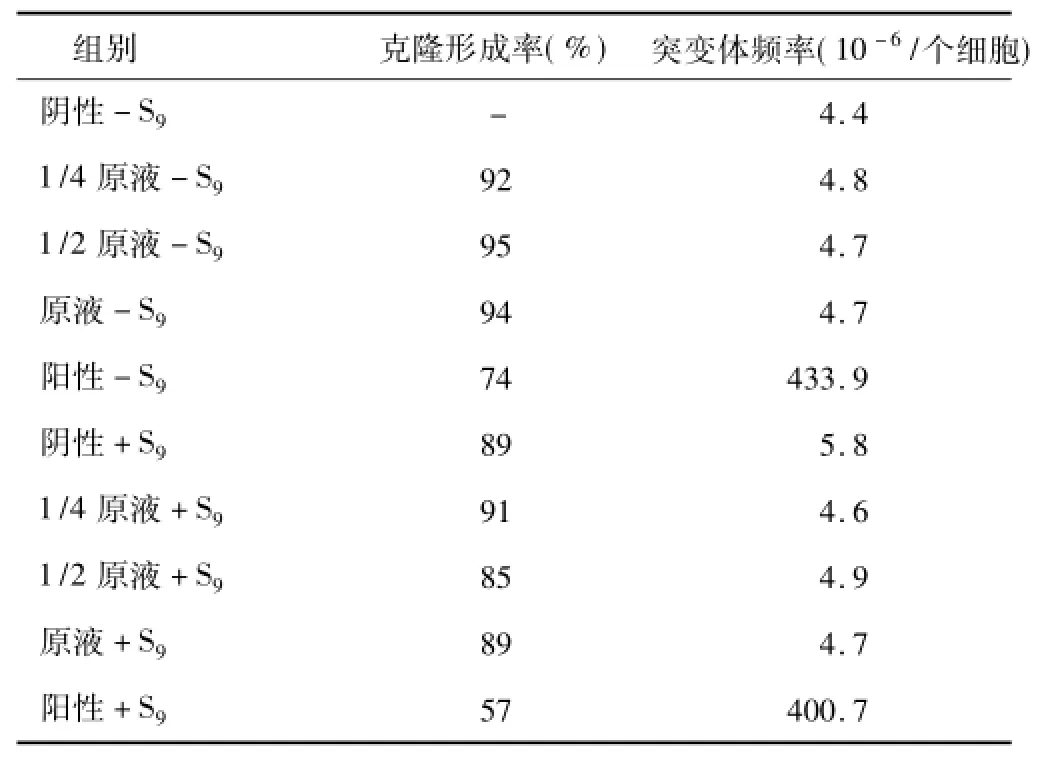
表4 哺乳动物细胞体外基因突变试验的克隆形成率和突变频率
3 讨论
目前可持续释放银离子的含银医用敷料已成功地应用于伤口护理中[2],在临床上使用并取得很好的效果。但是该类产品大多是与人体直接接触,所以必须考虑其细胞的遗传毒性,且其生物安全性均需在上市前进行评价。
本项研究依据毒理学研究原则设计的三项遗传毒性试验[3,4],其结果可最大限度地覆盖该银离子敷料的遗传毒性作用。由结果可看出,该材料在一定的剂量下未引起细胞的基因突变、染色体结构的改变或DNA和基因的改变。而其浸提原液的剂量下,对Ames试验和体外哺乳动物细胞染色体畸变试验中,有明显的抑菌作用和细胞毒性。可能由于银粒子比较容易透过细胞膜上的孔隙进入细胞内或进入包括线粒体、内质网、溶酶体、高尔基体和细胞核等细胞器内,并且和生物大分子发生结合或催化化学反应,使生物大分子和生物膜的正常立体结构发生改变,从而产生相应的细胞毒性[5]。由于该项研究中对材料的浸提液浓度进行了稀释,其遗传毒性是否与稀释剂量有依赖性关系还需进一步研究。目前,银离子敷料的生物安全性如何及其组成成分羧甲基纤维素钠及尼龙丝是否影响银离子的释放量尚无定论,也是该材料在临床使用中亟待解决的问题。
1焦展,安胜军,温昕,等.载银敷料研究现状与展望[J].中华创伤杂志,2009,25(10):958-960
2秦益民.银离子的释放及敷料的抗菌性能[J].纺织学报,2007,28 (1):120-123
3GB/T 16886.3-2008.医疗器械生物学评价第3部分:遗传毒性、致癌性和生殖毒性试验[S].
4袁伯俊,王治乔.新药临床前安全性评价与实践[M].北京:军事医学科学院出版社,1997:78-88
5黄清泉,王蓉蓉,王春仁,等.纳米银医疗产品的体外细胞毒性比[J].药物分析杂志,2009,29(12):2150-2153
The genotoxic study of silver ions dressing
Cheng Peng,Gao Ping,Cheng Lin,Li Guangyuan,Zhu Junmei,Shi Mengrou,Li Yimin
(Tianjin Institute of Medical and Pharmacoutical Sciences,Tianjin 300020)
Objective:to study genotoxic of silver ions dressing by using mammal cell and bacterial.Method:to observe if it can cause gene mutations,changes in chromosome structure,or other dna and gene changing by amas test,in vitro mammalian chromosome aberration test and in vitro mammalian cell gene mutation test.Result:the concentration of 3.0 cm2/ml cause inhibition in Salmonella typhimurium,and toxic action in chl.but wouldn’t cause gene mutations in V79.Conclusion:in certain dose silver ions dressing can’t cause genotoxic,but at the concentration of 3.0 cm2/ml,it can cause genotoxic.
genotoxic,silver ions,dressing
R969.3
A
1006-5687(2014)02-0001-03
2013-10-15
