三合激素注射液含量测定方法的研究*
2014-06-05周建玉
周建玉,王 卫
(天津市药品检验所,天津300070)
药品质量与检验
三合激素注射液含量测定方法的研究*
周建玉,王 卫
(天津市药品检验所,天津300070)
目的:采用高效液相色谱(HPLC)法测定三合激素注射液的含量。方法:色谱柱为Agilent ZORBAX Eclipse XDB C18柱(250 mm×4.6 mm,5 μm),流动相为甲醇-水(80∶20),流速:1.0 ml/min,柱温:40℃,检测波长为230 nm。结果:黄体酮在25~250 μg/ml浓度范围内,与峰面积呈良好线性关系,线性方程为A=1.84×104C+1.22×104,平均回收率为99.00%(n=9),RSD为1.01%;丙酸睾酮在50~500 μg/ml浓度范围内,与峰面积呈良好线性关系,线性方程为A= 1.59×104C+2.25×104,平均回收率为98.18%(n=9),RSD为0.97%;苯甲酸雌二醇在3.0~30.0 μg/ml浓度范围内,与峰面积呈良好线性关系,线性方程为A=2.5×104C-8.30×102,平均回收率为99.18%(n=9),RSD为0.54%。结论:该方法简便、精密、回收率高、重现性好,可用于三合激素注射液的含量测定。
高效液相色谱法,三合激素注射液,含量测定
三合激素注射液(tristerone injection)为复方制剂,其组分为每ml含苯甲酸雌二醇1.5 mg、黄体酮1.5 mg、丙酸睾酮25 mg,辅料为注射用油,临床主要用于月经不调、功能性子宫出血。三合激素注射液在国外药典中均未收载,仅在国家标准[WS-10001-(0494)-2002]中收载。现行标准采用紫外显色法测定丙酸睾酮与黄体酮的总量,没有设定苯甲酸雌二醇的含量测定项,专属性不强且不能准确定量。在2010—2011国家药品标准提高工作中,笔者着重对上述存在的问题进行了考查,拟定了高效液相色谱(HPLC)法同时测定三个组分的含量,所建立的方法将收载于国家食品药品监督管理局国家药品标准。
1 仪器与试药
1.1 仪器安捷伦Agilent 1200型高效液相色谱仪; Autoscience AS10200超声仪;色谱柱:Agilent ZORBAX Eclipse XDB-C18柱(250 mm×4.6 mm,5 μm)。
1.2 试剂和药品苯甲酸雌二醇对照品(批号100006-200504,中国食品药品检定研究院);黄体酮对照品(中国食品药品检定研究院,批号100027-201208);丙酸睾酮对照品(中国食品药品检定研究院,批号100008-200505);甲醇(天津市康科德科技有限公司,色谱纯),水为纯化水;三合激素注射液(A药厂批号100405,规格为含苯甲酸雌二醇1.5 mg/ml、黄体酮1.5 mg/ml、丙酸睾酮25 mg/ml)。
2 方法和结果
2.1 色谱条件与系统适用性试验色谱柱:Agilent ZORBAX Eclipse XDB-C18柱(250 mm×4.6 mm,5 μm);以甲醇-水(80∶20)为流动相;流速:1.0 ml/min,柱温:40℃,检测波长为230 nm。理论板数按黄体酮峰计算应不低于4 000,黄体酮、丙酸睾酮和苯甲酸雌二醇峰之间的分离度应符合要求。
2.2 方法专属性考查
2.2.1 高温破坏试验取三合激素注射液(玻璃安瓿瓶)置沸水中煮沸8 h后取出,放冷,量取1 ml,置100 ml量瓶中,按拟定标准处理后,作为待测溶液。
2.2.2 氧化破坏试验量取三合激素注射液1 ml,置100 ml量瓶中,加甲醇适量摇匀后,加30%过氧化氢溶液1 ml,摇匀,室温放置2 h,按拟定标准处理后,作为待测溶液。
2.2.3 光照破坏试验取三合激素注射液(玻璃安瓿瓶)5支,在太阳光下照射20 d后,量取1 ml,置100 ml量瓶中,按拟定标准处理后,作为待测溶液。
2.2.4 酸破坏试验量取三合激素注射液1 ml,置100 ml量瓶中,加甲醇适量摇匀后,加0.1 mol/L盐酸甲醇溶液5 ml,摇匀,置水浴上放置30 min,放冷,用0.1 mol/L氢氧化钠甲醇溶液调至中性,按拟定标准处理后,作为待测溶液。
2.2.5 碱破坏试验量取三合激素注射液1 ml,置100 ml量瓶中,加甲醇适量摇匀后,加0.1 mol/L氢氧化钠甲醇溶液5 ml,摇匀,置水浴上放置30 min,放冷,用0.1 mol/L盐酸甲醇溶液调至中性,按拟定标准处理后,作为待测溶液。
本研究应用HPLC法检测大鼠心衰实验中不同给药组动物心肌样品,附子提取物组、山茱萸提取物组、附子+山茱萸提取物组与模型组比较其ATP(及其代谢产物 ADP、AMP)、PCr、creatinine等能量物质均有不同程度升高,且附子+山茱萸提取物组比附子提取物组、山茱萸提取物组更为显著,这一结果提示对于慢性心衰大鼠而言,附子+山茱萸联合用药较附子或山茱萸单用,更能有效提高心衰大鼠的心肌活性,其可能与药物促使心肌组织更好的生成和使用ATP、PCr等能量物质有关[5,7]。
2.2.6 专属性试验结果拟定质量标准所选择的色谱条件,能将三种成分主峰与苛刻条件下降解产生的杂质峰进行有效分离,专属性较好,见图1。
2.3 线性试验分别称取黄体酮对照品、丙酸睾酮对照品和苯甲酸雌二醇对照品各适量,加甲醇溶解并定量稀释制成每1 ml中约含1 250、2 500和300 μg的溶液,作为对照品储备液。精密量取对照品储备液适量,分别置50 ml量瓶中,加甲醇稀释至刻度,摇匀,作为线性试验的系列溶液。按照确定的色谱条件,精密量取上述各溶液10 μl,分别注入液相色谱仪,记录色谱图。以浓度为横坐标(C),以相对应的峰面积为纵坐标(A),进行线性回归。试验结果表明,黄体酮在25~250 μg/ml浓度范围内,与峰面积呈良好线性关系,线性方程为A=1.84×104C+1.22×104(r=1,n=8);丙酸睾酮在50~500 μg/ml浓度范围内,与峰面积呈良好线性关系,线性方程为A=1.59×104C+2.25×104(r=1,n=8)。苯甲酸雌二醇在3.0~30.0 μg/ml浓度范围内,与峰面积呈良好线性关系,线性方程为A= 2.5×104C-8.30×102(r=1,n=8)。
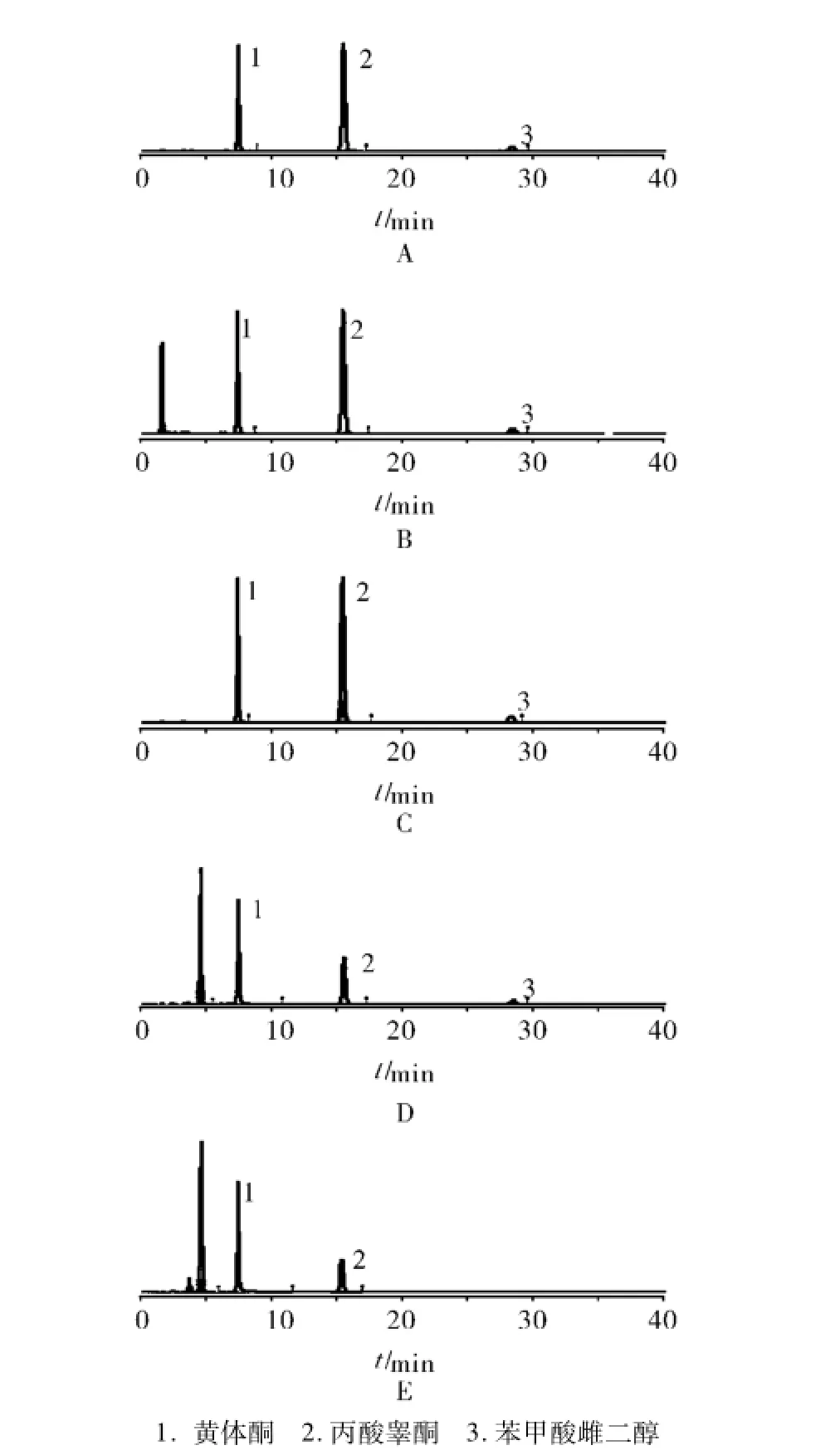
图1 高温破坏(A)氧化破坏(B)光照破坏(C)酸破坏(D)碱破坏(E)高效液相色谱图
2.4 回收率试验按规格量的80%、100%和120%,分别称取已知含量的丙酸睾酮、黄体酮和苯甲酸雌二醇原料药适量,加注射用油溶解制成模拟样品,每个浓度3份。按照确定的色谱条件,分别测定每个模拟样品的含量,以测得药量与加入药量之比计算回收率。经试验,本方法平均回收率丙酸睾酮为98.18%(n= 9),RSD为0.97%;黄体酮为99.00%(n=9),RSD为1.01%;苯甲酸雌二醇为99.18%(n=9),RSD为0.54%,结果见表1-3。
2.5 精密度试验
2.5.1 系统精密度取对照品溶液连续进样6次,按黄体酮峰面积计算RSD,结果为0.1%;按丙酸睾酮峰面积计算RSD,结果为0.03%;按苯甲酸雌二醇峰面积计算RSD,结果为0.2%,表明该色谱系统精密度良好。
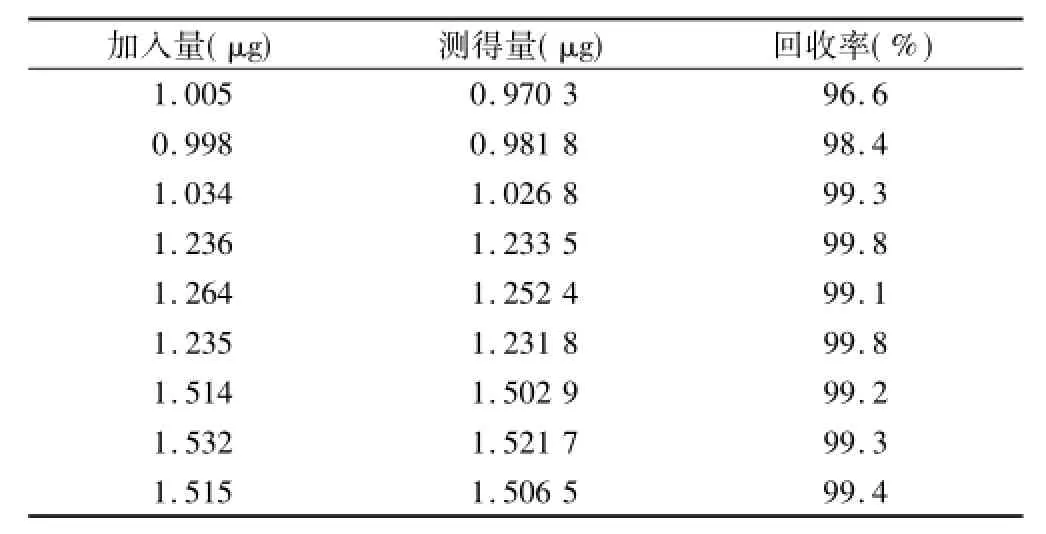
表1 黄体酮回收率试验结果
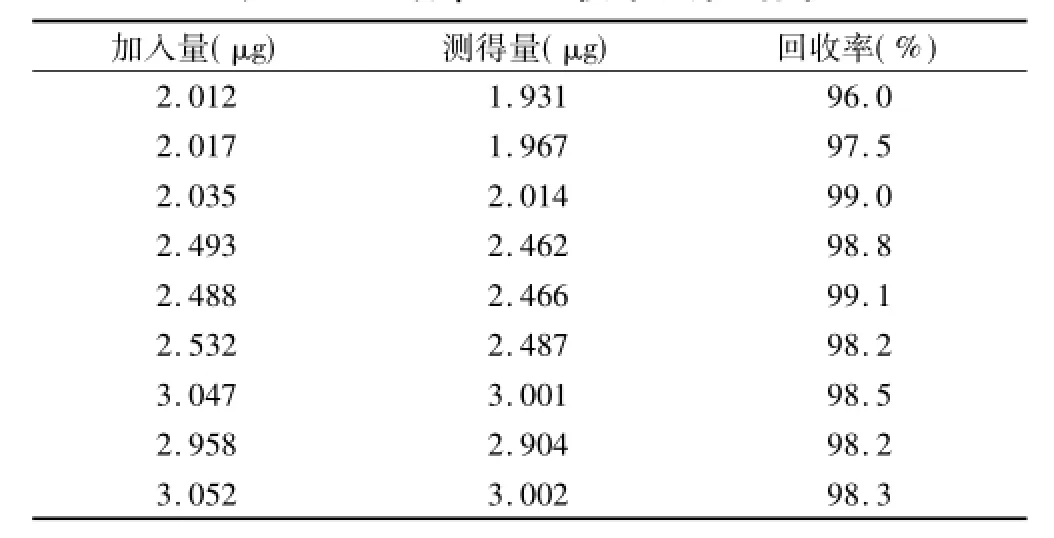
表2 丙酸睾酮回收率试验结果
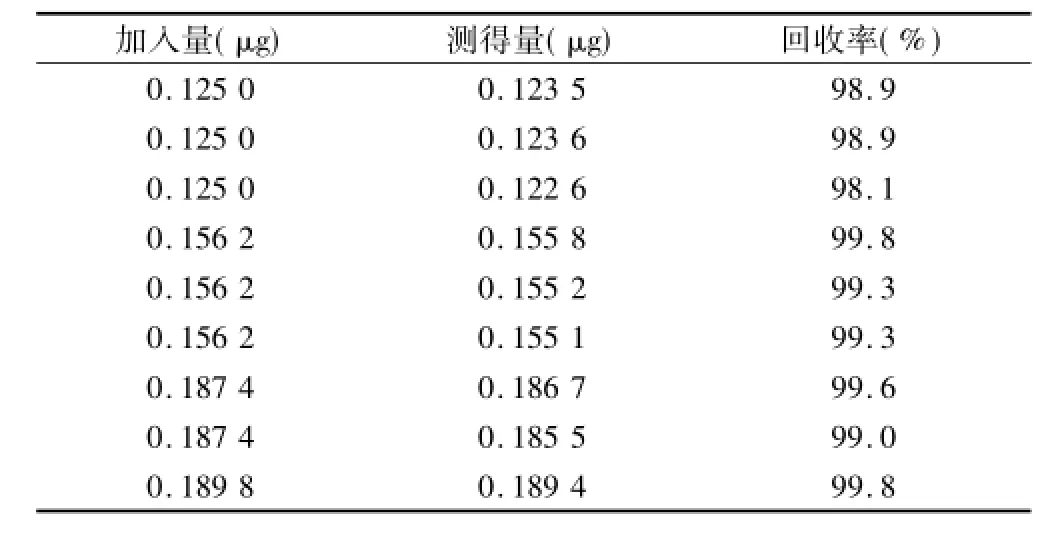
表3 苯甲酸雌二醇回收率试验结果
2.5.2 方法精密度精密量取样品6份,按上述方法制备供试品溶液并进样测定含量,结果见表4。
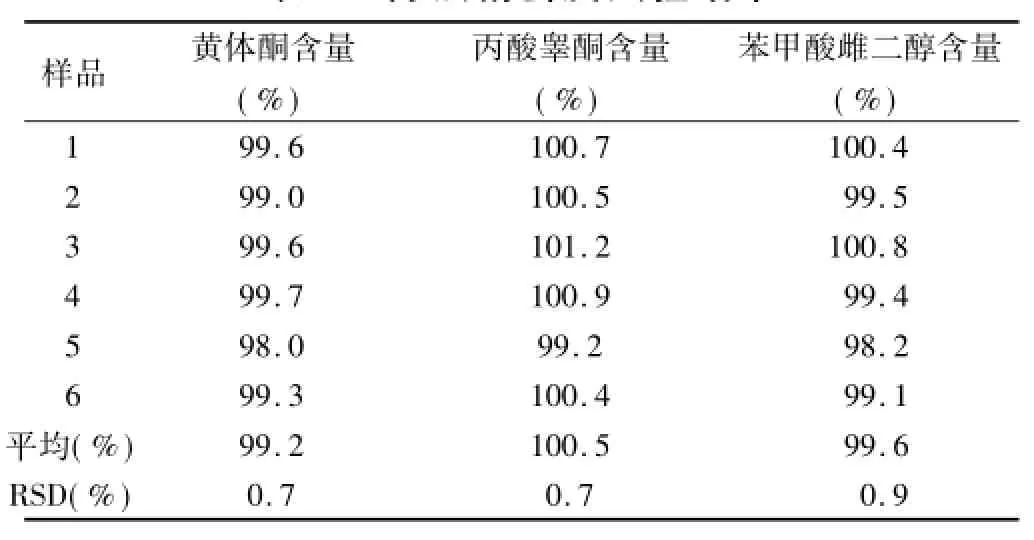
表4 方法精密度试验结果
2.6 定量限精密量取对照溶液适量,采取逐步稀释法测定,本方法最低定量浓度黄体酮为1.39 μg/ml (S/N=10),丙酸睾酮为2.62 μg/ml(S/N=10),苯甲酸雌二醇为3.14 μg/ml(S/N=10)。
2.8 含量测定方法
2.8.1 色谱条件与系统适用性试验用十八烷基硅烷键合硅胶为填充剂;以甲醇-水(80∶20)为流动相;检测波长为230 nm。理论板数按黄体酮计算应不低于4 000,黄体酮、丙酸睾酮和苯甲酸雌二醇峰与相邻峰的分离度应符合要求。
2.8.2 测定法用内容量移液管精密量取本品适量(约相当于黄体酮12.5 mg),置100 ml量瓶中,加甲醇适量超声溶解,放冷,加甲醇稀释至刻度,摇匀;取上述溶液置离心管中离心15 min(4 000 r/min),取上清液作为供试品溶液,精密量取10 μl注入液相色谱仪,记录色谱图;另取黄体酮、丙酸睾酮和苯甲酸雌二醇对照品适量,加甲醇溶解并定量稀释制成每1 ml中分别含黄体酮、丙酸睾酮和苯甲酸雌二醇125、250和15 μg的溶液,同法测定,按外标法以峰面积计算,即得。
2.9 样品测定样品分别按本方法和法定方法测定含量,结果见表5。含量测定的色谱图见图2。
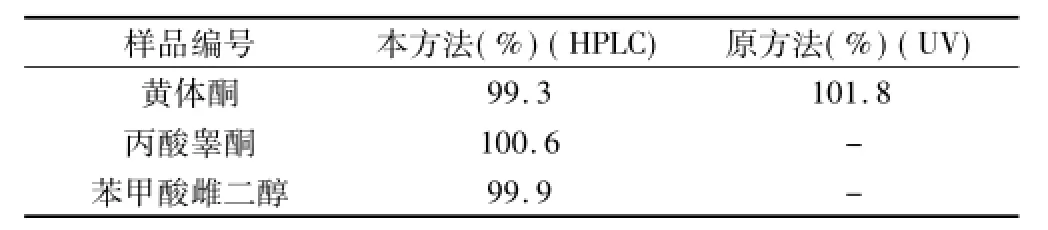
表5 含量测定新方法及原方法比较结果
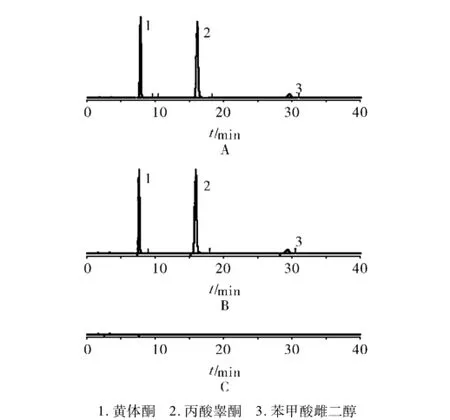
图2 对照品(A)供试品(B)阴性对照(C)HPLC色谱图
3 讨论
3.1 色谱条件的选择参考《中国药典》2010年版二部丙酸睾酮注射液、黄体酮注射液和苯甲酸雌二醇原料及注射液[1]标准,结合各成分紫外光谱最大吸收波长选择色谱条件。由于处方中苯甲酸雌二醇的量最低,故根据以上条件选定拟定色谱条件:C18柱,甲醇-水(80∶20),230 nm,溶剂:甲醇,见表6。

表6 色谱条件的种类
3.2 粗放度按照拟定方法测定一批样品的含量,并进行了耐用性试验,各条件的测定结果基本一致,结果见表7。其中①岛津LC-2010液相色谱仪,迪马Diamonsil C18(2)柱(250 mm×4.6 mm,5 μm);②Agilent 1200液相色谱仪,Agilent ZORBAX Eclipse XDB C18柱(250 mm×4.6 mm,5 μm)。
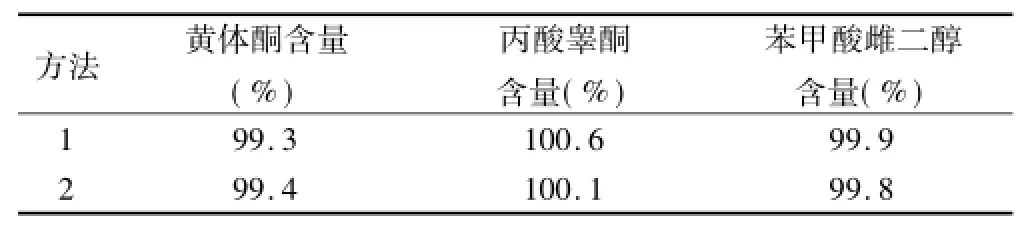
表7 粗放度试验结果
1中国药典[S].二部.2010:103,438,872
Content determination of tristerone injection by HPLC
Zhou Jianyu,Wang Wei
(Tianjin Municipal Institute for Drug Control,Tianjin 300070)
Objective:To establish a HPLC method to determine the content of tristerone injection.Methods:The Agilent ZORBAX Eclipse XDB C18(250 mm×4.6 mm,5 μm)column was adopted,the mobile phase was methanol-water(80∶20),the flow rate was 1.0 ml/min,the column temperature was 40℃and detecting wavelength was 230 nm.Results:The mass concentration of progesterone in the range of 25~250 μg/ml(r=1,n=8)at the detecting wavelength of 230 nm had good linear correlation with the area of the test peak,the average recovery rate was 99.00%(n=9,RSD was 1.01%);The mass concentration of Testosterone in the range of 50~500 μg/ml(r=1,n=8)had good linear correlation with the area of the test peak,the average recovery rate was 98.18%(n=9,RSD=0.97%);The mass concentration of estradiol benzoate in the range of 3.0~30.0 μg/ml(r=1,n=8)had good linear correlation with the area of the test peak,the average recovery rate was 99.18%(n=9,RSD was 0.54%). Conclusion:The method is simple and precise with high recovery rate,high accuracy and good reproducibility,which can be used for the determination of the content of tristerone injection.
tristerone injection,content determination,HPLC
R927.2
A
1006-5687(2014)02-0014-04
2013-12-03
国家药典委员会国家基本药物标准提高课题(No.2010-780)
