LC-MS/MS法定量研究比格犬注射 liguzinediol的血浆药代动力学
2014-05-19朱晓雯文红梅单晨啸范乃兵
朱晓雯,李 伟,文红梅,张 路,单晨啸,柴 川,范乃兵
(南京中医药大学药学院,江苏 南京 210023)
liguzinediol是一种毒性较小[1],具有心脏安全性,可用于治疗急性心衰的化合物。它通过影响肌浆网钙释放,增加大鼠在体和离体的心脏收缩力[2-3],对正常大鼠及其离体心脏起到较好的正性肌力作用[4-5]。
前期对liguzinediol在大鼠体内的药代动力学、♀♂差异及药物代谢进行了研究报道[6-8]。根据一类新药研制的要求,比格犬体内的药代动力学研究对指导临床具有更为重要的意义[9-10],本文首次研究了比格犬静注 liguzinediol后的血浆药代动力学,为liguzinediol的进一步开发和临床研究提供了必要的实验依据。
1 材料与方法
1.1 药品和试剂 liguzinediol对照品(自制,HPLC测定纯度 >98% );咖啡因(中国食品药品检定研究院,批号:171215-200507);甲醇、甲酸为色谱纯;水为质谱纯。
1.2 仪器 AB Sciex QTRAP 5500质谱仪(美国AB公司);LC 20A快速液相色谱仪 (日本Shimadzu公司);VortexGenius 3涡旋混合仪(德国IKA公司);TGL 16G离心机(上海安亭科学仪器厂)。
1.3 比格犬药代动力学试验 健康比格犬,每组6只,♀♂各半,体质量6~8 kg,由上海交通大学农学院教学实验实习场提供,动物许可证号SCXK(沪20120005)。给药前禁食12 h,并空腹抽血2 ml,动物随机编号并称重,按 1.6、3.2、6.4 mg·kg-1剂量给药,不同时间点 0.083、0.25、0.5、0.75、1、1.25、1.5、1.75、2、3、4、5、6、8、12 h于股静脉取血约 2 ml,肝素抗凝,离心分取血浆,冷冻保存。
1.4 色谱与质谱条件 色谱条件:Shim-pack GVP-ODS保护柱(5.0 mm×2.0 mm,4.6μm);Shim-pack XR-ODS色谱柱50 mm×2.0 mm,2.2μm);柱温40℃;流动相为甲醇(A)-0.1% 甲酸(B),梯度洗脱:0~1 min,5%A;1~2 min,5%~75%A;2~3 min,75%A;3~3.1 min,75% ~5%A;3.1~5 min,5%A。流速0.4 ml·min-1,进样量 2μl。质谱条件:电喷雾离子源(ESI);采用多反应监测模式(MRM)进行正离子检测;离子源喷雾电压5500 V;离子源温度 500℃;气帘气 40 psi;雾化气60 psi;辅助加热气 60 psi;经优化后,liguzinediol和咖啡因的参数:DP、EP、CE、CXP分别为51、10、27、14 V和 146、10、31、12 V。liguzinediol和咖啡因的检测离子分别为 m/z 169.2→122.2和 m/z 195.2→110.2。
1.5 对照品溶液的配制 取 liguzinediol对照品10 mg,精密称定,置10 ml量瓶中,加水溶解并稀释至刻度,摇匀,制成每ml含liguzinediol为1 mg的储备液。取咖啡因对照品适量,精密称定,加甲醇制成每ml含10μg的咖啡因内标溶液。
1.6 血浆样品处理 取血浆100μl,加入内标(咖啡因10 mg·L-1)100μl,混匀,再加入甲醇 1.8 ml,涡旋震荡 3 min,12 000 r·min-1离心 5 min。吸取上清液 1 ml,过 0.22μm微孔滤膜,滤液进样。
1.7 方法学考察 按药代动力学研究的相关要求,考察专属性、线性范围、检测限、提取回收率和方法回收率、日内精密度和日间精密度、样品稳定性、基质效应。
2 结果
2.1 方法学考察 在上述条件下进行检测,liguzinediol和咖啡因的保留时间分别为2.29和2.78 min左右,峰形对称,达基线分离,空白血浆中无内源性物质的干扰,专属性好。
liguzinediol在 5~1×104μg·L-1浓度范围内呈现良好的线性关系,最低检测限为0.02μg·L-1。
配制质量浓度为5、50、500及 5 000μg·L-1的血浆质控样品,按“血浆样品处理”项下方法操作,进行提取回收率、方法回收率、日内精密度、日间精密度以及基质效应等试验,结果见Tab 1,均符合生物样品的检测要求。
取上述4种浓度的质控样品,分别考察反复冻融3次,室温保存24 h,以及冷冻保存1个月的样品稳定性,其RSD不超过8.0%,表明liguzinediol血浆样品稳定。
2.2 比格犬静注药代动力学测定 采用上述LC-MS/MS方法测定静脉注射给予低、中、高3个剂量(1.6、3.2、6.4 mg·kg-1)liguzinediol后的犬血浆样品。药代动力学参数用DAS 2.0软件进行计算和处理,主要药代动力学参数见Tab 2。
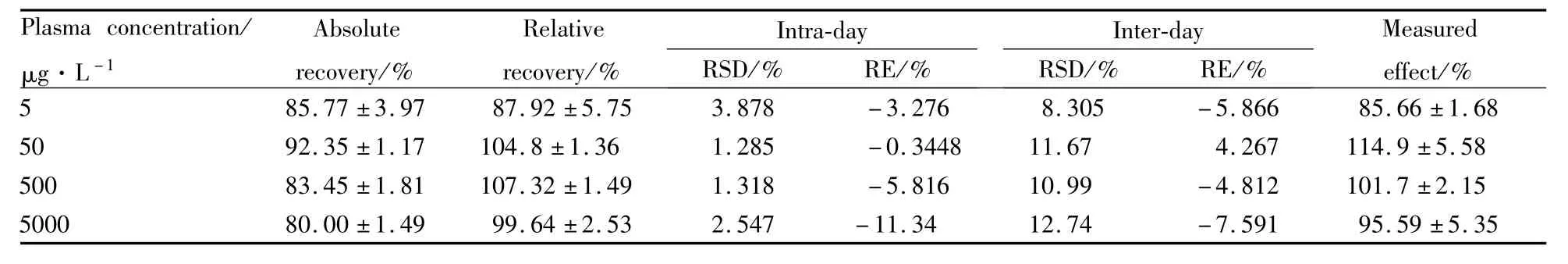
Tab 1 Precision,accuracy and measured effect of the assay for liguzinediol in beagle dog plasma(¯x±s,n=5)

Tab 2 Pharmacokinetic parameters of liguzinediol in beagle dogs after intravenous administration of 1.6,3.2,6.4 mg·kg-1 liguzinediol(¯x±s,n=6)
3 讨论
由静脉注射liguzinediol后比格犬的血浆药代动力学可见,liguzinediol在比格犬体内的清除速度较快,半衰期T12约为0.5 h,♀♂犬的药动学参数无明显差异。而前期研究[6-7]的大鼠血浆药代动力学,♀♂大鼠的T12差异明显,♂鼠的半衰期为0.3~0.5 h,而♀鼠的半衰期为1.5~2 h,♂鼠的清除速率(CL)也是♀鼠的4~5倍,是由于♀♂大鼠代谢酶差异所引起的。
分别单次静脉给予比格犬低、中、高 (1.6、3.2、6.4 mg·kg-1)3个剂量的liguzinediol后,其在动物体内的药物动力学行为具有线性特征,在实验的剂量范围内Cmax和AUC0-t均呈现剂量依赖式的增长趋势。各剂量组间的T12经统计学检验差异无显著性,说明在实验的剂量范围内药物可以在动物体内正常代谢并顺利消除,未发现明显的蓄积和饱和现象。
药效学与药代动力学实验研究表明,liguzinediol作为正性肌力药,静脉注射于动物体内起效快,作用迅速,清除完全,可为急性心衰的治疗提供实验依据。
参考文献:
[1]闻 侃,刘 峥,李 伟,等.Liguzinediol的急性毒性 [J].中国新药与临床杂志,2011,30(3):234-5.
[1]Wen K,Liu Z,Li W,et al.Acute toxicity of liguzinediol[J].Chin J New Drugs Clin Rem,2011,30(3):234-5.
[2]徐 毅,罗卓卡,陈 龙,等.Liguzinediol的正性肌力作用机制及心脏安全性 [J].中国药理学与毒理学杂志,2012,26(2):151-6.
[2]Xu Y,Luo Z K,Chen L,et al.Positive inotropic mechanism of liguzinediol and heart safety evaluation[J].Chin J Pharmacol Toxicol,2012,26(2):151-6.
[3]Chen L,Xu Y,Li W,et al.The novel compound liguzinediol exerts positive inotropic effects in isolated rat heart via sarcoplasmic reticulum Ca2+ATPase-dependent mechanism [J].Life Sci,2012,91(11):402-9.
[4]刘 峥,周淑媛,李 伟,等.Liguzinediol对正常大鼠离体心脏的正性肌力作用 [J].中国新药与临床杂志,2009,28(4):293-6.
[4]Liu Z,Zhou SY,Li W,et al.Liguzinediol induced positive inotropic effect in normal isolated rat hearts[J].Chin J New Drugs Clin Rem,2009,28(4):293-6.
[5]刘 峥,卞慧敏,李 伟,等.Liguzinediol对正常大鼠心脏血流动力学的影响 [J].中国药学杂志,2009,15(44):1155-8.
[5]Liu Z,Bian H M,Li W,et al.Effect of liguzinediol on cardiac hemodynamics in healthy rats[J].Chin Pharm J,2009,15(44):1155-8.
[6]张 路,李 伟,文红梅,等.LC-MS/MS测定大鼠血浆中liguzinediol浓度及药动学[J].中国新药杂志,2013,09:1024-8,1046.
[6]Zhang L,Li W,Wen H M,et al.An LC-MS/MSmethod for determining liguzinediol in rat plasma and studying its pharmacokinetics[J].Chin J New Drugs,2013,09:1024-8,1046.
[7]单晨啸,李 伟,文红梅,等.Liguzinediol大鼠灌胃给药的绝对生物利用度[J].中国新药与临床杂志,2012,11:668-71.
[7]Shan C X,Li W,Wen H M,et al.Study on absolute bioavailability of liguzinediol in rats[J].Chin J New Drugs Clin Rem,2012,11:668-71.
[8]Shan C X,Li W,Wen H M,et al.Identification of liguzinediol metabolites in rats by ultra performance liquid chromatography/quadrupole-time-of-flight mass spectrometry[J].J Pharm Biomed Anal,2012,62(3):187-90.
[9]彭真珍,原 梅,温 泉,等.四氢小檗红碱及其前药的比格犬药代动力学研究[J].中国药理学通报,2012,28(7):1010-4.
[9]Peng Z Z,Yuan M,Wen Q,et al.Pharmacokinetic study of tetrahydroberberrabine and its prodrug in Beagle dogs[J].Chin Pharmacol Bull,2012,28(7):1010-4.
[10]胡会青,王永利,绳晶伟,等.盐酸双苯氟嗪在Beagle犬体内的药代动力学[J].中国药理学通报,2009,25(8):1107-10.
[10]Hu H Q,Wang Y L,Sheng J W,et al.Pharmacokinetics of dipfluzine hydrochloride in Beagle dogs after single intravenous dose[J].Chin Pharmacol Bull,2009,25(8):1107-10.