纯化自体外周血CD34+细胞移植治疗肢体重度缺血的中期疗效
2014-05-05董智慧魏征符伟国廉维帅陈斌郭大乔张祥满王志梅邹善华徐欣蒋俊豪杨珏史振宇竺挺王玉琦
董智慧 魏征 符伟国 廉维帅 陈斌 郭大乔 张祥满 王志梅 邹善华 徐欣 蒋俊豪 杨珏 史振宇 竺挺 王玉琦
纯化自体外周血CD34+细胞移植治疗肢体重度缺血的中期疗效
董智慧 魏征 符伟国 廉维帅 陈斌 郭大乔 张祥满 王志梅 邹善华 徐欣 蒋俊豪 杨珏 史振宇 竺挺 王玉琦
目的探讨纯化CD34+细胞移植治疗肢体重度缺血的中期疗效。方法自2009年5月至2011年12月录入30例肢体重度缺血患者,男性29例,女性1例,平均年龄43±12岁(23~75岁),均不具备外科血管重建条件,共治疗31条下肢和4条上肢。G-CSF(5~10 μg/kg)动员,第5天采集外周血单个核细胞,分选获得纯化CD34+细胞,肢体肌肉局部注射。根据移植细胞数分为3组:低剂量组(105/kg)、中剂量组(5×105/kg)和高剂量组(106/kg)。结果随访16~48个月,1个月和2个月时Wong-Baker FACES疼痛评分由术前7±2降到3±3(P< 0.001)和1±2(P< 0.001)。术后3个月和6个月:最长无痛步行时间由术前的(5±3)min分别延长至(12±6)min(P< 0.001)和(19±5)min(P< 0.001);踝肱指数由术前的0.44±0.20提高至0.62±0.18(P= 0.04)和0.66±0.14(P< 0.001);经皮氧分压由术前(26±11)mmHg分别上升至(42±11)mmHg(P< 0.001)和(56±12)mmHg(P< 0.001)。16例溃疡患者愈合11例。Kaplan Meier生存分析法计算16个月保肢率为84﹪(95﹪可信区间为0.63~0.94)。3个不同剂量组之间的比较,治疗效果差异无统计学意义,除了1个月时WFPRSC检测结果显示:高剂量组明显优于低、中剂量组。结论纯化自体外周血CD34+细胞移植治疗肢体重度缺血性疾病安全、可行,能够较为持久地缓解缺血,挽救肢体,改善患者生活质量。
细胞移植;CD34;四肢;缺血
由于生活水平的提高,生活方式的改变,人口老龄化等因素,周围动脉疾病发病率不断上升,旁路或者腔内治疗是治疗肢体重度缺血(critical limb ischemia,CLI)的主流方法,但是有30﹪~50﹪的患者因各种原因不具备重建条件,最终无法避免截肢[1]。为此,本研究自2009年5月开始了纯化自体外周血CD34+细胞移植治疗CLI的临床研究,期间分别总结了于2011年基于7例的平均8个月随访和2012年基于25例的平均18个月随访,结果显示该方法安全、可行、初期疗效满意[2-3],此次将基于30例的平均30个月随访,评估其中期疗效。
资料和方法
一、一般资料
2009年5月至2011年12月收治CLI 30例,其中男性29例,女性1例,中位年龄(43±12)岁(23~75岁)。其中血栓闭塞性脉管炎(thromboangiitis obliterans,TAO)患者23人,动脉硬化闭塞症(atherosclerosis obliterans,ASO)患者3人,动脉炎4人(系统性红斑狼疮,Crohn病或结节状红斑)。纳入和排除标准既往已述[2-3]。
二、分组
根据应用剂量不同,患者被分成3组:低剂量,105/kg;中等剂量,(5×105)/kg;高剂量106/kg。每组预期病例数≥5例。鉴于CLI的截肢率和死亡率较高,以及伦理问题,未设安慰剂对照组。对双侧病变,先治疗了缺血较重一侧,另一侧若缺血程度< Rutherford 3级则作为自身对照。治疗方案通过复旦大学附属中山医院伦理委员会审批。每位患者签署知情同意书。
三、治疗方案
具体方案既往已述[2-3],简要过程如下:粒细胞集落刺激因子(granulocyte colony stimulating factor,G-CSF)(惠尔血)动员5 d,每日注射低分子肝素,检查外周血细胞计数;第5天采集(德国,Fresenius Hemocare公司),采集物体积一般200~300 ml,行细胞计数与分类,FACS检测CD34+细胞纯度;经洗涤,调整体积至100~150 ml;加入CD34抗体试剂3.75ml(德国,Miltenyi Biotec GMBH);应用CliniMACS分选仪(德国,Miltenyi Biotec GMBH)完成细胞纯化分选,获得终产物约45 ml,其中40 ml用于细胞移植,其余进行细胞计数与分类,苔盼蓝染色检测细胞活力,FACS检测CD34+细胞纯度和微生物检测;分点肌肉注射纯化产物,移植细胞总数(1×105~1×106)/kg,同时对伴有感染的溃疡、坏疽清创/截肢,若为干性坏疽,无伴发感染则Ⅱ期处理;术后长期口服西洛他唑和拜阿司匹林。
四、随访及观测指标
所有病例术后前3个月每月随访1次,术后4~12个月每2个月随访1次,以后每6个月随访1次。此外,在术后的第1个月内每周通过电话随访1次,了解静息痛开始缓解时间。随访内容包括:Wong-Baker FACES疼痛评分;溃疡愈合、皮肤营养状况;运动平板2.5 km/h、10﹪坡度条件下最长无痛步行时间(peak pain-free walking time,PPFWT);踝肱指数(ankle-brachial index,ABI);经皮氧分压(transcutaneous partial oxygen pressure,TcpO2),眼底检查和无不良反应。
五、统计学分析方法
采用SPSS 13.0统计软件分析,16个月保肢率采用Kaplan-Meier生存分析法;疼痛评分、PPFWT、ABI和TcpO2以表示,比较治疗前后差异采用两样本均数t检验,以P< 0.05为差别有统计学意义。
结 果
一、动员、采集及分选
动员至第5天,患者外周血白细胞计数由动员前的(8.07±2.31)×109/L上升至(42.86±12.49)×109/L,外周血CD34+细胞纯度0.21﹪± 0.11﹪(0.07﹪~ 0.38﹪)。
采集终产物体积(265±24)ml(235~315),单个核细胞浓度(158.0±61.2)×109/L[(86.8~269.9)×109/L],其中CD34+细胞纯度0.48﹪± 0.13﹪(0.31﹪~ 0.67﹪),分选获得的纯化采集物平均体积(43.7±2.5)ml(40~48),苔盼蓝染色测细胞活力平均为99﹪± 0.3﹪(98﹪~ 99﹪),单个核细胞数(1.6±0.6)× 109/L [(1.1~2.7)× 109/L],CD34+细胞纯度80.4﹪± 12.1﹪(70﹪~98﹪)。移植细胞数平均(7.5±2.5)×105/kg [(4.5 ×105~1×106)/kg],细胞绝对数平均(4.79±1.95)×107[(2.63~8.47)×107]。
二、移植、清创及截趾
30例患者中,7例给予低剂量移植,12例给予中剂量,11例给予高剂量。1例患者血管病变在踝关节和腕关节已远,细胞仅移植与双侧手足。1例患者病变局限于踝关节已远,细胞移植仅在足部进行。其他患者细胞均移植于小腿和足部或前臂和手。16例合并溃疡,如果没有合并感染,截趾术一般细胞移植2~4周后进行(图1)。
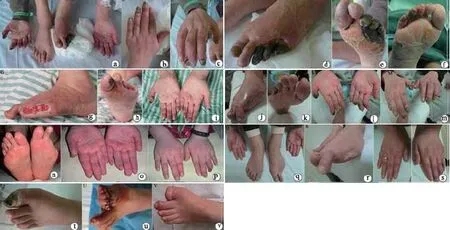
图1 系统性红斑狼疮合并四肢缺血患者(a-s)以及TAO患者(t-v)移植前后比较
三、并发症
动员期间,12例出现不良反应如恶心,腰痛,低热,2~3 d内自行缓解。采集期间,13例出现口唇麻木,口服2 g葡萄糖酸钙即缓解。围手术期无死亡。随访期间未发现病理性眼底视网膜血管新生。
四、随访结果
共治疗31条下肢,4条上肢,其中4例双侧缺血的缺血较轻一侧保守治疗作为自身对照。1例初次细胞移植后足趾溃疡愈合,术后6个月因车祸致新伤口不愈而再次行移植。3例ASO患者均有高血压,1例合并高脂血症并有冠脉搭桥史,1例脑梗史。除1例(系统性红斑狼疮女性患者)外所有患者均有吸烟史。其中27例完成随访16~48个月,平均(30±8)月,失访3例。
静息痛平均缓解时间在3±1周(2~8 w)。在术后1个月和2个月时,Wong-Baker FACES疼痛评分从术前的7±2降到3±3(P< 0.001)和1±2(P< 0.001),术后1个月和2个月对比也有显著差别(P= 0.02)。15例患者能完成PPFWT检测,术后3个月和6个月由术前的(5±3)min分别延长至(12±6)min(P< 0.001)和(19±5)min(P< 0.001),术后6个月与3个月相比也有改善,但无统计学差异(P= 0.06)。术后3个月和6个月的ABI由术前的0.44±0.20提高至0.62±0.18(P= 0.04)和0.66±0.14(P< 0.001),术后3个月和6个月相比差异无统计学意义。术后3个月和6个月,TcpO2由术前(26±11)mmHg分别上升至(42±11)mmHg(P< 0.001)和(56±12)mmHg(P< 0.001),术后3个月和6个月相比仍有统计学差异。3例失访患者最后随访时间和结果分别为:2周,静息痛缓解;2月静息痛无缓解,建议截肢,统计时作为截肢处理;3月,静息痛缓解,溃疡结痂。16例伴溃疡的患者中,11例(69﹪)在(5±4)个月(2~14个月)内愈合。未愈的5例溃疡患者,2例ASO和1例TAO患者在移植3个月内行膝上/下截肢术,1例TAO患者溃疡在足底着力区,另1例TAO患者因跟骨外露而溃疡进一步扩大。7例坏疽患者中,1例失访,1例自行脱落,其余5例行截趾术,其中4例(3±1)个月(3~4个月)内愈合,1例未愈,1月后行膝下截肢,另1例ASO患者因静息痛持续加重行膝上截肢术。Kaplan Meier法评估16个月保肢率为84﹪(95﹪可信区间为0.63~0.94)
讨 论
动脉旁路手术或者腔内治疗作为目前治疗CLI的主要方法,要求患者具备基本的解剖条件——较好的流出道。然而,临床实际工作中高达30﹪~ 50﹪的患者不具备该条件[1],该部分患者截肢率高达40﹪,6月内死亡率高达20﹪。干细胞移植作为一种新方法,为此提供了治疗的可能。2002年,Tateishi-yuyama等[4]全球首次报道骨髓单个核细胞(bone marrow mononuclear cells,BM-MNCs)和外周血单个核细胞(peripheral blood mononuclear cells,PB-MNCs)移植治疗下肢缺血的前瞻性随机对照研究,取得缓解静息痛,促进溃疡愈合,挽救肢体的满意效果。之后,治疗性血管再生治疗CLI的研究逐渐增多[5-6]。
干细胞移植治疗下肢缺血的确切机制尚未完全明了,目前普遍认为主要通过移植细胞直接分化、成熟形成新生血管和旁分泌细胞因子两个环节来发挥作用。EPCs是分化成血管内皮细胞、形成新生血管的重要细胞。1997年Asahara等[7]首次从成人外周血中分离出内皮祖细胞(endothelial progenitor cells,EPCs)。之后EPCs可以促进血管新生,缓解缺血的作用在众多临床前研究中获得证实。目前尚缺乏高度特异性的EPCs表面标志物,CD34和CD133是目前常用的EPCs识别和分离因子。CD34是造血干细胞、EPCs和成熟内皮细胞的共同表面分子,通过CD34+免疫磁珠纯化获得的细胞群中包含以上3种细胞,造血干细胞在缺血环境下可以分化成为EPCs,继而发挥缓解缺血的作用,因此CD34+细胞是干细胞移植治疗下肢缺血中的主要功能细胞,这也是上述采用BM-MNCs或者PB-MNCs移植治疗CLI的国内外临床研究均将移植物中CD34+细胞含量作为重要质控指标的主要原因之一[4-5]。CD133是造血干细胞和EPCs的共同表面标志,成熟的内皮细胞不表达。目前国内尚缺乏可以应用于临床的CD133+分选试剂。
对于细胞移植,因为BW-MNCs中CD34+细胞的数量比PB-MNCs中高500倍[4,6],人们选择BM-MNCs进行移植,但是BW-MNCs也存在其缺点,如需提取约500 ml左右的骨髓血和操作需要全麻或其他麻醉等,于是人们开始寻找更好的方法。经G-CSF动员后外周血中的CD34+细胞同骨髓血中的相当[5,8],于是外周血干细胞移植开始兴起。虽然CD34+细胞为EPCs,造血干细胞和成熟内皮细胞的共同表面标志物,但在缺血的情况下,造血干细胞可向EPCs转化[9-10]。
至今,全球仅有少数纯化CD34+细胞移植治疗下肢缺血的临床研究。2009年11月Kawamoto等[11]进行了全球首次报道,治疗17例下肢重度缺血,分别采用了1×105/kg、5× 105/kg和1×106/kg 3种不同的移植细胞数量,随访12周,所有患者缺血明显改善,而3个剂量组之间差异无统计学意义。外周血CD34+细胞含量一般仅为骨髓的0.2﹪,然而G-CSF动员后明显提高,本组最终移植的CD34+细胞绝对数量平均(4.79±1.95)×107,Tateishi-yuyama等[4]采用BW-MNC移植治疗下肢缺血22例,移植物中CD34+细胞绝对数(3.5±1.3)×107,与本研究相近,提示G-CSF动员后外周血采集可以获得与骨髓采集相当的CD34+细胞数量。
本组中30例患者均不具备旁路或者腔内手术条件,且经药物治疗> 3个月无效,缺血程度重。经纯化CD34+细胞移植后,大多数缺血明显缓解,成功保肢,PPFWT明显延长,提高了生活质量,而且4例双下肢缺血患者中有3例原先缺血相对严重的一侧移植后PPFWT超过了原先相对较轻的另一侧,形成了“自身对照”,进一步提示移植有效。PPFWT虽然属于“主观”指标,但是借助运动平板设定恒定速度和坡度,避免了单纯“间跛距离”测定受到的行走强度不一的干扰,增强了治疗前后的可比性和说服力,而且,该指标可以直接反映患者的生活质量,具有较高的实用价值。与ASO相比,TAO和动脉炎患者平均年龄轻,考虑到预期寿命和对生活质量的要求,成功挽救肢体的价值相对更大。同时此类群体也相对容易获得较好的移植效果,国外学者比较了BWMNCs和PB-MNCs移植治疗TAO和ASO的疗效,有效率分别80﹪和50﹪[5-6,12]。原因可能为:(1)引起内皮功能异常或缺失的因素如高龄、高糖和高血脂在ASO患者中更常见;(2)在高龄的患者中,血浆中各种促血管生长因子含量下降明显[13-16]。
纯化自体外周血CD34+细胞移植的中期结果显示安全和较为持久的缓解缺血、挽救肢体疗效,改善了患者生活质量,为临床治疗提供了一种新的思路,进一步深入研究具有较强的临床实用价值。
1 Hankey GJ,Norman PE,Eikelboom JW.Medical treatment of peripheral arterial disease[J].JAMA,2006,295(5):547-553.
2 董智慧,魏征,符伟国,等.纯化自体外周血CD34+细胞移植治疗下肢重度缺血[J].中华普通外科杂志,2011,26 (3):184-187.
3 Dong ZH,Chen B,Fu WG,et al.Transplantation of purified CD34+cells in the treatment of critical limb ischemia[J].J Vasc Surg,2013,58(2):404-411.
4 Tateishi-Yuyama E,Matsubara H,Murohara T,et al.Therapeutic angiogenesis for patients with limb ischaemia by autologous transplantation of bone-marrow cells: a pilot study and a randomized controlled trial[J].Lancet,2002,360(9331):427-435.
5 Horie T,Onodera R,Akamastu M,et al.Long-term clinical outcomes for patients with lower limb ischemia implanted with G-CSF-mobilized autologous peripheral blood mononuclear cells[J].Atherosclerosis,2010,208(2): 461-466.
6 Matoba S,Tatsumi T,Murohara T,et al.Long-term clinical outcome after intramuscular implantation of bone marrow mononuclear cells (Therapeutic Angiogenesis by Cell Transplantation [TACT] trial) in patients with chronic limb ischemia[J].Am Heart J,2008,156(5):1010-1018.
7 Ashara T,Masuda H,Takahashi T,et al.Bone marrow origin of endothelial progenitor cells responsible for postnatal vasculogenesis in physiological and pathological neovascularization[J].Circ Res,1999,85(3):221-228.
8 Huang PP,Li SZ,Han MZ,et al.Autologous transplantation of peripheral blood stem cells as an effective therapeutic approach for severe arteriosclerosis obliterants of lower extremities[J].Thromb Haemost,2004,91(3):606-609.
9 Kawamoto A,Asahara T.Role of Progenitor endothelial cells in cardiovascular disease and upcoming therapies[J].Catheterization and Cardiovascular Interventions,2007,70(4):477-484.
10 Flamme I,Risau W.Induction of vasculogenesis and hematopoiesisin vitro[J].Development,1992,116(2):435-439.
11 Kawamoto A,Katayama M,Handa N,et al.Intramuscular transplantation of G-CSF-mobilized CD34(+) cells in patients with critical limb ischemia: a phase I/IIa,multicenter,single-blinded,dose-escalation clinical trial[J].Stem Cells,2009,27(11):2857-2864.
12 Saito Y,Sasaki K,Katsuda Y,et al.Effect of autologous bone marrow cell transplantation on ischemic ulcer in patients with Burger's disease[J].Circ J,2007,71(8): 1187-1192.
13 Tepper OM,Galiano RD,Capla JM,et al.Human endothelial progenitor cells from type II diabetics exhibit impaired proliferation,adhesion,and incorporation into vascular structures[J].Circulation,2002,106(22): 2781-2786.
14 Shalaby F,Rossant J,Yamaguchi TP,et al.Failure of bloodisland formation and vasculogenesis in Flk-1 deficient mice[J].Nature,1995,376(6535):62-66.
15 Ferrara N,Carver-Moore K,Chen H,et al.Heterozygous embryonic lethality induced by targeted inactivation of the VEGF gene[J].Nature,1996,380(6573):439-442.
16 Carmeliet P,Ferreira V,Breier G,et al.Abnormal blood vessel development and lethality in embryos lacking a single VEGF allele[J].Nature,1996,380(6573):435-439.
Mid-term outcomes of transplantation of purified CD34+ cells from peripheral blood in treatment of critical limb ischemia
Dong Zhihui,Wei Zheng, Fu Weiguo,Lian Weishuai,Chen Bin,Guo Daqiao,Zhang Xiangman,Wang Zhimei, Zou Shanhua,Xu Xin,Jiang Junhao,Yang Jue,Shi Zhenyu,Zhu Ting,Wang Yuqi.Department of Vascular Surgery,Zhongshan Hospital,Fudan University,Shanghai 200032,China
Weiguo Fu,Email: fu.weiguo@zs-hospital.sh.cn
ObjectiveTo evaluate the mid-term outcomes of transplantation of purified peripheral blood CD34+cells in treatment of critical limb ischemia.MethodsFrom May 2009 to November 2011,30 patients with critical limb ischemia underwent transplantation of purified peripheral blood CD34+cells.Mean age was 43±12 years(23-75),and all patients were not suitable for surgical or endovascular revascularization.G-CSF was subcutaneously injected for 5 days before apheresis for peripheral blood mononuclear cells.Then CliniMACS system was used to isolate CD34+cells.The patients were divided into 3 groups: low-dose (105/kg); medium-dose (5×105)/kg; and high-dose (106/kg).The outcomes were compared among 3groups.ResultsThe follow-up was accomplished in 27 cases,ranging from 16 - 48 months (30±8).One month after transplantation,the rest pain was obviously relieved in all cases,and the Wong-Baker FACES pain rating score significantly decreased from 7±2 to 3±3(0-2),P< 0.001.The peak pain-free walking time was significantly improved from (5±3) min to (12±6) min at 3 month and (19±5) min at 6 month respectively.The ankle-brachial index increased from 0.44±0.20 to 0.62±0.18 at 3 month and 0.66±0.14 at 6 month,respectively.Of 14 cases with ulcer,11 healed.Transcutaneous partial oxygen pressure rose from (26±11) mmHg to (42±11) mmHg at 3 month and (56±12) mmHg at 16 month,respectively.No serious complications were observed either perioperatively or postoperatively.The Kaplan Meier estimate of the rate of freedom from major amputation at 16 months was 84﹪ (95﹪ confidence interval,0.63 to 0.94 ).Conclusions Transplantation of purified peripheral blood CD34+ cells appeared to be effective and safe for critical limb ischemia
Cell therapy;CD34+;Extremities;Ischemia
2013-12-18)
(本文编辑:蔡晓珍)
10.3877/cma.j.issn.2095-1221.2014.03.007
上海市人才发展资金(2010017)
200032 上海,复旦大学附属中山医院血管外科(董智慧、符伟国、廉维帅、陈斌、郭大乔、张祥满、徐欣、蒋俊豪、杨珏、史振宇、竺挺、王玉琦),血液科(魏征、王志梅、邹善华)
符伟国,Email:fu.weiguo@zs-hospital.sh.cn
董智慧,魏征,符伟国,等.纯化自体外周血CD34+细胞移植治疗肢体重度缺血的中期疗效[J/CD].中华细胞与干细胞杂志:电子版,2014,4(3):189-194.
