硝酸铵氧化法制备氯化亚铜技术研究
2014-05-04姚佐胜孙晓庆
姚佐胜,孙晓庆
(1.铜陵化学工业集团有限公司,安徽 铜陵 244000;2.铜陵瑞莱科技有限公司)
工业技术
硝酸铵氧化法制备氯化亚铜技术研究
姚佐胜1,孙晓庆2
(1.铜陵化学工业集团有限公司,安徽 铜陵 244000;2.铜陵瑞莱科技有限公司)
介绍了硝酸铵氧化分解海绵铜生产氯化亚铜的方法。工艺过程:将海绵铜加入硝酸铵和硫酸的混合液中,海绵铜中的铜溶解得到硫酸铜溶液;向硫酸铜溶液中加入亚硫酸铵和氯化铵,亚硫酸铵将硫酸铜还原为硫酸亚铜,氯化铵将硫酸亚铜氯化沉淀为氯化亚铜;氯化亚铜经酸洗、醇洗、烘干得到成品;滤液经蒸发浓缩得到硫酸铵副产品。最佳制备条件:(1)海绵铜溶解过程,反应温度为60℃,硫酸浓度为0.2~0.3mol/L,硝酸铵用量为过量10%~20%;(2)沉淀氯化亚铜过程,亚硫酸铵与硫酸铜的物质的量比为0.6,氯化铵与硫酸铜的物质的量比为1.0~1.1;(3)沉淀氯化亚铜用质量分数为2%的硫酸水溶液洗涤,再用质量分数为95%的乙醇洗涤,再经烘干得到氯化亚铜产品,所得产品质量符合GB/T 27562—2011《工业氯化亚铜》要求。
硝酸铵;氧化分解;硫酸铜;氯化亚铜
氯化亚铜是重要的铜盐系列化工产品,广泛应用于石油化工、纺织印染、颜料、医药、电镀、选矿、有机合成等行业。目前工业氯化亚铜的主要生产方法是海绵铜煅烧酸解法和空气氧化酸解法。煅烧酸溶法的主要缺点是工艺流程长、能耗高、生产能力小。空气氧化酸解法是将废铜粉置于塔式反应器中采用稀硫酸喷淋空气逆流接触氧化,缺点是反应时间长、动力消耗大、生产成本高。笔者选取工业海绵铜为原料,采用硝酸铵氧化分解技术生产硫酸铜进而生产氯化亚铜。该方法生产原料易得,生产成本较低,无环境污染,具有较好的经济和社会效益[1]。
1 实验部分
1.1 实验原料
实验所用原料海绵铜、硫酸、氯化铵、亚硫酸铵等均为工业级,其指标见表1~表4。

表1 海绵铜化学成分及含量%

表2 硫酸指标
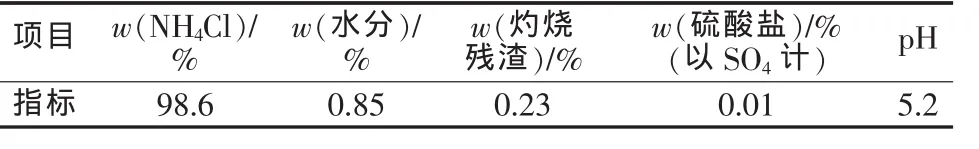
表3 氯化铵指标
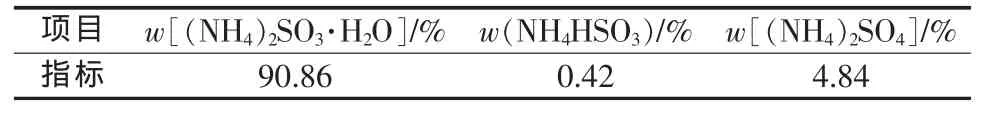
表4 亚硫酸铵指标
1.2 实验原理
1.2.1 海绵铜的溶解
海绵铜的主要成分是氧化铜和金属铜,氧化浸出反应原理:
CuO+H2SO4
=CuSO4+H2O 4Cu+NH4NO3+5H2SO4=4CuSO4+(NH4)2SO4+3H2O
1.2.2 硫酸铜的还原和氯化
2CuSO4+(NH4)2SO3+2NH4Cl+H2O=2CuCl↓+2(NH4)2SO4+H2SO4
1.3 实验流程简述
将一定量硝酸铵和硫酸混合,加入过量海绵铜,在一定温度条件下搅拌。随着反应的进行海绵铜中的铜不断浸出,料浆中硫酸铜含量不断升高。当溶液中Cu2+质量浓度约为100 g/L时将料浆固液分离,固体为未反应完全的海绵铜可以用于再溶解,液体为澄清的硫酸铜溶液。
将硫酸铜溶液在一定温度下加入定量的亚硫酸铵和氯化铵,将硫酸铜还原和氯化,制备沉淀氯化亚铜。将此料浆固液分离后得到滤液以及氯化亚铜滤饼。氯化亚铜滤饼先用pH=2的硫酸溶液洗涤,再用95%的乙醇洗涤,烘干后得到氯化亚铜产品。滤液循环用于铜的溶解以及硫酸铜的还原和氯化沉淀工序得到较高浓度的硫酸铵溶液,用于回收硫酸铵[2]。
以海绵铜为原料采用硝酸铵氧化分解技术生产硫酸铜进而生产氯化亚铜工艺流程示意图如图1所示。

图1 氯化亚铜生产工艺流程示意图
2 实验结果与讨论
2.1 海绵铜的溶解
2.1.1 反应温度对浸出效果的影响
取相同质量的海绵铜粉,加水配成质量分数为15%的料浆,按n(Cu2+)∶n(NH4NO3)∶n(H2SO4)=4∶1.1∶5.1加入硝酸铵和硫酸,测定不同反应温度下铜的浸出率,实验结果见表5。表5为不同反应温度下浸出液中Cu2+的质量浓度以及总铜的浸出率。

表5 不同反应温度下Cu2+的质量浓度以及总铜的浸出率
由表5可以看出,反应温度不同铜的浸出率变化很大。海绵铜中氧化铜的质量分数约为8%,这部分铜在反应初期就和硫酸反应生成硫酸铜,所以在前1 h内铜的浸出率较大。常温下铜的溶解很慢,随着反应温度的升高铜的溶解速度增加,但是当反应温度达到80℃时有NO2生成,污染环境不利于操作,因此溶解温度控制在60~70℃为宜。
2.1.2 硫酸浓度对浸出效果的影响
取相同质量的海绵铜粉,加水配成质量分数为15%的料浆,反应温度为60℃,按n(Cu2+)∶n(NH4NO3)=4∶1.1加入硝酸铵,测定不同硫酸浓度下铜的浸出率,实验结果见表6。表6为不同硫酸浓度下Cu2+的质量浓度以及总铜的浸出率。
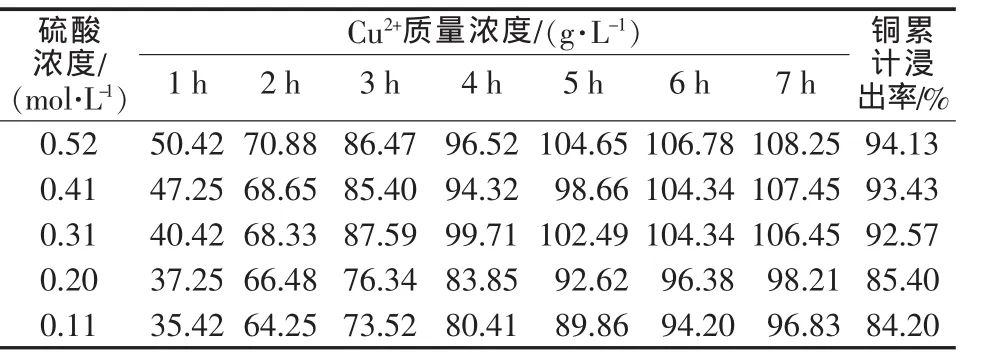
表6不同硫酸浓度下Cu2+的质量浓度以及总铜的浸出率
由表6可以看出,硫酸浓度越高铜溶解所需的时间越短。但是,当硫酸浓度太高时,在生产过程中会产生黄烟污染环境而且增加硝酸铵的用量;而当硫酸浓度太低时,反应速度太慢,反应时间太长。因此,硫酸浓度控制在0.2~0.3mol/L为宜[3-4]。
2.1.3 硝酸铵用量对浸出效果的影响
取相同质量的海绵铜粉,加水配成质量分数为15%的料浆,反应温度为60℃,按n(Cu2+)∶n(H2SO4)= 4∶5.1加入硫酸(硫酸浓度控制在0.25mol/L),测定不同硝酸铵用量下铜的浸出率,实验结果见表7。表7为不同硝酸铵用量下Cu2+的质量浓度以及总铜的浸出率。
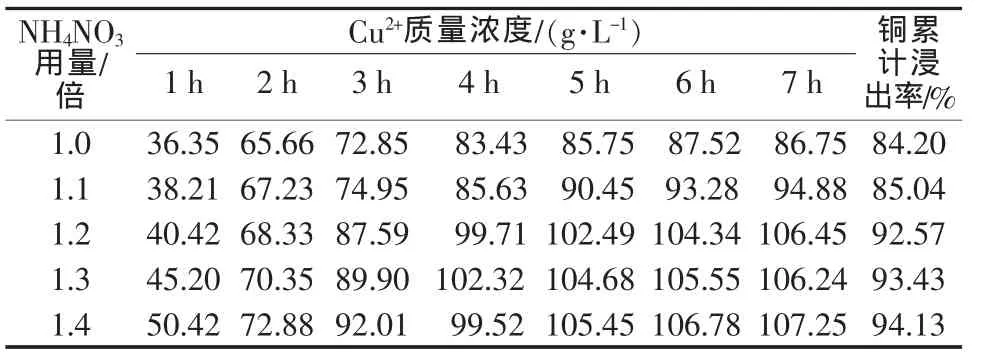
表7不同硝酸铵用量下Cu2+的质量浓度以及总铜的浸出率
由实验可知,铜的浸出率与硝酸铵用量有着密切的关系,在一定范围内铜的浸出量随着硝酸铵用量增加而增加,而且反应时间随着硝酸铵用量增加而缩短。硝酸铵用量太多在反应过程中会产生棕色气体污染环境同时造成成本增加。由实验结果得出,硝酸铵用量控制在过量10%~20%为宜。
2.2 氯化亚铜的制备
2.2.1 亚硫酸铵用量对氯化亚铜沉淀的影响
在硫酸铜溶液中加入还原剂将硫酸铜还原为硫酸亚铜再加入氯化铵生成氯化亚铜。将硫酸铜溶液中的二价铜还原为一价铜的还原剂可以为(NH4)2SO3、Na2SO3、SO2等。综合考虑生产成本以及便于回收硫酸铵,选用亚硫酸铵作为还原剂。图2为亚硫酸铵用量{n[(NH4)2SO3]/n(Cu2+)}与Cu2+沉淀率的关系。
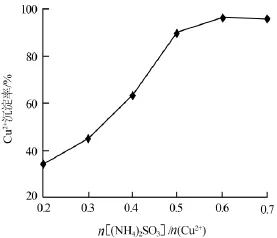
图2(NH4)2SO3用量与Cu2+沉淀率的关系
从图2可以看出,随着(NH4)2SO3用量的增加Cu2+沉淀率呈现上升趋势。当n[(NH4)2SO3]/n(Cu2+)= 0.5时,溶液中ρ(Cu2+)+ρ(Cu+)=10.68 g/L,Cu2+沉淀率达到90.26%;当n[(NH4)2SO3]/n(Cu2+)=0.6时,溶液中ρ(Cu2+)+ρ(Cu+)=3.92 g/L,Cu2+沉淀率达到96.45%;当n[(NH4)2SO3]/n(Cu2+)=0.7时,溶液中ρ(Cu2+)+ρ(Cu+)=3.63 g/L,Cu2+沉淀率达到95.86%。(NH4)2SO3适当过量可以保证Cu2+的还原速度,阻止已经还原的Cu+被空气氧化。实验表明n[(NH4)2SO3]/ n(Cu2+)=0.6比较适宜。
2.2.2 氯化铵用量对氯化亚铜沉淀的影响
硫酸亚铜和氯离子结合可以生成氯化亚铜沉淀。亚铜的沉淀剂可以为提供Cl-的盐类,如NH4Cl、NaCl等。综合考虑硫酸铵的回收选用NH4Cl作为沉淀剂。图3为氯化铵用量[n(NH4Cl)/n(Cu2+)]与Cu2+沉淀率的关系。

图3氯化铵用量与Cu2+沉淀率的关系
图3显示,随着氯化铵用量的增加氯化亚铜沉淀率增加,但当氯化铵用量增加到一定程度后氯化亚铜的沉淀率减少,这是因为生成的氯化亚铜又溶解于氯化铵溶液中。
CuCl+NH4Cl=NH4CuCl2
当n(NH4Cl)/n(Cu2+)=1.0时,溶液中ρ(Cu2+)+ ρ(Cu+)=8.93g/L,Cu2+沉淀率达到91.25%;当n(NH4Cl)/ n(Cu2+)=1.1时,溶液中ρ(Cu2+)+ρ(Cu+)=3.54 g/L,Cu2+沉淀率达到96.53%;当n(NH4Cl)/n(Cu2+)=1.2时,溶液中ρ(Cu2+)+ρ(Cu+)=10.42 g/L,Cu2+沉淀率达到89.79%。实验结果表明n(NH4Cl)/n(Cu2+)=1.0~1.1比较适宜。
2.3 硫酸铵的回收
氯化亚铜沉淀过滤后,滤液中(NH4)2SO4质量浓度为145.26 g/L。将此滤液回用于海绵铜的溶解以及硫酸铜的还原和氯化沉淀后,滤液中(NH4)2SO4的质量浓度达到265.84g/L。再将此滤液重复循环后所得滤液中(NH4)2SO4的质量浓度达到351.92 g/L。此溶液硫酸铵浓度较高,不能再循环使用,否则硫酸铵结晶将影响产品质量,将此溶液蒸发浓缩可以回收硫酸铵。试验表明,采用滤液蒸发浓缩,每产1 t氯化亚铜产品可以回收硫酸铵1.2 t,冷凝液回生产系统用于海绵铜的溶解。通过回收硫酸铵实现工艺水闭路循环,不仅降低了生产成本[5-6],而且解决了生产系统的环保问题。
2.4 氯化亚铜的后处理
2.4.1 氯化亚铜的酸洗
制备的氯化亚铜沉淀因为含有(NH4)2SO4、FeSO4等需要用水洗去可溶性杂质。选用pH=1~2的H2SO4溶液将滤饼打浆洗涤后过滤,初期滤液回到(NH4)2SO4母液中用于回收硫酸铵,后期再用pH= 1~2的H2SO4溶液漂洗,洗后的滤液用于下一次的打浆洗涤,这样即减少水的用量又能保证系统水量的平衡[7]。
2.4.2 氯化亚铜的醇洗涤和烘干
酸洗后的氯化亚铜还需要用95%的乙醇洗涤,否则氯化亚铜极易被氧化为氯化铜。氯化亚铜用乙醇洗涤后经烘干得到成品。所得氯化亚铜产品质量分析结果见表8。

表8 氯化亚铜产品质量指标
3 结论
采用硝酸铵氧化法分解海绵铜,选用亚硫酸铵和氯化铵作为还原剂和沉淀剂制备氯化亚铜,并且回收硫酸铵副产品,实验结果表明该工艺是可行的。该方法生产成本低,工艺条件合理,生产系统母液循环利用,铜收率高,氯化亚铜产品质量稳定。因此,该工艺具有较好的经济效益和环境效益。
[1]于剑昆.硫酸铜的制备[J].黎明化工,1996(5):25-27.
[2]武汉大学,吉林大学.无机化学[M].北京:高等教育出版社,2010.
[3]司霖.黄铜矿的湿法冶金工艺研究进展[J].山西冶金,2011(4):54-56.
[4]谷万成.以硫化铜精矿为原料生产氯化亚铜工艺研究[J].湿法冶金,2004,23(1):29-33.
[5]Hietala kari,Hyvarinen olli.A new technology for copper production[C]∥Alta Copper-8 Technical Proceedings.Perth,Australia,2003.
[6]刘学雷.含铜废液制备氯化亚铜工艺研究[J].安徽化工,1999,25(3):41-43.
[7]徐旺生,宣爱国.催化转化法由低品位铜矿制备活性氯化亚铜[J].无机盐工业,2000,32(5):34-36.
联系方式:sunxiaoqing7648@sina.com
Preparation of cuprous chlorideby ammonium nitrateoxidation process
Yao Zuosheng1,Sun Xiaoqing2
(1.Tongling Chemical Industry Group Co.,Ltd.,Tongling 244000,China;2.Tongling Rely Technology Co.,Ltd.)
The cuprous chloride production process by sponge copper oxidative-decomposed from ammonium nitrate was introduced and technologicalprocesswas as follows:adding sponge copper into themixture ofammonium nitrate and sulfuric acid,and dissolved the copper in sponge copper to obtain copper sulfate solution;to join ammonium sulfite and ammonium chloride into the copper sulfate solution,and then ammonium sulfite reduced copper sulfate into the copper sulfite,and ammonium chloridemake the copper sulfite into the cuprous chloride precipitation;finished cuprous chloride productwas finally got by pickling,alcohol washing,and drying;By-product ammonium sulfate also obtained by evaporation and concentration to the filtrate.The best preparation conditions were obtained:1)In the sponge copper dissolving process,reaction temperaturewas60℃,sulfuric acid concentration wasat0.2~0.3mol/L,the amountofammonium nitratewasexcess of10%~20%;2)In the precipitation process of cuprous chloride,amount-of-substance ratio ofammonium sulfite and copper sulfatewas 0.6,and amount-of-substance ratio ofammonium chloride and copper sulfatewas 1.0~1.1;3)Using sulfuric acid aqueous solutionwithmass fraction of2%towash the cuprous chloride precipitation,and then washingwith ethanolwith the mass fraction of 95%,and finally drying cuprous chloride to get products.The product quality was in line with the GB/T 27562—2011 IndustrialCuprous Chloride requirements.
ammonium nitrate;oxidative decomposition;coppersulfate;cuprous chloride
TQ131.21
A
1006-4990(2014)09-0044-04
2014-03-11
姚佐胜(1961—),男,高级工程师,现任铜陵化学工业
集团有限公司总工程师。
孙晓庆
