基于1H-NMR-PLS-DA技术的参麦注射液质量控制方法研究
2014-04-11杨晓燕
杨晓燕, 冉 坚, 张 琦*, 黄 静*
(1.西南民族大学生命科学与技术学院, 四川 成都 610041; 2.四川大学华西药学院, 四川 成都 610041)
基于1H-NMR-PLS-DA技术的参麦注射液质量控制方法研究
杨晓燕1, 冉 坚2, 张 琦1*, 黄 静2*
(1.西南民族大学生命科学与技术学院, 四川 成都 610041; 2.四川大学华西药学院, 四川 成都 610041)
目的 建立一种基于氢核磁共振-偏最小二乘法-判别分析的参麦注射液质量控制新方法。 方法 将参麦注射液、 仿制品以及缺味样品 (缺红参,缺麦冬制剂) 经柱分离处理后, 利用氢核磁共振技术测定样品的全成分化学信息, 并将其转化为数据矩阵, 利用 SIMCA-P软件进行偏最小二乘法 (PLS) 判别分析。 结果 得分散点图显示合格参麦注射液能够很好的聚集在一起,但不同厂家产品之间存在微小差异;参麦注射液仿制品在合格样品聚集范围边缘,表明有一定差异; 而缺味样品与合格样品之间有明显区分。 结论 氢核磁共振-偏最小二乘法-判别分析法是一种操作简便,并且能够从整体上控制参麦注射液质量的新方法。
参麦注射液;红参;麦冬;氢核磁共振;偏最小二乘法
目前中药注射剂年销售额已超过 200 亿元, 年使用量达4亿人次,在临床上得到越来越广泛的应用[1], 然而有关其发生不良反应的报道日益增多,致人死亡的严重不良反应屡见报道,国家药品不良反应监测中心也多次发出中药注射剂严重不良反应警示。因此,中药注射剂的安全性再评价势在必行。考虑到不良反应在一定程度上与药品的整体内在质量存在相关性,中药注射剂的安全性再评价也应该包括其质量控制方法的再评价。
参麦注射液是国家基本药物目录收载的益气复脉类常用复方中成药注射液,属于国家中药保护品种,由红参、麦冬制成,具有益气固脱、养阴生津, 生脉之功效, 在临床上得到广泛应用[2], 然而其不良反应和不良事件报道在 33 种国家基本药物目录 (2004 年版) 收载的中药注射剂中排列第9 位, 共有 74 篇文献报道[1]。 目前参麦注射液的生产厂家有6家,虽然有统一的生产工艺和质量控制标准,但是各厂家间其设备条件不尽相同,原料来源不一、加工炮制存在差异等,这种综合的因素也导致不同厂家产品的外观、价格、疗效上存在差异。参麦注射液的构成药材味数虽然少,但其化学成分仍然非常复杂,例如红参中就含有皂苷、挥发油、脂肪酸、甾醇、黄酮、氨基酸等多种类型的化合物成分[3]。 现行参麦注射液质量标准 ( 标准号WS3-B-3428-98-2010Z) 中的指纹图谱项下, 也设立了对多达16个特征成分的信号峰进行高效液相色谱指纹测定的标准;但这些特征成分信号峰只代表在测定波长下有吸收的部分有效成分的情况,仍然不能完全反映参麦注射液的整体构成成分。
1H-NMR作为有机化合物结构测定中不可或缺的技术,能够提供足够丰富的有机化学成分的氢谱信息。 而模式识别 (Pattern Recognition) 能在复杂的数据中根据其内在的相关性,最大限度地提取出综合性的、有价值的化学成分信息,并转化成直观的样品信 息 以 供 分 析[4-5]。 将1H-NMR结 合模 式 识别的 技 术 应 用 在 食 品[6-8]、药 物 制 剂[9-10]、 中 药材[11]等的分类和质量控制方面也有一定的报道。
本研究基于参麦注射液的质量标准现状,提出了在 现 有 标 准 的 基 础上, 探索采 用1H-NMR-PLSDA方法,建立针对全成分的参麦注射液质量控制新方法。
1 仪器与材料
SENCOR-201 旋转蒸发器仪 (上海申顺生物科技有限公司); INOVA 400 核磁共振仪 (Varian 公司)
分析纯甲醇, 大孔吸附树脂 (D101)(成都市科龙 化 工 试剂 厂); 氘 代 二 甲 亚 砜 (DMSO-d6,Cambridge Isotope Laboratories,Inc); Excell(Microsoft Co.USA); MestReNova(Mestrelab Research S L, Spain); SIMCA-P11.5(Umetrics AB, Sweden)。
本实验所用的参麦注射液样品于 2010—2012年间购自山东、广州、四川等地的各大医院。样品的生产企业分别为四川川大华西药业股份有限公司(HX)、 四川三精升和制药有限公司 (SJ) 和河北神威药业有限公司 (SW)。红参和麦冬药材均购于成都北京同仁堂药店,且均已经过鉴定。仿制品和缺味样品均按照参麦注射液生产工艺自制 (见表 1)。
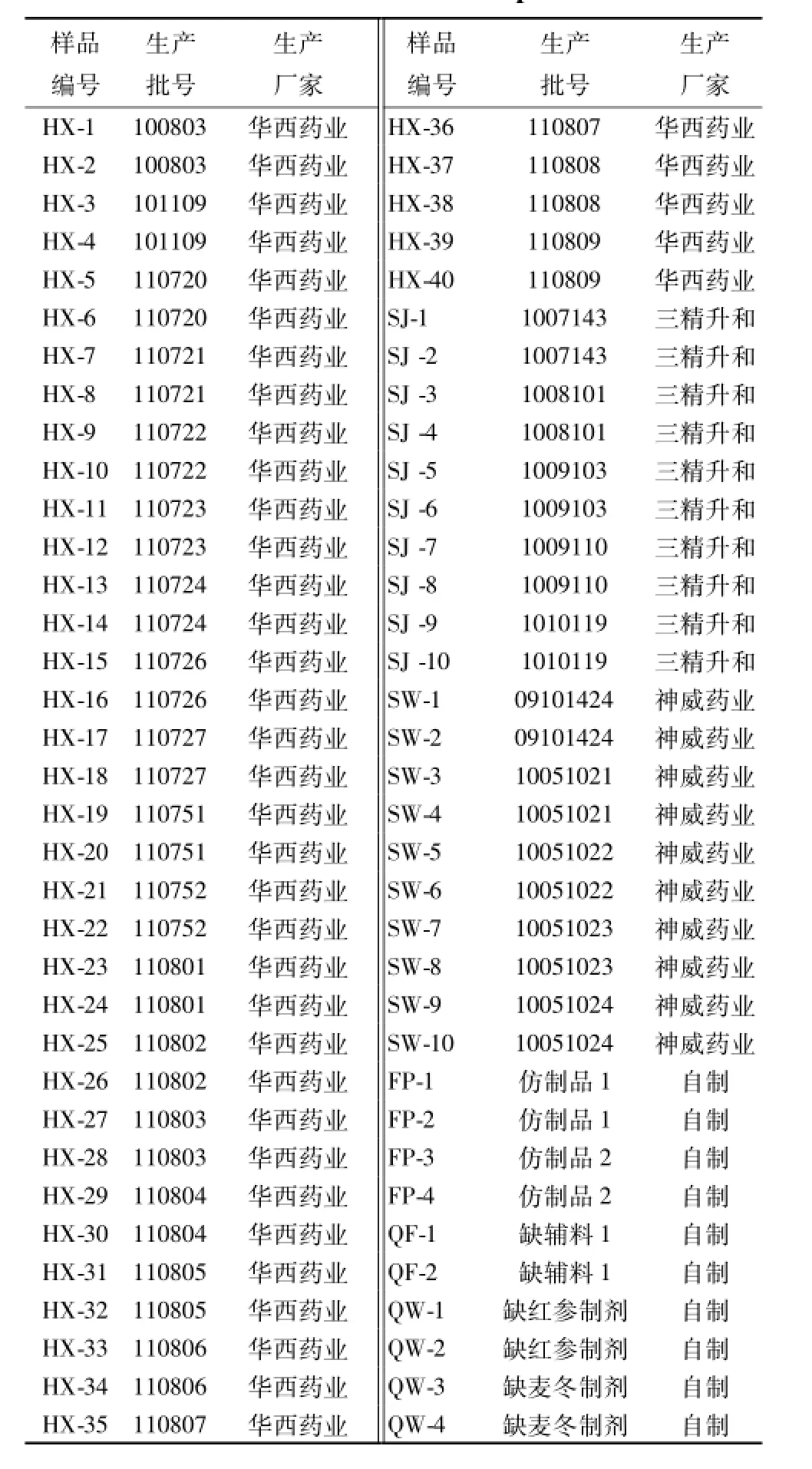
表1 样品来源信息Tab.1 Sources of sam p les
2 方法与结果
2.1 样品制备方法 精密吸取参麦注射液 5 mL,加入到大孔吸附树脂柱内, 用 50 mL蒸馏水洗脱后, 以30 mL甲醇冲洗树脂柱。 收集甲醇洗脱液,45 ℃减压蒸干, 残留物用 0.5 mL DMSO-d6溶解后, 转入核磁管 ( φ5 mm) 中, 供1H-NMR检测。每批次参麦注射液平行制备两个样品。
2.21H-NMR的测定条件 恒温 302 K, 以 DMSO-d6作为内锁, 采样时间域 64 k, 谱宽 7 251.6 Hz,脉冲间隔 D1 为 3.00 s, 采样时间 3.73 s,扫描 32次, 采用标准的预饱和脉冲序列 (zgpr) 压制水峰信号。
二是交融性。①课程教学内容与会计工作内容相融合;②会计学专业教学环境与企业工作环境相融合,从而改变传统师生身份的界定,高校师生关系转化成企业员工关系,而企业员工也同时兼任“教师”职务。
2.3 图谱及数据处理 将样品按 “2.2” 项的1H-NMR测定条件进行测定,获得各样品的自由衰减 (FID) 信号。 将 FID信号导入 MestReNova软件进行傅里叶转换获得1H-NMR图谱。 各图谱分别进行象限和基线调整,并以溶剂 (DMSO-d6) 化学位移值 (δ=2.50) 为内标进行化学位移值校准。
对得到的每张图谱的化学位移值区间 (δ0.00~9.00), 以每 0.05 ×10-6的化学位移值段进行分段积分, 获得与化学位移值段 (175 段) 相应的面积积分值 (考虑到溶剂峰可能对分析结果产生影响, 特将 δ2.40 ~2.65 段去除)。
将获得的积分数据导入 Excel软件, 采用面积归一化法进行标准化处理后,供以下的数据分析。
2.4 数据分析 将 “2.3” 项中得到的各样品数据导入 SIMCA-P11.5 软件, 启 动 PLS-DA分析程序,依次提取主成分 (主成分1, 主成分2 等等), 使各主成分的累积贡献率达到 85%(即表示提取的主成分能够代表原变量 85%的信息), 符合分析要求。
分别以主成分 1(PC1) 对主成分 2(PC2)的得分值为横纵坐标绘制得分散点图并进行相关分析。
2.5 分析方法的考察 参照 《中国药典》 2010 年版一部附录 XVIIIA中药质量标准分析方法验证指导原则,结合本实验的具体情况,对样品制备方法的重复性、样品的稳定性以及仪器精密度进行了考察。 本实验结果采用夹角余弦[12]作为判定指标。
2.5.1 样品制备方法重复性考察 随机取参麦注射液 ( 川 大 华 西 药 业, 批 号:110723), 按 照“2.1”项样品制备方法, 平行制备 6 份样品, 按“2.2”项下测定条件进行测定, 获得1H-NMR图谱, 将图谱按 “2.3” 项下的图谱处理方法处理后得到6组积分面积数据。计算6份样品之间的夹角余弦值分别为:1.000、 0.999 8、 0.999 6、 0.998 1、 0.994 4、0.995 0。计算值均在 0.99 以上, 说明本实验样品制备方法具有良好的重复性。
2.5.3 仪器精密度考察 随机取供试参麦注射液(川大华西药业, 批号 110809), 按照 “2.1” 项下样品制备方法制备 1 份样品, 按 “2.2” 项中样品测定条件连续测定 6次,得到该样品的 6个1H-NMR图谱, 将图谱按 “2.3” 项中的图谱处理方法处理后得到6组积分值数据。计算6组数据之间的夹角余弦值分别为 1.000、 0.999 9、 0.999 9、0.999 8、 0.999 9、 0.999 9,说明本实验所用核磁共振仪精密度良好。
2.6 参麦注射液 PLS-DA分析结果
2.6.1 3 厂家参麦注射液样品之间的 PLS-DA分析将参麦注射液样品 (HX1 ~38,SJ1 ~8, SW 1 ~8) 数据矩阵 (54 ×175, 此次分析共 54 个样品,每个样品 175 个积分段) 作为训练集, 按照 “2.4” 项中方法进行分析。前6个主成分的累积贡献率已达到 86.9%(各 主 成 分 贡 献 率 为:PC1=27.1%,PC2=24.8%, PC3=17.8%, PC4=8.9%,PC5= 5.4%, PC6=2.9%)。 得分散点图见图 1。
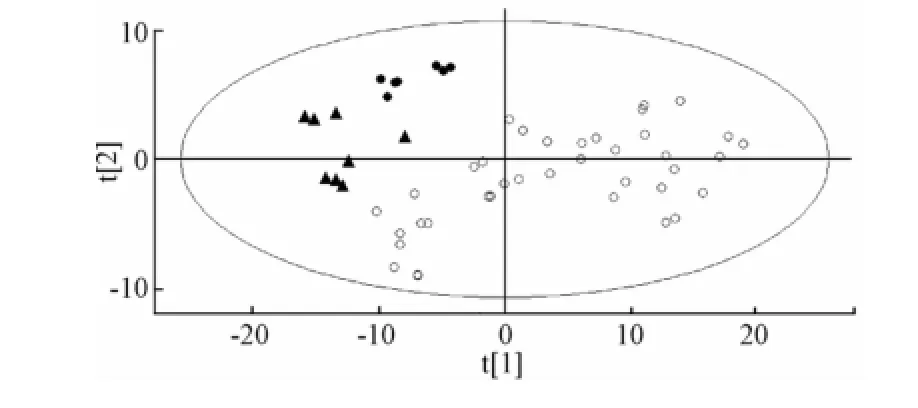
图 1 PLS-DA主成分 1 对主成分 2 的得分散点图Fig.1 Score scatter p lots of PC1/PC2 through PLS-DA
由图1可知,3个厂家的参麦注射液样品的数据点均落在了 95%置信区间内, 说明参麦注射液的产品质量趋于稳定,化学成分相似,并且实验操作过程也没有引入较大误差。因此,这些数据可以作为参麦注射液合格样品的数据库用于进一步分析。另一方面,3个厂家生产的参麦注射液各自有对应的样品数据点集中区域,说明各厂家生产的参麦注射液在整体质量上存在一定的差异,而同一厂家的制剂由于原料来源和制备工艺相对更稳定,所以差异更小。
2.6.2 参麦注射液样品与验证品、 缺辅料样品间的 PLS-DA 分 析 将 各 厂 家 参 麦 注 射 液 样 品(HX1 ~38, SJ1 ~8, SW1 ~8)、 验证样品 (HX39~40, SJ9 ~10, SW 9 ~10) 以 及 缺 辅 料 样 品(QF1 ~QF2) 数据矩阵 (62 ×175) 作为训练集,按照 “2.4” 项中方法进行分析, 前 12 个主成分的累积贡献率已达到87.8%(各主成分贡献率为: PC1=23.0%, PC2=17.1%, PC3=8.8%, PC4= 5.4%, PC5=4.6%, PC6=5.5%, PC7=2.6%,PC8=3.9%, PC9=6.5%, PC10=4.9%, PC11= 2.0%, PC12=3.5%), 得分散点图见图 2。
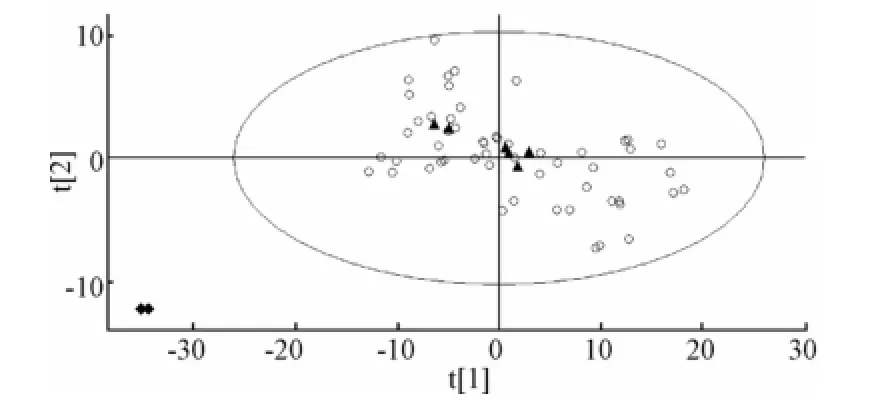
图 2 PLS-DA主成分 1 对主成分 2 的得分散点图Fig.2 Score scatter plot of PC1/PC2 through PLS-DA
由图2可知,随机选取的3厂家的验证品与参麦注射液样品 (HX1 ~38,SH1 ~8, SW1 ~8) 训练集数据聚集在了一起, 说明验证样品 (HX39 ~40, SJ9 ~10, SW9 ~10) 与参麦注射液样品化学成分基本一致,为质量合格的产品,故可以纳入参麦注射液训练集样品数据中,用于进一步分析。而缺辅料样品 (QF1 ~QF2) 数据点落在了 95%置信区间之外,说明缺辅料样品与参麦注射液样品存在明显差异,而与之分开。
2.6.3 参麦注射液样品与仿制品、 缺味样品间的PLS-DA分析 将 “2.3”项下获得的各厂家参麦注射液样品 (HX1 ~40, SH1 ~10, SW1 ~10) 以及仿制品 (FP1 ~4)、 缺味样品 (QW1 ~4) 数据矩阵 (68 ×175) 作为训练集, 按照 “2.4” 项中方法进行分析,前4个主成分的累积贡献率已达到86.9%( 各 主 成 分 贡 献 率 为:PC1=27.2%,PC2=25.1%, PC3=17.4%, PC4=17.2%), 得分散点图见图3。

图 3 PLS-DA主成分 1 对主成分 2 的得分散点图Fig.3 Score scatter p lot of PC1/PC2 th rough PLS-DA
由图3可知,3个厂家参麦注射液数据点均落在了 95%置信区间内, 而缺红参样品 (QW1 ~QW2) 和缺麦冬样品 (QW3 ~QW4) 数据点均落在了95%置信区间之外, 说明缺味样品与合格参麦注射液样品在化学成分上存在明显差异,可以很容易与之区分。 参麦注射液仿制品 (FP1 ~FP4)数据点落在了 95%置信区间边缘, 游离在合格参麦注射液样品训练集之外,说明采用小试设备自制的参麦注射液仿制品与各厂家统一工艺后的大生产样品存在一定差异,这种差异应该是药材产地、工艺设备及操作参数等因素差异的综合效应。提示中成药注射液不同生产厂家可以采用1H-NMR-PLSDA法作为质量评价手段,共同探讨不同工艺操作等因素对产品内在质量的影响。
3 讨论
本实验采用氢核磁共振-偏最小二乘法-判别分析方法,以川大华西药业生产的参麦注射液为主,三精升和制药、河北神威药业生产的参麦注射液为辅建立了参麦注射液样品数据库;以随机选取的合格参麦注射液样品为验证样本,以缺味样品和仿制品作为测试样本,对本方法进行验证和测试;验证和测试结果表明,该法能准确地判断参麦注射液合格品以及多种类型的不合格品,故该方法可作为控制参麦注射液质量的一种有效方法。
本实验选用3个厂家生产的合格参麦注射液初步建立合格参麦注射液样品数据库,能比较全面地反应国内参麦注射液生产厂家的产品情况,并且随着其他厂家的合格品数据的不断纳入,训练集样本数量不断加大,数据库的代表性随之增加,判别的准确性也就随之提高,这将能够有效的对参麦注射液实施更全面的质量控制。
本法能全面地反映参麦注射液的实际生产情况, 实验结果显示,通过1H-NMR-PLS-DA方法建立参麦注射液标准数据库,可以很好地监测不同厂家生产的参麦注射液质量差异,并且应用该法能够区分不同厂家的参麦注射液样品,这对评价不同厂家间样品质量稳定性以及同一厂家制剂工艺的稳定性具有积极的意义,可以推广到生产厂家众多的各种大品种复方中成药,通过其内在质量差异的监控比较,有助于不同生产厂家联合制订出共同遵守的工艺规程并统一操作方式,从而为医药市场的广大病患者提供优质稳定的大品种复方中成药,为这些品种走向国际市场打下良好的基础。
[ 1 ] 袁 强, 王 莉, 成 岚, 等.国家基本药物目录 (2004年版)33 种中药注射剂不良反应 /不良事件文献分析[ J].中国循证医学杂志, 2010, 10(2):132-139.
[ 2 ] 张 冰, 李 莉, 田临红.参麦注射液临床应用进展[J].现代中西医结合杂志, 2007, 16(10):1444-1445.
[3] 王久粉,刘 丹,钱士辉,等.中国红参化学成分的研究[J].中国野生植物资源, 2011, 30(6):55-59.
[ 4 ] Zhu C, Liang Q L, Wang Y M, et al.Integrated development ofmetabonomics and its new progress[ J] .Chin J Anal Chem,2010, 38(7):1060-1068.
[ 5 ] Son H S, Kim K M, Berg F V D, et al.1H Nuclear magnetic resonance-based metabolomic characterization of wines by grape varieties and production areas[ J] .J Agric Food Chem, 2008, 56(17):8007-8016.
[6] 史玉峰, 靳奉祥.高维数据有效特征的提取方法及其在测绘信息模式识别中的应用[J].有色金属, 2004, 56(4): 114-118.
[7] 冉 坚,张 琦,刘 淼,等.基于氢核磁共振和偏最小二乘法-判别分析建立鹿龟酒质量控制方法的研究[ J].食品科学, 2012, 33(7):69-72.
[ 8 ] Charlton A J, Farrington W H H, Brereton P.Application of1HNMR and multivariate statistics for screening complex mixtures:quality control and authenticity of instant coffee[ J] .J Agric Food Chem, 2002, 50(11):3098-3103.
[ 9 ] 罗乔奇, 田祥琴, 张 琦, 等.基于氢核磁共振-主成分分析建立洁尔阴洗液质量控制的研究[J].中草药, 2009, 40 (12):1907-1911.
[10] Rasmussen B, Cloarec O, Tang H R, et al.Multivariate analysis of integrated and full-resolution1H-NMR spectral data from complex pharmaceutical preparations:St.John's wort[ J]. Planta Med, 2006, 72(6):556-563.
[11] 谭小燕, 罗乔奇, 马郑红, 等.不同产地麦冬1H-NMR模式识别研究[J].中草药, 2009, 40(5):792-797.
[12] 王龙星, 肖红斌, 梁鑫淼, 等.一种评价中药色谱指纹谱相似性的新方法: 向量夹角法[J].药学学报, 2002, 37 (9):713-717.
Quality control of Shenmai Injection by1H-NMR-PLS analysis
YANG Xiao-yan1, RAN Jian2, ZHANG Qi1*, HUANG Jing2*
(1.Collegeof Life Scienceand Technology, SouthwestUniversity for Nationalities, Chengdu 610041, China; 2.West China School of Pharmacy, Sichuan University, Chengdu 610041, China)
AIM To establish a new method of quality control for Shenmai Injection.METHODS Shenmai Injection, replicas and different kinds of agents(without Ginseng Rubra Radix, without Ophiopgonis Radix)were treated with the same column separation, and then1H-NMR spectroscopy was used to analyze the chemical components of the samples in combination with partial least squares(PLS)to get visualized overall information.RESULTS In the scatter plot, it revealed that the projection values of Shenmai Injection tented to gather together with small differences among'samples from differentmanufactures.Values of different replicaswere obviously distributed themargin of Shenmai Injection data, and Shenmai Injection without one of ingredients could be distinguished to a certain extent.CONCLUSION1H-NMR-PLSestimator is a simple and usefulmethod to fully reflect the quality of Shenmai Injection.
Shenmai Injection; Ginseng Rubra Radix; Ophiopgonis Radix;1H-NMR; partial least squares (PLS)
R284.1
:A
:1001-1528(2014)02-0333-06
10.3969/j.issn.1001-1528.2014.02.026
2013-04-09
四川省科技支撑计划项目 (2010SZ0127)
杨晓燕 (1986—) , 女, 硕士生, 研究方向: 民族药与质量标准。 E-mail:yangxiaoyanccaa@163.com
*通信作者: 张 琦 (1958—) , 女, 教授, 研究方向: 中药质量控制。 Tel:(028)85522310, E-mail:zhangqi8-8@aliyun.com黄 静 (1961—) , 男, 教授, 研究方向: 天然药物化学。 Tel:(028)85503045, E-mail:huangj-pharm@scu.edu.cn
