Fe-Cr合金在Na2SO4盐膜下的热腐蚀行为
2014-03-25付广艳林立海唐晓鹏
付广艳, 林立海, 刘 群, 苏 勇, 唐晓鹏
(沈阳化工大学 机械工程学院, 辽宁 沈阳 110142)
Fe基高温合金,即耐热钢,具有较好的力学性能,优良的抗氧化、抗腐蚀性能[1],而且价格相对低廉,被广泛应用于矿山、冶金、电力等行业[2],一直都受到材料界的重视.特别地,铁基高温合金广泛应用于民用锅炉、火力发电站等工业锅炉及其它燃烧装置中,它们的耐高温腐蚀性能,特别是耐沉积物引起的热腐蚀性能,对上述装置的安全运行至关重要[3-4].人类发现的第一个热腐蚀事例就是电站锅炉管耐热钢由硫酸盐沉积导致的破坏[5].
近年来,Fe基高温合金的热腐蚀行为得到了广泛研究[6-13],研究方法主要以在合金表面涂覆单组分或混合的硫酸盐和氯化盐为主[14-16].Shi等人[6]对表面沉积Na2SO4的纯Fe在750 ℃条件下的热腐蚀行为进行研究,发现沉积的Na2SO4大大提高了合金的腐蚀速率,这与硫化物的形成和充足的供应有关.为了提高Fe基高温合金的综合力学性能和耐热腐蚀性能,在合金表面涂覆抗腐蚀涂层是一种比较常用的方法.Harpreet Singh[7]等研究了表面分别涂覆NiCrAlY、Ni-20Cr、Ni3Al 和Stellite-6涂层的Fe基超合金在900 ℃条件下的热腐蚀行为,在腐蚀性盐膜Na2SO4-60V2O5(质量分数,以下同)的作用下,未涂覆保护涂层的Fe基合金具有较大的腐蚀增重,而NiCrAlY涂层使合金具有最小的腐蚀增重和最好的热腐蚀抗力;Sidhu等[8]研究了表面分别涂覆NiCrBSi、Cr3C2-NiCr、Ni-20Cr和Stellite-6涂层的Fe基合金在Na2SO4+V2O5混合盐作用下900 ℃时的热腐蚀行为,结果表明涂层对Fe基合金的热腐蚀起到了很好的保护作用,其中Ni-20Cr涂层的保护效果最好;Mahesh 等[9]研究了在Fe基高温合金表面涂覆Ni-5Al涂层的热腐蚀行为,表明涂覆涂层的合金在Na2SO4-60 V2O5混合盐膜作用下,900 ℃时的热腐蚀抗力优于未涂覆涂层的Fe基合金,腐蚀增重降低了57 %;贺定勇[10]等研究了表面电弧喷涂Fe-Cr合金复合涂层(其中Cr质量分数为20 %~44 %)的Q235钢的热腐蚀行为,结果表明:随着表面涂层Cr含量的增加,合金的抗热腐蚀能力得到了较为明显的提高.然而,涂层不同于整体合金化材料,它会发生退化,即由于涂层内的抗氧化元素与基体合金在界面处发生的互扩散或向外扩散,使之较快地消耗掉,造成涂层失效[17].
实际上,除了在Fe基合金表面涂覆涂层外,在合金内添加适量的Al和Cr,以形成保护性的Al2O3和Cr2O3膜,也可以起到保护合金基体的作用.Wang等[11]研究了由NaCl导致的Fe基Fe-Mn-Al-C合金的热腐蚀行为,发现合金涂覆NaCl在900 ℃下的热腐蚀速率高于在此温度下单纯合金的高温氧化速率,而且随着合金内Al含量的提高,合金的热腐蚀抗力得到了提高.在Fe基合金热腐蚀行为的研究中,Banip Mohanty等人[12]和史良权等人[13]的工作值得注意,Mohanty等[12]研究了(K,Na)2SO4盐膜和(K,Na)2SO4+(K,Na)Cl混合盐膜对高Cr含量的Fe-Cr-Ni合金腐蚀行为的影响,结果表明:单一(K,Na)2SO4盐膜作用下合金的热腐蚀速率为合金单纯高温氧化速率的近200倍,而(K,Na)2SO4+(K,Na)Cl混合盐膜作用下合金的热腐蚀速率提高了近20 000倍;史良权等人[13]研究了Na2SO4+MgSO4+CaSO4三元盐膜对Fe-5Cr、Fe-10Cr和Fe-20Cr合金在空气中、700~800 ℃条件下热腐蚀行为的影响,得出提高铬含量能降低三元硫酸盐引起的铁铬合金的热腐蚀的结论,但在Mohanty和史良权等人的研究中,合金的腐蚀增重未考虑腐蚀过程中盐膜挥发失重的因素.
虽然对Fe基合金热腐蚀行为的研究已经进行了几十年,然而目前对Fe基高温合金热腐蚀行为的研究远不如对Ni基高温合金热腐蚀行为的研究那么深入[12,18-20].本文通过研究表面涂覆20~25 g/m2和40~45 g/m2两种厚度Na2SO4盐膜的Fe-10Cr和Fe-20Cr合金在900 ℃空气中的热腐蚀行为,综合考虑合金热腐蚀过程中盐膜的失重因素,来揭示不同Cr含量和涂盐厚度对Fe基合金热腐蚀行为的影响,为合金热腐蚀行为的研究提供一种更为细致、更为周全的方法.
1 实 验
实验所用的合金分别为Fe-10Cr和Fe-20Cr(质量分数,以下同),在真空非自耗电弧炉中反复熔炼而成.将熔炼好的金属锭在950 ℃下真空退火24 h后,线切割成片状试样(10 mm×6 mm×1 mm).试样经1 000#砂纸打磨,丙酮除油,酒精去污、清洗,干燥后待用.
用涂盐法在Fe-10Cr和Fe-20Cr合金表面分别涂覆20~25 g/m2和40~45 g/m2两种不同厚度的Na2SO4盐膜.将试样倾斜置于刚玉坩埚中,在箱式电阻炉中空气气氛下进行静态常压热腐蚀实验,利用梅特勒AG285高精度电子天平(称重天平感量为1×10-5g)称量试样质量的变化.热腐蚀实验在900 ℃空气中进行,腐蚀时间为24 h,充分考虑热腐蚀过程中Na2SO4盐膜的挥发失重因素后,绘制出腐蚀动力学曲线.用带能谱的扫描电镜(SEM/EDX)对腐蚀膜产物的断面进行分析,从而获得腐蚀产物的元素分布和相组成特征.
2 实验结果
2.1 腐蚀动力学
为了排除Na2SO4盐膜挥发对实验结果的影响,在Al2O3坩埚碎片表面涂覆20~25 g/m2和40~45 g/m2两种厚度的Na2SO4盐膜,并置于900 ℃箱式电阻炉中,测出不同时刻Na2SO4盐膜的挥发量,并绘制出两种厚度Na2SO4盐膜的挥发失重曲线,如图1所示.

图1 900 ℃空气中Na2SO4盐膜的挥发失重曲线
从图2(a)中可以看出:涂盐量40~4.5 g/m2的Fe-10Cr合金在前1.5 h腐蚀增重比较快,1.5 h增重量达到228.23 g/m2,约是相同时刻该合金单纯氧化增重的27.87倍.腐蚀24 h后,涂盐量分别为40~45 g/m2和 20~25 g/m2的Fe-10Cr合金增重分别为327.88 g/m2和204.69 g/m2,分别约为单纯氧化增重的13.42倍和8.38倍.
从图2(b)中可以看出:涂盐量分别为40~45 g/m2和20~25 g/m2的Fe-20Cr合金前1.5 h增重都比较快,1.5 h增重分别为8.76 g/m2和5.33 g/m2,分别约是单纯氧化增重的9.84倍和6倍.1.5 h至24 h,两种涂盐量的Fe-20Cr合金重量几乎没有变化,说明1.5 h后合金腐蚀层已经具有较强的热腐蚀抗力.腐蚀24 h后,涂盐量分别为40~45 g/m2和20~25 g/m2的Fe-20Cr合金增重分别为9.09 g/m2和5.84 g/m2,分别约是单纯氧化的2.18倍和1.40倍.
通过图2(a)、(b)对比可知:腐蚀24 h后,涂盐量分别为40~45 g/m2和20~25 g/m2的Fe-10Cr合金增重分别约是同等涂盐量Fe-20Cr合金的36.05倍和35.02倍,可见提高Cr元素的含量,明显提高了Fe-Cr合金的热腐蚀抗力.具体数值见表1.

图2 Fe-10Cr和Fe-20Cr合金涂覆不同厚度Na2SO4 盐膜后腐蚀24 h的动力学曲线

合金涂盐量/(g·m-2)单位面积质量增量/(g·m-2)1.5 h24 hFe-10CrFe-20Cr08.1924.4320~2540.00204.6940~45228.22327.8800.894.1720~255.345.8440~458.769.09
图3为Fe-10Cr和Fe-20Cr合金单位面积增重的平方值与时间的关系曲线,可看出,在不同涂盐量情况下,Fe基合金的热腐蚀动力学曲线分段符合抛物线规律,其抛物线速率常数列于表2.

图3 Fe-10Cr和Fe-20Cr合金单位面积增重的 平方与腐蚀时间的关系曲线

合金涂盐量/(g·m-2)时间段/hKp/ (g2·cm-4·s-1)Fe-10CrFe-20Cr0~33.65×10-920~253~117.24×10-911~243.80×10-90~1.59.65×10-840~451.5~113.95×10-911~248.07×10-90~1.54.93×10-1120~251.5~53.15×10-125~24≈00~12.00×10-1040~451~31.48×10-113~24≈0
由表2可以看出:Fe-10Cr合金的热腐蚀抛物线速率常数比相同条件下的Fe-20Cr合金的大;两种Cr含量的Fe基合金在涂盐量为20~25 g/m2的腐蚀增重速率明显小于涂盐量为40~45 g/m2的腐蚀增重速率,但在Fe-10Cr合金腐蚀中期,涂盐量为20~25 g/m2的热腐蚀速率略高于涂盐量为40~45 g/m2的腐蚀速率;随着Cr元素含量的提高,相同涂盐量合金的抛物线速率常数明显降低,降低幅度达2~3个量级.
2.2 腐蚀膜的结构与组成
图4为Fe-10Cr合金在900 ℃腐蚀24 h后腐蚀膜的断面形貌.图5为SEM/EDX 测得的Fe-10Cr合金涂覆40~45 g/m2Na2SO4盐膜在900 ℃腐蚀24 h后的腐蚀膜横断面元素面分布.从图4可以看出:Fe-10Cr合金腐蚀膜疏松有孔洞,有明显的开裂现象.随着盐膜厚度的增加,Fe-10Cr合金表面的腐蚀程度也随之增加;Fe-10Cr合金在两种厚度的盐膜下的腐蚀膜均可分为三层,即腐蚀膜外层、中间层和内腐蚀层;从图5可知Fe-10Cr合金外层是疏松单一的Fe2O3;中间层连续致密,以Fe2O3和Cr2O3的混合物为主;靠近合金基体的内腐蚀区颜色较深,有少量的Cr的硫化物.

图4 涂覆20~25 g/m2和40~45 g/m2厚度盐 膜的Fe-10Cr合金腐蚀24 h后横断面形貌

图5 Fe-10Cr基合金涂40~45 g/m2Na2SO4 盐膜的腐蚀膜截面元素面分布
图6为Fe-20Cr合金在900 ℃腐蚀24 h后腐蚀膜的横断面形貌.图7为SEM/EDX 测得的Fe-20Cr合金涂覆40~45 g/m2Na2SO4盐膜在900 ℃腐蚀24 h后的腐蚀膜横断面元素面分布.从图6可以看出:Fe-20Cr合金在两种厚度的盐膜下都形成了连续的腐蚀膜.腐蚀膜厚度都比较薄,厚度均只有5μm左右.腐蚀膜均没有明显的分层.从图7可知:Fe-20Cr合金的腐蚀层主要以Cr2O3为主,未出现内硫化现象.
通过图4和图6对比可知:Fe-20Cr合金的抗腐蚀性能在相同涂盐量情况下均比Fe-10Cr合金好,涂盐量为40~45 g/m2的两种合金对基体的腐蚀深度均比涂盐量为20~25 g/m2的腐蚀深度深,这与腐蚀动力学曲线图2和图3是一致的.

图6 涂覆20~25 g/m2和40~45 g/m2厚度盐膜的 Fe-20Cr合金腐蚀24 h后横断面形貌

图7 Fe-20Cr合金涂40~45 g/m2 Na2SO4 盐膜的腐蚀膜截面元素面分布
3 讨 论
Na2SO4盐膜的熔点为884 ℃,低于900 ℃的实验条件,因此,盐膜处于熔融状态,合金系将发生典型的高温热腐蚀.实验开始后,熔融态Na2SO4盐膜中溶解的氧首先与合金基体发生反应,但从热力学上,在实验条件下,Cr2O3的标准生成自由能较Fe氧化物的标准生成自由能更负[21],因此,合金基体表面将优先生成Cr2O3;而从动力学上,Fe氧化物的生长速度却大于Cr2O3的生长速度.综合考虑热力学和动力学因素,理想情况下,在合金和熔融态的盐界面上,将自内向外生成Cr2O3、FeO、Fe3O4和Fe2O3.但实际上,合金的热腐蚀不同于单纯的高温氧化,合金表面存在熔融态的Na2SO4盐膜.随着盐膜内部氧的消耗,在盐膜内靠近合金基体和盐膜界面附近硫活度相对增大,在化学势梯度的作用下,硫穿过氧化膜到达金属与氧化膜的界面,在该界面上生成硫化物.同时,在熔融态的盐膜内部,硫的消耗使Na2SO4中的Na2O含量相对上升,使熔盐碱化且氧离子活度增大,在熔盐和氧化膜界面上会发生如下反应,生成可溶性的铁酸根离子:
(1)

(2)
这样,熔融态盐膜内部的氧化膜层溶解并使熔盐向内渗透,同时,外层生成的Fe2O3由于其下层熔融态的盐和氧的向内扩散导致其结构疏松,熔融盐的向内渗透和原始氧化膜的不断溶解导致氧化层剥离,翘起,并出现裂纹,而氧化膜层内裂纹的出现又不断地加剧着上述过程的进行,如此重复进行,产生了疏松多孔的Fe2O3膜层,此时氧化物膜层无保护性能.
然而,实验合金中Cr含量较高,虽然Cr2O3的生长速度不及Fe氧化物的生长速度,但Cr2O3颗粒形成越多,其对氧和硫向内扩散的阻碍作用越明显.在实验条件下,熔融的Na2SO4会和Cr2O3反应,使Cr2O3发生碱性溶解,降低Cr2O3的保护性能,其反应如下[22]:
Na2SO4+Cr2O3+O2→Na2CrO4+SO2
(3)
其中,Na2CrO4在900 ℃为液态且具有挥发性,从而造成部分Cr的损失,这弱化了Cr2O3的保护性,但同时应该注意到,不是所有的Na2CrO4都挥发消耗,在O2-活度较低的地方会重新析出Cr2O3.对Fe-10Cr合金,较低含量的Cr不足以支持连续致密且具有保护性的Cr2O3膜的生成,造成了其较快的腐蚀增重速率,如图2(a)和图3(a)所示.
对Fe-20Cr合金,由于Cr的含量进一步增加,一方面在热腐蚀初期有较多Cr2O3生成,限制了热腐蚀初期氧和硫的向内扩散,因此,在Fe-20Cr合金中未发现内硫化现象,另一方面,贫Cr现象在整个过程中发生较晚,较高含量的Cr支持了Cr在反应式(3)中的消耗,最终能形成较连续的Cr2O3膜,对合金有较好的保护作用.
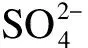
(4)
在腐蚀膜和熔盐膜界面,氧反应后被消耗,使得界面处的氧压降低,同时硫压相对升高[23-24].硫通过腐蚀膜中的空洞、晶界等缺陷向内扩散,随着硫的消耗,腐蚀膜和熔盐膜界面处的碱度随之升高.此时腐蚀膜中Cr2O3和Fe2O3被碱性溶解,使得盐膜中的碱度由内至外降低.增大盐膜厚度后,被消耗的硫得到及时补充,增大了腐蚀膜和熔盐膜界面处的碱度升高速度,从而加快了Cr2O3和Fe2O3溶解速度.因此,Fe-Cr合金在表面涂覆硫酸盐后,涂盐量为40~45 g/m2比涂盐量为20~25 g/m2腐蚀增重大.
4 结 论
(1) 两种涂盐量的Fe-10Cr和Fe-20Cr合金腐蚀均比单纯氧化严重.其中两种涂盐量的Fe-10Cr合金腐蚀增重分别约为单纯氧化增重的13.42倍和8.38倍,而两种涂盐量Fe-20Cr合金腐蚀增重分别约为单纯氧化增重的2.18倍和1.40倍.
(2) Fe-20Cr合金涂两种厚度Na2SO4盐膜在900 ℃腐蚀24 h的增重较Fe-10Cr合金小,对相同Cr含量的Fe-Cr合金,涂盐量为40~45 g/m2时腐蚀增重比涂盐量为20~25 g/m2时腐蚀增重大.
(3) Fe-10Cr合金腐蚀膜可分为3层结构,外层是Fe2O3,中间层以Cr2O3和Fe2O3的混合氧化物为主,内腐蚀区有少量的Cr的硫化物.Fe-20Cr合金腐蚀膜在两种厚度Na2SO4盐膜下腐蚀24 h后腐蚀膜为单一的Cr2O3.
参考文献:
[1] 王海涛,张国玲,于化顺,等.铬、铝、硅对铁基高温合金抗氧化性能的影响[J].材料工程,2008,33(12):73-78.
[2] 高雪云,陈守良,王海燕,等.利用经验电子理论(EET)分析Al对Fe-Cr高温合金冲击韧性的影响[J].特殊钢,2012,33(4):67-70.
[3] 张允书,石声泰.热腐蚀的电化学机理初探[J].腐蚀科学与防护技术,1993,5(1):23-31.
[4] 张宏亮,付广艳,储昭贶.Fe-Y合金的高温热腐蚀[J].稀土,2007,28(6):53-58.
[5] 张允书,史良权,石声泰.表面有Na2SO4沉积时铁基合金的低温热腐蚀行为[J].中国腐蚀与防护学报,1992,12(3):189-195.
[6] SHI L Q.Accelerated Oxidation of Iron Induced by Na2SO4Deposits in Oxygen at 750 ℃-New Type Low-temperature Hot Corrosion[J].Oxidation of Metals,1993,40(1/2):197-211.
[7] HARPREET S,PURI D,PRAKASH S.Some Studies on Hot Corrosion Performance of Plasma Sprayed Coatings on a Fe-based Superalloy[J].Surface and Coatings Technology,2005,192(1):27-38.
[8] SIDHU T S,PRAKASH S,AGRAWAL R D.Performance of High-velocity Oxyfuel-sprayed Coatings on an Fe-based Superalloy in Na2SO4-60 %V2O5Environment at 900 ℃ Part II:Hot Corrosion Behavior of the Coatings[J].Journal of Meterials Engineering and Performance,2006,15(1):130-138.
[9] MAHESH R A,JAYAGANTHAN R,PRAKASH S.A Study on Hot Corrosion Behaviour of Ni-5Al Coatings on Ni-and Fe-based Superalloys in an Aggressive Environment at 900 ℃[J].Journal of Alloys and Compounds,2008,460(1/2):220-231.
[10] 贺定勇,王晓芳,蒋建敏.铁基高铬涂层热腐蚀行为的研究[J].热喷涂技术,2009,1(1):63-66.
[11] WANG C J,CHANG Y C.NaCl-induced Hot Corrosion of Fe-Mn-Al-C Alloys[J].Materials Chemistry and Physics,2002,76(2):151-161.
[12] BANI P M,DAVID A S.Role of Chlorides in Hot Corrosion of a Cast Fe-Cr-Ni Alloy.Part I:Experimental Studies[J].Corrosion Science,2004,46(12):2893-2907.
[13] 史良权,张允书,石声泰.Na2SO4+ MgSO4+ CaSO4沉积引起的铁基合金的热腐蚀[J].中国腐蚀与防护学报,1990,10(2):127-134.
[14] ZHENG L,ZHANG M C,DONG J X.Hot Corrosion Behavior of Powder Metallurgy Rene95 Nickel-base Superalloy in Molten NaCl-Na2SO4Salts[J].Materials and Design,2011,32(4):1981-1989.
[15] CHO S H,HUR J M,SEO C S,et al.Hot Corrosion Behavior of Ni-base Alloys in a Molten Salt under an Oxidizing Atmosphere[J].Journal of Alloys and Compounds,2009,468(1/2):263-269.
[16] Li M H,Sun X Y,Hu W Y,et al.Hot Corrosion of a Single Crystal Ni-base Superalloy by Na-salts at 900 ℃[J].Oxidation of Metals,2006,65(1/2):137-150.
[17] 贾志涛.K38合金热浸镀铝抗高温氧化性能的研究[D].哈尔滨:哈尔滨工程大学,2003.
[18] BRUCE M W,FRED S P,GERALD H M.Hot-corrosion Resistance of Ni-Cr-Al-Y and Ni-18 % Si Slloys in Sulfate Eutectic and Sulfate Plus Vanadate Melts at 973 K[J].Oxidation of Metals,2002,58(5/6):487-498.
[19] KAMAL S,JAYAGANTHAN R,PRAKASH S.High Temperature Cyclic Oxidation and Hot Corrosion Behaviours of Superalloys at 900 ℃[J].Bulletin of Materials Science,2010,33(3):299-306.
[20] FRED P.Hot Corrosion of Metals and Alloys[J].Oxidation of Metals,2011,76(1/2):1-21.
[21] 李美栓.金属的高温腐蚀[M].北京:冶金工业出版社,2001:5.
[22] 赵双群,谢锡善.新型Ni-Cr-Co基高温合金的热腐蚀行为[J].材料科学与工艺,2006,14(5):506-510.
[23] 张允书.热腐蚀的盐溶机理及其局限性[J].中国腐蚀与防护学报,1992,12(1):1-10.
[24] 娄世松,于凤昌,左禹.渗铝钢在Na2SO4-V2O5熔盐体系中的热腐蚀行为[J].材料保护,2005,38(4):1-6.
