立构复合聚乳酸的制备及表征
2014-03-25谢文靖朱志国张秀芹
谢文靖,王 锐,朱志国,张秀芹,戈 欢
(北京服装学院材料科学与工程学院,北京100029)
聚乳酸(PLA)是一种以可再生的植物资源为原料经过化学合成制备的生物降解高分子材料,摆脱了对石油资源的依赖,具有良好的可堆肥性和生物降解性,降解产生的二氧化碳和水可以返回大自然,不会对环境造成污染[1]。因此,PLA材料具有广泛发展前景,在工农业生产及生物医用材料领域应用广泛,其研究与生产备受瞩目,但是其性能还有待进一步提高。提高PLA耐热性的主要技术是改善PLA的结晶性能,提高PLA的结晶度,另外还有与高玻璃化转变温度高分子共混、引入交联结构、纤维增强以及纳米复合等技术[2]。将聚左旋乳酸(PLLA)和聚右旋乳酸(PDLA)共混形成的立构复合型聚乳酸(sc-PLA)的熔点约为230℃,比各自均聚物高出50℃左右,有利于提高PLA的耐热性和结晶性,有望成为一种高性能聚合物[3-5]。作者采用直接熔融缩聚分别制备PLLA和PDLA预聚物,选择相对分子质量相近的两种预聚物进行不同比例混合,经过溶液混合形成立构复合晶体结构,再通过固相聚合提高产物的相对分子质量[6-7],以期达到改善 PLA耐热性和结晶性的目的。
1 实验
1.1 原料
L-乳酸,D-乳酸:90%溶液,武藏野化学(中国)有限公司产;对甲苯磺酸(TSA):分析纯,天津福晨化学试剂厂产;氯化亚锡、二氯甲烷、无水乙醇、丙酮:均为分析纯,北京化工厂产;六氟异丙醇(HFIP):百灵威科技有限公司产。
1.2 直接熔融缩聚法制备PLLA及PDLA
首先将L-乳酸在100℃下进行逐步减压蒸馏除去自由水,得到纯度较高的L-乳酸,然后称取一定量L-乳酸加入250 mL三口烧瓶中,并加入质量分数0.4%氯化亚锡和等摩尔的TSA,体系逐渐减压,在机械搅拌下加热升温,从130℃逐步升至160℃,反应4 h;然后在高真空下,1 h从160℃升至170℃,于170℃反应4 h,结束反应。用二氯甲烷溶解,用乙醇沉淀提纯,真空干燥4 h,得到PLLA预聚物,标记为1#试样。采用同样方法制备PDLA预聚物,标记为2#试样。
1.3 sc-PLA 的制备
从直接熔融缩聚的产物中选择相对分子质量相近的PLLA和PDLA,以不同质量比混合并用二氯甲烷溶解,磁力搅拌2 h,使其充分混合溶解,室温下等待其溶剂挥发,即得到sc-PLA,PLLA/PDLA质量比为50/50,80/20,90/10得到的sc-PLA依次标记为3#,4#,5#试样。将sc-PLA磨成粉末,在105℃真空环境下热处理2 h,冷却后各称取4 g粉末进行固相缩聚,温度分别控制在140,150,160℃各反应10 h[8],反应过程中聚合物保持粉末状态,最终得到产物为白色粉末,试样3#,4#,5#对应的固相缩聚产物依次标记为6#,7#,8#。
1.4 分析与测试
差示扫描量热(DSC)分析:采用Seiko Instruments Inc公司的Seiko DSC-6200差示扫描量热仪测试。试样质量约为6.5 mg,升温速度为10℃/min,测试温度室温~250℃,氮气气氛,流速为50 mL/min。
凝胶渗透色谱(GPC)分析:采用Waters公司的L GPC 515-2410凝胶渗透色谱仪测试,色谱柱温为100℃,间甲酚为流动相,流速1.0 mL/min,以聚苯乙烯为标样进行校正。
广角X射线衍射(WAXD)分析:采用日本理学电机公司的Rigaku XRD-6000广角X射线衍射仪测试。主单色器为Cu Kα辐射,λ为0.154 nm,扫描速率 4(°)/min,扫描范围 4°~40°。
热失重(TG)分析:采用耐驰公司的TG209 F1热失重分析仪测试,测试温度40~500℃,升温速率为10℃/min,氮气流量为50 mL/min。
2 结果与讨论
2.1 DSC分析
从图1可以看出,两种构型的PLA预聚物在升温热扫描过程中在160℃附近出现明显吸热峰,经过溶液共混形成的立构复合物熔点提高到210℃左右,其中3#试样仅在217℃附近出现1个吸热峰,说明3#试样的结晶几乎全部为立构复合物的晶体结构,而4#试样在156℃和211℃出现2个熔融吸热峰,分别对应为PLA均聚物晶体和sc-PLA晶体的熔融吸热峰。5#试样在升温扫描过程中有3个熔融吸热峰,在159℃和166℃附近出现的吸热峰,主要是PLLA和PDLA晶体形成的,因为试样相对分子质量分布不均匀,在初始熔融区域形成的分子链能促进其他区域分子链运动,并提高其他结晶区域的形成,结果导致第2个熔融峰的出现[9]。
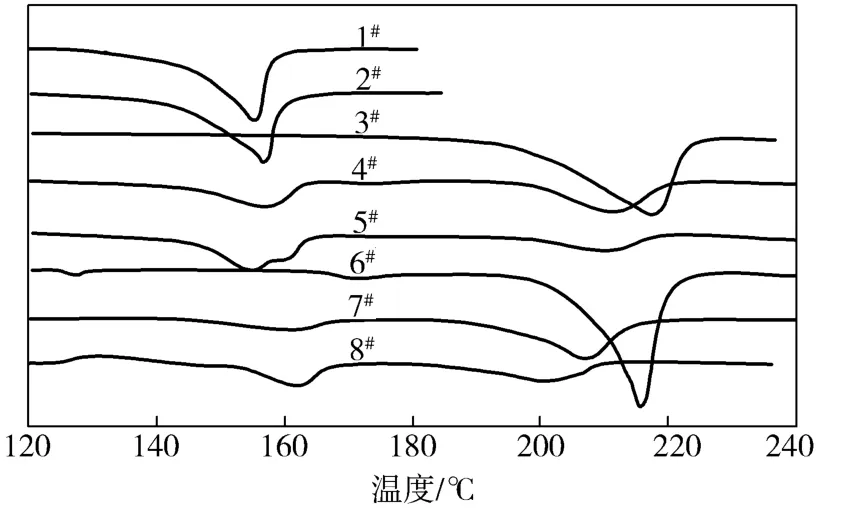
图1 PLA试样的DSC曲线Fig.1 DSC curves of PLA samples
当PLLA的质量分数偏离50%越多,所形成sc-PLA 的含量也相应减少。6#,7#,8#分别是 3#,4#,5#固相缩聚后的产物,经过固相聚合后,聚合物中形成的立构复合晶体的熔融温度都有所下降,这是因为经过固相缩聚反应,产物中立构复合晶区链规整度变差,而均聚物晶区熔融温度提高,且PLA均聚物链运动能力强,经过固相聚合相对分子质量明显提高,其熔点也相应升高。DSC分析结果表明 ,溶液共混是制备sc-PLA的一种有效方法,可使聚合物熔点提高50℃,对改善PLA的耐热性有利。当PLLA质量分数为50%时,可以得到几乎全部是立构复合的晶体结构,随着PLLA含量增大,出现均聚物晶区,相应地,立构复合物结构晶体比例减小。当PLLA质量分数接近100%时,结晶区域主要为均聚物的晶体结构。
2.2 WAXD 分析
从图2可知:曲线1和曲线2为PLLA和PDLA 的衍射峰,均在2 θ为15°,16°,18.5°,22.5°位置出现明显衍射峰,证明PLLA和PDLA晶体为α晶型;3#和 6#试样的曲线仅在 2 θ为 12°,21°,24°出现明显衍射峰,表明其全部为立构复合物的β晶型结构,从而提高了 PLA 的熔点[1,10];而 4#,5#及相应的固相缩聚产物(7#和8#)既有均聚物晶体的特征峰,又有立构复合物晶体的特征峰 ,并且随着PLLA含量的增大,其均聚物晶体衍射峰增强,立构复合晶体衍射峰减弱。
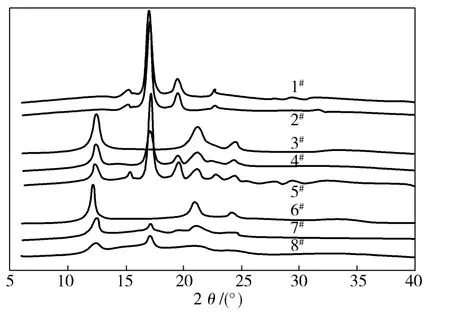
图2PLA试样的WAXD曲线Fig.2 WAXD curves of PLA samples
另外,在PLLA含量相同时,固相缩聚后产物6#~8#试样的均聚物晶体和立构复合晶体的衍射峰都比对应的3#~5#试样的峰小,这表明经过30 h固相缩聚后,聚合物中均聚物区域和立构复合区域的结晶度比固相缩聚之前均有所减小,原因是在固相聚合过程中随着相对分子质量增加,分子链变长,链规整度变差,结晶度下降。
2.3 GPC 分析
从表1可看出,经过固相聚合后,产物的相对分子质量与固相聚合之前相比得到了一定的提高,其中3#,4#,5#经过固相聚合后,重均相对分子质量(Mw)分别增加到 3.2 ×104,4.3 ×104,5.3×104。随着共混物中 PLLA含量增大,固相缩聚产物相对分子质量增加程度越大。这是因为立构复合晶体结构更加紧密,对末端功能基团(羟基及羧基)运动与扩散有阻碍作用,尤其是3#为全立构复合物,其结构最为稳定和紧密,功能团运动能力最差,所以固相聚合后相对分子质量增加程度最弱[11]。此外,固相缩聚后产物相对分子质量分布变宽,这是因为在固相聚合中,固体反应物链运动能力相差较大,从而造成聚合物相对分子质量增长程度差异较大。实验结果表明,PLA均聚物部分对固相聚合产物相对分子质量的增加具有较大的贡献,与文献[12]的结果一致。
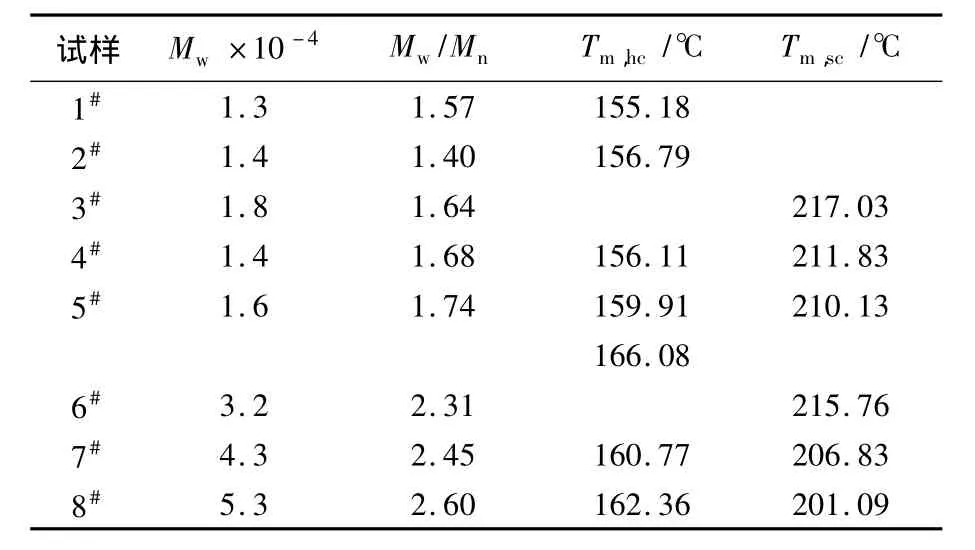
表1PLA试样的GPC结果Tab.1 GPC results of PLA samples
2.4 TG 分析
从图3可以看出,溶液共混形成的sc-PLA与PLLA和PDLA预聚物的TG曲线类似,其热分解温度相近(220~280℃),可能因为这些聚合物中金属离子、相对分子质量以及乳酸残余量基本相同,其热降解机理也相似[9];同时,立构复合结构虽然能够提高PLA的熔点,但是不能改善PLA的热降解稳定性。固相聚合后,产物(6#~8#)的起始热分解温度明显提高,并且随着PLLA含量增大,其热稳定性越好,这是因为随着PLLA比例增大,固相聚合对聚合物相对分子质量增长的贡献越明显,使得聚合物的热分解温度得到提高。TG分析结果表明,相对分子质量对于提高PLA的热稳定性具有重要作用,而是否形成立构复合结构仅对其熔点有明显影响。
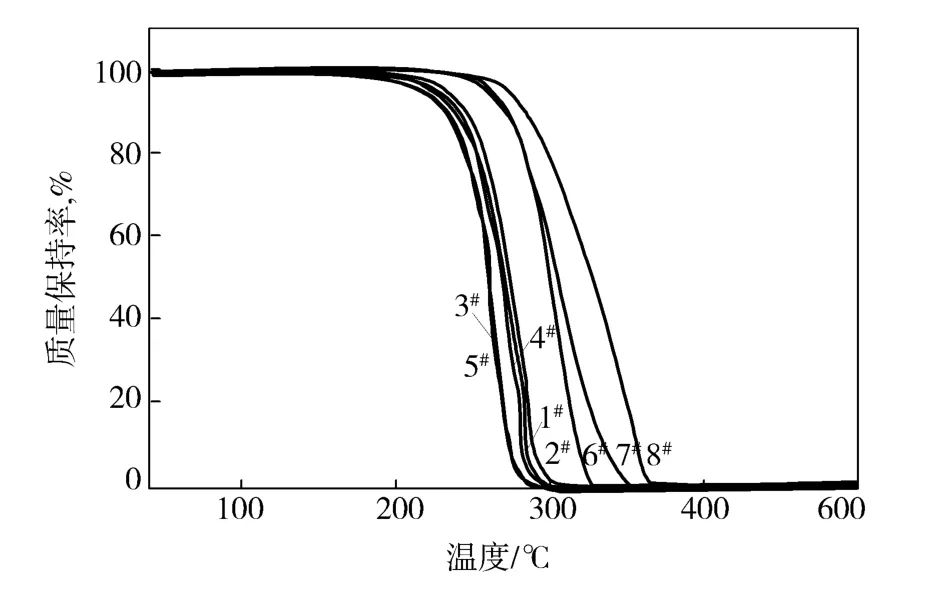
图3 PLA试样的TG曲线Fig.3 TG curves of PLA samples
3 结论
a.相对分子质量相近的PLLA与PDLA共混后,形成的sc-PLA具有更致密和紧凑的晶体结构,其熔点较其均聚物约高55℃;当PLLA质量分数越接近50%,形成的立构复合晶体比例越多,在PLLA质量分数为50%时,共混物完全形成立构复合结构,其熔点也最高,为217℃。
b.固相缩聚能够提高PLA共混物的相对分子质量,且主要通过PLA均聚物部分的链增长实现。PLA的热分解稳定性主要与其相对分子质量大小有关,而形成立构复合结构与否及其含量多少并不能提高其热分解温度,仅对其熔点有影响。
[1] 李菁,陈大凯,任杰.聚乳酸立构复合物的研究最新进展与应用展望[J].高分子通报,2011(1):33-39.
[2] 杨斌.绿色塑料聚乳酸[M].北京:化学工业出版社,2007:72-82.
[3] Ikada Y,Jamshidi K,Tsuji H,et al.Stereocomplex formation between enantiomeric poly(lactides)[J].Macromolecules,1987,20(4):904 -906.
[4] Jamshidi K,Hyon S H.Ikada Y.Thermal characterization of polylactides[J].Polymer,1988,29(12):2229 -2234.
[5] Tsuji H.Poly(lactide)stereocomplexs:Formation,structure,properties,degradation,and applications[J].Macromol Biosci,2005,5(7):569 -597.
[6] Tsuji H,Tezuka Y.Stereocomplex formation between enantiomeric poly(lactic acid)s.12.Spherulite growth of low-molecular-weight poly(lactic acid)s from the melt[J].Biomacromolecules,2004,5(4):1181 -1186.
[7] Fukushima K,Furuhashi Y,Sogo K,et al.Stereoblock poly(lactic acid):Synthesis via solid-state polycondensation of a stereocomplexed mixture of poly(L-lactic acid)and poly(D-lactic acid)[J].Macromol Biosci,2005,5(1):21 -29.
[8] Chen Dakai,Li Jing,Ren Jie.Crystal and thermal properties of PLLA/PDLA blends synthesized by direct melt polyconsendation[J].J Polym Environ,2011,19(3):574 -581.
[9] Hirata M,Kimura Y.Thermomechanical properties of stereoblock poly(lactic acids)with different PLLA/PDLA block compositons[J].Polymer,2008,49(11):2656 -2661.
[10]Brizzolara D,Cantow H J,Diederichs K,et al.Mechanism of the stereocomplex formation between enactiomeric poly(lactide)s[J].Macromolecules,1996,29(1):191 -197.
[11]Fukushima K,Kimura Y.An efficient solid-state polycondensation method for synthesizing stereocomplexed poly(lactic acid)s with high molecular weight[J].J Polym Sci A:Polym Chem,2008,46(11):3714-3722 .
[12]Fukushima K,Hirata M,Kimura Y.Synthesis and characterization of stereoblock poly(lactic acid)s with nonequivalent D/L sequence ratios[J].Macromolecules,2007,40(9):3049 -3055.
