参麦注射液辅助治疗恶性肿瘤的有效性及安全性系统评价❋
2014-02-09吴玖斌谢雁鸣王连心陈弘东
吴玖斌,谢雁鸣,王连心△,陈弘东,李 蒙
(1.中国中医科学院中医临床基础医学研究所,北京 100700;2.中国中医科学院望京医院,北京 100102;3.中国中医科学院广安门医院,北京 100053)
恶性肿瘤是指恶性细胞不受控制的进行性增长和扩散,浸润和破坏周围正常组织,可以经血管、淋巴管和体腔扩散转移到身体其他部位的疾病。对于恶性肿瘤的治疗,目前尚无很好的控制疗法。西医主要运用放疗、化疗、手术及免疫治疗,但毒性反应和副作用很大,中医药辅助治疗可兼顾局部与全身,能有效地减轻西医治疗的毒性反应和副作用,且能有效提高生活质量。
参麦注射液参是由红参、麦冬组成的中药制剂,具有益气固脱、养阴生津、生脉的功效。从中医角度分析,参麦注射液有益气扶正之功,能提高机体抗病能力,正如《内经》云:“正气存内,邪不可干”;其益气、养阴生津功效,能减轻病人气阴耗伤之弊,如减轻患者因放化疗而呈现出的气阴亏耗的表现。从现代药理研究看,其具有抗多脏器缺血、抗炎、增强免疫功能、保护心脏及减轻某些药物毒性作用和副作用等[1,2]。中医学认为肿瘤为癥瘕,多为气滞、血瘀、痰凝而成,化疗更是耗伤气阴。参麦注射液益气固脱、养阴生津及生脉之功,临床常用于粒细胞减少、心血管疾病、免疫力低下、肿瘤[3]及各种慢性疾病的辅助治疗。
1 资料与方法
1.1 纳入和排除标准
1.1.1 有效性研究 纳入随机对照试验(RCTs)或半随机对照试验(quasi-RCTs),语种限制为中英文。研究对象为恶性肿瘤患者,年龄、性别、种族不限。治疗组干预措施是在常规治疗基础上加用参麦注射液(简称参麦),用药方式为静脉滴注;对照组为常规治疗,常规治疗除静卧、营养支持、止痛、镇静、补充电解质外,一般包括放疗和化疗等。主要结局指标为白细胞下降发生率(I、II、III、IV),次要结局指标为血小板下降发生率(I、II、III、IV)和生活质量改善率。骨髓抑制根据世界卫生组织(WHO)分级标准,生活质量根据卡氏(Karnofsky,KPS,百分法)功能状态评分标准。排除以下类型文献:研究类型不符;文献综述;干预措施/使用方式不符;对重复发表或雷同的文献,仅保留最后发表的1篇;对同一研究多次发表的情况,仅保留样本量最大和信息最全的1篇;无本研究关注指标;试验组/对照组样本例数<40例;数据不完整或错误。
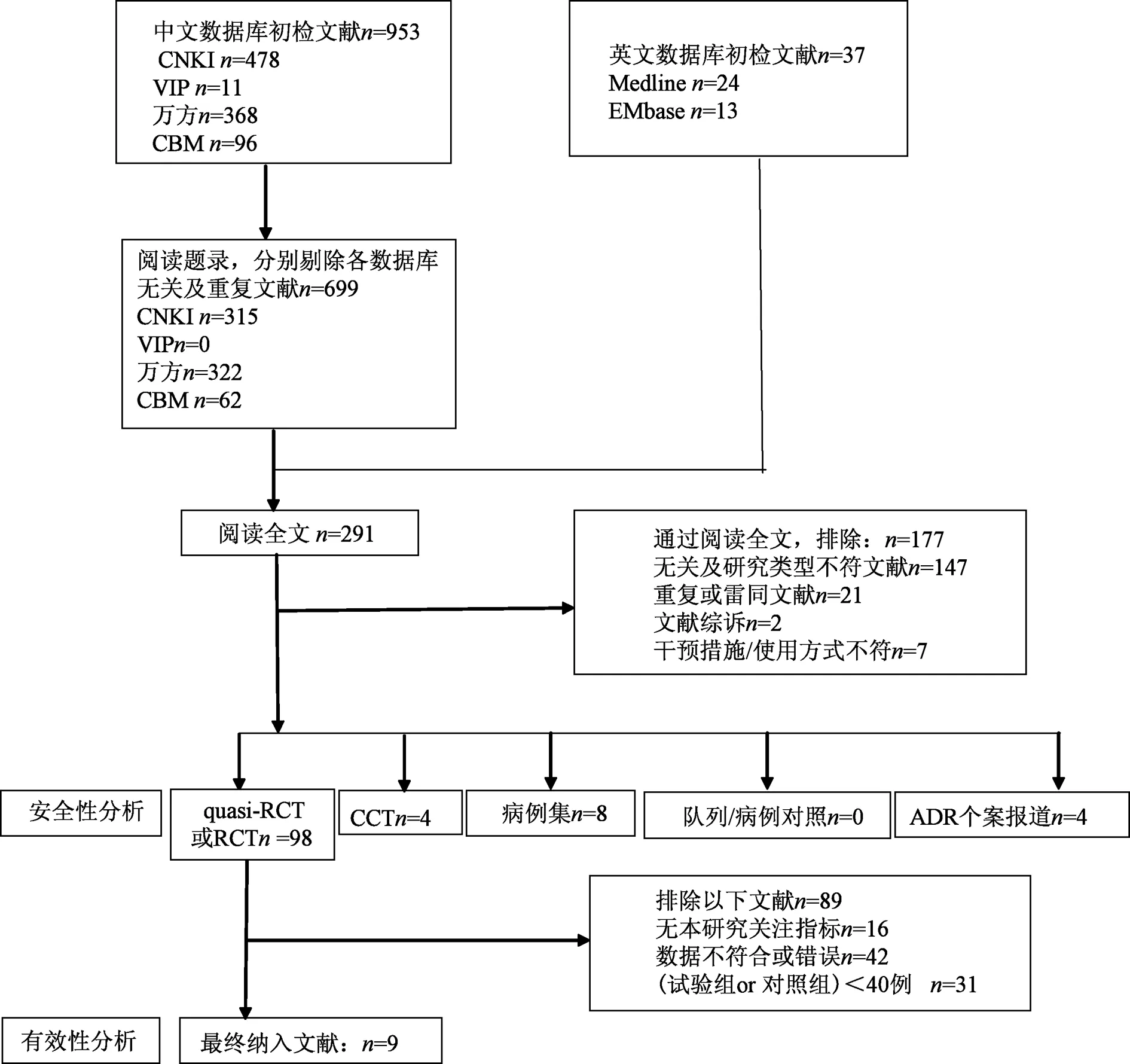
图1 文献筛选流程图
1.1.2 安全性研究 纳入所有类型的临床研究,包括RCTs、quasi-RCTs、临床对照研究(CCT)、病例对照研究、队列研究、病例集、不良反应个案报道等,语种限制为中英文。研究对象同有效性研究。只要使用参麦注射液的均纳入,不论是否合用其他药物以及对照组采用何种治疗。结局指标为所有报告因参麦注射液引起的不良反应/不良事件(ADR/AE)。
1.2 文献检索
以“shenmai”、“shen mai”、“ginseng”、“Chinese herb medcine”、“Chinese traditional medicine herb”、“tumor”、“ cancer”、“chemotherapy”等为检索词,检索Cochrane图书馆、Medline和EMbase;以“参麦”、“肿瘤”、“癌”、“化疗”、“正大”“青春宝”、“登峰牌”等为检索词,检索中国生物医学文献数据库(CBM)、中国期刊全文数据库(CNKI)、万方以及中文科技期刊全文数据库(VIP),各数据库的检索时间均为各库起始年代至2014年4月。尚无Cochrane图书馆相关资源,故未检索。
1.3 质量评价与资料提取
文献筛选、资料提取及质量评价均为2人独立进行,并对结果进行比对,如有分歧,通过讨论或咨询第3位评价者解决。质量评价采用Cochrane Reviewer′s Handbook 5.0评价标准,对随机分配方法、分配隐藏、盲法、不完整资料、选择性报告偏倚和其他偏倚来源等6个方面内容进行评价。
1.4 资料分析
有效性研究采用Cochrane协作网提供的RevMan5.2软件进行数据处理。本研究分析指标均为二分类变量,采用比值比(RiskRatio,RR)表示。采用卡方检验,P以及l2综合判断各研究间异质性,安全性研究采用描述性分析。
2 结果
2.1 数据库检索结果
2.2 有效性研究
2.2.1 纳入研究的一般特征 表1显示,9个研究共纳入1544个受试者,试验组和对照组分别为846例和698例,最大样本量为380例,最小为80例,所有结局指标均为住院期间发生的情况。9个研究中有1个说明采用随机数字表法,其他仅有随机字样而未描述具体方法。所有研究均未提及分配隐藏、盲法、偏倚及失访等。
2.2.2 白细胞下降发生率 图2显示,白细胞I下降发生率共纳入8个研究,合并显示RR及95%CI为1.33(1.04,1.71),差异无统计学意义。图3显示,白细胞II下降发生率共纳入8个研究,合并显示RR及95%CI为0.59(0.48,0.72),差异有统计学意义,表明参麦加常规组在降低白细胞II下降发生率方面优于单纯常规治疗组。图4显示,白细胞III下降发生率共纳入8个研究,合并显示RR及95%CI为0.35(0.19,0.63),差异有统计学意义,表明参麦加常规组在降低白细胞III下降发生率方面优于单纯常规治疗组。图5显示,白细胞IV下降发生率共纳入8个研究,合并显示RR及95%CI为0.25(0.13,0.47),差异有统计学意义,表明参麦加常规组在降低白细胞IV发生率方面优于单纯常规治疗组。
2.2.3 血小板下降发生率 图6显示,血小板I下降发生率共纳入5个研究,合并显示RR及95%CI为0.90(0.56,1.45),因I2=81%>75%,各研究之间存在高度异质性,差异无统计学意义。图7显示,血小板II下降发生率共纳入5个研究,合并显示RR及95%CI为0.70(0.53,0.94),差异有统计学意义,表明参麦加常规组在降低血小板II下降发生率方面优于单纯常规治疗组。图8显示,血小板III发生率共纳入5个研究,合并显示RR及95%CI为0.26(0.12,0.57),差异有统计学意义,表明参麦加常规组在降低血小板III发生率方面优于单纯常规治疗组。
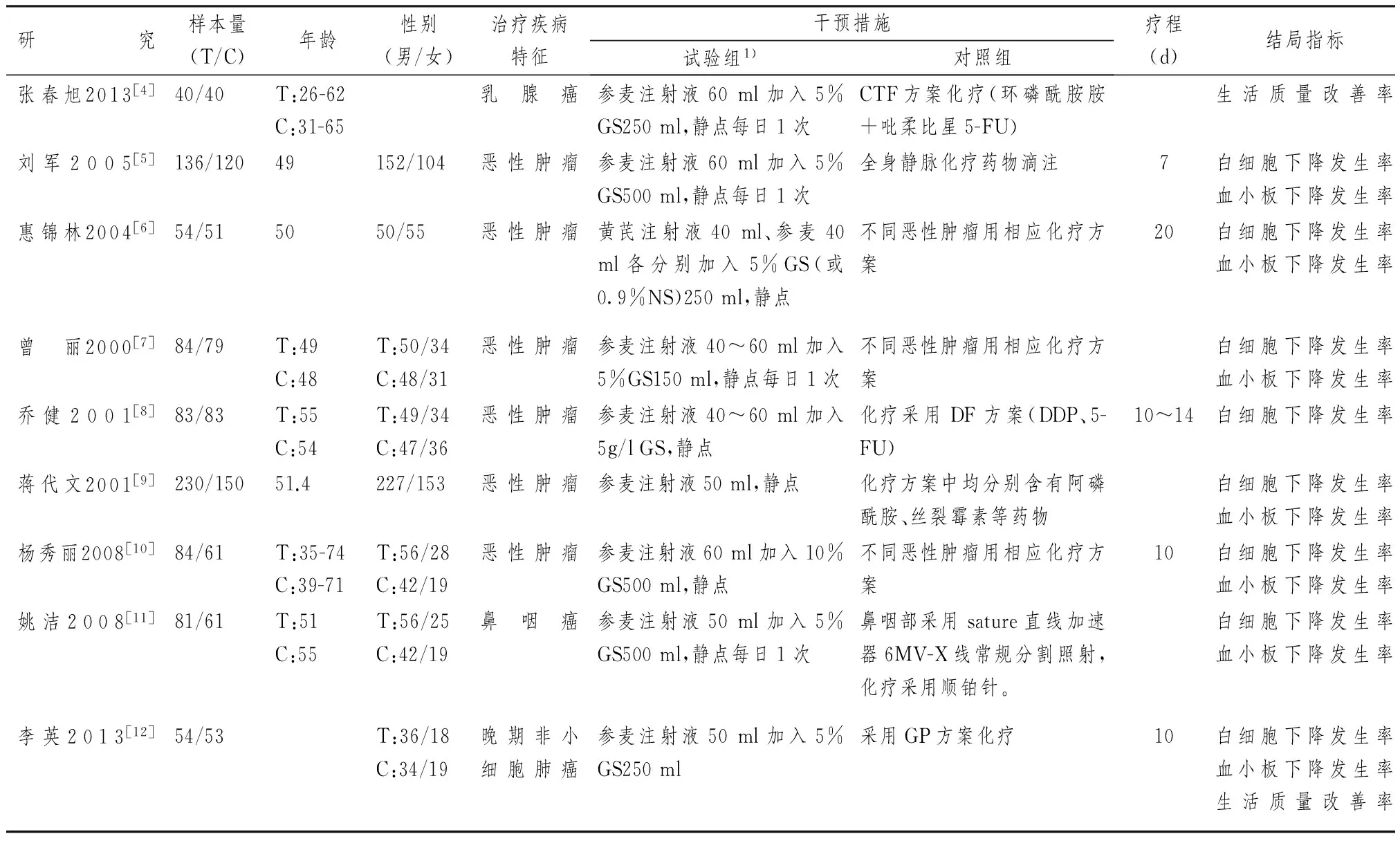
表1 纳入研究基本情况表
注:T:试验组;C:对照组。1)治疗组均是在对照组的基础上加用参麦注射液
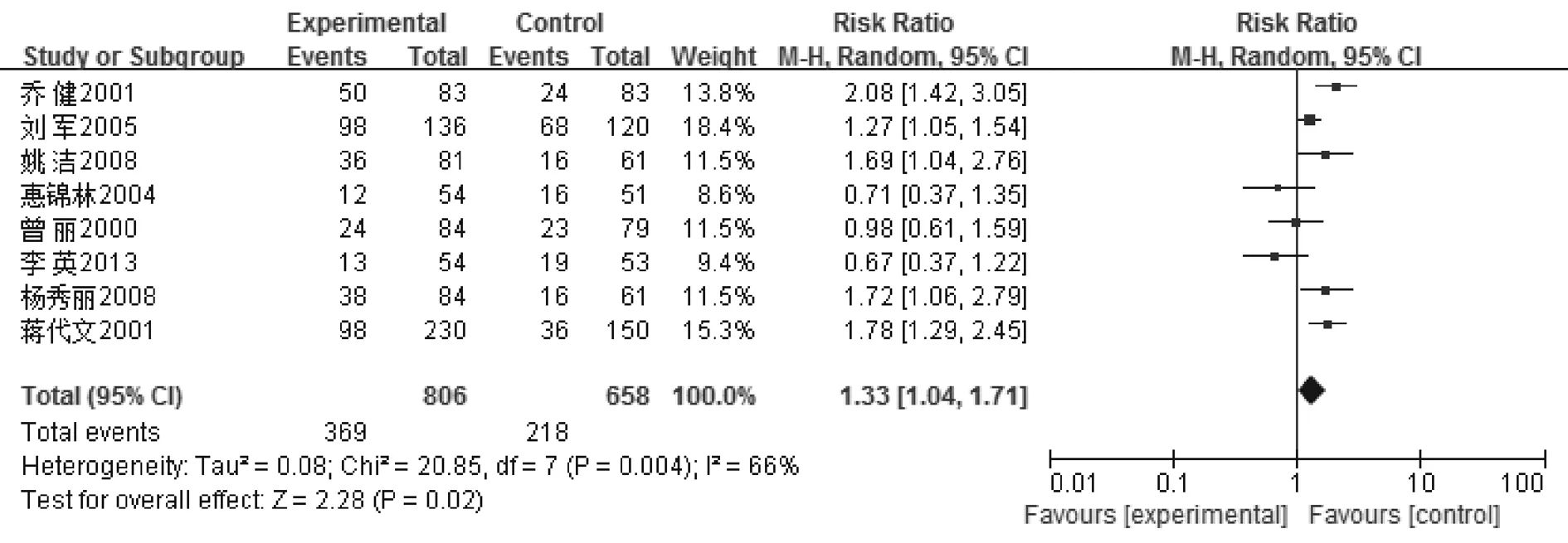
图2 白细胞I下降发生率森林图
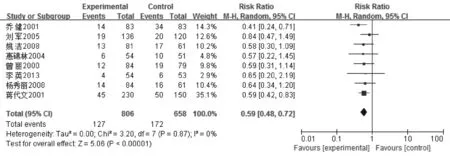
图3 白细胞II下降发生率森林图

图4 白细胞III下降发生率森林图

图5 白细胞IV下降发生率森林图

图6 血小板I下降发生率森林图
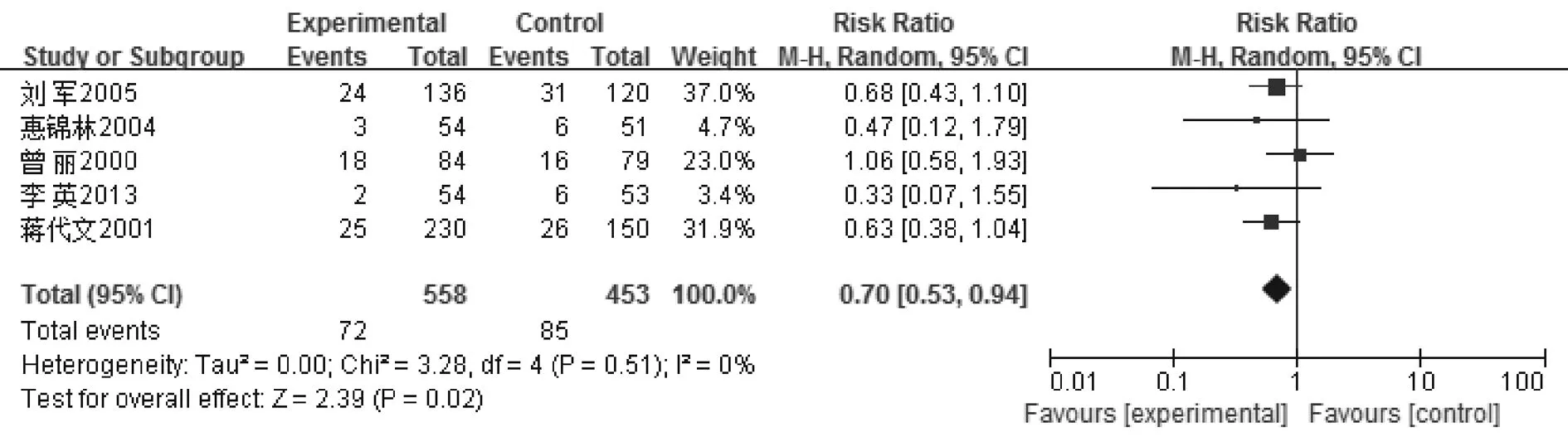
图7 血小板II下降发生率森林图
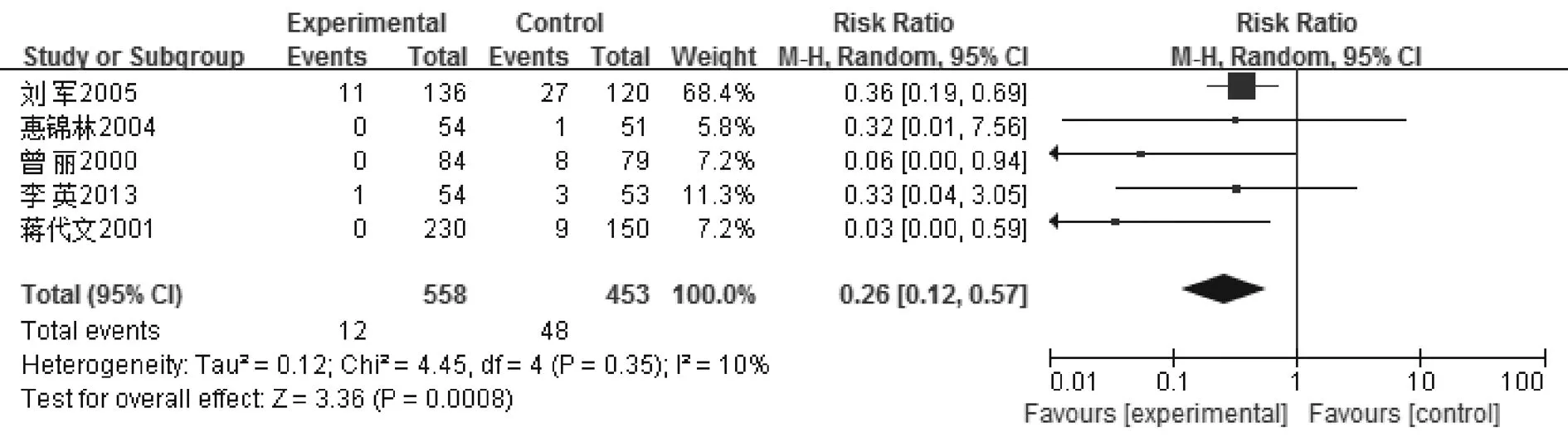
图8 血小板III下降发生率森林图

图9 血小板IV下降发生率森林图
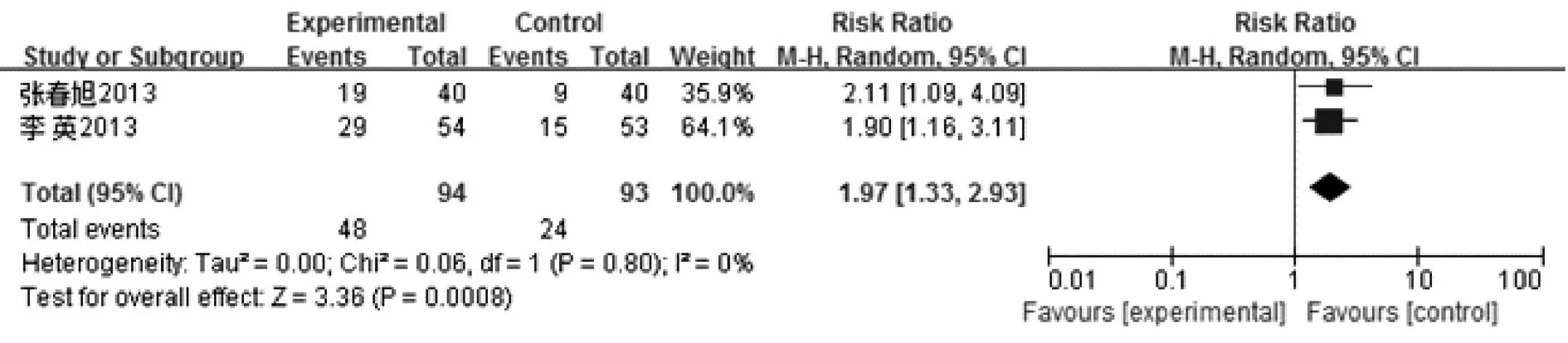
图10 生活质量改善率森林图
图9显示,血小板IV发生率共纳入5个研究,合并显示RR及95%CI为0.16(0.03,0.72),差异有统计学意义,表明参麦加常规组在降低血小板IV发生率方面优于单纯常规治疗组。图10显示,生活质量改善率共纳入2个研究,合并显示RR及95%CI为1.97(1.33,2.93),差异有统计学意义,表明参麦加常规组在生活质量改善率方面优于单纯常规治疗组。
2.3 安全性研究
2.3.1 共纳入112个研究,包括98个RCT或quasi-RCT和4个CCT。其中94个未提及因参麦注射液引起的ADR/AE,5个报道未出现ADR,3个报道了ADR。邹彦等[13]报道了参麦注射液在使用过程中有个别病人出现一过性面色潮红,可自行缓解;刘鲁明等[14]报道了参麦静脉给药过程中,有4例患者出现皮肤瘙痒,其中2例出现皮疹,中止用药后即消失;龙建安等[15]报道了使用参麦注射液过程中,有3例病人出现皮肤瘙痒,1例出现过皮疹,经对症处理后消失。
2.3.2 病例集共纳入8个研究,7个未提及ADR/AE,1个报道了使用参麦注射液过程中未出现ADR。
2.3.3 不良反应个案报道共纳入4个研究。王洪燕等[16]报道了1例70岁男性胃癌术后患者,静点参麦注射液40 ml+5%GS500 ml后,当天即出现间断呃逆、上腹不适但未在意。第2天继续滴注,约30 min后出现烦躁不安、精神紧张、面色潮红、呃逆频作,继则出现恶心呕吐物约200 ml,血压下降等。考虑胆汁反流刺激吻合口致出血,即给予立即止血、凝血酶止血等处理,未再出血,3 d后诸症消失。舒春花等[17]报道了1例60岁男性粒细胞肉瘤患者,当日18∶30静点参麦注射液50 ml+5%GS250 ml+水溶性维生素1.0 g后,无明显不适,20∶35患者出现四肢瘙痒、呼吸急迫、喉头水肿,考虑因参麦引起的过敏反应立即停止输液,给予地塞米松5 mg静推,并予吸氧,症状稍有好转;20∶37再次给予地塞米松5 mg静推,给予葡萄糖酸钙缓慢静推后症状好转。魏立云[18]报道了1例52岁女性左乳癌术后淋巴结转移患者,静点参麦注射液60 ml+5%GS250 ml10 min后突然出现胸闷、咽喉部不适、发痒、呼吸急促、不能言语,立即停止滴注,给予非那更、吸氧,约20 min后症状缓解。张红等[19]报道了1例59岁男性肺癌患者,静点参麦注射液60 ml+10%GS500 ml 3 d后,患者感到四肢皮肤瘙痒,以双下肢更甚,四肢伸侧皮肤出现对称性斑丘疹且压之不褪色,部分融合。因患者未用其他药物,考虑参麦所致,停用后症状消失;同时还报道了1例37岁男性恶性黑色素瘤患者,静点参麦注射液60 ml+10%GS500 ml后,当日出现四肢及躯干皮肤瘙痒明显,搔抓后出现散在风团块样斑丘疹,给予炉甘石洗剂外涂后瘙痒减轻,皮疹渐退。次日再次输入参麦后,上述症状依然出现,考虑为参麦过敏所致,停用后症状消失。
3 讨论
3.1 有效性
本系统评价纳入的所有研究仅提及采用随机,仅1个研究描述了采用随机数字表的方法,所有研究均未报告分配隐藏、盲法及失访等情况。白细胞总下降发生率、血小板总下降发生率森林图都显示I2=99%,出现这种高度异质性的原因,可能由于各研究者间研究设计质量及纳排标准差异、治疗方案不同、药品剂量不同以及测量差异等因素所致。因纳入原始研究存在多种偏倚,使本研究结果的精确性受到一定影响。但我们还是可以看出,参麦注射液辅助治疗恶性肿瘤,能减轻因化疗等治疗引起的严重毒副反应,如降低白细胞II、III、IV下降发生率等,还能相对提高患者生活质量改善率。当然,参麦注射液的临床有效性需前瞻性的研究给予证实[20]。
3.2 安全性
本系统评价纳入参麦辅助治疗恶性肿瘤所有类型的临床研究进行安全性分析。在用药方面,未发现超量使用、滴速过快等不合理用药。在不良反应个案报道方面,发现3例因参麦治疗引起的严重不良反应,1例上消化道出血,2例严重过敏反应,另外还有2例出现皮肤瘙痒、斑丘疹等。在对照临床研究中,3个研究报道了不良反应,主要以皮肤瘙痒、皮疹等为主。建议临床上静脉滴注参麦前详细询问患者有无相关过敏史,滴注时剂量要适宜,速度不宜过快;在用药过程中,主动询问有无不适,如发现不良反应立即采取相应措施,保证用药安全。
3.3 启示
该系统评价表明,常规治疗基础上加用参麦可以减轻放化疗引起的毒副反应,如骨髓抑制(白细胞/血小板下降发生率)等,还可以改善患者生活质量。另笔者发现,肿瘤标志物和恶性肿瘤患者生存率方面的研究甚少,各研究者可从这个角度进一步观察和证实参麦注射液等其他药物的临床疗效[21]。本系统评价纳入的研究样本量小,随机方法、分配隐藏、盲法及失访等描述不全或未提及,研究者们可从这些方面入手,科学地设计临床试验,提高RCTs质量[22]。对于参麦注射液安全性方面,该评价发现严重不良反应,这就要求临床工作者或研究者要重视上市后药物安全性评价,以期能及时掌握药物不良反应发生情况及影响因素,保证用药安全[2],使其更好地服务于临床。
[1] 王连心,谢雁鸣,杨薇,等.基于HIS真实世界的参麦注射液临床实效研究[J].中国中药杂志,2012,37(18):2710-2713.
[2] 王连心,谢雁鸣. 基于文献计量分析的参麦注射液临床安全性评估[J]. 中国中药杂志,2012,37(18):2779-2781.
[3] 王连心,谢雁鸣. 参麦注射液辅助治疗肿瘤临床应用文献分析[J]. 中国中药杂志,2012,37(18):2804-2806.
[4] 张春旭. 参麦注射液联合CTF方案对乳腺癌术后化疗的疗效观察[J]. 浙江中医杂志,2013,48(4):287-288.
[5] 刘军. 参麦注射液减轻恶性肿瘤化疗后毒副作用的临床观察[J]. 医药产业资讯,2005,2(15):47-48.
[6] 惠锦林. 黄芪注射液及参麦注射液在肿瘤化疗中的应用[J]. 现代中医药,2004,5:5-7.
[7] 曾丽,陈志侠,郭德芝,等. 参麦注射液联合化疗治疗恶性肿瘤近期疗效及毒副作用观察[J].浙江中医学院学报,2000,24(3):43-44.
[8] 乔健,白晓梅,孙晓东,等. 参麦注射液配合化疗治疗恶性肿瘤[J]. 西安医科大学学报,2001,22(6):586-587.
[9] 蒋代文. 参麦注射液在“围抗癌化疗期”的临床应用[J]. 湖北省卫生职工医学院学报,2001,14(2):32-33.
[10] 杨秀丽,徐国荣. 参麦注射液在恶性肿瘤化疗中的减毒作用[J]. 中医研究,2008,21(6):40-41.
[11] 姚洁,叶永来. 参麦注射液在鼻咽癌放化疗中的减毒作用[J]. 江西中医药,2009,4:34.
[12] 李英,李海金,尚官敏,等. 参麦注射液联合化疗治疗晚期非小细胞肺癌的临床观察[J]. 浙江中医杂志,2013,48(1):14-15.
[13] 邹彦,张逸群,柏玉举. 参脉注射液对癌症患者放射治疗的辅助疗效观察[J]. 贵阳中医学院学报,2001,23(1):26-27.
[14] 刘鲁明,林胜友,吴良村,等. 参麦注射液对恶性肿瘤化学药物治疗增效减毒作用的临床观察[J]. 中国中药杂志,1996,21(5):50-52.
[15] 龙建安,朱锦匙. 参麦注射液在肺癌化疗中应用的临床观察[J]. 河北医学,2004,10(9):811-812.
[16] 王洪燕,林雁,曹景涛. 静滴参麦注射液出现不良反应2例[J]. 中国中药杂志,2002,27(7):81.
[17] 舒春花,肖轶雯. 参麦注射液致严重过敏反应1例[J]. 中南药学,2010,8(4):318.
[18] 魏丽云. 参麦注射液静滴引起过敏反应1例[J]. 江苏药学与临床研究,2004,12(S1):83.
[19] 张红,张强,姜宁西. 参麦注射液致皮肤过敏2例[J]. 药物流行病学杂志,2000,9(3):159.
[20] 胡晶,张雯,谢雁鸣,等. 参麦注射液治疗急性心肌梗死的Meta分析[J]. 中国中药杂志,2012,37(18):2760-2767.
[21] Xie Y, Tian F. Regulations and guidelines should be strengthened urgently for re-evaluation on post-marketing medicines in China[J]. Chinese journal of integrative medicine, 2013, 19(7): 483-487.
[22] 申浩, 胡晶, 谢雁鸣, 等. 参麦注射液联合西医常规用药治疗不稳定性心绞痛的系统评价[J]. 中华中医药杂志, 2014, 29(1): 285-288.
