用电气石提高二氧化锰电极的电容性能
2014-01-16季辰辰包淑娟
杨 帆,季辰辰,卫 华,包淑娟
(新疆大学应用化学研究所,新疆乌鲁木齐 830046)
二氧化锰(MnO2)因价格低廉、制备工艺简单和理论容量高的特点,成为超级电容器电极材料二氧化钌(RuO2)的替代材料之一[1]。MnO2的充放电机理可分为初级还原过程和次级还原过程。在Na2SO4电解液中,MnO2先在微粒表面吸附M+(M+=H+或Na+),将Mn4+还原为低价锰的氧化物[见式(1)[2]],之后,以两种方式离开电极表面:式(2)的歧化过程,以及质子和电子不断向MnO2内部转移的固相质子扩散过程。
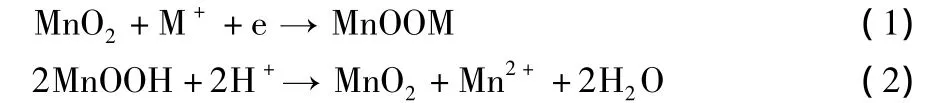
MnO2在初级还原为MnOOH时是可逆的,次级还原过程则不可逆,如歧化反应过程,因Mn2+的生成而很快脱离反应界面,会引起锰损失,因此反应需要控制在初级还原阶段,避免MnOOH的进一步还原[2]。若选取一种吸附物质改性MnO2材料,有望提高MnO2电极的比电容。
电气石是一种天然的硼硅酸盐类矿物,晶体化学通式为XY3Z6B3Si6O27W4,其中,X、Y和Z为三位置的原子或离子。电气石的自发极化性取决于自身的结构特征[3]。电气石的晶体一端为电荷正极、另一端为电荷负极,自身可形成电流和静电场。电气石的吸附作用主要是矿物表面吸附(包含静电作用、表面键合和氢键作用等),同时也有极性吸附。极性吸附是由电气石两极的电荷产生电场,将溶液中带电的正、负离子聚集于电气石周围;表面吸附时,吸附的离子没有进入晶格,仅浓集于表面,且可同时吸附阴、阳离子[4]。
本文作者尚未见到关于电气石作为超级电容器电极材料的报导。基于电气石具有独特的吸附特性,可以将质子、Na+等快速吸附到电极表面,使MnO2电极能够迅速发生还原反应,因此将两者物理混合,试图提高电容器的比电容。
1 实验
1.1 MnO2样品的制备和分析
将1.7 g硫酸锰(天津产,AR)和0.7 g高锰酸钾(天津产,AR)在玛瑙碾钵中研磨1 h,再移入盛有100 ml蒸馏水的烧杯中,边搅拌,边滴加30 ml 1 mol/L H2SO4(天津产,AR),持续搅拌30 min。沉淀物用蒸馏水和无水乙醇(天津产,AR)洗涤至溶液中性,过滤后,在100℃下干燥12 h[5]。
用D8型X射线衍射仪(德国产)测试样品的晶体结构,CuKα,管压 30 kV、管流40 mA,扫描速度为 5(°)/min,步长为0.5°;用JSM-6700F型扫描电子显微镜(日本产)观察样品的表面形貌。
1.2 电极的制作与电化学性能测试
将10 mg MnO2样品或电气石(阿勒泰产,AR)与导电剂乙炔黑(河南产,电池级)、粘结剂聚四氟乙烯(上海产,电池级)按质量比85∶10∶5混匀调浆,涂覆于面积为1.0 cm2的正方形泡沫镍(110 PPI,上海产,AR)上,压制成电极,在60℃下过夜干燥。另将4份10 mg MnO2样品与5.0 mg、10.0 mg、12.5 mg和15.0 mg电气石分别混合,作为电极活性材料,按上述步骤制成电极。
将上述工作电极、Pt对电极、饱和甘汞参比电极与电解液1 mol/L Na2SO4(天津产,AR)组成三电极体系,常温下用CHI660D型电化学工作站(上海产)进行循环伏安和恒流充放电测试,电压均为-0.1~0.7 V。循环伏安测试的扫描速度为5 mV/s;恒流充放电测试的电流为0.25 A/g、0.50 A/g、1.00 A/g、1.50 A/g 和 2.00 A/g。
2 结果与讨论
2.1 结构与形貌分析
图1为MnO2样品与电气石的XRD图。
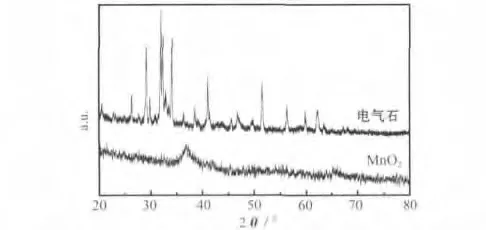
图1 MnO2与电气石的XRD图Fig.1 XRD patterns of MnO2and tourmaline
从图1可知,合成的MnO2没有明显的尖锐衍射峰,只在37°处存在1个较弱且宽化的衍射峰,表明晶化的程度较低,属于无定形的MnO2。电气石的组成较为复杂,主要成分为SiO2、FeO、Fe2O3、B2O3、Al2O3、Na2O、MgO、Li2O 和 MnO2[4]等。电气石在29°、32°、34°、41°及51°附近分别有较强的衍射峰,与Ca54MgAl2Si16O90(JCPDS:13-0272)相符,说明所用电气石中,SiO2、CaO、MgO和Al2O3的含量相对较高。
图2为MnO2样品与电气石的SEM图。

图2 MnO2与电气石的SEM图Fig.2 SEM photographs of MnO2and tourmaline
从图2可知,合成的MnO2尺寸分布相对较窄,颗粒表面的“绒刺”结构可增加样品的比表面积及表面的活性位点;电气石的尺寸较大,且分布相对较宽,结构较致密。
2.2 电化学性能
电气石-MnO2电极的循环伏安曲线见图3。
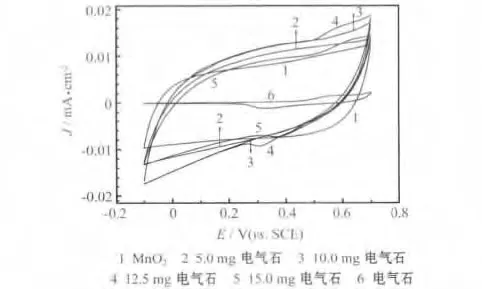
图3 电气石-MnO2电极的循环伏安曲线Fig.3 CV curves of tourmaline-MnO2electrodes
从图3可知,纯MnO2电极的循环伏安曲线呈较好的矩形特征,阴、阳极曲线基本对称,具有较好的电化学电容特性,而纯电气石电极的电容极低。添加一定量电气石的电极,曲线面积增大,即电容增大,原因可能是电气石特有的吸附性能使更多的质子与Na+浓集于电极表面,促使电极表面更多的活性物质MnO2参与电化学反应,使电极的电容增大,且电气石自身也可提供一定的电容。当电气石质量为12.5 mg时,曲线的面积最大,还出现了一对较明显、与电气石的氧化还原峰位置一致的氧化还原峰,表明一定量的电气石参与了氧化还原反应。
电气石-MnO2电极在电流为0.25 A/g时的恒流充放电曲线见图4。
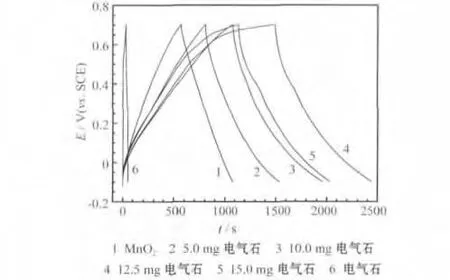
图4 电气石-MnO2电极在电流为0.25 A/g时的恒流充放电曲线Fig.4 Galvanostatic charge-discharge curves of tourmaline-MnO2electrodes at the current of 0.25 A/g
从图4可知,随着电气石掺入量的增加,电极的比电容逐步提高,当电气石质量为12.5 mg时达到最大值。此外,当电气石质量为10.0 mg时,充放电曲线的对称性开始降低,充电时间长于放电时间,即充电电容大于放电电容,表明电极的库仑效率有所降低。这可能是由于电气石的掺入使电极本身的电阻增大,降低了离子迁移速率,且电极表面的电气石与电活性物质MnO2混合得不够均匀。
根据式(3)可计算电极的比电容C。

式(3)中:I为放电电流,Δt为放电时间,m为电极活性物质MnO2的质量,ΔE为电位差。经计算:电气石电极、MnO2电极的比电容分别为6.7 F/g、183.9 F/g,电气石质量为5.0 mg、10.0 mg、12.5 mg和15.0 mg的电极,比电容分别为 283.1 F/g、324.6 F/g、347.0 F/g 和 326.1 F/g。
不同电流下电气石-MnO2电极的比电容见图5。
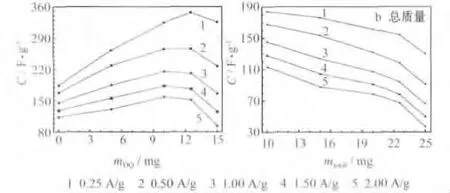
图5 不同倍率下电气石-MnO2电极比电容随质量的变化Fig.5 Changes of specific capacitance of tourmaline-MnO2 electrodes with mass at different rates
从图5a可知,在不计电气石质量的条件下,掺入一定量的电气石,可提高MnO2电极的比电容,尤其是在小电流放电时。在大电流工作时,由于电气石自身为硅酸盐矿物,导电性较差,导致电极的倍率性能不理想。从图5b可知,当把电气石作为电极活性物质计入总质量考虑时,虽然电气石对电容的贡献有限,但有助于提高MnO2的电容性能。
MnO2电极与电气石质量为12.5 mg的电气石-MnO2电极以1.00 A/g电流循环,电容保持率的变化情况见图6。
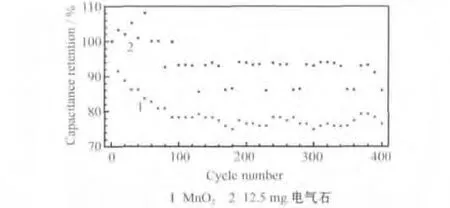
图6 MnO2电极与电气石质量为12.5 mg的电气石-MnO2电极以1.00 A/g电流循环的电容保持率Fig.6 Capacitance retention of MnO2electrode and tourmaline-MnO2electrode with tourmaline mass of 12.5 mg cycled with the current of 1.00 A/g
从图6可知,循环400次,两种电极的电容均有所衰减,纯MnO2电极的循环稳定性较低,电容保持率不到80%;掺入电气石后,电容保持率可提高到约90%。这可能是由于电气石的表面吸附特性,阻碍了MnOOH的进一步还原,使MnO2的还原反应控制在初级可逆阶段,减少了锰的损失。
3 结论
将具有特殊吸附特性的电气石与MnO2活性物质相结合,制备了高性能电极材料。循环伏安、恒流充放电等电化学性能测试结果表明:当MnO2质量为10 mg、电气石质量为12.5 mg时,电极的比电容最高,可达347.0 F/g。这可能是由于电气石将质子与Na+快速吸附到电极表面,使更多的活性物质MnO2参与了电化学反应。电极的循环稳定性能也得到了改善,可能是由于电气石的表面吸附特性,有助于将MnO2的还原反应控制在可逆的初级阶段,减少锰的损失。
[1]WANG Jia-wei(王佳伟),CHEN Bai-zhen(陈白珍),CHEN Ya(陈亚),et al.溶胶-凝胶法制备超级电容器用二氧化锰[J].Battery Bimonthly(电池),2012,42(5):270 -273.
[2]Zhu J,Shi W,Xiao N,et al.Oxidation-etching preparation of MnO2tubular nanostructures for high-performance supercapacitors[J].ACS Applied Materials & Interfaces,2012,4(5):2 769 -2 774.
[3]ZHANG Zhi-xiang(张志湘),FENG An-sheng(冯安生),GUO Zhen-xu(郭珍旭).电气石的自发极化效应在环境与健康领域的应用[J].China Non-Metallic Mining Industry(中国非金属矿工业导刊),2003,(1):48 -50.
[4]XU Huan-yan(胥焕岩),WANG Peng(王鹏),MAO Gui-jie(毛桂洁),et al.电气石在环境领域的最新应用研究:处理雅格素蓝BF-BR染料废水[J].Chinese Journal of Environmental Engineering(环境工程学报),2007,1(4):65 -66.
[5]Fu X B,Feng J Y,Wang H,et al.Fast synthesis and formation mechanism of γ-MnO2hollow nanospheres for aerobic oxidation of alcohols[J].Mater Res Bull,2010,45(9):1 218-1 223.
