间充质干细胞移植对缺血/再灌注大鼠心肌胶原与去甲肾上腺素转运蛋白的影响
2013-12-23赵丽霞马洪滨李春祥洪绍彩孟庆莲贝俊杰高全胜
赵丽霞,马洪滨,李春祥,洪绍彩,孟庆莲,贝俊杰,高全胜
骨髓间充质干细胞移植(b o n e m a r r o w mesenchymal stem cells,BMSCs)是再生医学领域研究的新进展。近年来,许多研究观察到BMSCs移植对心肌梗死(myocardial infarction,MI)后心功能、心肌重塑有较好的改善作用,为心力衰竭(heart failure,HF)的治疗提供了新的治疗方法[1,2]。
1 材料与方法
1.1 实验动物 43只(8~l0)周龄Wistar大鼠,体重(200~250)g(由中国人民解放军军事医学科学院实验动物中心提供)。室温(18~25)℃,湿度45%~65%,氨浓度<20mg/L,给光7am~7pm,普通饲料,自由饮水。分对照组(14只),MI组(14只),BMSCs移植组(BMSCs组,15只)。
1.2 缺血/再灌注动物模型建立 大鼠以40 mg/kg戊巴比妥钠麻醉后,腹腔内注射阿托品2 mg/kg,呼吸机辅助呼吸,消毒后胸骨左缘(1~2)mm处剪断第4肋骨,在(2~3)mm处将缝合针自左心室侧穿入约(1/3~1/2)层心肌,连同结扎置入的1cm软胶棒(直径为3mm)及心肌后关闭胸腔。冠状动脉结扎60min后开胸剪断结扎线,逐层缝合肌肉、皮下组织及皮肤[3]。
1.3 骨髓间充质干细胞的原代培养 4周龄雄性Wistar大鼠(100-120g)断颈处死,无菌状态下暴露出股骨、胫骨干骺端骨髓腔,用不完全的DMEM/F12(Invitrogen公司)培养基约5 mL冲洗骨髓腔至中空,收集冲洗液15 kr/min离心10min,弃去上清,以10%完全DMEM/F12培养基重悬细胞。计数活细胞后,调整活细胞的浓度为(1~5)×107/cm ,接种至25cm培养瓶中,37.5%CO2、95%湿度的细胞培养箱中培养;分别于24 h、48 h换半量、全量培养基,弃去未贴壁悬浮的细胞,以后每3天换半量培养基,待细胞汇合至70%~80%,弃去培养基,用不完全DMEM/F12培养基冲洗后,加入0.25%的胰蛋白酶消化贴壁细胞,镜下可见细胞变圆,部分脱壁,停止消化,吹打使所有细胞脱壁,15 kr/min离心细胞悬液;弃去上清,以15%完全DMEM/F12培养基重悬细胞,调整细胞浓度到1×106/cm,按1:1或1:2比例传代培养[4]。
1.4 骨髓间充质干细胞心脏移植 心肌再灌注前在左心室前壁MI周边5点注射,MI对照组注射不完全DMEM/F12培养基100μL;MSC组注射BMSC1×1010/L,每只100μL。
1.5 血流动力学检测 大鼠分别于术后7d、28d血流动力学的检测,2%戊巴比妥钠(40 mg/kg)腹腔内麻醉,分离右颈总动脉,将充满1%肝素的聚乙烯管(内径0.5mm,外径1 mm)经右颈总动脉逆行插入至左心室,另一端连接至MP150 16导生理记录仪记录左室收缩压(LVSP)、左室舒张末压(LVEDP)、左室内压上升、下降的最大速率(±dp/dtmax)。
1.6 心肌组织图像分析 术后7d和28d分别处死大鼠进行组织学分析。在10倍视野下,应用Image Pro Plus 4.5图像分析软件测定。①随机选取5~6个完全包含梗死区自心内膜至心外膜的区域,计算其平均厚度;②梗死范围的计算:梗死范围=(梗死区心内膜长度+梗死区心外膜长度)/(左心室心内膜周长+左心室心外膜周长);③扩展指数的计算:扩展指数=(左室心腔面积/左室面积)×(室间隔厚度/梗死区厚度);④胶原分析:胶原容积分数(Collagen Volume Fraction,CVF)=胶原总面积/图像总像素数,代表胶原在所测组织中的相对含量;胶原成熟程度=(红色胶原总面积+橙色胶原总面积)/(黄色胶原总面积+绿色胶原总面积);⑤NET免疫组织化学检测。
1.7 统计学方法 应用SPSS16.0处理,计量资料以 (±s)表示,符合正态分布的计量资料采用单因素方差分析及t检验,方差齐时组间两两比较采用LSD 法,方差不齐时采用Games-Howell 法。P<0.05为差异有统计学意义。
2 结果
2.1 各组模型大鼠术后体重、心脏重量变化 各组大鼠术后7d、28d处死,体重、心室重量变化无统计学意义(表1)。
2.2 血流动力学指标 术后第7天与第28天,对照组、MI组、BMSCs组三组间大鼠LVSP无统计学差异(P>0.05);与对照组比较,MI组、BMSCs组LVEDP增高(P<0.05),与MI组比较,BMSCs组降低(P<0.05);与对照组比较,MI组、BMSCs组左心室内压力+dp/dtmax及-dp/dtmax降低(P<0.05);但BMSCs组+dp/dtmax及-dp/dtmax较MI组增加(P<0.05,表2)。
2.3 心肌组织病理学分析
2.3.1心肌梗死面积及心室重塑 左室横断面苦味酸-天狼猩红染色大体观(图1):在镜下可观察MI组7天时梗死面积约30%,28天约26%,多为透壁性梗死,累及室壁厚度超过50%,BMSCs组7天的梗死面积约23%,28天约17%,梗死范围往往只限于中层心肌,心内膜下和心外膜下均可见岛状存活心肌(表3)。
2.3.2 心肌梗死区胶原成熟度比较 与MI组比较,①CVF变化:术后第7天,MI区与非MI区MSCs组CVF差异无显著性(P>0.05);术后第28天,BMSCs组MI区、非MI区CVF降低(P<0.05);②胶原成熟度:术后第7天,MI区与非MI区BMSCs移植组胶原成熟度无明显变化(P>0.05);术后第28天,MI区与非MI区MSCs组成熟程度降低(P<0.05,表4)。
2.3.3 心肌NET免疫组织化学检测 术后第7天,与对照组相比,MI组与MSCs组心肌NET蛋白均增高(P<0.05),术后第28天NET表达均低于第7天,MSCs组仍高于对照组和MI组(P<0.05)(表5,图2)。
3 讨论
心肌梗死(MI)后,由于成熟的心肌细胞缺乏再生能力,心肌细胞的丧失和病理性心室重构是发展为心功能不全的主要成因。而在心梗时心脏交感神经变化目前已引起了重视,包括神经支配密度和神经再摄取功能的改变。
心肌梗死后出现心脏交感神经变化(neuroplasticity),包括神经密度降低、不均匀分布(heterogeneous innervation)、神经再生(regeneration)及神经再摄取功能(reuptake 1)异常等,这些变化常同时存在。无论是否同时存在神经密度变化,甚至神经密度增加,均可出现神经摄取功能降低[8-13]。正常情况下,交感神经释放的NE 90%以上由神经突触前膜上的去甲肾上腺素转运蛋白(NET)重新摄取回到突触前膜中[14,15]。交感神经功能异常,神经再摄取作用下降,导致心肌间质中NE水平长期增高是导致HF进展的重要原因。
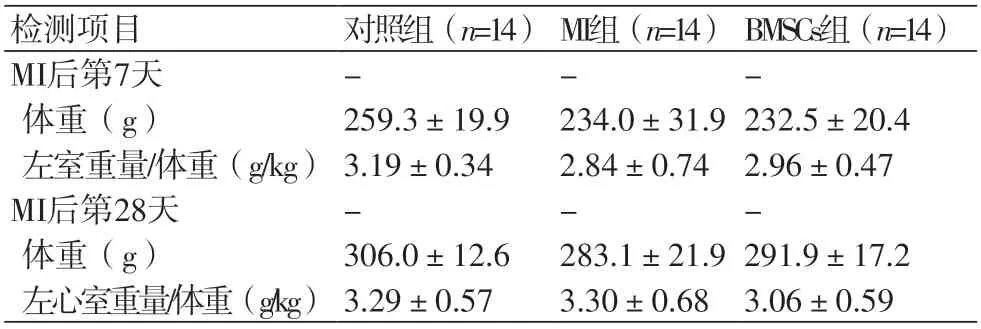
表1 各组大鼠体重及左心室体重比变化情况
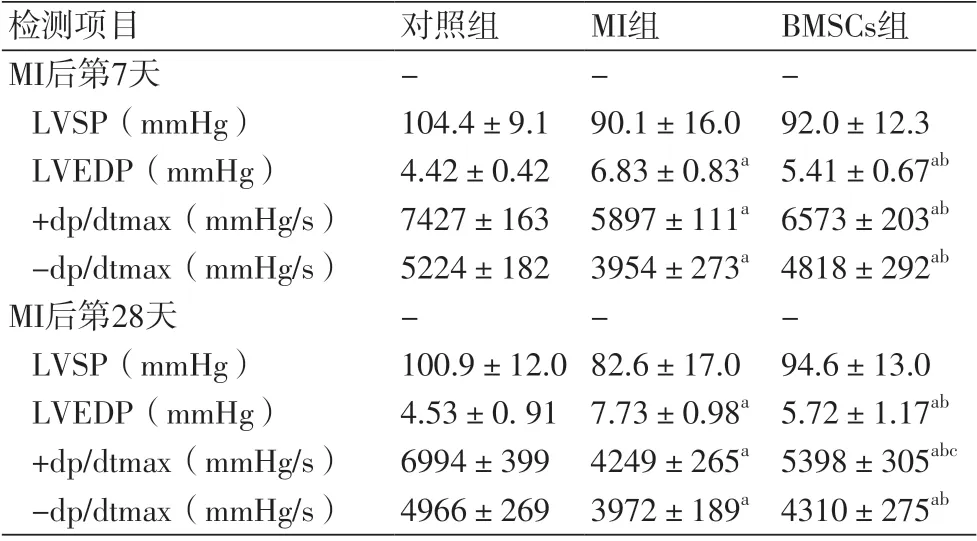
表2 各组大鼠超声血流动力学检测情况
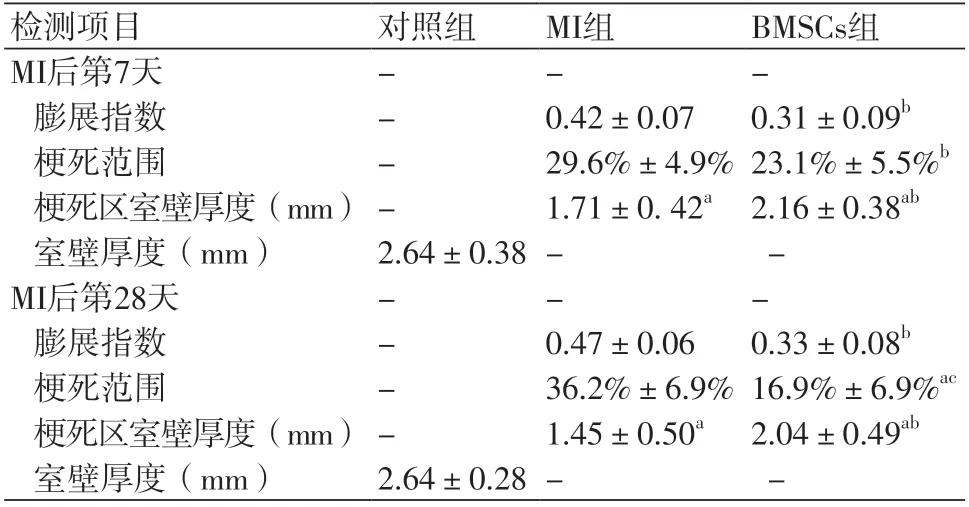
表3 左心室梗死范围、厚度及膨展指数
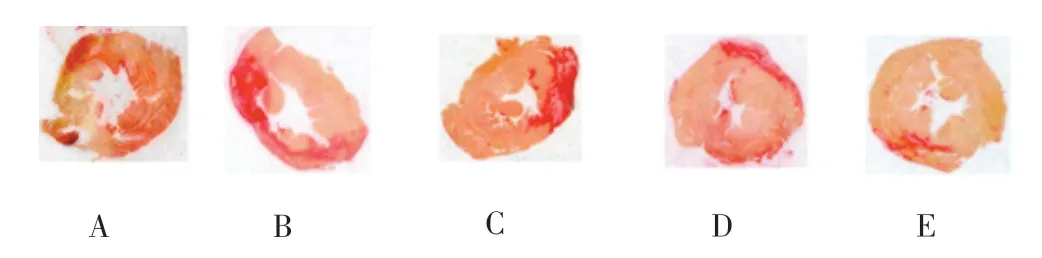
图1 左心室横断面(苦味酸-天狼猩红染色,×10;A:假手术组,B:MI对照组MI后7d,C:MI对照组MI后28d,D:MSC组MI后7d,E:MSC组MI后28d)。
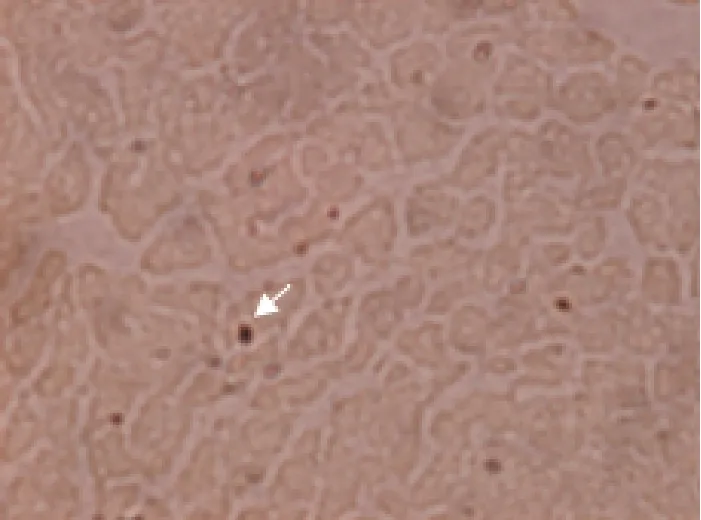
图2 NET免疫组化标本(伊红染色,×200);箭头所示为NET蛋白
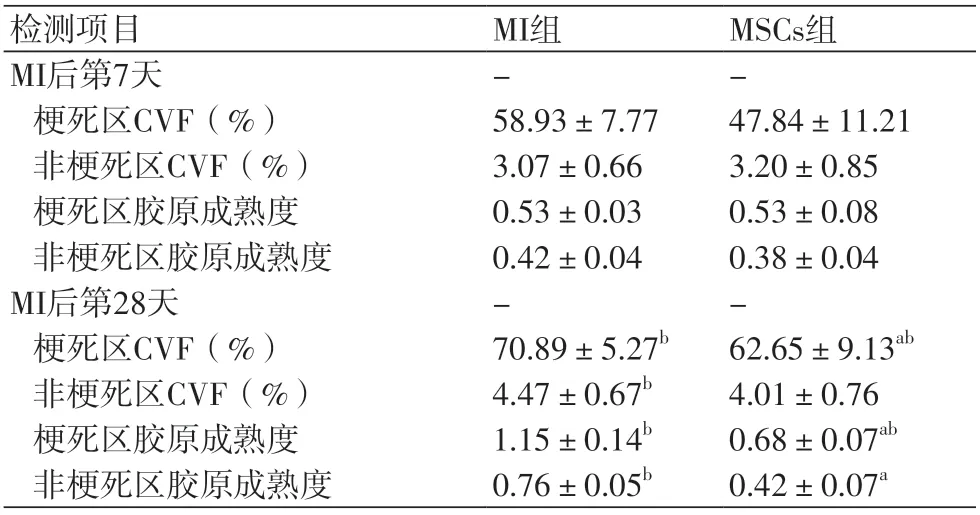
表4 左心室梗死区、非梗死区胶原成熟度、容积分数

表5 大鼠非梗死区去甲肾上腺素转运蛋白阳性数
众所周知,心肌间质即细胞外基质(ECM)的主要成分是胶原,而胶原中又以I型和Ⅲ型胶原为主,约占心肌胶原总量90%以上,这些物质对维持相邻心肌细胞构成完整的功能单位起着重要的作用[5-7]。MI区胶原形成替代了坏死的心肌细胞有助于维持心脏的几何形态,而MI区和非MI区的胶原则过度增生并且结构紊乱,导致纤维化,进而心脏重塑损害心脏的功能。心脏重塑除了纤维化以外,还有心肌细胞的凋亡、肥大,由于非MI区不存在组织的缺损,因此非MI区对心脏重塑的贡献主要体现在心肌细胞的凋亡、肥大。
本实验中MSCs组的胶原成熟度比MI组低,不成熟胶原较多,这一变化抑制心室腔的进行性扩张,延缓心室重构的进展。既往研究已经发现,交感神经对胶原生成可能存在着一定的关系。El-Helou等也观察到[16],与对照组比较,糖皮质激素(地塞米松)干预可使MI后非MI区心肌胶原(myocardial collagen)mRNA 显著降低,同时心肌交感神经密度、生长相关蛋白43(growth associated protein 43,GAP43)、NGFmRNA及蛋白表达均下降。说明抑制胶原合成,可降低交感神经支配密度,但这个影响可能不是直接的,被很多复杂的机制所掩盖。有研究发现,通过不同途径阻断交感神经兴奋,均可减少心肌梗死大鼠模型的心脏胶原沉积,提示交感神经系统过度激活在诱导心肌肥厚的同时,亦参与了心梗后心脏胶原重塑的发生、发展。这提示神经因素对心脏重塑是有一定影响的[17]。研究显示,MI后发生改变的物质可影响神经因素、胶原重塑:①血管紧张素(Ang)—交感神经参与激活局部组织肾素-血管紧张素系统[18]催化AngI转化为AngⅡ,AngⅡ与特异性受体AT1结合通过丝裂原激活蛋白激酶/胞外信号调节激酶(IVIAPK/ERK)途径促进胶原合成[19];②蛋白激酶C(PKC)—机械压力的变化和AngⅡ可以激活PKC,从而影响基质金属蛋白酶家族等调控胶原的物质[20,21],同时,PKC还可以介导突触前膜上表面表达的NET发生内化,从而使NET表面表达数量减少[22,23],间接升高NE加重对组织重构的影响[24];③神经肽—交感神经的异常增生可能过度释放神经肽,从而致神经肽的积累,即使在没有机械应力的作用下,仍然能导致胶原的形成[25]。
本实验结果表明,交感神经再生与胶原含量二者间关系密切,调控交感神经功能或影响胶原合成的因素可能互相影响,确切机制需要进一步研究。心肌间质、交感神经功能异常对MI后心脏重塑均有重要影响,阐明二者间互相影响机制对治疗心血管病后心脏重塑及对心功能不良影响意义重要。
[1] Reffelmann T,Konemann S,Kloner RA. Promise of Blood-and Bone Marrow-Derived Stem Cell Transplantation for Functional Cardiac Repair.Putting It in Perspective With Existing Therapy[J]. J Am Coll Cardiol, 2009,53(4):305-8.
[2] Rasmussen TL,Raveendran G,Zhang J,et al. Getting to the Heart of Myocardial Stem Cells and Cell Therapy[J]. Circulation,2011,123(16): 1771-9.
[3] Gnecchi M,He H,Liang OD,et al. Paracrine action accounts for marked protection of ischemic heart by Akt-modified mesenchymal stem cells[J]. Nat Med,2005,11(4):367-8.
[4] Bowers SL,Banerjee I,Baudino TA. The exteacellular matrix:at the center of it all[J]. J Mol Cell Cardiol,2010,48(3):474-82.
[5] 李贺,周欣,舒珺,等. 骨髓间充质干细胞移植对心肌缺血-再灌注大鼠心肌胶原与血管新生的影响[J]. 中国动脉硬化杂志,2008,16(10):813-8.
[6] Grassi G. Assessment of Sympathetic Cardiovascular Drive in Human Hypertension,Achievements and Perspectives[J]. Hypertension, 2009,54(4):690-7.
[7] 马晶,马晓青,叶帆,等. 心脏交感神经与老龄过程中心瓣膜交感神经变化[J]. 心血管病学进展,2008,29(增刊):81-4.
[8] Machado C,Camargos RS,Guerra LB,et al. Cardiac Autonomic Denervation in Congestive Heart Failure:Comparison of Chagas Heart Disease With Other Dilated Cardiomyopathy[J]. Hun Pathol,2000,31(1):3-10.
[9] Amino T,Uchihara T,Tsunekawa H,et al. Myocardial nerve fibers are preserved in MPTP-treated mice,despite cardiac sympathetic dysfunction[J]. Neurosci Res,2008,60(3):314-8.
[10] Orimo S,Oxawa E,Nakade S,et al.(123)Imetaiodobenzlguanidine myocardial scintigraphy in Parkinson’s disease[J]. J Neurol Neurosurg Psychiatry,1999,67(2):189-94.
[11] Stevens MJ,Parkinson’s DM,Allman KC,et al. Cardiac Sympathetic Dysinnervation in Diabetes:Implications for Enhanced Cardiovascular Risk[J]. Circulation,1998,98(10):961-8.
[12] Biaggioni I. Parkinson’s Disease.Autonomic Neuronopathy With Impaired Cardiovascular Regulation[J]. Hypertension,2007,49(1):21-2.
[13] Li H,Ma XQ,YE F,et al. The expression of cardiac sympathetic norepinephrine transporter andβ1-adrenergic receptor was decreased in the aging rats[J]. JZU Science B,2009,10(3):203-10.
[14] 梁栋,刘旭东,李贺. 去甲肾上腺素转运蛋白在心力衰竭中的作用[J]. 心血管病学进展.2006,27(6):793-7.
[15] Zahniser NR,Doolen S. Chronic and acute regulation of Na/Cldependent neurotransmitter transporters:drugs,substrates,p resynaptic receptors,and signaling systems[J]. Pharmacol & Therap,2001,92(1):21-55.
[16] El-Helou V,Proulx C,Gosselin H,et al. Dexamethasone treatment of post-MI rats attenuates sympathetic innervation of the infarct region[J]. J Appl Physiol, 2008, 104(1):150-6.
[17] Latini R,MasSon S,Jeremic G,et al. Comparative efficacy of a DA2/alpha2 agonist and a beta-blocker in an reducing adrenergic drive and cardiac fibrosis in an experimental mode of left ventricular dysfunction after coronary artery occlusion[J]. J Cardiovasc Pharmacol, 1998,31(4):601-8.
[18] Ieda M,Fukuda K,Hisaka Y,et al. Endothelin-1 regulates cardiac sympathetic innervation in the rodent heart by controlling nerve growth factor expression[J]. J Clin Invest. 2004;113(6):876-84.
[19] Tharaus PL,Chatziantoniou C,Fakhouri F,et al. Angiotensin Ⅱ activates collagen I geng through a mechnanism involving the MAP/ER kinase pathwnys[J]. Hypertension,2000,36(4):330-6.
[20] Mann DL,Spinale FG. Activation of matrix metaloproteinases in the failing human heart:breaking the tie that binds[J].Circulation,1998,98(17): 1699-702.
[21] Husse B,Briest W,Homagk L,et al. Cyclical mechanical stretch modulates expression of collagen Ⅰ and collagen Ⅲ by PKC and tyrosine kinase in cardiac fibroblasts[J]. Am J Physiol Regul Integr Comp Physiol,2007,293(5):1898-907.
[22] Backs J,Bresch E,Lutz M,et al. Endothelin-1 causes a reduced norepinephrine re-uptake by a endothelin receptor-A and a protein kinase C-mediated mechanism within the rat heart[J]. Eur Heart J,2000,21(7):626-31.
[23] Apparsundaram S,Schroeter S,Giovanetti E,et al. Acute regulation of norepinephrine transport:Ⅱ PKC-modulated surface expression of human norepinephrine transporter proteins[J]. J Pharmacol Exp Ther,1998,287(2): 744-51.
[24] Luisi AJ,Fallavollita JA,Suzuki G,et al. Spatial in homogeneity of sympathetic nerve function in hibernating myocardium[J]. Circulation,2002,106(7):779-81.
[25] Akaishi S,Ogawa R,Hyakusoku H. Keloid and hupertrophi scar: neurogenic inflammation hypotheses[J]. Med Hypotheses,2008,71(1):32-8.
